 江西省 化学中考特训方案 考点精讲精炼 11.docx
江西省 化学中考特训方案 考点精讲精炼 11.docx
- 文档编号:10559613
- 上传时间:2023-02-21
- 格式:DOCX
- 页数:21
- 大小:206.19KB
江西省 化学中考特训方案 考点精讲精炼 11.docx
《江西省 化学中考特训方案 考点精讲精炼 11.docx》由会员分享,可在线阅读,更多相关《江西省 化学中考特训方案 考点精讲精炼 11.docx(21页珍藏版)》请在冰豆网上搜索。
江西省化学中考特训方案考点精讲精炼11
第八单元 金属和金属材料
第1课时 金属材料 金属资源的利用和保护
江西五年中考命题规律
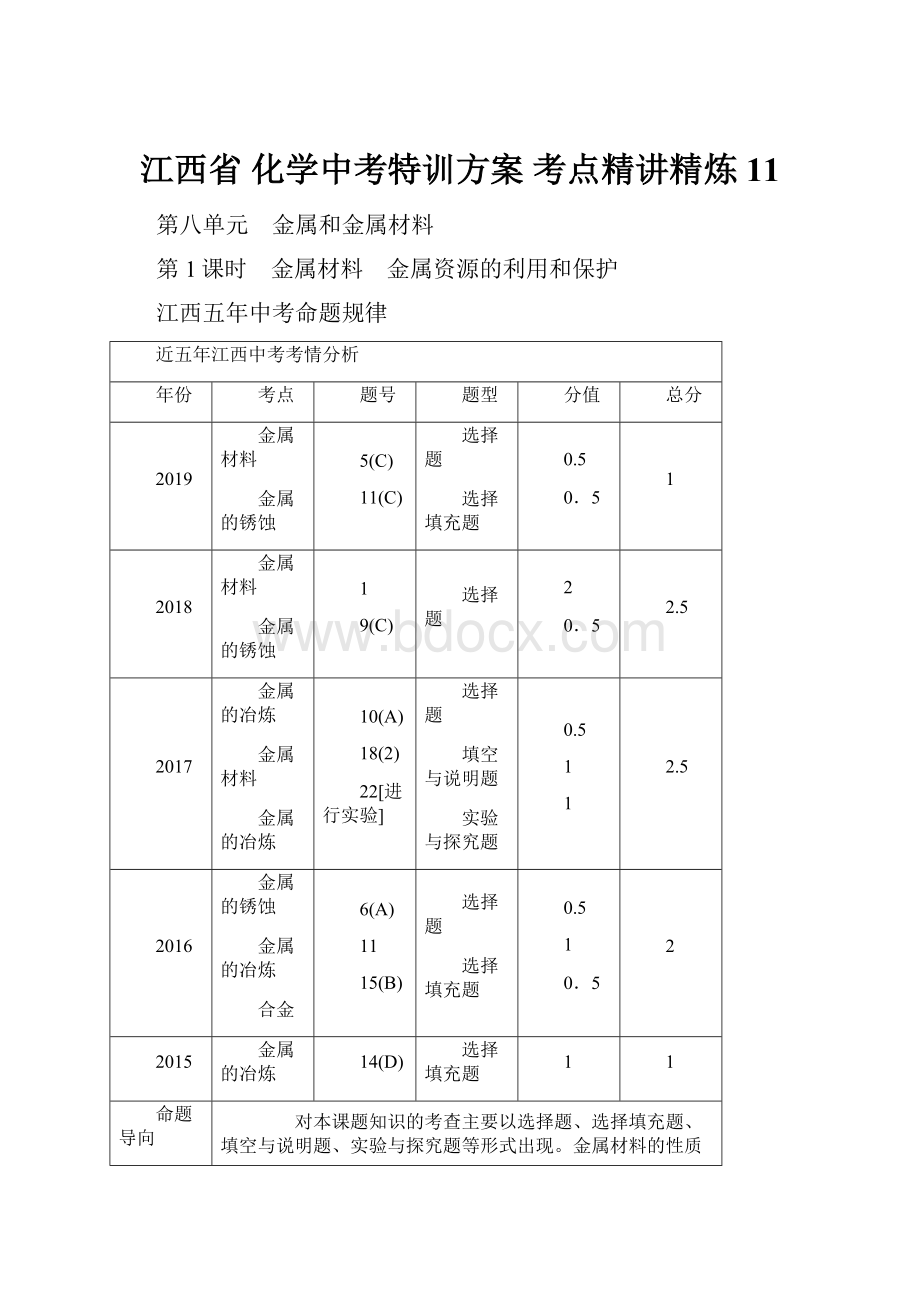
近五年江西中考考情分析
年份
考点
题号
题型
分值
总分
2019
金属材料
金属的锈蚀
5(C)
11(C)
选择题
选择填充题
0.5
0.5
1
2018
金属材料
金属的锈蚀
1
9(C)
选择题
2
0.5
2.5
2017
金属的冶炼
金属材料
金属的冶炼
10(A)
18
(2)
22[进行实验]
选择题
填空与说明题
实验与探究题
0.5
1
1
2.5
2016
金属的锈蚀
金属的冶炼
合金
6(A)
11
15(B)
选择题
选择填充题
0.5
1
0.5
2
2015
金属的冶炼
14(D)
选择填充题
1
1
命题导向
对本课题知识的考查主要以选择题、选择填充题、填空与说明题、实验与探究题等形式出现。
金属材料的性质和用途、材料的分类、金属的锈蚀、金属的冶炼等是中考考查的热点
金属和金属矿物一
金属和金属矿物二
中考考点清单
金属材料(高频考点)
1.金属材料包括__纯金属__和__合金__,日常生活中使用最多的金属材料是__合金__。
2.金属的物理性质
共性
①有金属光泽——金银饰品等;②有良好的__导电__性——制电线、电缆;③有良好的__导热__性——用作铁锅;④有良好的__延展__性——作铝箔
特性
①颜色:
铁、铝等大多数金属呈__银白色__,但__铜__呈紫红色,金呈黄色;②状态:
常温下,大多数金属呈__固态__,但__汞__是液体;③不同的金属熔点、沸点、导电性、导热性、密度、硬度等都差别较大
3.合金
(1)定义:
在金属中加热熔合某些金属或非金属而制得的具有金属特性的物质。
合金属于__混合__物。
(2)性能:
由于合金的组成与其成分金属不同,所以性能上存在差异,一般合金与其成分金属相比,__硬度__较大,__熔点__较低,__抗腐蚀能力__较强。
(3)常见的合金:
①铁的合金有__生铁__和__钢__(它们的区别是__含碳量不同__);
②铜的合金__黄铜__和__青铜__;
③钛合金熔点高,密度小,与人体有很好的相容性,可制成人造骨。
特别提醒
①合金中一定含有金属元素,也可能含有非金属元素。
②合金一定是混合物。
③合金一定有金属特性。
④金属氧化物是纯净物,不属于合金。
金属的冶炼(高频考点)
1.金属资源的存在形式:
地球上的金属资源广泛存在于地壳和海洋中,除少数很不活泼的金属,如金、银等以__单质__形式存在外,其他都以__化合物__形式存在。
2.常见的金属矿物:
赤铁矿的主要成分是__氧化铁(Fe2O3)__,磁铁矿的主要成分是__四氧化三铁(Fe3O4)__,铝土矿的主要成分是氧化铝。
3.铁的冶炼
(1)一氧化碳还原氧化铁
①反应原理:
__3CO+Fe2O3
2Fe+3CO2__,实验中炼得的铁是__纯净__物。
②实验装置
③实验步骤:
实验开始时,先通一会儿CO,再用酒精喷灯加热,以排尽装置中的空气,防止__加热一氧化碳和空气的混合物引起爆炸__。
实验完毕时,先熄灭酒精喷灯,再继续通入CO至玻璃管冷却,防止__还原出来的铁重新被氧化__。
(可记为“一氧化碳早出晚归,酒精喷灯迟到早退”)
④实验现象:
玻璃管内红色粉末逐渐变成__黑色__,试管内澄清石灰水__变浑浊__,导管内尾气燃烧产生__蓝__色火焰。
⑤尾气处理:
一氧化碳有毒,是空气污染物之一,处理原则是利用一氧化碳的可燃性,使其燃烧转化为二氧化碳。
特别提醒
一氧化碳还原氧化铁实验的“一通、二点、三灭、四停、五处理”:
“一通”即先通一氧化碳;“二点”即点燃酒精喷灯加热;“三灭”即实验完毕后,先熄灭酒精喷灯;“四停”即等到玻璃管冷却至室温时再停止通一氧化碳;“五处理”即处理尾气,防止CO污染空气。
(2)工业炼铁
①原理:
__3CO+Fe2O3
2Fe+3CO2__。
②设备:
高炉。
③原料:
铁矿石、焦炭(作用:
一是__产生热量,提高炉温__,二是__产生CO作还原剂__)、石灰石、空气。
④产物:
工业炼得的铁为__生铁__,属于__混合__物(实验室模拟工业炼铁炼得的铁为纯净物)。
金属锈蚀及防护(高频)
1.铁锈蚀条件的探究
实验
①
②
③
现象
__不生锈__
__不生锈__
__生锈__
分析
实验①③说明铁生锈一定与__氧气__有关;实验②③说明铁生锈一定与__水__有关;实验①蒸馏水煮沸后使用的原因是__除去蒸馏水中溶解的氧气__
结论
分析对比实验①②③可知,铁生锈的条件:
铁与__O2__、__H2O__同时接触,铁锈的主要成分是__氧化铁(Fe2O3)__。
2.防止铁锈蚀的措施(即破坏铁生锈的条件)
(1)保持铁制品表面的洁净与干燥(隔水)。
(2)在铁制品表面涂保护膜,如涂油、刷油漆、电镀等(隔水、隔氧)。
(3)制成不锈钢(改变性能)。
3.保护金属资源的途径
(1)回收废旧金属。
(2)防止金属锈蚀。
(3)有计划、合理开采金属矿物。
(4)寻找金属替代品。
知识整合——构建物质网络
以Fe为核心的物质网络图
① 3CO+Fe2O3
2Fe+3CO2
或3H2+Fe2O3
2Fe+3H2O
或3C+2Fe2O3
4Fe+3CO2↑
②__3Fe+2O2
Fe3O4__
③ Fe+2HCl===FeCl2+H2↑
或Fe+H2SO4===FeSO4+H2↑
④ Fe2O3+6HCl===2FeCl3+3H2O
或Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
⑤ Fe+CuSO4===FeSO4+Cu
或Fe+CuCl2===FeCl2+Cu等,合理即可
⑥__Cu+2AgNO3===2Ag+Cu(NO3)2__
⑦__Fe+2AgNO3===Fe(NO3)2+2Ag__
⑧__2Cu+O2
2CuO__
⑨ C+2CuO
2Cu+CO2↑
或H2+CuO
Cu+H2O
或CO+CuO
Cu+CO2
⑩ CuO+2HCl===CuCl2+H2O
或CuO+H2SO4===CuSO4+H2O
中考重难突破
金属材料(金属的物理性质及用途、合金)
例1 (2018·江西中考)常温下为液态金属的是( )
A.汞B.金
C.银D.铝
【解析】汞是熔点最低的金属,常温下呈液态。
1.(2019·江西模拟)教室里的物品伴随着我们每天的学习,下列物品属于金属材料制作的是( D )
A.磨砂玻璃黑板B.木制桌椅
C.玻璃钢讲台面板D.铝合金窗框
2.(2019·江西样卷)下列属于合金的是( A )
A.不锈钢B.铜片
C.硫磺D.氧化铁
方法技巧
记住金属的物理共性的同时,对一些金属的物理特性也需了解。
常温下,大多数金属是银白色(铜为紫红色,金为黄色),大多数金属呈固态(汞为液态)。
金属的冶炼
例2 如图为“一氧化碳与氧化铁反应”的装置,该反应利用CO的还原性,将Fe2O3中的铁还原出来。
(1)写出高温条件下CO与Fe2O3反应的化学方程式:
____________________。
(2)加热氧化铁前需通一会CO,其目的是________。
实验过程中,常在装置图末端的导管口放一盏燃着的酒精灯(灯焰处于导管口),这样做的目的是____________________。
(3)通过B装置可检验A中的生成物含有CO2,该反应的化学方程式为____________________。
(4)待A中玻璃管内物质冷却至室温,取玻璃管中物质适量,加入足量的稀盐酸,可观察到的现象为____________________。
【解析】
(1)一氧化碳还原氧化铁,生成铁和二氧化碳。
(2)一氧化碳中混合一定量的空气时,加热可能发生爆炸,所以实验前要先通一段时间的CO,以排出装置中的空气,防止发生爆炸;一氧化碳是空气污染物,实验过程中可能有剩余的CO没有反应完,实验结束后也要继续通一段时间的CO,至玻璃管冷却至室温,为防止CO污染空气,导管口安放一盏点燃的酒精灯。
(3)二氧化碳与氢氧化钙反应生成碳酸钙和水。
(4)铁能与稀盐酸反应生成氯化亚铁和氢气,有气泡产生。
例3 (2019·湘潭中考)钢铁厂会利用焦炭产生的还原性气体来炼铁,某同学用此原理按如图装置进行实验。
下列说法正确的是( )
A.该实验不需要增加尾气处理装置
B.该实验应先通入一段时间的CO验纯后再加热
C.NaOH溶液可以检验气体产物
D.反应结束后,含有未反应的Fe2O3固体,可以采用加入盐酸的方法来提纯铁
【解析】一氧化碳有毒,反应后排放到空气中,会污染空气,且CO不溶于水,不与NaOH溶液反应,需要进行处理;实验时应先通入一段时间的CO,排出装置内的空气,以防止加热时发生爆炸;NaOH可与二氧化碳反应,吸收二氧化碳,反应没有明显现象,不能用来检验二氧化碳;铁也能与稀盐酸反应,反应后若加入盐酸,则产物铁会被消耗,达不到提纯的目的。
3.(2019·河南中考)如图为一氧化碳还原氧化铁实验。
下列说法中正确的是( D )
A.开始时应先预热玻璃管,后通入一氧化碳
B.实验中玻璃管里粉末由黑色逐渐变成红棕色
C.参加反应的氧化铁和一氧化碳质量比为40∶7
D.将尾气点燃或收集,可防止一氧化碳污染空气
4.实验室根据工业炼铁的原理设计了如图所示装置进行实验。
请回答:
(1)主要成分为氧化铁的矿石名称为__赤铁矿__。
图中还原氧化铁的化学方程式为:
__3CO+Fe2O3
2Fe+3CO2__。
(2)“加热”和“通气”(通入CO)的操作顺序是__先通气再加热__。
5.多数金属以矿物形式存在于自然界,金属矿物可用来冶炼金属。
冶炼方法
反应表示式(其他产物略去)
代表性金属
热还原法
金属A的氧化物+碳(或一氧化碳等)
金属A
锌、铜
电解法
金属B的化合物
金属B
钾、铝
热分解法
金属C的氧化物
金属C
汞、银
(1)工业上常用赤铁矿(主要成分是Fe2O3)与CO在高温下炼铁,反应的化学方程式是__Fe2O3+3CO
2Fe+3CO2__。
(2)用氧化铝冶炼金属铝的化学方程式是__2Al2O3
4Al+3O2↑__。
(3)若从铅的矿物中冶炼铅,可使用上述方法中的__热还原法__,理由是__铅在金属活动顺序中位于锌和铜之间__。
6.如图为铁制品循环利用的示意图,根据图示回答:
(1)在“①”“②”“③”过程中,一定发生化学变化的是__①__(填序号)。
(2)废旧金属“循环利用”的意义是__节约金属资源、节约冶炼金属消耗的能源、可以减少对环境的污染__(写一点即可)。
方法技巧
(1)金属资源很广泛,存在形式有两样:
①很不活泼的金属如金、银,能以单质形式存在;②比较活泼的金属,以化合物形式存在。
(2)工业高炉炼生铁,杂质较多易断裂;高温冶炼铁矿石,一氧化碳还原剂;一氧化碳是毒气,应将尾气来处理。
金属的锈蚀和防护
例4 (2019·常州中考)按如图装置进行实验,一周后发现铁钉锈蚀最严重的位置是( )
A.a处B.b处
C.c处D.三处同样严重
【解析】铁与氧气和水充分接触时容易生锈,水和氧气同时存在是铁生锈的必须条件;缺少水或缺少氧气,或者缺少氧气和水,铁不容易生锈。
从图中可以看出b处铁钉最容易与氧气、水同时接触,故一周后发现铁钉锈蚀最严重的位置为b处。
例5 (2019·南宁中考)下列措施中,不能防止金属制品锈蚀的是( )
A.在表面刷漆B.在表面涂油
C.在表面镀铬D.用湿布擦拭
【解析】金属与水、氧气等充分接触时容易生锈,使金属制品与氧气和水隔绝可以防止生锈,在表面刷漆,能隔绝氧气和水,能防止金属制品锈蚀;在表面涂油,能隔绝氧气和水,能防止金属制品锈蚀;在表面镀铬,能隔绝氧气和水,能防止金属制品锈蚀;用湿布擦拭,金属制品能与氧气、水分充分接触,不能防止金属制品锈蚀。
7.分析下图所示的铁钉生锈实验的设计,得出的结论不正确的是( B )
A.对比①②可以说明铁生锈一定要有氧气参加
B.对比②③可以说明铁生锈一定要有水参加
C.对比①③可以说明铁生锈一定要有水参加
D.对比①②③可以说明铁生锈必须要有水和氧气同时参加
8.(2019·苏州中考)下列说法正确的是( B )
A.铁是地壳中含量最多的金属元素
B.铁制品在潮湿的空气中容易生锈
C.多数合金的熔点高于它的成分金属
D.铝制品在空气中耐腐蚀是因为铝不活泼
9.钢铁是人类广泛使用的金属材料,每年因锈蚀而损失的钢铁占世界年产量的四分之一。
请完成下列填空:
(1)车轮的钢圈在潮湿的空气中会锈蚀,这是因为铁与空气中的氧气和__水__等物质发生了化学反应。
铁锈的主要成分是氧化铁,其铁元素与氧元素的质量比是__7∶3__(填最简比),铁元素的质量分数为__70%__。
(2)新型食品保鲜剂“纳米α铁粉”被称为“双吸剂”,其实质就是利用了铁生锈的原理:
用化学方法检验使用一段时间的“纳米α铁粉”是否完全失效,可选用__稀盐酸__检验,若出现__有气泡冒出__现象,说明该双吸剂仍可使用。
(3)用磁铁矿冶炼铁的原理可用4CO+Fe3O4
3Fe+4CO2表示,检验产物CO2常用的试剂是__澄清的石灰水__,化学反应方程式为__Ca(OH)2+CO2===CaCO3↓+H2O__。
方法技巧
(1)金属资源的保护途径有:
回收废旧金属;防止金属锈蚀;合理开采金属矿物;寻找金属替代品。
(2)防止铁生锈实质是破坏铁生锈的条件,防止铁锈蚀的方法有:
涂油、刷漆、镀金属保护层。
防止菜刀生锈的方法是洗净、擦干。
必做教材基础实验6 铁钉锈蚀条件的探究
1.铁制品锈蚀条件的探究
编号
Ⅰ
Ⅱ
Ⅲ
条件
铁钉与空气和水接触
铁钉全部在水中
铁钉在干燥的空气中
装置
现象
生锈
不生锈
不生锈
分析
能得出铁生锈需要氧气的组合是__Ⅰ、Ⅱ__,需要水的组合是__Ⅰ、Ⅲ__,编号Ⅱ中将蒸馏水煮沸的目的是除去水中溶解的__氧气__,加入植物油的目的是__隔绝空气__
结论
铁制品锈蚀的条件:
铁与__氧气__和__水__同时接触
2.其他实验装置:
(1)借助U型管探究铁制品锈蚀的条件
①钢丝棉1、2、3、4中发生锈蚀的是__1、2__,其中锈蚀程度最严重的是__1__。
②由该实验现象得到的结论有:
__铁制品的锈蚀需要与氧气和水同时接触;盐溶液能加快铁的锈蚀__。
(2)用下图装置探究铁制品锈蚀的条件
①打开K1、K2通入氧气一段时间,然后关闭K1、K2,2天后观察到A处铁丝表面布满铁锈,C处铁丝依然光亮,D中铁丝表面有部分铁锈。
②B装置中浓硫酸的作用是__除去氧气中的水分__;A、C处实验现象对比说明铁生锈的条件之一是__需要与水接触__;A、D处实验现象对比说明__氧气的浓度__会影响铁生锈的快慢。
(3)用下图装置探究铁制品锈蚀的条件
向a、b两支试管中加入形状和大小完全相同的铁片,再向a中加入植物油,均塞上橡皮塞,U型玻璃管内为红墨水(开始时两端液面水平),放置一段时间后,可得到的结论是__铁生锈需要与空气(或氧气)接触__。
3.实验拓展:
铜的锈蚀与哪些因素有关
铜锈的主要成分是铜绿[Cu2(OH)2CO3],铜生锈的条件除氧气和水外,还必须有二氧化碳。
为证明“必须有二氧化碳”,需进行如图所示实验中的__甲和丁__。
例6 如图为某实验小组同学设计的探究铁生锈条件的实验。
A B C
(1)一段时间后,可观察到铁钉明显发生锈蚀的是________(填试管编号)。
(2)对比A、B两支试管中出现的现象,得出影响铁锈蚀的因素是________。
(3)B试管中植物油的作用是________。
(4)通过这个实验我们得出的实验结论是________。
(5)实验中选用煮沸过的蒸馏水的目的是________。
(6)C试管中也可以放入一团包有CaO固体的棉花,作用是________。
(7)从上述实验中我们可以得出防止铁锈蚀的措施为________。
【解析】
(1)铁生锈是铁与空气和水同时接触,共同作用的结果,所以只有A装置中的铁钉既与水接触,又与氧气接触而生锈。
(2)(3)B试管中水上有一层植物油,隔绝了空气进入水中,使铁钉不会生锈,与A对比,可说明铁生锈需要与空气接触。
(4)A、B、C三处的现象一起对比可知,铁生锈需要与空气和水同时接触才会生锈。
(5)氧气的溶解度随温度的升高而减小,沸腾后的蒸馏水中基本不含氧气。
(6)CaO能与水反应生成氢氧化钙,可用除去空气中的水分。
(7)只要保持铁表面干燥,即可防止铁生锈。
防止铁生锈的方法有涂油、刷漆、镀金属保护层,原理都是隔绝水和空气。
10.(2019·广东中考)探究铁生锈的条件,有利于寻找防止铁制品锈蚀的方法。
下列对比实验设计与所探究的条件(蒸馏水经煮沸并迅速冷却),对应关系正确的是( D )
A.甲和乙:
水B.乙和丙:
空气
C.甲和丙:
空气D.甲和丁:
水
11.小金为探究铁制品锈蚀的条件,进行如下实验:
步骤1:
利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好,药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mLO2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:
一段时间后,观察U形管内的铁丝,其现象如表所示。
观察对象
现象
①干燥的普通铁丝
没有明显变化
②潮湿的普通铁丝
较多红褐色锈斑
③潮湿的纯铁丝
没有明显变化
(1)步骤1中,检查U形管内是否已充满O2的方法是__将带火星的木条放置在b导管口,若木条复燃,则证明U形管内已充满O2__。
(2)铁制品锈蚀的条件之一是需要O2,在此实验中能支持此条件的证据是__观察到注射器活塞向左移动(或注射器内O2体积减小)__。
(3)通过对比实验现象,此实验还可得出铁制品锈蚀的条件是__水分和金属的内部结构__。
课堂作业评价
1.(2019·南昌模拟)铜能被加工成厚度仅为7微米的超薄铜箔,说明铜具有良好的( D )
A.抗腐蚀性B.导电性
C.导热性D.延展性
2.(2019·江西模拟)下列餐厅中的用品所用的材料属于金属材料的是( B )
A.木质餐桌B.不锈钢餐具
C.陶瓷茶杯D.涤纶围裙
3.为保证航母的使用寿命,下列防锈措施不可行的是( C )
A.用抗锈蚀性能优异的合金制造航母零部件
B.刷防锈漆
C.船体表面镀一层黄金
D.给某些部位涂油
4.(2019·内江中考)下列有关金属资源的利用与防护不合理的是( A )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用,是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
5.(2019·泰安中考)如图是某化学兴趣小组设计的观察铁制品锈蚀的实验装置。
下列相关叙述正确的是( B )
①一段时间后,铁丝会由下向上出现锈蚀现象
②一段时间后,水面处铁丝锈蚀严重
③一段时间后,塑料瓶会变膨胀,因为铁生锈要放热
④一段时间后,塑料瓶要变瘪,因为铁生锈与空气有关
A.①②B.②④
C.②③D.③④
6.(2019·眉山中考)某化学兴趣小组用以下装置探究炼铁原理。
关于该装置和反应过程描述错误的是( C )
A B C D
A.盛放药品前应先检查装置气密性
B.加热前要先通CO,加热后B中出现浑浊
C.已知方框中连接的是C和D,导管口的连接顺序为a→b→c→d
D.这种方法“炼”出的铁与工业上炼出的生铁在组成上最大的区别是不含碳
7.炼铁的主要原料是赤铁矿(主要成分是Fe2O3)、焦炭、空气等,转化过程如下:
(1)②中,反应为CO2+C
2CO,其中化合价发生改变的元素是__C(或碳元素)__。
(2)③中,CO与Fe2O3反应的化学方程式为__3CO+Fe2O3
2Fe+3CO2__,体现了CO的__还原__性。
(3)相比于黄铁矿(主要成分FeS2),工业上选用赤铁矿(主要成分Fe2O3)为原料炼铁的优点是__不产生污染环境的SO2__。
8.下图装置可以做CO还原Fe2O3的实验并检验该反应的气体生成物。
已知由一氧化碳发生装置得到的CO中混有杂质CO2和H2O。
A B C
(1)写出B装置玻璃管内反应的化学方程式:
__3CO+Fe2O3
2Fe+3CO2__。
(2)从环保角度考虑,请写出一种尾气处理方法__在装置C的短导管处放一盏燃着的酒精灯__。
(3)若没有A装置,则该实验不能达到检验气体生成物的目的,请说明原因:
__无法证明使澄清石灰水变浑浊的气体是否来自于反应后新生成的__。
(4)有同学提出在一氧化碳还原氧化铁实验后的黑色粉末中还可能含有Fe3O4(Fe3O4不与CuSO4溶液反应),为验证黑色粉末成分,可取少量黑色固体于试管中,向其中加入过量的硫酸铜溶液。
证明黑色固体是Fe粉的现象是__黑色固体全部变为红色固体__;证明黑色固体成分是Fe粉和Fe3O4的现象是__黑色固体部分变为红色固体__。
9.(2019·福建中考)改革开放以来,我国钢铁工业飞速发展,近年来钢铁产量己稳居世界首位。
某钢铁厂采用赤铁矿(主要成分为Fe2O3)炼铁,反应原理为3CO+Fe2O3
2Fe+3CO2,若该厂日产含铁1.4×104t的生铁,至少需要含Fe2O380%的赤铁矿的质量是多少?
(要求写出计算过程)
解:
需要赤铁矿的质量为x。
Fe2O3+3CO
2Fe+3CO3
160112
80%·x1.4×104t
=
x=2.5×104t
答:
需要含Fe2O380%赤铁矿的质量为2.5×104t。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 江西省 化学中考特训方案 考点精讲精炼 11 化学 中考 方案 考点 精炼
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
