 试验室常用溶液及试剂配制试验室常用溶液试剂的配制表一普通酸Word格式文档下载.docx
试验室常用溶液及试剂配制试验室常用溶液试剂的配制表一普通酸Word格式文档下载.docx
- 文档编号:14214650
- 上传时间:2022-10-20
- 格式:DOCX
- 页数:23
- 大小:29.28KB
试验室常用溶液及试剂配制试验室常用溶液试剂的配制表一普通酸Word格式文档下载.docx
《试验室常用溶液及试剂配制试验室常用溶液试剂的配制表一普通酸Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《试验室常用溶液及试剂配制试验室常用溶液试剂的配制表一普通酸Word格式文档下载.docx(23页珍藏版)》请在冰豆网上搜索。
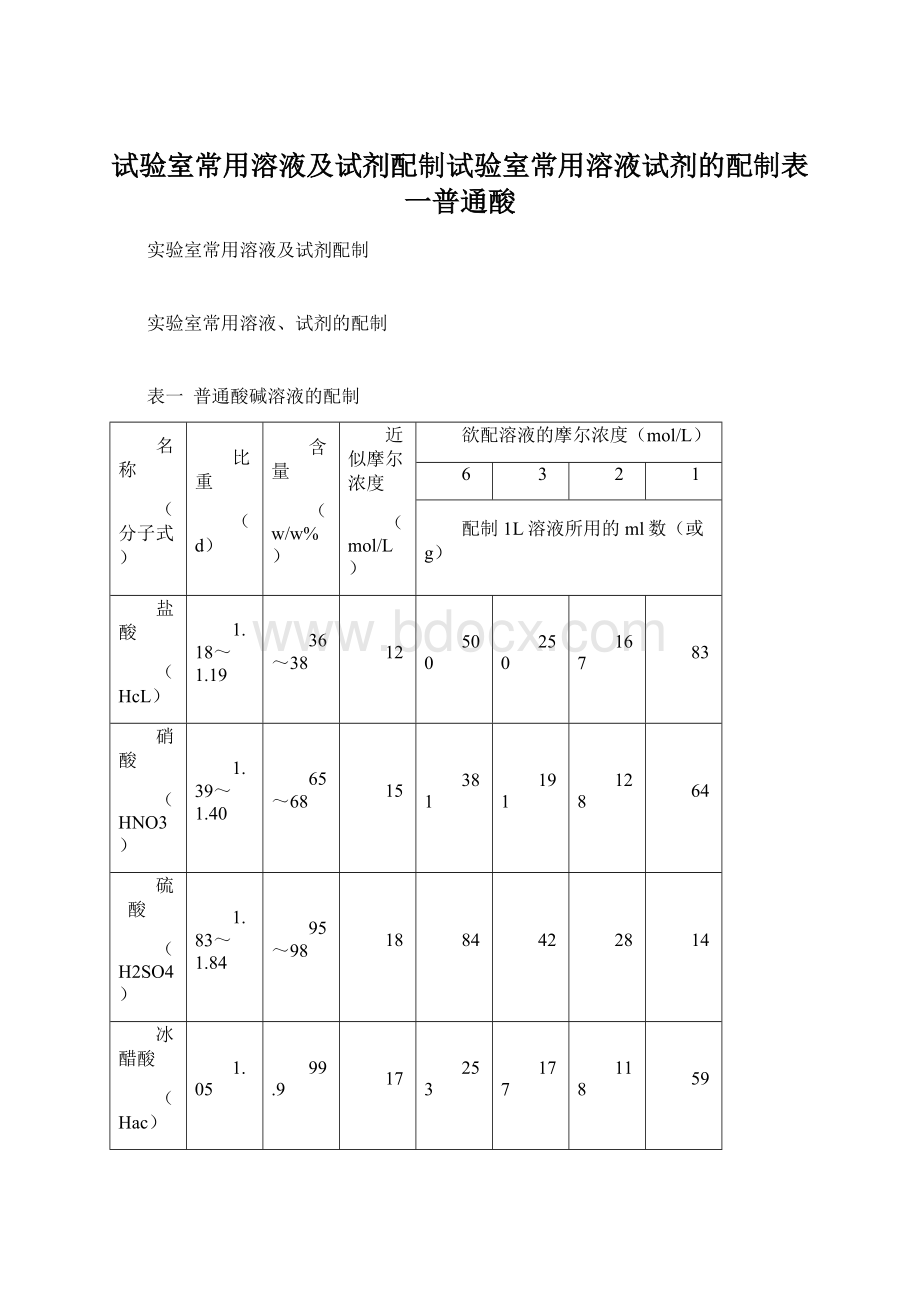
1.83~1.84
95~98
18
84
42
28
14
冰醋酸
(Hac)
1.05
99.9
17
253
177
118
59
磷
(H3PO4)
1.69
85
39
19
氨水(NH3·
H2O)
0.90~0.91
400
200
134
77
氢氧化钠(NaOH)
(240)
(120)
(80)
(40)
氢氧化钾(KOH)
(339)
(170)
(113)
(56.5)
表二
常用酸碱指示剂
指示剂
PKHIn
变色范围pH
酸色
碱色
配制方法
百里酚蓝
(麝香草酚蓝)
1.65
12.~2.8
红
黄
0.1%的20%乙醇溶液
甲基橙
3.4
3.1~4.4
橙黄
0.05%水溶液
溴甲酚绿
4.9
3.8~5.4
蓝
0.1%的20%乙醇溶液或0.1g指示剂溶于2.9ml0.05mol/LNaOH加水稀释至100ml
甲基红
5.0
4.4~6.2
0.1%的60%乙醇溶液
溴百里酚蓝
7.3
6.2~7.3
中性红
7.4
6.8~8.0
黄橙
(第二变色范围)
9.2
8.0~9.6
酚酞
9.4
8.0~10.0
无色
0.5%的90%乙醇溶液
百里酚酞
10.0
9.4~10.6
0.1%的90%乙醇溶液
表三
混合酸碱指示剂
指示剂组成(体积比)
变色点pH
备注
一份0.1%甲基橙水溶液
一份0.25%靛蓝二磺酸钠水溶液
4.1
紫
绿
灯光下可滴定
一份0.02%甲基橙水溶液
一份0.1溴甲酚绿钠盐水溶液
4.3
橙
蓝绿
PH3.5黄色
PH4.05绿黄
PH4.3浅绿
三份0.1%溴甲酚绿20%乙醇溶液
一份0.2%甲基红60%乙醇溶液
5.1
酒红
颜色变化极鲜明
一份0.2%甲基红乙醇溶液
一份0.1%次甲基蓝乙醇溶液
5.4
红紫
PH5.2红紫
PH5.4暗蓝
PH5.6绿色
一份0.1%溴甲酚绿钠盐水溶液
一份0.1%绿酚红钠盐水溶液
6.1
黄绿
蓝紫
PH5.6蓝绿
PH5.8蓝色
PH6.0浅紫
PH6.2蓝紫
一份0.1%溴甲酚紫钠盐水溶液
一份0.1溴百里酚蓝钠盐水溶液
6.7
紫蓝
PH6.2黄紫
PH6.6紫
PH6.8蓝紫
一份0.1中性红乙醇溶液
一份0.1次甲基蓝乙醇溶液
7.0
PH7.0为蓝绿
必须保存在棕色瓶中
一份0.1甲酚红钠盐水溶液
三份0.1%百里酚蓝钠盐水溶液
8.3
PH8.2玫瑰色
PH8.4紫色
一份0.1%百里酚蓝50%乙醇溶液
三份0.1酚酞50%乙醇溶液
9.0
PH9.0绿色
表四
容量分析基准物质的干燥
基准物质
干燥温度和时间
碳酸钠(NaCO3)
500~650℃,40-50min
氯化物(NaCl)
500-650℃,干燥40-50min
草酸钠(H2C2O4)
150-200℃,1-1.5h
硝酸银(AgNO3)
室温,硫酸干燥器中至恒温
草酸(H2C2·
2H2O)
室温,空气干燥2-4h
碳酸钙(CaCO3)
120℃,干燥至恒重
硼砂(Na2B2O·
10H2O)
室温,在NaCl和蔗糖饱和液的干燥器中,4h
氧化锌(ZnO)
800℃灼烧至恒重
邻苯二甲酸氢钾(KHC6H4O4)
100-120℃,干燥至恒重
锌(Zn)
室温,干燥器24h以上
重铬酸钾(K2Cr2O7)
100-110℃,干燥3-4h
氧化镁(MgO)
表五
缓冲溶液的配制
1、
氯化钾-盐酸缓冲溶液
0.2mol/LKCl(ml)
50
0.2mol/LHCl(ml)
97.0
64.3
41.5
26.3
16.6
10.6
水(ml)
53.0
85.5
108.5
123.7
133.4
139.4
143.3
PH(20℃)
1.0
1.2
1.4
1.6
1.8
2.0
2.2
2、
邻苯二甲酸氢钾-氢氧化钾缓冲溶液
0.2mol/LKHC6H4O4(ml)
46.70
32.95
20.32
9.90
2.63
103.30
117.05
129.68
140.10
147.37
2.6
3.0
3.8
3、
0.40
7.50
17.70
29.95
39.85
149.60
142.50
132.20
120.05
110.15
4.0
4.4
4.8
5.2
5.6
4、
乙酸-乙酸钠缓冲溶液
0.2mol/LHAc(ml)
185
164
126
80
0.2mol/LNaAc(ml)
36
74
120
158
181
3.6
5、
磷酸二氢钾-氢氧化钠缓冲溶液
0.2mol/LKH2PO4(ml)
0.2mol/LNaOH(ml)
3.72
8.60
17.80
29.63
39.50
45.20
146.26
141.20
120.37
110.50
104.80
5.8
6.2
6.6
7.8
6、
硼砂-氢氧化钠缓冲溶液
0.2mol/L硼砂(ml)
90
70
60
40
10
20
30
9.35
9.48
9.66
9.94
11.04
12.32
7、
氨水-氯化铵缓冲溶液
0.2mol/LNH3·
H2O(ml)
8
32
0.2mol/LNH4Cl(ml)
8.0
8.58
9.1
9.8
10.4
11.0
8、
常用缓冲溶液的配制
PH
配制方法
NaAc·
3H2O8g,溶于适量水中,加6mol/LHAc134ml,稀释至500ml
3H2O20g
溶于适量水中,加6mol/LHAc134ml,稀释至500ml
4.5
3H2O32g
溶于适量水中,加6mol/LHAc
68ml,稀释至500ml
3H2O50g
34ml,稀释至500ml
NH4Cl
50g
溶于适量水中,加15mol/LNH3·
H2O
3.5ml,稀释至500ml
8.5
40g
8.8ml,稀释至500ml
35g
24ml,稀释至500ml
9.5
30g
65ml,稀释至500ml
27g
197ml,稀释至500ml
实验室常用试验方法2
九、柠檬酸(C6H8O7·
称取试样1.5g(精确到0.0002g)于三角瓶内,加入水50ml溶解,加酚酞指示剂3滴,用1mol/L氢氧化钠标准溶液滴定至粉红色为终点,同时做空白试验。
计算:
X%(一水)=(V1-V0)×
C×
0.06404
m×
(1-0.08566)×
100
X%(无水)=(V1-V0)×
V1-----消耗氢氧化钠标准溶液的体积,ml;
V0-----空白所消耗氢氧化钠标准溶液的体积,ml;
C------氢氧化钠标准溶液浓度,mol/L;
m---样品质量。
十、钙含量测定(磷酸氢钙CaHPO4、磷酸二氢钙Ca(H2PO4)2·
H2O、钙粉等)
称取2g(精确到0.0002g)样品,用10ml盐酸(1+1)溶解,转移至100ml容量瓶中定溶,用移液管吸取10ml于250ml锥形瓶中,加50ml水,5ml蔗糖溶液(25g/L),2ml三乙酸胺(1+1),1ml乙二胺(1+1),1滴孔雀绿指示液(1g/L),滴加氢氧化钾溶液(200g/L)至无色,再过量10ml,加0.1g盐酸羟胺(每加一种试剂都要摇匀),加钙黄绿素少许,在黑色背景下用0.05mol/L的EDTA标准溶液滴定至绿色荧光消失呈现紫红色为滴定终点。
Ca%=
C×
V×
0.4008
m×
C------EDTA标准溶液的浓度,mol/L;
V-----消耗EDTA标准溶液的体积,ml;
m----样品质量。
(二)氟(Fˉ)含量的测定:
1、标准曲线的绘制;
2、试样含量的测定:
称取0.5g(精确到0.0002g)置于50ml纳氏比色管中,加1mol/L盐酸10ml,密闭提取1h(不时摇动),避免粘于管壁,提取后加总离子强度缓冲液25ml,加水至刻度,以滤纸过滤。
以氟电极测平衡电位值。
结果计算:
X=C×
50×
1000
1000=50C
m
X-----试样中氟含量,
m---试样质量,g;
C-----据电位值查得的浓度,
总
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 试验室 常用 溶液 试剂 配制 普通
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
