 高考化学压轴题推断题强化训练Word文件下载.docx
高考化学压轴题推断题强化训练Word文件下载.docx
- 文档编号:15706989
- 上传时间:2022-11-15
- 格式:DOCX
- 页数:17
- 大小:557.72KB
高考化学压轴题推断题强化训练Word文件下载.docx
《高考化学压轴题推断题强化训练Word文件下载.docx》由会员分享,可在线阅读,更多相关《高考化学压轴题推断题强化训练Word文件下载.docx(17页珍藏版)》请在冰豆网上搜索。
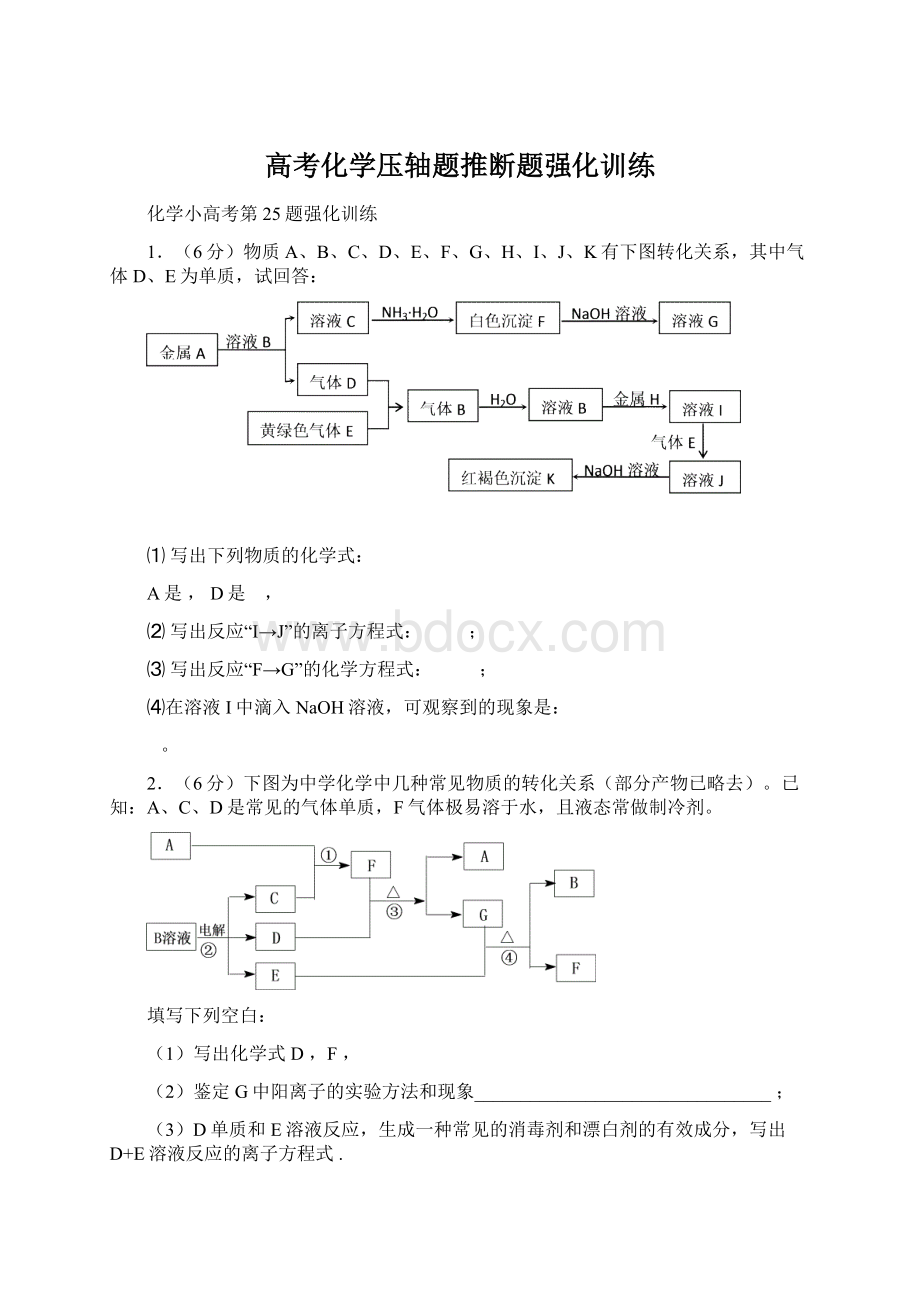
3.(6分)下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
(1)写出化学式:
A,B。
(2)写出反应⑤的离子方程式:
(3)写出反应⑥的化学反应方程式:
4.(6分)如图所示:
已知A和E为金属单质,B是化合物且常温下为液态,F为两性化合物。
按要求回答下列问题:
⑴E在元素周期表中位于第周期;
第族。
⑵写出A和B反应的化学方程式:
⑶写出E与烧碱溶液反应的离子方程式为:
⑷C和D反应的化学反应方程式为。
5.(6分)下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。
气体B与气体C相遇产生大量的白烟,D是海水中浓度最高的盐(部分反应物和生成物及溶剂水已略去)。
请回答下列问题:
⑴甲的化学式是,C的电子式为;
⑵写出A溶液和丁反应生成D的离子方程式:
;
⑶写出A和E反应的化学方程式:
6.(6分)下列物质A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;
E在常温下是黄绿色气体;
在适当的条件下,它们之间可以发生如下图所示的转化。
⑴A的化学式是;
⑵反应F→D的化学方程式是。
⑶检验F中金属阳离子的常用方法是。
⑷工业上冶炼金属A的化学方程式是。
7.(6分)A、B、C等八种物质有如下框图所示转化关系。
又知,A是由地壳中含量最多的金属元素形成的单质,C、D、E是常见的由短周期元素形成的气体单质,气体F与气体G相遇产生大量的白烟,H是厨房中必备一种调味盐(部分反应物和生成物及溶剂水已略去)。
⑴B的化学式是,F的化学式是,H的电子式为;
⑵写出A和B溶液反应的离子方程式:
⑶写出D和E反应的化学方程式:
⑷如何检验I中的阳离子。
8.(6分)由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转换关系,工业上电解熔融的甲可制取金属A。
请回答:
(1)写出下列物质的化学式:
A、甲。
(2)写出乙物质的溶液中通入过量CO2的现象:
(3)写出丁与过量氨水反应的离子方程式:
9.(6分)下图所示各物质是由短周期部分元素组成的单质或其化合物,图中部分反应条件及物质未列出。
A、C、D、F均为单质,C、E、F、G常温下是气体,J为白色沉淀,既能溶于B,又能溶于E;
物质B、G可以使湿润的红色石蕊试纸变蓝,且B的焰色反应呈黄色。
反应④是化肥工业的重要反应。
⑴A的元素在元素周期表中的位置是,物质B的电子式为。
⑵上述反应①~⑥中,属于化合反应的是,反应⑤的离子方程式为。
⑶在I的水溶液滴加B溶液至过量的过程中,所观察到的现象为:
10.(6分)下图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如下转化关系。
(反应中生成的水已略去)请回答以下问题:
(1)E是,F是(填化学式)。
(2)C物质在日常生活中可作剂。
(3)写出反应①的化学方程式:
参考答案
1.
(1)Al、H2
(2)2Fe2++Cl2===2Cl-+2Fe3+(3)生成白色沉淀,沉淀立即变成灰绿色,最后变成红褐色
2.
(1)Cl2、NH3、
(2)取少量D的溶液加人试管中,用胶头滴管加入少量NaOH浓溶液,加热用湿润的红色石蕊试纸在试管口检验放出的气体,试纸变蓝色
(3)2OH-+Cl2=ClO-+Cl-+H2O
(4)
3.
(1)Na NaHCO3
(2)2Na+2H2O=2Na++2OH-+H2↑
(3)2Na2O2+2CO2=2Na2CO3+O2
4.⑴三、ⅢA
⑵3Fe+4H2O(g)===Fe3O4+4H2
⑶2Al+2OH—+2H2O=2AlO2—+3H2↑
⑷4H2+Fe3O4
3Fe+4H2O
5.
(1)Fe
(2)2OH-+Cl2===Cl-+ClO-+H2O
(3)NH4Cl+NaOH==NH3+NaCl+H2O
6.
⑴Al
⑵2FeCl3+Fe=3FeCl3
⑶加入KSCN溶液,显血红色则含Fe3+
⑷Fe2O3+3CO
2Fe+3CO2
7.⑴NaOHNH3
⑵2Al+2H2O+2OH_=2AlO2_+3H2↑
⑶H2+Cl2=(点燃)2HCl⑷取样,加入碱,加热,在试管口以湿润红色石蕊试纸检验,变蓝色,说明存在铵根离子
8.
(1)Al、Al2O3
(2)产生白色胶状沉淀(3)Al3++3NH3·
H2O=Al(OH)3↓+3NH4+
9.⑴第三周期、ⅠA族
⑵④Al3++3NH3·
⑶有白色沉淀产生,后渐渐溶解至消失
10.
(1)CaCO3、HCl
(2)消毒(或漂白)(3)2C12+2Ca(OH)2=CaCl2+Ca(C1O)2+2H2O
化学小高考第26题强化训练
1、“阳光”牌小包装“脱氧剂”成份为Fe粉、活性炭及少量NaCl、水。
某校化学兴趣小组欲探究该“脱氧剂”中Fe粉和活性炭质量之比,设计并进行了如下探究过程,请你参与实验并回答有关问题。
步骤⑴取某食品包装袋中的“阳光”牌“脱氧剂”一袋,将里面的固体倒在滤纸上,仔细观察,固体为灰黑色粉末,夹杂着一些红棕色粉末。
由此得出的结论为上述“脱氧剂”中的铁已部分被;
步骤⑵将步骤⑴中的固体溶于水,过滤,将滤渣洗涤、干燥,以除去“脱氧剂”中NaCl和水;
步骤⑶取步骤⑵中的滤渣,将其分为两等份,每一份质量为8.0g。
将其中一份在氧气流中充分灼烧,生成的气体全部通入足量得澄清石灰水,得到干燥、纯净的沉淀20.0
g。
8.0
g滤渣中活性炭的质量为g;
步骤⑷将步骤⑶中的另一份滤渣放入烧杯中,加入一定体积2.0mol/L的稀H2SO4,微热至反应完全。
为保证滤渣充分溶解,加入的稀H2SO4的体积应大于或等于mL;
步骤⑸向步骤⑷中的混合物中加入过量的氢氧化钠溶液,得到的固体经洗涤后转移到坩埚中充分加热,冷却、称量,得到6.86g固体。
结论:
该“脱氧剂”中的Fe粉和活性炭质量之比为。
2、二氧化硫(SO2)是形成酸雨的因素之一,它的含量是空气质量监测的一个重要指标。
某兴趣小组同学刚取到热电厂(燃煤电厂)附近的雨水进行实验。
①测得该雨水样品的pH为4.73;
②向雨水样品中滴加BaCl2溶液,有白色沉淀生成;
③每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
测定时间/h
1
2
3
4
雨水样品的pH
4.73
4.62
4.56
4.55
根据以上信息,回答下列问题:
⑴分析上述数据变化,你认为形成这一变化的原因是_________________________(用化学方程式表示)
⑵常温下,取该雨水与一定量的蒸馏水相混合,则pH将____________(填“变大”、“变小”或“不变”)
⑶兴趣小组同学取3小时后这种雨水VL,加入1.00mol/L的Ba(OH)2溶液至不再产生沉淀时,恰好消耗20.0mLBa(OH)2溶液。
请你计算:
①生成沉淀物的质量是多少?
②该VL雨水中溶解SO2的体积(标准状况)。
3、已知某燃料含碳、氢、氧三种元素,为了测定该燃料的组成:
将该燃料放入足量氧气中燃烧,并使产生的CO2和H2O蒸气及剩余的O2全部通过如图所示的装置,得到如下表所列的实验数据(假设生成的气体全部被吸收)。
实验前
实验后
甲的质量/g
101.1
103.8
乙的质量/g
82.0
86.4
根据实验数据填空:
(1)该燃料完全燃烧生成水的质量为 g,生成CO2的质量为 g。
(2)该燃料分子中碳、氢原子的数目比为 。
(3)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为
,结构简式为 。
4、铝镁合金现已成为轮船制造、化工生产等行业的重要原料。
现有一块铝镁合金,欲测定其中镁的质量分数,几位同学分别称取3.9克样品,并设计了不同的实验方案:
甲:
铝镁合金测得生成气体的体积Vml(已折算成标准状况);
乙:
铝镁合金测得剩余固体的质量a克;
过量NaOH
溶液
丙:
铝镁合金溶液测得沉淀的质量b克。
⑴写出实验设计甲有关反应的离子方程式:
该方案能否测定出镁的质量分数?
(填“能”或“不能”)
⑵实验设计乙所加入的试剂是 ,测得的镁的质量分数为
⑶实验设计丙测得沉淀的质量为2.9克,加过量的NaOH溶液充分反应后,_________________(填一种分离方法),洗涤烘干沉淀,测得镁的质量分数为(保留小数点后一位小数) ,如果未洗涤沉淀,测得镁的质量分数将 (填“偏大”、“偏小”或“无影响”)。
5、某化学研究性学习小组用CO还原Fe2O3,并在实验结束后用磁铁吸出生成的黑色粉末X进行探究。
[探究目的]
分析黑色粉末X的组成,并进行相关实验。
[查阅资料]
①CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引。
②Fe3O4+8H+=2Fe3++Fe2++4H2O
③Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
8Fe+30HNO3(更稀)=8Fe(NO3)3+3NH4NO3+9H2O
④3Fe3O4+28HNO3(稀)=9Fe(NO3)3+NO↑+14H2O
[实验探究]
I.定性检验
编号
实验操作
实验现象
①
取少量黑色粉末X放入试管1中,注入浓盐酸,微热
黑色粉末逐渐溶解,溶液呈黄绿色;
有气泡产生
②
向试管1中滴加几滴KSCN溶液,振荡
溶液出现血红色
③
另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置
有极少量红色物质析出,仍有较多黑色固体未溶解
⑴实验③发生的反应的离子方程式为。
⑵上述实验说明黑色粉末X中含有。
II.定量测定
根据下图所示的实验方案进行实验并记录数据:
⑴操作Z的名称是。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 压轴 推断 强化 训练
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
