 培优 易错 难题铝及其化合物推断题辅导专题训练及详细答案Word文件下载.docx
培优 易错 难题铝及其化合物推断题辅导专题训练及详细答案Word文件下载.docx
- 文档编号:18784953
- 上传时间:2023-01-01
- 格式:DOCX
- 页数:16
- 大小:433.63KB
培优 易错 难题铝及其化合物推断题辅导专题训练及详细答案Word文件下载.docx
《培优 易错 难题铝及其化合物推断题辅导专题训练及详细答案Word文件下载.docx》由会员分享,可在线阅读,更多相关《培优 易错 难题铝及其化合物推断题辅导专题训练及详细答案Word文件下载.docx(16页珍藏版)》请在冰豆网上搜索。
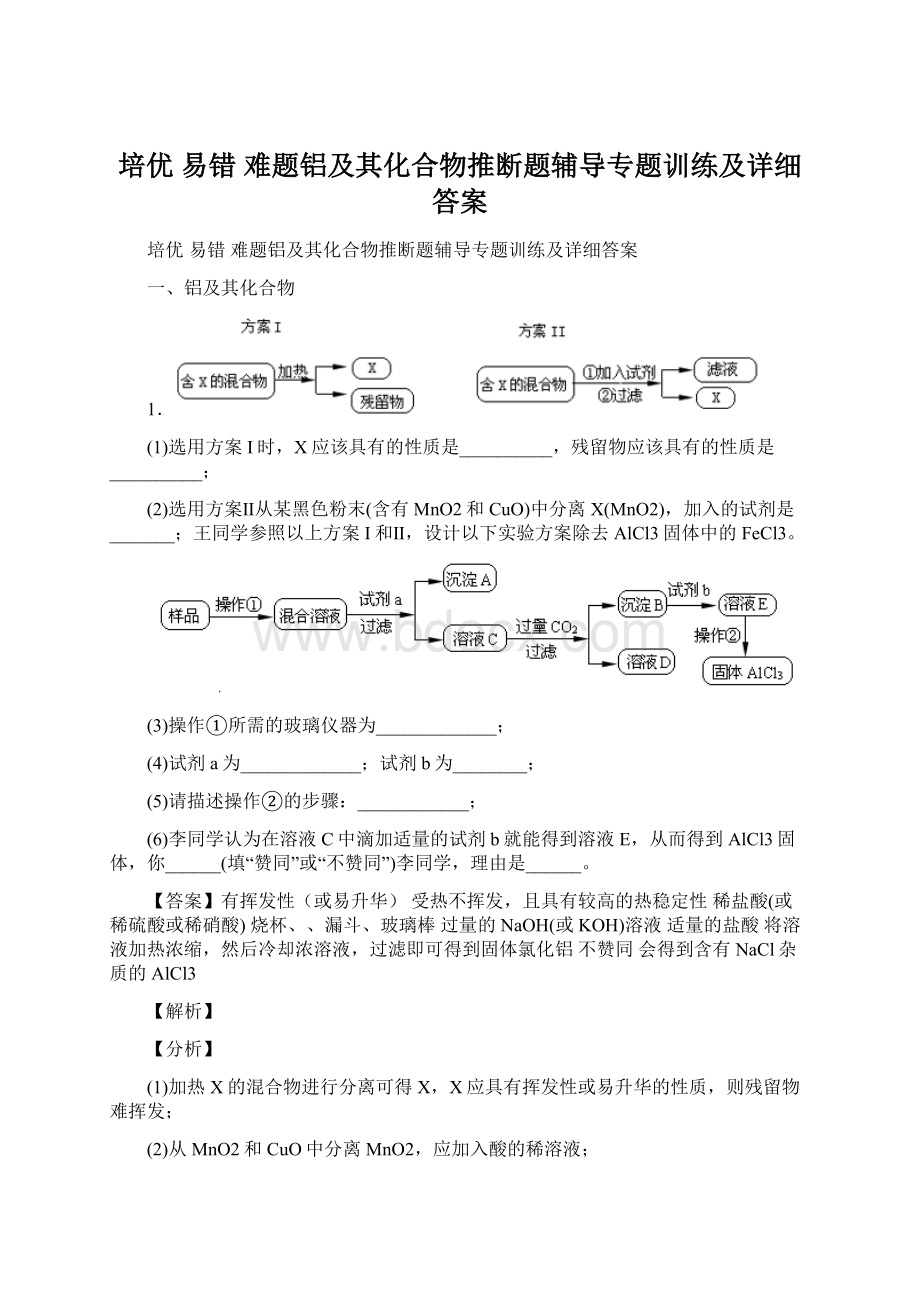
本题考查物质的分离提纯的实验设计,注意把握物质的分离、提纯的基本操作方法,要结合Al(OH)3的两性分析判断,注意把握物质的性质,根据性质设计实验方案。
2.铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。
工业上从铝土矿中提取铝可采用如下工艺流程:
请回答下列问题:
(1)玻璃中含有B,刻蚀玻璃的化学方程式为___。
(2)沉淀C的成分是___,溶液D中存在较多的阴离子是___。
(3)步骤③所加入的试剂是___,生成沉淀F的离子方程式是___。
【答案】
、
和
首先加入过量盐酸,几种物质里只有
不溶于盐酸,即沉淀B,其它元素全部进入溶液A,再加入过量烧碱,
转化为氢氧化物,即沉淀C,而所有铝转变为
进入溶液D,接下来要进行一下逆推,工业上铝是电解氧化铝得到的,因此物质M是氧化铝,氧化铝又是从不溶于水的F转化来的,因此F是
,反应③其实是向
溶液中通入二氧化碳气体,故溶液E为碳酸氢钠(此步骤二氧化碳一般都是过量的),据此来分析本题即可。
(1)蚀刻玻璃是用氢氟酸来溶解玻璃中的
,其反应方程式为
;
(2)沉淀C的成分为
,而溶液D中存在较多的阴离子是
(3)步骤③所加入的试剂是二氧化碳,生成沉淀F的离子方程式为
。
3.(某混合物甲中含有明矾[KAl(SO4)2·
12H2O]、Al2O3和Fe2O3。
在一定条件下由甲可实现如图所示的物质之间的转化:
(1)写出A、B的化学式:
A___,B___。
(2)试剂a最好选用下列试剂中的(______)
A.NaOH溶液B.稀盐酸C.二氧化碳D.氨水
写出相应的离子方程式___。
(3)写出反应②(生成溶液C和沉淀)的离子方程式___。
(4)固体D可以作为复合性的化学肥料,D中所含物质的化学式为___。
【答案】Fe2O3Al2O3DAl3++3NH3·
H2O=Al(OH)3↓+3NH4+AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-K2SO4和(NH4)2SO4
KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物甲加水溶解后,溶液中是KAl(SO4)2,沉淀是Al2O3和Fe2O3;
向沉淀中加NaOH溶液,Fe2O3不反应,Al2O3可与NaOH溶液反应生成NaAlO2,AFe2O3,为向NaAlO2溶液中通入过量CO2可得Al(OH)3沉淀和碳酸氢钠,Al(OH)3受热分解生成B为Al2O3;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4
和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4和(NH4)2SO4,以此来解答。
(1)由上述分析可知,A为Fe2O3,B为Al2O3,
故答案为:
Fe2O3;
Al2O3;
(2)依据流程分析,向溶液中加入的试剂a应沉淀铝离子,应向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,反应方程式为Al3++3NH3·
H2O=Al(OH)3↓+3NH4+,
A.NaOH溶液若加入过量会使氢氧化铝沉淀溶解,故A错误;
B.加稀盐酸不能得到氢氧化铝沉淀,故B错误;
C.通入二氧化碳不能得到氢氧化铝沉淀,故C错误;
D.加入氨水可生成氢氧化铝沉淀,且过量氨水不与氢氧化铝反应,故D正确;
D;
Al3++3NH3·
H2O=Al(OH)3↓+3NH4+;
(3)反应②中二氧化碳过量,反应生成沉淀和碳酸氢钠,向NaAlO2溶液中通入过量CO2可得Al(OH)3沉淀和碳酸氢钠,其离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)向溶液中加入的试剂a应沉淀铝离子,应向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中剩余的是K2SO4和(NH4)2SO4,经过蒸发、结晶,得到的是K2SO4和(NH4)2SO4;
固体D可以作为复合性的化学肥料,D中所含物质的化学式为K2SO4和(NH4)2SO4;
K2SO4和(NH4)2SO4。
4.某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是__。
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
固体B__;
沉淀C__;
沉淀D__;
溶液E___。
(3)写出①、②、③、④四个反应的化学方程式或离子方程式
①__;
②___;
③___;
④__。
【答案】过滤Al2O3Al2O3、Fe2O3Fe2O3K2SO4、(NH4)2SO4Al2O3+2NaOH=2NaAlO2+H2OAl3++3NH3·
H2O=Al(OH)3↓+3NH4+NaAlO2+HCl+H2O=Al(OH)3↓+NaCl2Al(OH)3
Al2O3+3H2O
KAl(SO4)2溶于水,Al2O3和Fe2O3均不溶于水,混合物A加水溶解后,溶液中是KAl(SO4)2,沉淀C为Al2O3和Fe2O3;
由转化关系图可知,向沉淀C中加NaOH溶液,Fe2O3不反应,沉淀D为Fe2O3,Al2O3可与NaOH溶液反应生成NaAlO2,向NaAlO2溶液中通入CO2可得Al(OH)3沉淀,Al(OH)3受热分解生成固体B为Al2O3;
向溶液中加过量氨水,溶液与过量氨水反应,Al3+被沉淀,得到氢氧化铝沉淀,溶液中E为K2SO4、(NH4)2SO4,经过蒸发、结晶,得到K2SO4和(NH4)2SO4,然后结合物质的性质及化学用语来解答。
(1)溶液和沉淀的分离利用过滤;
(2)由上述分析可知B为Al2O3,C为Al2O3、Fe2O3,D为Fe2O3
溶液E为K2SO4、(NH4)2SO4;
(3)反应①为Al2O3+2NaOH=2NaAlO2+H2O;
反应②为Al3++3NH3∙H2O=Al(OH)3↓+3NH4+;
反应③为NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;
反应④为2Al(OH)3
Al2O3+3H2O。
5.某小组同学用一种铝铁合金为原料,模拟相关的工业生产,反应过程如图所示(部分产物和条件已略去),请回答:
(1)铁铝合金是一种高电磁性能合金,下列有关推测可能正确的是_____(填序号).
A.铁铝合金可由铁和铝熔融混合制成
B.铁铝合金的熔点高于铝和铁
C.铁铝合金硬度高于纯铝
(2)反应①中铝元素发生反应的离子方程式为_______________________。
(3)反应②的化学方程式为____________________________________。
(4)反应③发生时观察到的现象是_____________________________,用化学方程式表示颜色变化的原因_____________________________________。
(5)反应④中的CO2不宜换成HCl,原因是_____________________。
(6)请举出固体A一种用途_________________________。
【答案】ACAl3++4OH﹣=AlO2﹣+2H2O2Al+2NaOH+2H2O=2NaAlO2+3H2↑先产生白色沉淀,之后迅速变成灰绿色最后变为红褐色4Fe(OH)2+O2+2H2O=4Fe(OH)3过量的氯化氢会使生成的氢氧化铝溶解做红色油漆和涂料
分析流程可知,①中的反应有硫酸与氢氧化钠酸碱中和,硫酸铝与过量氢氧化钠反应生成偏铝酸钠,硫酸亚铁在空气中与氢氧化钠反应生成氢氧化铁;
④中二氧化碳能与偏铝酸钠发生反应生成氢氧化铝和碳酸氢钠;
固体A为氧化铁,固体B为氧化铝;
②中铝单质能与氢氧化钠反应生成偏铝酸钠;
③中硫酸亚铁在空气中与氢氧化钠反应生成氢氧化铁。
(1)A.铁铝合金可由铁和铝熔融混合制成具有特征性质的混合物,故A正确;
B.合金熔点低于各成分,则铁铝合金的熔点低于铝和铁,故B错误;
C.合金硬度高于各成分,则铁铝合金硬度高于纯铝,故C正确;
综上所述,故答案为:
AC;
(2)①中硫酸铝与过量氢氧化钠反应生成偏铝酸钠,其反应的离子方程式为Al3++4OH﹣=AlO2﹣+2H2O,故答案为:
Al3++4OH﹣=AlO2﹣+2H2O;
(3)②中铝单质能与氢氧化钠反应生成偏铝酸钠,其反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故答案为:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(4)③中硫酸亚铁在空气中与氢氧化钠反应生成氢氧化铁,现象是先产生白色沉淀,之后迅速变成灰绿色最后变为红褐色,其反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:
先产生白色沉淀,之后迅速变成灰绿色最后变为红褐色;
4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(5)④中二氧化碳能与偏铝酸钠发生反应生成氢氧化铝和碳酸氢钠,若将二氧化碳换成氯化氢,则生成的氢氧化铝会继续与过量的盐酸发生反应而溶解,故答案为:
过量的氯化氢会使生成的氢氧化铝溶解;
(6)固体A为红棕色的氧化铁,可以用来做红色油漆和涂料,故答案为:
做红色油漆和涂料。
6.重铬酸钾(K2Cr2O7)在皮革、火柴印染化学、电镀等方面应用广泛。
工业上对制革工业污泥中(主要含有Cr3+、Fe3+、Fe2+、Al3+等)Cr元素的回收与再利用工艺如图:
已知:
①Al(OH)3与Cr(OH)3性质相似。
②2CrO42-+2H+
Cr2O72-+H2O。
③有关物质的溶解度曲线如图。
回答下列问题:
(1)含铬污泥预处理包括高温煅烧粉碎等步骤,其中高温煅烧的目的是__(写一条即可),滤渣III的成分是__(填化学式)。
(2)步骤③中操作需要的玻璃仪器有__,步骤①加入H2O2的作用是__。
(3)步骤⑦反应能够发生的原因是__,写出步骤④的反应离子方程式:
__。
(4)为测定产品中K2Cr2O7的含量,某兴趣小组将mg产品溶于水配制为500mL溶液,准确量取50.00mL,加入稀硫酸酸化,然后加入过量的KI充分还原,加___作指示剂,到达终点消耗30.00mL0.0500mol·
L-1的Na2S2O3溶液。
则该次生产的样品中K2Cr2O7含量为__%。
(已知:
Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI)
【答案】除去蛋白质等有机物(改变污泥构造,便于酸浸等合理即可)Al(OH)3烧杯、玻璃棒、漏斗将Fe2+氧化成Fe3+K2Cr2O7的溶解度小3Cl2+2CrO2-+8OH-=2CrO42-+6Cl-+4H2O淀粉溶液
硫酸浸取液中的金属离子主要是Cr3+,其次是Fe2+、Al3+和Cu2+,加入过量氢氧化钠,Fe3+、Cu2+生成沉淀,滤液的成分是NaAlO2和NaCrO2,通入氯气,NaCrO2被氧化为Na2CrO4,通入过量二氧化碳会生成氢氧化铝和碳酸氢钠,同时在酸性条件下,铬酸根转化为重铬酸根,即2CrO4-+2H+=Cr2O72-+H2O;
然后析出重铬酸钠,溶解加入氯化钾可得重铬酸钾。
(1)从动物皮到皮革需要加入铬酸鞣制,因此制革厂含铬污泥含有蛋白质等有机质,高温煅烧可以除去蛋白质等有机质,同时改变污泥构造,便于溶解;
根据流程,AlO2-溶液中通入过量CO2,会生成Al(OH)3,可得滤渣II的成分是Al(OH)3;
(2)经过步骤③得到滤液和滤渣Ⅱ,可知步骤③中操作为过滤,需要的玻璃仪器有烧杯、玻璃棒、漏斗;
根据流程,步骤①加入双氧水,目的是将Fe2+氧化为Fe3+,便于除去;
(3)加入KCl的目的是使Na2Cr2O7转化为K2Cr2O7,根据信息,一定温度下,K2Cr2O7溶解度最小,故步骤⑦反应能够发生;
由信息Al(OH)3与Cr(OH)3性质相似,根据流程,可知加入过量氢氧化钠,滤液的成分是NaAlO2和NaCrO2,通入氯气,NaCrO2被氧化为Na2CrO4,故离子方程式为3Cl2+2CrO2-+8OH-=2CrO42-+6Cl-+4H2O;
(4)有碘单质存在,可以选用淀粉溶液做指示剂;
根据化学反应:
Cr2O72-+6I-+14H+=2Cr3+3I2+7H2O和I2+2S2O32-=2I-+S4O62-,可得Cr2O72-~3I2~6S2O32-,ag产品最终消耗n(S2O32-)=0.0500mol/L×
30.00×
10-3L×
=0.0150mol,则n(Cr2O72-)=0.0150mol×
=0.00250mol,则样品中K2Cr2O7含量为
7.工业上制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的Al2O3,然后电解Al2O3得到铝。
下图是从铝土矿中提纯Al2O3的简单示意图。
其中涉及到的一个反应:
2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓。
(1)图示中实验操作
(1)是________;
加入的试剂②是__________(填化学式)
(2)试写出B溶液中的溶质的化学式:
_____________
(3)写出化学方程式:
①铝土矿→A:
_________________________________________________。
②E→F:
_______________________________________________________。
【答案】过滤Ca(OH)2或Ba(OH)2NaAlO2Al2O3+2NaOH=2NaAlO2+H2O2Al(OH)3
Al2O3+3H2O
溶液B中通入CO2产生沉淀,说明B溶液为NaAlO2溶液,则是向铝土矿中加入的试剂①是NaOH溶液,操作
(1)过滤,沉淀C为Fe2O3,则溶液D为Na2CO3,反应②为:
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,故沉淀H为CaCO3,沉淀E为Al(OH)3,F为Al2O3,反应④是电解氧化铝得到Al与氧气,据此分析。
(1)将沉淀从溶液中分离出来的操作是过滤;
根据反应2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓可知,D中含有碳酸钠,E是氢氧化铝,则F是氧化铝,电解氧化铝即得到金属铝。
碳酸钠要生成氢氧化钠和沉淀,需要进入的试剂是氢氧化钙,即②中加入的试剂是Ca(OH)2或Ba(OH)2;
(2)由上述分析可知,B为NaAlO2;
(3)①铝土矿→A是氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,反应的化学方程式为:
Al2O3+2NaOH=2NaAlO2+H2O;
②E→F是氢氧化铝受热分解生成氧化铝和水,反应的化学方程式为:
2Al(OH)3
Al2O3+3H2O。
8.粉煤灰是燃煤产生的工业固体废料,主要成分有Al2O3、SiO2,还含有少量Fe2O3、CaO等。
采用酸碱联合的方法从粉煤灰中综合回收氧化铝及二氧化硅的工艺流程如下:
硫酸熟化过程中发生的反应有:
Al2O3∙2SiO2+3H2SO4=Al(SO4)3+2SiO2+3H2O
3Al2O3∙2SiO2+9H2SO4=3Al2(SO4)3+2SiO2+9H2O
(1)“结晶”操作:
缓缓加热,浓缩至______,放置冷却,得到Al2(SO4)3∙18H2O。
(2)Al2(SO4)3∙18H2O在250~300℃下失重40.5%得Al2(SO4)∙xH2O,x=______。
(3)“还原焙烧”过程中发生反应的化学方程式为_________。
(4)设计实验检验粗氧化铝中是否含有Fe2O3:
__________。
(5)向硅酸钠溶液中通入过量CO2制备白炭黑的化学方程式为___________。
(6)粗氧化铝制备冶金级氧化铝过程中发生反应[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-,该反应的平衡常数为_______[已知Al(OH)3+H2O
[Al(OH)4]-+H+K1=4×
10-13;
H2CO3
H2O+CO2K2=600;
Kal(H2CO3)=4.2×
10-7、Ka2(H2CO3)=5.6×
10-11]。
【答案】表面出现结晶薄膜32Al2(SO4)3+3C
2Al2O3+3CO2↑+6SO2↑取粗氧化铝少许于试管中加稀硫酸溶解,静置,滴加KSCN溶液,若溶液变红,则粗氧化铝中含有Fe2O3杂质Na2SiO3+2CO2+(n+1)H2O=2NaHCO3+SiO2∙nH2O↓1.75×
103
粉煤灰主要成分有Al2O3、SiO2,还含有少量Fe2O3、CaO等,加入浓硫酸反应生成硫酸铝,水浸主要得到SiO2高硅渣,滤液经过结晶脱水得到硫酸铝,硫酸铝与焦炭反应生成粗氧化铝,验证粗氧化铝是否含有氧化铁,先将物质溶于稀硫酸后加KSCN溶液,观察现象;
向硅酸钠溶液中通入足量二氧化碳反应生成碳酸氢钠和白炭黑SiO2∙nH2O。
缓缓加热,浓缩至表面出现结晶薄膜,放置冷却,得到Al2(SO4)3∙18H2O;
表面出现结晶薄膜。
(2)假设100gAl2(SO4)3∙18H2O在250~300℃下失重40.5%,剩余100g×
(1−40.5%)=59.5gAl2(SO4)∙xH2O,
,解得x=3;
3。
(3)根据“还原焙烧”产物之一经过烟气制酸,硫酸铝和碳“还原焙烧”生成氧化铝、二氧化碳和二氧化硫,发生反应的化学方程式为2Al2(SO4)3+3C
2Al2O3+3CO2↑+6SO2↑;
2Al2(SO4)3+3C
2Al2O3+3CO2↑+6SO2↑。
(4)实验检验粗氧化铝中是否含有Fe2O3,将粗品溶于稀硫酸中,利用生成的铁离子与KSCN溶液反应是否有红色物质生成;
取粗氧化铝少许于试管中加稀硫酸溶解,静置,滴加KSCN溶液,若溶液变红,则粗氧化铝中含有Fe2O3杂质。
(5)向硅酸钠溶液中通入过量CO2生成碳酸氢钠和白炭黑SiO2∙nH2O,其化学方程式为Na2SiO3+2CO2+(n+1)H2O=2NaHCO3+SiO2∙nH2O↓;
Na2SiO3+2CO2+(n+1)H2O=2NaHCO3+SiO2∙nH2O↓。
(6)①Al(OH)3+H2O
[Al(OH)4]-+H+,②H2CO3
H2O+CO2,③H2CO3
HCO3-+H+,根据盖斯定律③−①−②得到[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-,方程式相减,平衡常数相除,因此[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-平衡常数为
1.75×
103。
9.马日夫盐[Mn(H2PO4)2·
H2O]主要用作磷化剂。
以软锰矿(主要成分为MnO2及少量的FeO、Al2O3和SiO2)为原料制备马日夫盐的主要工艺流程如图:
(1)按照无机物命名规律,马日夫盐[Mn(H2PO4)2·
2H2O]的化学名称为______。
在反应中,Mn2+若再失去一个电子比Fe2+再失去一个电子难,从原子结构解释其原因_______。
(2)“浸锰”过程中主要反应的离子方程式为_______。
滤渣X主要成分为_________。
检验“沉锰”已完成的实验操作及现象是_________。
步骤五产生马日夫盐晶体的化学方程式为_________。
(3)Fe3+的萃取率与溶液的pH和接触时间之间的关系如图,据此分析,萃取的最佳条件为__________。
(4)马日夫盐作防锈磷化剂的原因是利用其较强的酸性以及在防锈处理过程中生成了具有保护作用的FeHPO4,马日夫盐显酸性的主要原因是__________(用相关化学用语回答)。
【答案】二水合磷酸二氢锰Mn2+外围电子为3d5的半充满稳定状态,而Fe2+外围电子为3d6,可失去一个电子变为3d5的半充满稳定状态2FeO+MnO2+8H+=2Fe3++Mn2++4H2O、SO2+MnO2=
+Mn2+Al(OH)3在上层清液中继续滴加Na2CO3溶液,若无沉淀生成则说明沉锰已经完成MnCO3+2H3PO4+H2O=Mn(H2PO4)2·
2H2O+CO2↑pH=1.7下萃取60min
软锰矿(主要成分为MnO2,还含有少量的FeO、Al2O3和SiO2)用稀硫酸浸取,MnO2、FeO
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 培优 易错 难题铝及其化合物推断题辅导专题训练及详细答案 难题 及其 化合物 推断 辅导 专题 训练 详细 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
