 物理化学下册试题及答案Word格式文档下载.docx
物理化学下册试题及答案Word格式文档下载.docx
- 文档编号:19449924
- 上传时间:2023-01-06
- 格式:DOCX
- 页数:41
- 大小:42.38KB
物理化学下册试题及答案Word格式文档下载.docx
《物理化学下册试题及答案Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《物理化学下册试题及答案Word格式文档下载.docx(41页珍藏版)》请在冰豆网上搜索。
CH3+CH4C2H6+H,E2=201kJmol-1;
H+CH4CH3+H2,E3=29kJmol-1;
H+CH3CH4,E-1=0kJmol-1。
已知该总反应的动力学方程式为:
=
试求总反应的表观活化能。
五.
(本大题8分)
下列电池的电动势在25℃时为1.448V:
Pt|H2(p)|HCl(b=0.1mol·
kg-1,=0.796)|Cl2(p)|Pt
(1)写出电极反应和电池反应;
(2)计算氯电极的标准电极电势E(Cl|Cl2|Pt)。
六.
推导题。
气相反应2A(g)Y(g),是二级反应,反应开始时只有A,压力为pA,0,试推导反应系统的总压力p与时间t的函数关系式。
七.
选择题。
在题后括号内,填上正确答案代号。
(本大题共22小题,总计60分)
1、本小题3分
在等温等压下影响物质的表面吉布斯函数的因素:
()
(1)是表面积A;
(2)是表面张力;
(3)是表面积A和表面张力;
(4)没有确定的函数关系。
2、本小题3分
弯曲液面的饱和蒸气压总大于同温度下平液面的蒸气压。
是不是?
3、本小题2分
微小颗粒物质的熔点与同组成大块物质的熔点的关系是:
()。
(1);
(2)=;
(3);
(4)不能确定。
4、本小题4分
朗缪尔等温吸附理论的基本假设为:
(1);
(2);
(3);
(4)。
5、本小题3分
某反应,若其反应速率方程式为A=AccB,则当cB,0>
>
cA,0时,反应速率方程可约化为假二级反应。
6、本小题6分
某化合物与水相作用时,该化合物初浓度为1moldm-3,1h后其浓度为0.8moldm-3,2h后其浓度为0.6moldm-3,则此反应的反应级数为,此反应的反应速率系(常)数k=。
7、本小题3分
反应CO(g)+Cl2(g)COCl2(g)实验测得其反应速率方程为dc(COCl2)/dt=kc(Cl2)n·
c(CO)。
当温度及CO浓度维持不变而使Cl2浓度增至原来的3倍时,反应速率加快到原来的9倍,则Cl2的分级数n为:
(1)1;
(2)2;
(3)3;
(4)1.5。
8、本小题3分
反应速率系(常)数随温度变化的阿仑尼乌斯经验式可适用于所有化学反应。
9、本小题3分
对行反应AB,当温度一定时由纯A开始,下列说法中哪一点是不对的:
(1)开始时A的反应消耗速率最快;
(2)反应的净速率是正逆二向反应速率之差;
(3)k1/k-1的值是恒定的;
(4)达到平衡时正逆二向的反应速率系(常)数相等。
10、本小题3分
低温下,反应CO(g)+NO2(g)==CO2(g)+NO(g)的速率方程是υ=k{c(NO2)}2试问下列机理中,哪个反应机理与此速率方程一致:
(1)CO+NO2CO2+NO;
(2)2NO2N2O4(快),N2O4+2CO2CO2+2NO(慢);
(3)2NO22NO+O2(慢),2CO+O22CO2(快)。
11、本小题2分
简单碰撞理论可以说明质量作用定律及温度对速率系(常)数的影响,但它不能从理论上算出活化能。
是不是?
12、本小题2分
催化剂只能加快反应速率,而不能改变化学反应的标准平衡常数。
()
13、本小题2分
电解质溶液的离子强度与其浓度的关系为:
(1)浓度增大,离子强度增强;
(2)浓度增大,离子强度变弱;
(3)浓度不影响离子强度;
(4)随浓度变化,离子强度变化无规律。
14、本小题2分
0.005molkg-1的BaCl2水溶液,其离子强度I=0.03molkg-1。
15、本小题2分
原电池的正极即为阳极,负极即为阴极。
16、本小题3分
电池Hg|Zn(a1)|ZnSO4(a2)|Zn(a3)|Hg的电动势:
(1)仅与a1,a3有关,与a2无关;
(2)仅与a1,a2有关,与a3无关;
(3)仅与a2,a3有关,与a1无关;
(4)与a1,a2,a3均无关。
17、本小题2分
在电解时,阴极电势必须于阳离子的析出电势,阳离子才能在阴极析出;
而阳极电位必须于金属的溶解电势,金属才能从阳极溶解。
18、本小题3分
电解质使溶胶发生聚沉时,起作用的是与胶体粒子带电符号相的离子。
离子价数越高,其聚沉能力越,聚沉值越
19、本小题2分
由瑞利公式可知,分散介质与分散相之间折射率相差愈大,则散射作用愈显著。
20、本小题2分
某水溶液发生负吸附后,在干净的毛吸管中的上升高度比纯水在该毛吸管中上升的高度低。
()
21、本小题2分
通常物理吸附的速率较小,而化学吸附的速率较大。
22、本小题3分
写出AgI正溶胶的胶团结构式:
2006-2007-1A卷答案
物理化学
(一)-2试卷A卷参考答案
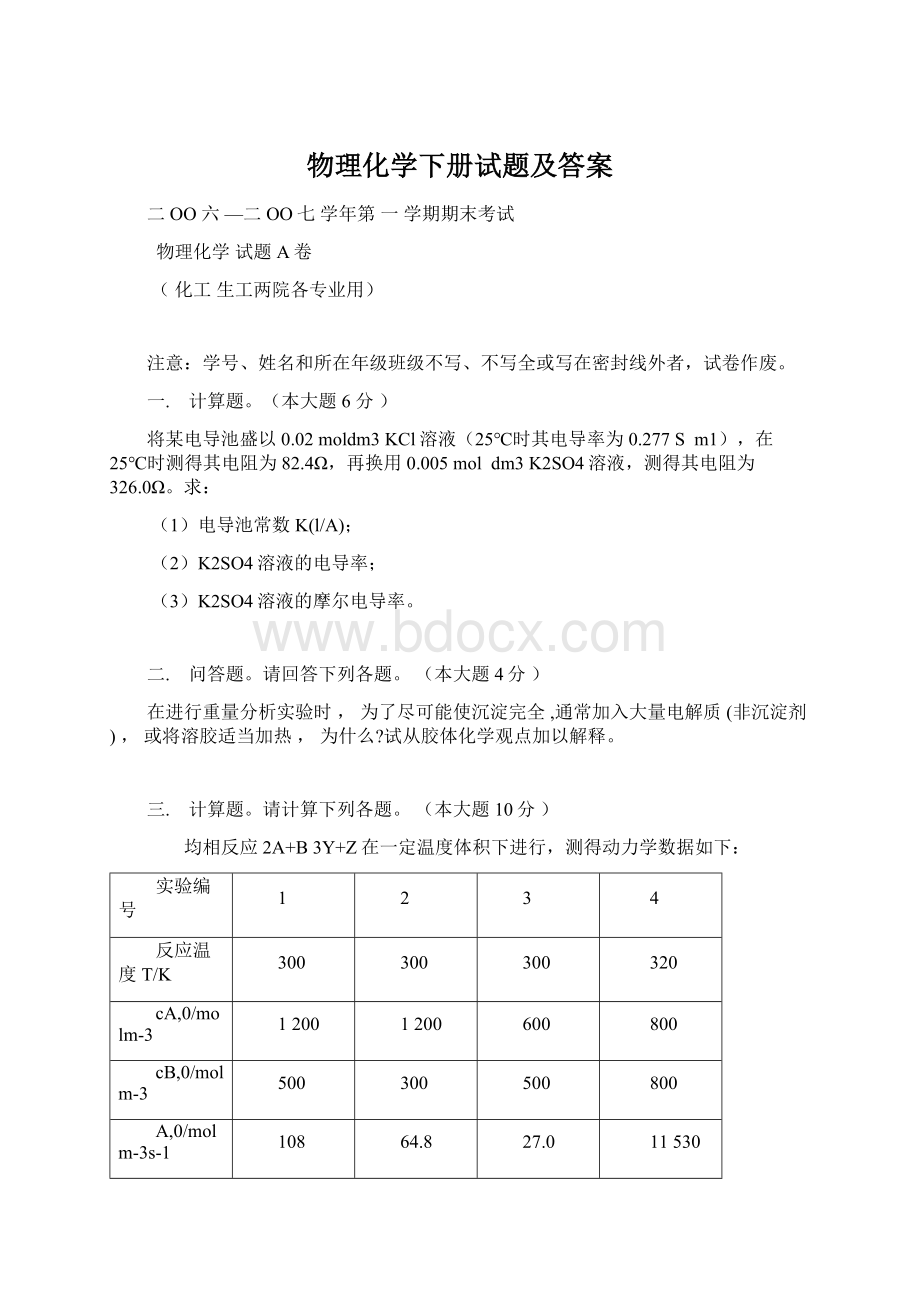
一.计算题。
解:
(1)K(l/A)=κR=0.277×
82.4=22.8m1(2分)
(2)κ(K2SO4)==22.8÷
326=0.07Sm1(4分)
(3)m(K2SO4)==0.07Sm1÷
0.005moldm3=0.014Sm2mol1(6分)
二.问答题。
加入大量电解质能显著降低动电电势,使溶胶易于聚沉。
适当的加热可加快胶粒的热运动,增加胶粒互相碰撞的频率,从而使聚沉机会增加。
二者都有利于沉淀完全。
(4分)
三.计算题。
(本大题10分)
(1)
由实验1,3知,cB,0不变,cA,0减半,而A,0仅为原来的1/4;
可知=2。
(2分)
由实验1,2知,cA,0不变,cB,0从500molm-3降到300molm-3,
而A,0从108molm-3s-1降到64.8molm-3s-1;
可知=1。
故
总反应级数n=+=3(6分)
从实验1,2,3可以计算出300K时,kA(300K)的平均值。
kA(300K)=1.5×
10-7m6·
mol-3·
s-1(7分)
从实验4可以计算出320K时,kA(320K)的平均值。
kA(320K)=2.25×
10-5m6·
mol-3·
s-1(8分)
(2)把
(1)的结果代入阿仑尼乌斯方程,得
解得:
Ea=200kJ·
mol-1(10分)
四.计算题。
k=,=;
(1分)
=++-(3分)
即=++-(4分)
Ea=(E1+E2+E3-E-1)(5分)
=(423+201+29-0)kJmol-1
&
nbsp;
=327kJmol-1(6分)
五.计算题。
(1)电极反应:
H2(p)===H++e
Cl2(p)+e===Cl-
电池反应:
H2(p)+Cl2(p)===HCl(b=0.1mol·
kg-1,=0.796)(3分)
(2)E=E(Cl|Cl2|Pt)E(H+|H2|Pt)lna(HCl)(4分)
=E(Cl|Cl2|Pt)lna2(5分)
E(Cl|Cl2|Pt)=E+lna=[1.4882×
0.05916lg(0.1×
0.796)]V(7分)
=(1.4880.130)V=1.358V(8分)
六.推导题。
2A(g)Y(g)
t=0pA,O0
pA(pA,0-pA)
总压力p=pA+(pA,0-pA)=(pA,0+pA)
pA=2p-pA,0
(1)(2分)
对于二级反应:
=kA,pt
(2)(4分)
将式
(1)代入式
(2),得:
-=kA,pt
经整理p=pA,0(6分)
七.选择题。
(本大题共19小题,总计60分)
1.本小题3分
(3)
2.本小题3分
不是
3.本小题2分
4.本小题4分(每空1分)
(1)吸附为单分子层
(2)固体表面是均匀的
(3)吸附于表面上的分子无相互作用力(4)吸附平衡是动态平衡
5.本小题3分
是
6.本小题6分
零级
0.2mol·
dm-3·
h-1
7.本小题3分
(2)
8.本小题3分
不是
9.本小题3分
(4)
10.本小题3分
11.本小题2分
是
12.本小题2分
√
13.本小题2分
14.本小题2分
15.本小题2分
16.本小题3分
17.本小题2分(每空1分)
低高
18.本小题3分(每空1分)
反,大,小
19.本小题2分
20.本小题2分
不是
21.本小题2分
22.本小题3分
2006-2007-1B
卷号:
物理化学试题B卷
八.问答题。
对于以等体积的0.008mol·
dm-3AgNO3溶液和0.01mol·
dm-3KI溶液混合制得的AgI溶胶,用下列电解质使其聚沉时,其聚沉能力的强弱顺序如何?
(1)MgCl2;
(2)NaCl;
(3)MgSO4;
(4)Na2SO4。
九.计算题。
用活性炭吸附CHCl3时,0℃时的最大吸附量为93.8dm3·
kg-1已知该温度下CHCl3的分压力为1.34×
104Pa时的平衡吸附量为82.5dm3·
kg-1,试计算:
(1)朗缪尔吸附等温式中的常数b;
(2)CHCl3分压力为6.67×
103Pa时的平衡吸附量。
一十.计算题。
21℃时,将等体积的0.0400mol·
dm-3CH3COOC2H5溶液和0.0400mol·
dm-3NaOH溶液混合,经25min后,取出100cm3样品,测得中和该样品需0.125mol·
dm-3的HCl溶液4.23cm3。
试求21℃时二级反应CH3COOC2H5+NaOHCH3COONa+C2H5OH的反应速率系(常)数。
45min后,CH3COOC2H5时转化率是多少?
一十一.计算题。
已知18℃,H2O的离子积=0.61×
10-14,试求该温度下纯水的电导率。
18℃时,H+,OH-的分别为315×
10-4Sm2mol-1和174×
10-4Sm2mol-1。
一十二.计算题。
已知298K时,E(Fe3+|Fe)=0.036V,E(Fe3+|Fe2+)=0.771V。
计算298K时:
(1)E(Fe2+|Fe);
(2)Fe+2Fe3+===3Fe2+反应的标准平衡常数K。
一十三.是非题。
在题后括号内,正确的打“√”,错误的打“×
”。
(本大题共21小题,总计60分)
一十四.1、本小题2分
由两种不互溶的液体A和液体B构成的双液系界面层中,A和B的浓度在垂直于界面方向上是连续递变的。
一十五.2、本小题3分
垂直插入水槽中一支干净的玻璃毛细管,当在管中上升平衡液面处加热时,水柱会上升。
一十六.
一十七.3、本小题3分
在定温下,同成分的两个大小不同的液球的饱和蒸气压pr,1*(大球)和pr,2*(小球)存在()的关系。
(A)pr,1*>
pr,2*(B)pr,1*=pr,2*
(C)pr,1*<
pr,2*(D)不能确定
一十八.4、本小题2分
反应系统体积恒定时,反应速率与反应物的消耗速率或产物的生成速率B的关系是=。
一十九.5、本小题3分
某反应的速率系(常)数k=5.0×
10-5dm3·
mol-1·
s-1,若浓度单位改为mol·
cm-3,时间单位改为min,则k的数值是:
(1)3;
(2)8.33×
10-10;
(3)8.33×
10-4;
(4)3×
10-3。
二十.6、本小题3分
在温度T时实验测得某化合物在溶液中分解的数据如下:
初浓度c0/mol·
dm-3
0.501.102.48
半衰期T1/2/s
4280885174
则该化合物分解反应的级数为:
(1)零级;
(2)一级;
(3)二级;
(4)三级。
二十一.7、本小题3分
反应CO(g)+Cl2(g)COCl2(g)的动力学方程式为=kc(CO)c(Cl2);
当温度及CO的浓度保持不变而使Cl2的浓度增至原来的3倍时,反应速率增至原来的9倍,则=。
二十二.
二十三.8、本小题3分
对同一反应,活化能一定,则反应的起始温度愈低,反应速率系(常)数对温度的变化愈敏感。
二十四.
二十五.9、本小题3分
在一个连串反应AYZ中,如果我们需要的是中间产物Y,那么为了得到产品的最高产率,我们应当:
( )。
(1)控制适当的反应时间;
(2)控制适当的反应温度;
(3)增加反应物A的浓度。
二十六.
二十七.10、本小题3分
以下复合反应由若干元反应所组成:
A
用质量作用定律写出反应中与各物浓度关系为:
()。
(1)=2k1cA+2k4cY-k3c;
(2)=k1cA+k4cY-k3c;
(3)=2k1cA+2k4cY-2k3c;
(4)=k1cA+k4cY-2k3c。
二十八.11、本小题3分
对于元反应,反应速率系(常)数总是随着温度的升高而增大。
二十九.12、本小题2分
过渡态理论中的活化络合物就是一般反应历程中的活化分子。
三十.13、本小题3分
298K时,相同浓度(均为0.01molkg1)的KCl,CaCl2和LaCl3三种电解质水溶液,离子平均活度因子最大的是LaCl3。
三十一.
三十二.14、本小题3分
设ZnCl2水溶液的质量摩尔浓度为b,离子平均活度因子(系数)为γ±
,则其离子平均活度a±
=γ±
b/b。
三十三.15、本小题2分
离子氛的电性与中心离子的电性,电量与中心离子的电量。
三十四.16、本小题3分
在等温等压下进行的一般化学反应,G0,电化学反应的G可小于零,也可大于零。
三十五.
三十六.17、本小题4分
下列电池中哪个电池的电动势与氯离子浓度无关()。
(1)Zn|ZnCl2溶液|Cl2,Pt;
(2)Zn|ZnCl2溶液||KCl溶液|AgCi,Ag;
(3)Ag,AgCl|KCl溶液|Cl2,Pt;
(4)Pt,H2|HCl溶液|Cl2,Pt。
三十七.
三十八.18、本小题3分
一储水铁箱上被腐蚀了一个洞,今用一金属片焊接在洞外以堵漏,为了延长铁箱的使用寿命,选用哪种金属为好?
(1)铜片;
(2)铁片;
(3)镀锡铁片;
(4)锌片。
三十九.
四十.19、本小题3分
由瑞利公式可知,入射光的波长愈短,散射愈弱。
四十一.20、本小题3分
溶胶是均相系统,在热力学上是稳定的。
()
四十二.
四十三.21、本小题3分
向碘化银正溶胶中滴加过量的KI溶液,则所生成的新溶胶在外加直流电场中的移动方向为()
(A)向正极移动(B)向负极移动(C)不移动
2006-2007-1B卷答案
物理化学
(一)-2试卷B卷参考答案
四十四.问答题。
MgCl2MgSO4NaClNa2SO4(6分)
四十五.计算题。
(本大题8分)
(1)设V和Vm分别为平衡吸附量和最大吸附量,则
即
=5.45×
10-4Pa-1(4分)
(2)V=
=73.5dm3·
kg-1(8分)
四十六.计算题。
cA,0=1/2×
0.0400mol·
dm-3=0.0200mol·
dm-3,(2分)
cA=(4.23/100)×
0.125mol·
dm-3=5.30×
10-3mol·
dm-3(4分)
=5.55dm3·
min-1(7分)
kA=
即5.55dm3·
min-1=
=0.834=83.4%(10分)
四十七.计算题。
c(H+)=c(OH-)=c=7.8×
10-8moldm-3(2分)
=(315+174)×
10-4Sm2mol-1
=489×
10-4Sm2mol-1(3分)
=c=[489×
10-4×
(7.8×
10-8×
103)]Sm-1
=3.8×
10-6Sm-1(6分)
四十八.计算题。
(1)Fe3++3eFe,G1=3E(Fe3+|Fe)F
Fe3++eFe2+,G2=E(Fe3+|Fe2+)F
Fe2++2eFe2+,G3=2E(Fe2+|Fe)F
G3=G1G2
E(Fe2+|Fe)=E(Fe2+|Fe)E(Fe3+|Fe)=0.439V(5分)
(2)设计电池:
Fe|Fe3+,Fe2+|Pt
电池反应:
Fe+2Fe3+3Fe2+(7分)
E=E(Fe3+|Fe2+)E(Fe3+|Fe)=0.807V
K=exp(zFE/RT)=exp(3×
96500×
0.807/8.315/298)=1.98×
1027
或E=E(Fe3+|Fe2+)E(Fe2+|Fe)=1.210V
K=exp(zFE/RT)=exp(2×
1.210/8.315/298)=1.98×
1027(10分)
四十九.是非题。
1、本小题2分
五十.解:
2、本小题3分
五十一.解:
3、本小题3分
五十二.解:
C
五十三.4、本小题2分
五十四.解:
五十五.5、本小题3分
五十六.解:
五十七.6、本小题3分
五十八.解:
五十九.7、本小题3分
六十.解:
2
六十一.8、本小题3分
六十二.解:
是
六十三.9、本小题3分
六十四.解:
六十五.10、本小题3分
六十六.解:
(3)
六十七.11、本小题3分
六十八.解:
六十九.12、本小题2分
七十.解:
七十一.13、本小题3分
七十二.解:
七十三.14、本小题3分
七十四.解:
七十五.15、本小题2分
七十六.解:
相反相等
七十七.16、本小题3分
七十八.解:
七十九.17、本小题4分
八十.解:
18、本小题3分
解:
(3)
19、本小题3分
不是
20、本小题3分
21、本小题3分
A
二OO七—二OO八学年第一学期期末考试
物理化学
(一)-2A卷试题
(05生工、化工除生技外各专业用)闭卷
学号、姓名和所在年级班级不写、不
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 物理化学 下册 试题 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
