 高考专题训练工艺流程题三Word文档格式.docx
高考专题训练工艺流程题三Word文档格式.docx
- 文档编号:21333320
- 上传时间:2023-01-29
- 格式:DOCX
- 页数:13
- 大小:269.30KB
高考专题训练工艺流程题三Word文档格式.docx
《高考专题训练工艺流程题三Word文档格式.docx》由会员分享,可在线阅读,更多相关《高考专题训练工艺流程题三Word文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
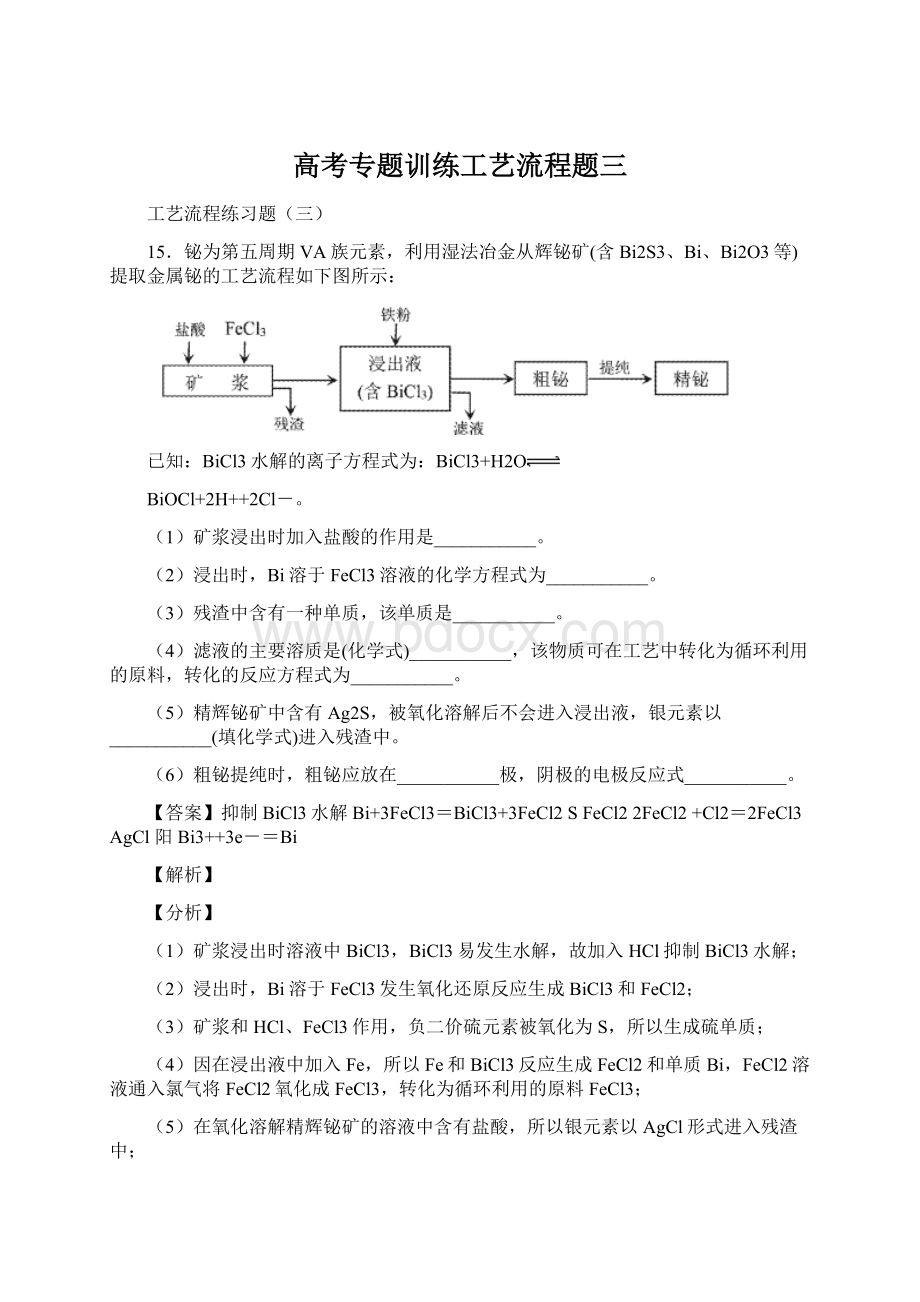
(1)矿浆浸出液中BiCl3,BiCl3易发生水解,故加入HCl抑制BiCl3水解;
本题答案为:
抑制BiCl3水解。
(2)浸出时,Bi溶于FeCl3发生氧化还原反应生成BiCl3和FeCl2,化学方程式为:
Bi+3FeCl3=BiCl3+3FeCl2;
Bi+3FeCl3=BiCl3+3FeCl2。
(3)矿浆中Bi2S3和FeCl3反应时,负二价硫元素被氧化为S,所以生成硫单质;
S。
(4)因在浸出液中加入Fe,所以Fe和BiCl3反应生成FeCl2和单质Bi,故滤液的主要溶质是FeCl2,FeCl2转化为循环利用的FeCl3,化学方程式为:
2FeCl2+Cl2=2FeCl3;
FeCl2,2FeCl2+Cl2=2FeCl3。
(5)精辉铋矿中含有Ag2S,被氧化溶解后不会进入浸出液,因为在氧化溶解精辉铋矿的溶液中含有大量的氯离子,所以银元素转化为难溶于水的AgCl进入残渣中;
AgCl。
阴极电极反应式为:
Bi3++3e-=Bi;
阳,Bi3++3e-=Bi。
【点睛】
利用电解原理提纯金属时,不纯的金属和电源的正极相连做阳极,纯金属和电源的负极相连做阴极,含有待提纯金属的阳离子的溶液做电解质溶液。
16.锌锰干电池是很古老的一次性电池,它的生产原料主要有软锰矿和闪锌矿。
已知闪锌矿中含ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分;
软锰矿中含MnO2约a%,SiO2约20%,Al2O3约4%,其余为水分。
科研人员开发了综合利用软锰矿和闪锌矿的同槽酸浸工艺,工艺流程如下图所示。
请回答下列问题:
(1)反应I需不断搅拌,目的是____________________________。
(2)检验反应I的滤液中含有Fe3+的试剂为____________;
写出反应I中由FeS生成Fe3+的离子方程式____________________________________。
(3)反应Ⅱ加入适量锌的作用是__________________;
反应III中MnO2的作用是________________。
(4)已知ZnCO3、MnCO3的Ksp分别为1.4×
10-10、2.2×
10-11;
要使反应IV之后的溶液中Zn2+、Mn2+浓度均降到1.0×
10-6mol/L,则溶液中残留的CO32-浓度至少为__________mol/L。
(5)图是Na2SO4和Na2SO4•10H2O的溶解度曲线(g/100g水),则Ⅳ中得到Na2SO4固体的操作是:
将分离出MnCO3和ZnCO3后的滤液________→__________→用乙醇洗涤→干燥。
用乙醇洗涤而不用水洗的原因是_________________________________________。
【答案】加快反应速率,提高原料利用率。
KSCN(或苯酚)2FeS+3MnO2+12H+=2Fe3++2S+3Mn2++6H2O将溶液中的Cu2+还原成Cu将Fe2+氧化成Fe3+1.4×
10-4蒸发结晶趁热过滤防止Na2SO4固体转化为Na2SO4•10H2O,并防止Na2SO4因溶于水而损耗
(1)反应I是闪锌矿、软锰矿在硫酸中的溶解过程,搅拌是为了加快反应速率,提高原料利用率;
(2)溶液中是否含有Fe3+,检验试剂一般选择KSCN(或苯酚);
反应I中由FeS和MnO2在酸性溶液中反应生成Fe3+、H2O、S、Mn2+;
(3)由图可知,反应Ⅱ加入适量锌有铜析出,故反应Ⅱ是将溶液中的Cu2+还原为Cu;
反应III中加入MnO2,将Fe2+氧化成Fe3+,最终生成Fe(OH)3沉淀;
(4)欲使Zn2+、Mn2+浓度均降到1.0×
10-6mol/L,依据ZnCO3、MnCO3溶度积常数,可求CO32-浓度;
(5)由图像溶解度曲线变化可知,Na2SO4的溶解度,在温度较高时,随温度升高而降低,而Na2SO4•10H2O的溶解度,随温度升高而升增大,欲得到Na2SO4晶体,应采取加热蒸发溶剂使Na2SO4结晶析出,并趁热过滤;
因Na2SO4在乙醇中难于溶解,所以用乙醇而不用水洗涤,即防止Na2SO4和水作用生成Na2SO4•10H2O,又能防止Na2SO4因溶于水而损耗。
加快反应速率,提高原料利用率。
(2)Fe3+遇到KSCN溶液变成血红色,Fe3+遇到苯酚溶液显紫色,故欲检验I的滤液中含有Fe3+的试剂为:
KSCN(或苯酚);
反应I中由FeS和MnO2在酸性溶液中反应生成Fe3+、H2O、S、Mn2+,反应的的离子方程式为:
2FeS+3MnO2+12H+=2Fe3++2S+3Mn2++6H2O;
KSCN(或苯酚)、2FeS+3MnO2+12H+=2Fe3++2S+3Mn2++6H2O。
将溶液中的Cu2+还原成Cu;
将Fe2+氧化成Fe3+。
10-6mol/L,根据ZnCO3的Ksp=1.4×
10-10,即c(Zn2+)c(CO32-)=1.4×
10-10,求得:
c(CO32-)=1.4×
10-10÷
(1.0×
10-6)=1.4mol/L,同理可求使Mn2+沉淀,当Mn2+浓度均降到1.0×
10-6mol/L时,c(CO32-)=2.2mol/L,所以溶液中残留的CO32-浓度至少为1.4mol/L;
1.4。
因Na2SO4在乙醇中难于溶解,所以用乙醇洗涤即防止Na2SO4和水作用生成Na2SO4•10H2O,又能防止Na2SO4因溶于水而损耗;
蒸发结晶、趁热过滤、防止Na2SO4固体转化为Na2SO4•10H2O,并防止Na2SO4因溶于水而损耗。
17.三盐基硫酸铅(3PbO·
PbSO4·
H2O)具有良好的热稳定性、耐热性、电绝缘性,是目前用量最大的热稳定剂,工业上利用铅废渣(主要含PbSO4、PbCl2、SiO2)制取三盐基硫酸铅及PbO2工艺流程如下:
①“浸出”过程发生的反应:
PbSO4(s)+2Cl-(aq)
PbCl2+SO42-(aq)和
PbCl2(s)+2Cl-(aq)
PbCl42-(aq)△H>
0,
②Ksp(PbCl2)=1.7×
10-5Ksp(PbSO4)=2.5×
10-8
回答下列问题:
(1)铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和___________。
(2)“操作1”通过多步操作得到PbCl2,分别为___________、___________、过滤、洗涤。
(3)“转化”后得到PbSO4,当c(Cl-)=0.100mol/L时,c(SO42-)=___________(结果保留一位小数);
“转化”时需要升高体系温度,其原因是_________________________________。
(4)写出合成三盐基硫酸铅的化学方程式_________________________________。
(5)氨水络合后铅的存在形态是[Pb(OH)SO4]-,写出“氧化”发生的离子反应方程式__________________________________________________________________。
(6)一种新型的铅锂电池的充放电示意图如下,写出放电时的正极反应式___________。
【答案】SiO2蒸发浓缩冷却结晶1.5×
10-5mol/L升高温度有利于HCl逸出,使PbCl2(s)+H2SO4(aq)
PbSO4(s)+2HCl(aq)向右移动4PbSO4+6NaOH=3PbO·
H2O+3Na2SO4+2H2O[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2OLi1-xMn2O4+xe-+xLi+=LiMn2O4
铅废渣(主要含PbSO4、PbCl2、SiO2)加入CaCl2、NaCl溶液,“浸出”过程发生的反应:
PbCl2+SO42-(aq)和PbCl2(s)+2Cl-(aq)
0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2,“操作1”通过多步操作得到PbCl2,分别为蒸发浓缩、冷却结晶、过滤、洗涤。
加入硫酸“转化”后得到PbSO4,溶液Ⅱ为HCl,加入NaOH合成三盐基硫酸铅,反应为:
4PbSO4+6NaOH=3PbO·
H2O+3Na2SO4+2H2O,加NH3·
H2O络合后溶解生成[Pb(OH)SO4]-,加入(NH4)2S2O82-发生[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O,得PbO2。
(1)铅废渣(主要含PbSO4、PbCl2、SiO2)加入CaCl2、NaCl溶液,“浸出”过程发生的反应:
PbCl2(s)+SO42-(aq)和PbCl2(s)+2Cl-(aq)
0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2;
(2)“操作1”分别经过蒸发浓缩、冷却结晶、过滤、洗涤得到PbCl2晶体。
(3)“转化”后得到PbSO4,PbSO4(s)+2Cl-(aq)
PbCl2(s)+SO42-(aq),当c(Cl-)=0.100mol/L时,c(SO42-)=c2(Cl-)Ksp(PbSO4)/Ksp(PbCl2)=0.1002×
2.5×
10-8/1.7×
10-5=1.5×
10-5;
“转化”时需要升高体系温度,其原因是升高温度有利于HCl逸出,使PbCl2(s)+H2SO4(aq)
PbSO4(s)+2HCl(aq)向右移动。
(4)已知三盐基硫酸铅(3PbO·
H2O),反应物为PbSO4和NaOH,合成三盐基硫酸铅的化学方程式4PbSO4+6NaOH=3PbO·
H2O+3Na2SO4+2H2O。
(5)3PbO·
H2O氨水络合后铅的存在形态是[Pb(OH)SO4]-,+2价铅氧化成+4价,“氧化”发生的离子反应方程式[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O。
(6)新型的铅锂电池放电时正极发生还原反应,正极反应式Li1-xMn2O4+xe-+xLi+=LiMn2O4。
18.高锰酸钾常用作消毒杀菌、水质净化剂等。
某小组用软锰矿(主要含MnO2,还含有少量SiO2、Al2O3、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。
试回答下列问题。
(1)配平焙烧时化学反应:
□MnO2+□_____+□O2
□K2MnO4+□H2O;
__________
(2)滤渣II的成分有_______(化学式);
第一次通CO2不能用稀盐酸代替的原因是_________。
(3)第二次通入过量CO2生成MnO2的离子方程式为_________。
(4)将滤液Ⅲ进行一系列操作得KMnO4。
由下图可知,从滤液Ⅲ得到KMnO4需经过_____、______、洗涤等操作。
(5)工业上按上述流程连续生产。
含MnO2a%的软锰矿1吨,理论上最多可制KMnO4___吨。
(6)利用电解法可得到更纯的KMnO4。
用惰性电极电解滤液II。
①电解槽阳极反应式为____________;
②阳极还可能有气体产生,该气体是__________。
【答案】24KOH122Al(OH)3、H2SiO3稀盐酸可溶解Al(OH)3,不易控制稀盐酸的用量3MnO42-+4CO2+2H2O=MnO2↓+2MnO4-+4HCO3-蒸发结晶趁热过滤0.018aMnO42--e-=MnO4-O2
软锰矿主要成分MnO2与KOH混合在空气中焙烧,冷却得到固体物质,溶于水过滤得到滤渣I和滤液I,滤液I中应含有K2SiO3,KAl(OH)4、K2MnO4等溶质,滤渣I为Fe2O3;
向滤液I中第一次通入CO2与K2SiO3、KAl(OH)4发生反应,过滤得到滤渣Ⅱ和滤液Ⅱ,滤渣Ⅱ为Al(OH)3、H2SiO3;
滤液Ⅱ含有KHCO3,K2MnO4等溶质;
向滤液Ⅱ中第二次通入过量CO2,再次过滤得到滤液Ⅲ和MnO2,滤液Ⅲ中含有KMnO4和KHCO3,再经过一系列操作得到较纯的KMnO4,MnO2可以循环利用。
(1)焙烧时MnO2与KOH在空气中O2的作用下反应得到K2MnO4和H2O,反应为氧化还原反应,Mn化合价升高2,O化合价降低2,根据电子转移数守恒,所以在MnO2前面配上2,O2前面配上1,根据Mn元素守恒,在K2MnO4前面配上系数2,再根据K元素守恒,在KOH前面配上4,最后根据H元素守恒,在H2O前面配上2,2MnO2+4KOH+1O2
2K2MnO4+2H2O。
(2)滤渣Ⅱ中含有的物质有Al(OH)3、H2SiO3,第一次通CO2不能用稀盐酸代替,这是由于稀盐酸酸性较强,可溶解Al(OH)3,不易控制稀盐酸的用量,溶液中便会再次混入Al3+;
(3)第二次通入过量CO2生成MnO2,溶液中原先是K2MnO4,第二次通入过量的CO2时发生歧化反应生成MnO2和KMnO4,此时CO2被转化为HCO3-,反应为氧化还原反应,则反应的离子方程式为:
3MnO42-+4CO2+2H2O=MnO2↓+2MnO4-+4HCO3-。
(4)将滤液Ⅲ进行一系列操作得KMnO4,此时溶液中还存在KHCO3,根据溶解度随温度变化的图象分析,随着温度升高,二者溶解度均不断增大,在40℃附近时二者溶解度相等,超过这一温度时,KHCO3溶解度不断增大,KMnO4溶解度则增大较缓慢,所以从溶液中提取较纯的KMnO4,需要蒸发结晶,趁热过滤,洗涤等操作。
(5)工业上按上述流程连续生产,含MnO2a%的软锰矿1吨,理论上第一步完全转化为K2MnO4,第二步转化为KMnO4时则是发生歧化反应,由于歧化反应产物得到MnO2可以循环使用,所以理论最多产量则是根据Mn元素守恒完全生成KMnO4的量,为1t×
a%×
158/87=0.018at;
(6)①电解池阳极发生氧化反应,用惰性电极电解滤液Ⅱ,滤液Ⅱ中含有MnO42-,电解转化为MnO4-,则阳极的电极反应为:
MnO42--e-=MnO4-;
②阳极还可以发生电解水的相关反应,产生O2,发生的电极反应有2H2O-4e-=O2↑+4H+,阳极还可能产生的气体为O2。
本题考查无机工艺流程,解题关键:
理解软锰矿制备KMnO4的流程,流程中每一步操作的内容及发生的相关反应,应用氧化还原反应和电化学相关知识。
19.钛是一种重要的金属,以钛铁矿[主要成分为钛酸亚铁(FeTiO3),还含有少量Fe2O3]为原料制备钛的工艺流程如图所示。
(1)滤液1中钛元素以TiO2+形式存在,则“溶浸”过程发生的主要反应的化学方程式为________。
(2)物质A为________(填化学式),“一系列操作”为________。
(3)“水解”步骤中生成TiO2·
xH2O,为提高TiO2·
xH2O的产率,可采取的措施有________、________。
(写出两条)。
(4)“电解”是以石墨为阳极,TiO2为阴极,熔融CaO为电解质。
阴极的电极反应式为________;
若制得金属Ti9.60g,阳极产生气体________mL(标准状况下)。
(5)将少量FeSO4·
7H2O溶于水,加入一定量的NaHCO3溶液,可制得FeCO3,写出反应的离子方程式________;
若反应后的溶液中c(Fe2+)=2×
10-6mol·
L-1,则溶液中c(CO32-)=________mol·
L-1。
(已知:
常温下FeCO3饱和溶液浓度为4.5×
L-1)
【答案】FeTiO3+2H2SO4
TiOSO4+FeSO4+2H2OFe蒸发浓缩、冷却结晶、过滤加水稀释反应物加碱中和生成的酸、加热等TiO2+4e-===Ti+2O2-4480(2分)Fe2++2HCO3—=FeCO3↓+CO2↑+H2O1×
10—5
钛铁矿和硫酸反应生成硫酸钛和硫酸亚铁,氧化铁和硫酸反应生成硫酸铁和水,根据最后生成绿矾分析,中间有铁离子变成亚铁离子的过程,所以加入物质A为铁,硫酸亚铁溶液通过加热浓缩,冷却结晶,过滤得到硫酸亚铁晶体。
根据电解池中阳极失去电子发生氧化反应,阴极得到电子发生还原反应分析电极反应方程式。
(1)因钛铁矿主要成分为FeTiO3,且滤液1中钛元素以TiO2+形式存在,所以其主要反应化学方程式为FeTiO3+2H2SO4
TiOSO4+FeSO4+2H2O。
(2)该流程中还有副产物FeSO4·
7H2O,故需将溶浸产物中的Fe3+除去,物质A为Fe,“一系列操作”包括蒸发浓缩、冷却结晶、过滤。
(3)“水解”反应为TiO2++(x+1)H2O===TiO2·
xH2O↓+2H+,根据平衡移动原理,为提高TiO2·
xH2O的产率可以加水稀释反应物、加碱中和生成的酸、加热等。
(4)“电解”过程中阴极反应:
TiO2+4e-===Ti+2O2-,阳极反应:
2O2--4e-===O2↑,若制得金属Ti9.60g,则n(Ti)=n(O2)=0.2mol,V(O2)=4480mL(标准状况下)。
(5)由题意知该反应化学方程式为:
Fe2++2HCO3—=FeCO3↓+CO2↑+H2O;
由常温下FeCO3饱和溶液浓度为4.5×
10—6mol·
L-1,KSP(FeCO3)=2.025×
10—11mol2·
L-2,则c(CO32—)==1.013×
10—5mol·
20.铝在生活中具有广泛用途。
现从含铝废料(含有A12O3的质量分数为51%,其余为NiO、SiO2、Fe3O4)中制取金属铝的流程如下:
(1)工艺过程中常把废料研细,其目的是_________________________________。
(2)步骤I中得到的滤渣的主要成分是___________(填化学式)。
步骤V的反应类型是______________________。
(3)步骤Ⅱ中加入稀双氧水的目的是______________________。
(4)步骤Ⅲ产生NiCO3的离子方程式是___________。
步骤Ⅳ产生沉淀的离子方程式是______________________。
(5)工业中常用惰性电极熔融电解法制备金属铝,其阴极反应式为___________。
(6)若用a吨该含铝废料通过上述流程,理论上可以生产铝___________吨
【答案】增大接触面积,加快反应速率,使反应更充分,提高原料转化率SiO2分解将Fe2+氧化为Fe3+Ni2++CO32—=NiCO3↓2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑Al3++3e—=Al0.27a
由实验流程可知,铝废料中加入加硫酸,Al2O3转化为Al3+,Fe3O4转化为Fe2+、Fe3+,NiO转化为Ni2+,只有SiO2不反应,则过滤得到的滤渣I为SiO2;
向滤液中加入过氧化氢,过氧化氢与亚铁离子发生氧化还原反应,使Fe2+转化为Fe3+,加入碳酸钠溶液调节溶液pH,使铁离子转化为氢氧化铁沉淀、Ni2+转化为NiCO3沉淀;
过滤,向滤液中继续加入碳酸钠溶液,碳酸钠溶液和硫酸铝溶液发生双水解反应生成Al(OH)3沉淀和硫酸铵;
Al(OH)3沉淀灼烧分解得到氧化铝;
一定条件下电解熔融氧化铝得到Al。
(1)工艺过程中常把废料研细,可以增大废料的表面积,增大与硫酸的接触面积,加快反应速率,使反应更充分,故答案为:
增大接触面积,加快反应速率,使反应更充分,提高原料转化率;
(2)步骤I中加入硫酸,Al2O3、Fe3O4、NiO与硫酸反应,只有SiO2不反应,则过滤得到的滤渣I为SiO2;
步骤V为Al(OH)3沉淀灼烧分解得到氧化铝,故答案为:
SiO2;
分解;
(3)步骤Ⅱ中加入稀双氧水,双氧水与亚铁离子发生氧化还原反应,使Fe2+转化为Fe3+,故答案为:
将Fe2+氧化为Fe3+;
(4)步骤Ⅲ,加入碳酸钠溶液调节溶液pH,使铁离子转化为氢氧化铁沉淀、Ni2+转化为NiCO3沉淀,产生NiCO3的离子方程式为:
Ni2++CO32—=NiCO3↓;
步骤Ⅳ向滤液中继续加入碳酸钠溶液,碳酸钠溶液和硫酸铝溶液发生双水解反应生成Al(OH)3沉淀和硫酸铵,反应的离子方程式为2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑,故答案为:
2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑;
(5)工业上用惰性电极电解熔融氧化铝制备金属铝,阴极上铝离子放电生成金属铝,电极反应式
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 专题 训练 工艺流程
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
