 泸县一中高级高三10班化学流程图题针对训练文档格式.docx
泸县一中高级高三10班化学流程图题针对训练文档格式.docx
- 文档编号:21335313
- 上传时间:2023-01-29
- 格式:DOCX
- 页数:10
- 大小:112.07KB
泸县一中高级高三10班化学流程图题针对训练文档格式.docx
《泸县一中高级高三10班化学流程图题针对训练文档格式.docx》由会员分享,可在线阅读,更多相关《泸县一中高级高三10班化学流程图题针对训练文档格式.docx(10页珍藏版)》请在冰豆网上搜索。
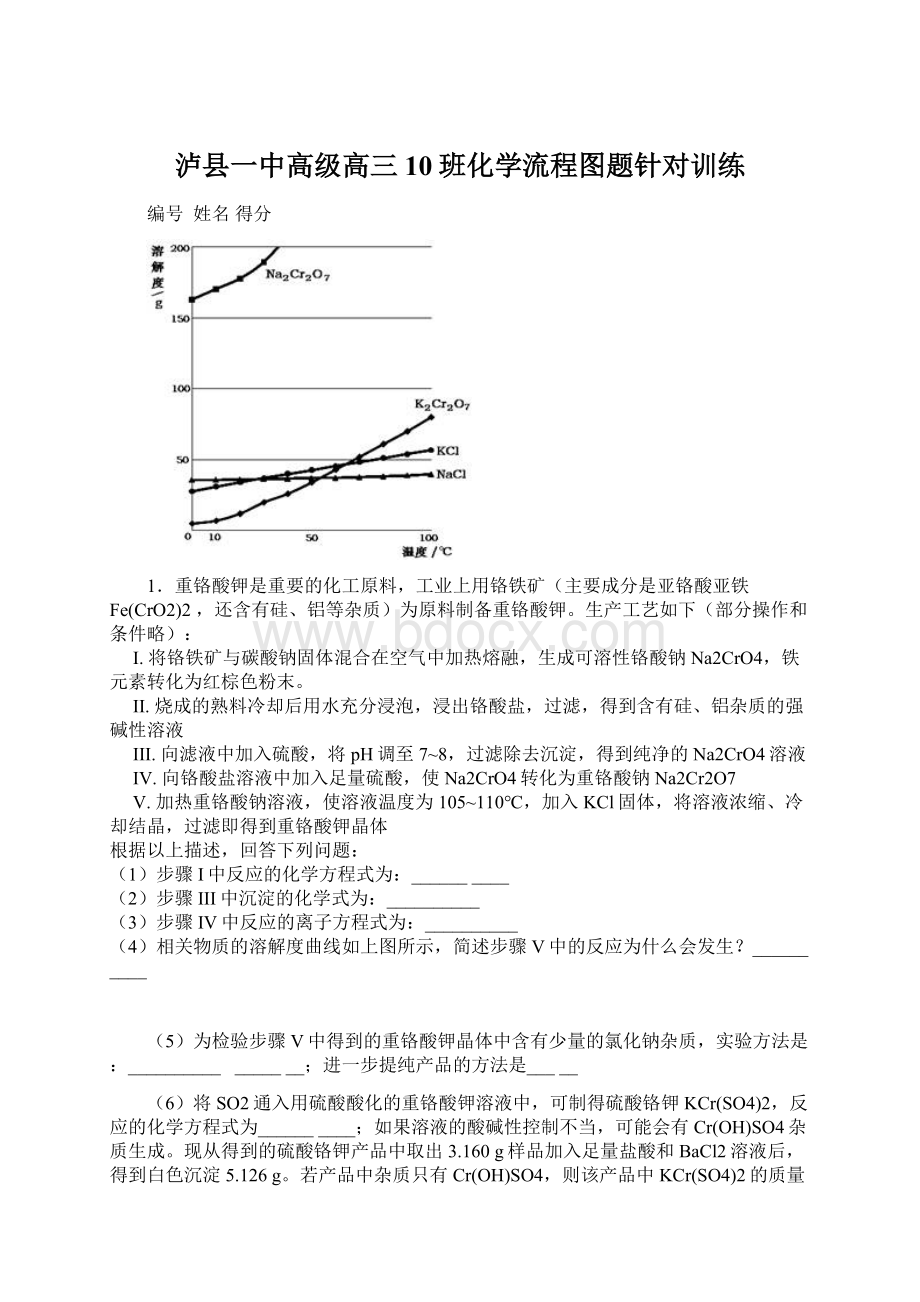
Cr(OH)SO4 165〗
2、四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:
回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。
该过程中有如下反应发生。
2Fe3++Fe===3Fe2+
2TiO2+(无色)+Fe+4H+===2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O===TiO2+(无色)+Fe2++2H+
加入铁屑的作用是____________。
(2)在②→③工艺中需要控制条件以形成TiO2·
nH2O溶胶,该分散质颗粒直径大小在_____________范围。
(3)若把③中制得的固体TiO2·
nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。
已知25℃时,Ksp[Fe(OH)3]=2.79×
10-39,该温度下反应Fe(OH)3+3H+
Fe3++H2O的平衡常数K=_____________。
(4)已知:
TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) △H=+140KJ·
mol-1
C(s)+O2(g)===2CO(g) △H=—221KJ·
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:
_____________。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。
依据绿色化学理念,该工艺流程中存在的不足之处是_____________(只要求写出一项)。
(6)依据右表信息,要精制含少量SiCl4杂质的TiCl4,可采用_____________方法。
TiCl4
SiCl4
熔点/℃
-25.0
-68.8
沸点/℃
136.4
57.6
3、欲降低废水中重金属元素铬的毒性,可将Cr2O72-转化为Cr(OH)3沉淀除去。
已知:
氢氧化物开始沉淀时的pH
氢氧化物沉淀完全时的pH
Fe2+
7.0
9.0
Fe3+
1.9
3.2
Cr3+
6.0
8.0
(1)某含铬废水处理的主要流程如下图所示:
①初沉池中加入的混凝剂是K2SO4﹒Al2(SO4)3﹒24H2O,用离子方程式表示其反应原理是 。
②反应池中发生主要反应的离子方程式是Cr2O72-+3HSO3-+5H+=2Cr3++3SO42-+4H2O。
根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是 、 。
证明Cr3+沉淀完全的方法是 。
(2)工业可用电解法来处理含Cr2O72-废水。
实验室利用如下图模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-=Fe2+,阴极反应式是2H++2e-=H2↑。
Fe2+与酸性溶液中的Cr2O72-反
应的离子方程式是 ,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是 。
用电解法处理该溶液中0.01molCr2O72-时,至少得到沉淀的质量是 g。
4、某电镀铜厂有两种废水需要处理,一种废水中含有CN-离子,另一种废水中含有Cr2O72-离子。
该厂拟定如图19所示的废水处理流程。
回答以下问题:
(1)上述处理废水的流程中主要使用的方法是 。
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因 。
(3)②中反应后无气体放出,该反应的离子方程式为 。
(4)③中反应时,每0.4molCr2O72-转移2.4mole-,该反应的离子方程式为 。
(5)取少量待检水样于试管中,先加入NaOH溶液,观察到有蓝色沉淀生成,继续加入NaOH溶液,直到不再产生蓝色沉淀为止,再加入Na2S溶液,有黑色沉淀生成,且蓝色沉淀逐渐减少。
请你使用化学用语,结合必要的文字解释其原因 。
5、铬铁矿的主要成分可表示为FeO·
Cr2O3,还含有SiO2、Al2O3等杂质,
以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示。
①NaFeO2遇水强烈水解。
②Cr2O72-+H2O
2CrO42-+2H+
请回答:
(1)K2Cr2O7中Cr元素的化合价是 。
(2)生成滤渣1中红褐色物质的反应的化学方程式是 。
滤液1的成分除Na2CrO4外,还含有(填化学式) 。
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是 。
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是 。
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:
加热浓缩、 、过滤、洗涤、干燥。
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是 。
6、金属钛被称为铁和铝之后崛起的“第三金属”,常见化合价为+4。
它是空间技术、航海、化工、医疗上不可缺少的材料。
Ⅰ.工业上用钛铁矿(主要成分FeTiO3)制备金属钛的一种工艺流程如下图(部分产物略去):
(1)步骤①反应的化学方程式为:
2FeTiO3+6C+7Cl2
2FeCl3+2TiCl4+6CO,还原剂是 。
(2)步骤②分离出TiCl4的方法,利用了TiCl4与FeCl3 的不同。
(3)步骤④反应的化学方程式为________________________________,该反应在氩气中进行的理由是______________________________。
(4)绿色化学提倡物料循环。
以上流程中,可用于循环的物质除Cl2、Mg外,还有__________。
II.工业上也可用TiO2通过下述两种方法制备金属钛:
方法一:
先将TiO2氯化为TiCl4,再还原得到Ti。
(5)氯化反应TiO2(s)+2Cl2(g)
TiCl4(l)+O2(g) 无法自发正向进行,在反应器中加入碳,则在高温条件下反应可顺利进行。
试从化学平衡角度解释,往氯化反应器中加碳的原因:
。
方法二:
以熔融盐为电解液电解TiO2获得Ti。
其中,碳块为阳极,电极反应式为:
2O2ˉ–4eˉ=O2↑;
TiO2作阴极,被还原。
(6)阴极的电极反应式为 。
(7)电解过程中需定期向电解槽中加入碳块的原因是 。
7、红矾钠[重铬酸钠,Na2Cr2O7·
2H2O]是重要的基础化工原料。
实验室模拟工业以铬铁矿(主要成分为FeCr2O4,含有Al2O3、SiO2等杂质)为原料生产红矾钠的主要流程如下:
请回答下列问题:
(1)步骤①中的主要反应生成Na2CrO4,反应的化学方程式为
。
步骤①中Al2O3和SiO2均可转化成可溶性盐,写出Al2O3参加反应的化学方程式
(2)步骤③中X的化学式为
,步骤④中滤渣Y的成分是
(3)步骤⑤酸化的离子方程式为
(4)右图是Na2Cr2O7·
2H2O和Na2SO4的溶解度曲线,操作I的步骤是蒸发浓缩,趁热过滤。
趁热过滤的目的是
8、随着铅蓄电池的广泛应用,使回收利用铅资源成为重要课题。
某研究性学习小组利用废旧铅蓄电池阴、阳极填充物(铅膏)制备塑料加工热稳定剂三盐基硫酸铅,实验流程如下:
(1)物质X是一种可循环利用的物质,该物质是 。
(2)生成三盐基硫酸铅的反应的离子方程式为 。
(3)将滤液I和滤液Ⅱ合并后可用来提取一种钠盐副产品(相对分子质量为322),已知副产品带10个结晶水的结晶水合物,则其化学式 ,由滤液提取该副产品的主要实验步骤依次为 、 、过滤、洗涤、干燥。
(4)过滤时洗涤沉淀(或固体)的操作方法是 。
(5)向铅膏浆液中加入Na2SO3溶液的目的是将PbO2还原为PbO,若实验中所取铅膏浆液质量为47.8g,其中PbO2的质量分数为15.0%,要将PbO2还原,至少需要加入 mL1.0mol·
L-1Na2SO3溶液。
9、电镀废水、废渣的处理和综合利用体现了绿色化学思想。
I.可采用以下方法处理含铬电镀废水。
(1)电解法。
往废水中加人适量NaCl,以Fe作电极进行电解。
电解过程中,阳极的电极反应式为_______。
(2)沉淀法。
含铬废水中存在平衡:
Cr2O72-+H2O
2CrO42-+2H+。
往废水中加入BaCl2,铬元素转化为BaCrO4沉淀,此过程中,还应加入NaOH,理由是______________
H.某工厂利用富含镍的电镀废渣(还含Cu、Zn、Fe、Cr等杂质)制备NiSO4•6H2O其生产流程如下图所示:
(3)步骤①中加入H2SO4后,需充分搅拌的目的是_______。
(4)步骤③中,在酸性条件下,H2O2使Fe2+转化为Fe3+的离子方程式为_______。
(5)巳知:
i.Ksp[Fe(OH)3]=2.5×
10-39、Ksp[Cr(OH)3]=6.3×
10-31;
ii.溶液中离子浓度小于10-5mol•L-1可视为沉淀完全。
250℃时,若沉淀E为Fe(OH)3,Cr(OH)3,步骤④中,应控制溶液的pH不小于_______。
(提示:
lg2.5×
10-39=-38.6,lg6.3×
10-31=-30.2)
(6)溶液C中,溶质的主要成分是_______。
10、已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。
因此,必须对含铬的废水进行处理,可采用以下两种方法。
★还原法在酸性介质中用FeSO4等将+6价铬还原成+3价铬。
具体流程如下:
有关离子完全沉淀的pH如下表:
有关离子
Fe2+
Fe3+
Cr3+
完全沉淀为对应氢氧化物的pH
5.6
(1)写出Cr2O72―与FeSO4溶液在酸性条件下反应的离子方程式 。
(2)还原+6价铬还可选用以下的 试剂(填序号)。
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。
则在操作②中可用于调节溶液pH的试剂为:
(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在 (填序号)最佳。
A.3~4 B.6~8 C.10~11 D.12~14
★电解法将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。
阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(4)写出阴极的电极反应式 。
(5)电解法中加入氯化钠的作用是:
。
答案:
1、
(1)4Fe(CrO2)2+8Na2CO3+7O2=====8Na2CrO4+2Fe2O3+8CO2
(2)Al(OH)3 H2SiO3
(3)2CrO42-+2H+==Cr2O72-+H2O
(4)(和Na2Cr2O7相比较,K2Cr2O7的溶解度较小,且)K2Cr2O7的溶解度随温度的变化变化幅度较大,因此在冷却过程中K2Cr2O7能以沉淀形式析出,使复分解反应:
Na2Cr2O7+KCl==K2Cr2O7+NaCl得以发生
(5)取少量重铬酸钾样品,加水溶解,加入足量的硝酸酸化后滴入硝酸银溶液,有白色沉淀生成即说明产品中含有氯化钠杂质;
重结晶
(5)K2Cr2O7+3SO2+H2SO4==2KCr(SO4)2+H2O;
89.6%
2、
(1)使Fe3+还原为Fe2+;
生成Ti3+保护Fe2+不被氧化。
(2)10-9~10-7m(或其它合理答案);
(3)2.79×
103
(4)TiO2(s)+2C(s)+Cl2(g)=TiCl4(l)+2CO(g) △H=—81KJ·
(5)产生三废
(6)蒸馏(或分馏或精馏)
3、
(1)①Al3++3H2O=Al(OH)3(胶体)+3H+ 或Al3++3H2O
Al(OH)3+3H+
②Cr3++3OH-=Cr(OH)3↓、H++OH-=H2O。
测定溶液的pH,若pH≥8,则证明Cr3+沉淀完全。
(2)Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,阴极反应消耗了水中的H+,打破了水的电离平衡,促进了水的电离,使溶液中OH-浓度增大,溶液的碱性增强。
8.48
4、
(1)氧化还原法)
(2)ClO-+H2O
HClO+OH-
(3)CN-+ClO-===CNO-+Cl-
(4)3S2O32-+4Cr2O72-+26H+===6SO42-+8Cr3++13H2O
(5)待检水样中还有Cu2+
Cu2++2OH-===Cu(OH)2↓
Cu(OH)2(s)+S2-(aq)===CuS(s)+2OH-(aq)
CuS比Cu(OH)2更难溶(或溶解度更小)
5、
(1)+6
(2)NaFeO2+2H2O=NaOH+Fe(OH)3↓;
NaAlO2、Na2SiO3和NaOH
(3)2Al2O3(熔融)
4Al+3O2↑
(4)加硫酸酸化(5)冷却结晶
(6)4FeO·
Cr2O3+7O2+20NaOH=8Na2CrO4+4NaFeO2+10H2O
6、
(1)FeTiO3、C
(2)沸点
(3)2Mg+TiCl4
2MgCl2+Ti;
防止Mg、Ti被氧化
(4)MgCl2
(5)碳单质与氧气反应减小产物浓度,平衡不断向右移动,使反应顺利进行
(6)TiO2+4eˉ=Ti+2O2ˉ
(7)碳与阳极产生的氧气反应而不断消耗
7、
(1)4FeCr2O4+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2
Al2O3+Na2CO3
2NaAlO2+CO2↑
(2)CO2
H2SiO3、Al(OH)3
(3)2CrO42-+2H+
Cr2O72-+H2O
(4)有利于Na2SO4结晶析出,又能防止Na2Cr2O7·
2H2O结晶析出而损失
8、
(1)硝酸
(2)4PbSO4+6OH-=3PbO·
PbSO4·
H2O+3SO42-+2H2O
(3)Na2SO4·
10H2O 蒸发浓缩 冷却结晶
(4)沿玻璃棒向漏斗(过滤器)中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复操作数次。
(5)30
9、
(1)Fe-2e-=Fe2+
(2)使平衡Cr2O72-+H2O
2CrO42-+2H+右移,有利于除铬
(3)提高废渣的溶解速率和溶解程度
(4)2Fe2++H2O2+2H+=2Fe3++2H2O
(5)5.6
(6)Na2SO4
10、
(1)Cr2O72―+6Fe2++14H+=2Cr3++6Fe3++7H2O
(2)BD
(3)CD;
B
(4)2H++2e―=H2↑或2H2O+2e―=H2↑+2OH―
(5)增强溶液导电性或盐析
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 泸县 一中 高级 10 化学 流程图 针对 训练
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
