 胶体离子习题教师版Word文档格式.docx
胶体离子习题教师版Word文档格式.docx
- 文档编号:21818291
- 上传时间:2023-02-01
- 格式:DOCX
- 页数:24
- 大小:52.51KB
胶体离子习题教师版Word文档格式.docx
《胶体离子习题教师版Word文档格式.docx》由会员分享,可在线阅读,更多相关《胶体离子习题教师版Word文档格式.docx(24页珍藏版)》请在冰豆网上搜索。
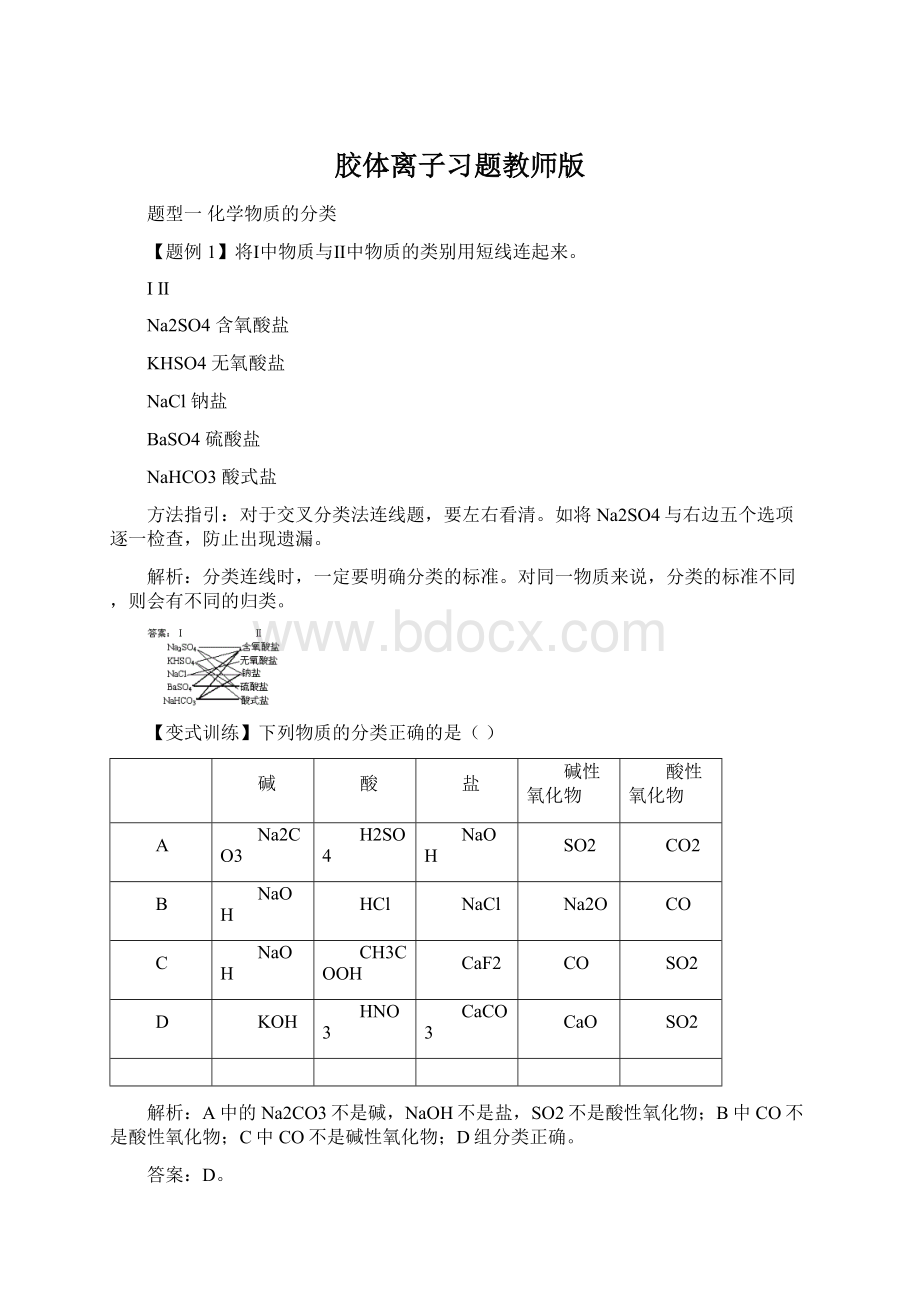
A中的Na2CO3不是碱,NaOH不是盐,SO2不是酸性氧化物;
B中CO不是酸性氧化物;
C中CO不是碱性氧化物;
D组分类正确。
答案:
D。
题型二化学反应的分类
【例题2】下列反应进行分类时(按初中的方法),既属于氧化反应又属于化合反应的是()
A.Zn+H2SO4=ZnSO4+H2↑ B.2KClO3
2KCl+3O2↑
C.S+O2
SO2 D.H2+Cl2
2HCl
根据初中化学中对化学反应的分类方法,物质得到氧的反应称为氧化反应;
由两种或两种以上的物质生成一种物质的反应叫化合反应。
在题目所给出的四个反应中,既属于化合反应又属于氧化反应的应当是C。
C。
【变式训练】下列化学方程式中有一个与其它三个在分类上不同,这个反应是()
A.3Fe+2O2
Fe3O4;
B.CO2+C
2CO;
C.NH4HCO3
NH3↑+H2O+CO2↑;
D.CaCO3+CO2+H2O=Ca(HCO3)2
A、B、D都属于化合反应,只有选项C属于分解反应。
达标体验
1.根据某种共性,可将CO2、SO2归为一类氧化物,下列物质中与它们属于同一类的是()
A.CaCO3B.P2O5C.CuOD.KMnO4
2.下列物质在我们的生活中常见,其中属于氧化物的是()
A.水B.食盐C.食醋D.酒
3.下列物质属于酸的是()
A.NH4ClB.NaHCO3C.NaHSO4D.HNO3
4.下列物质中属于纯净物、化合物、无机化合物、盐、碳酸盐的是( )
A.石灰石 B.Ca(OH)2 C.CaCO3 D.CH4
5.对下列物质进行分类:
HNO3、O2、CO2、CaO、NaOH、Na2SO4、H2SO4、Ca(OH)2。
课时作业
1.Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是( )
A.Na2CO3是碱B.Na2CO3是盐C.Na2CO3是钠盐D.Na2CO3是碳酸盐
2.下列物质中既属于无机物,又属于碱的是( )
A.Na2CO3 B.CH3OHC.CH3CH2OHD.Cu(OH)2
3.下列物质中,是纯净物的是()
A.冰水混合物B.用排空气法收集的二氧化碳
C.天然气D.纯净的没有污染的空气
4.某物质经分析,只含一种元素,则此物质(0
A.一定是纯净物B.一定是一种单质
C.一定是混合物D.可以是纯净物也可能是混合物
5.对于反应A+B===C+D来说,下列说法错误的是()
A.若生成物C、D分别为氯化钙和水,该反应一定是中和反应
B.若A、C为单质,B、D为化合物,该反应一定是置换反应
C.若A为可溶性碱,B为可溶性盐,则该反应可能是复分解反应
D.参加反应的A、B的质量之和一定等于生成的C、D的质量之和
6.农药波尔多液不能用铁或铝的容器贮存,是因为铁或铝能跟该农药中的硫酸铜发生化学反应,该反应属无机物反应基本类型中的()
A.置换反应B.分解反应C.化合反应D.复分解反应
7.只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称为氢化物。
下列物质不属于氢化物的是()
A.H2OB.NH3C.NaHD.H2SO4
8.按单质、氧化物、酸、碱、盐分类,下列各组中,两种物质的类别相同的是()
A.氧气、氧化镁B.硫酸铜、氯化钠C.硫酸、硫酸钠D.硝酸银、氢氧化钠
9.每组中都有一种物质与其他几种物质在分类上不同,试分析每组物质组成上的规律,将这种不同于其它物质的物质找出来。
⑴NaCl、KCl、NaClO3、BaCl2⑵HClO3、KClO3、Cl2、NaClO3
⑶H3PO4、HNO3、HCl、H2SO4⑷空气、N2、HCl气体、CuSO4·
5H2O
10.现有铁、稀硫酸、碳、碳酸钠、氧气、氢氧化钠6种物质。
⑴以这6种物质作反应物,写出它们相互反应的化学方程式:
。
⑵将这六种物质和⑴中发生的化学反应后所得生成物,按不同分类方法进行分类。
参考答案达标体验:
1.解析:
CaCO3和KMnO4属于盐类;
CuO属于金属氧化物;
而CO2、SO2属于非金属氧化物,故P2O5属于同类。
2.解析:
水的成分为H2O;
食盐的成分是NaCl;
食醋是CH3COOH的水溶液;
而酒是的C2H5OH水溶液。
3.解析:
酸是指电离时生成的阳离子全部是H+的化合物,只有D符合;
而A、B、C都属于盐类物质。
4.解析:
石灰石是混合物,它的主要成分是CaCO3。
Ca(OH)2是碱,CH4是有机物,故正确选项应为C。
5.解析:
根据不同标准,可以对物质进行不同的分类。
方法
(1)根据化学物质的属类:
单质:
O2酸:
HNO3、H2SO4碱:
NaOH、Ca(OH)2盐:
Na2SO4氧化物:
CO2、CaO
方法
(2)根据物质的状态:
气体:
O2、CO2液体:
HNO3、H2SO4固体:
CaO、NaOH、Na2SO4、Ca(OH)2。
所谓碱是指电离时生成的阴离子全部是氢氧根离子的化合物叫做碱;
而盐是指电离时生成金属离子和酸根离子的化合物叫做盐。
由Na2CO3的电离方程式Na2CO3=2Na++CO32-知Na2CO3应该属于盐,而不属于碱。
Na2CO3是无机物,但属于盐;
CH3OH和CH3CH2OH为有机物;
Cu(OH)2为碱且为无机物,故答案应选D。
3。
不论是冰还是水都是由H2O组成的,因此冰水混合物仍然是纯净物;
用排空气法收集的二氧化碳气体一定会混有空气,因此是混合物;
天然气的主要成分是甲烷,因此是混合物;
空气不论是否被污染都属于混合物。
既然该物质只含有一种元素,说明这种物质一定不是化合物;
由于一种元素可以形成多种单质,例如金刚石和石墨都是由碳元素构成的,单二者混合在一起确是混合物。
做这类试题一般采用举例排除法。
例如CaO+2HCl===CaCl2+H2O不属于中和反应。
因此A不正确。
6.解析:
由于铁或铝的活泼性比铜要强,因此它们可以把铜从其溶液中置换出来,反应的方程式为:
Fe+CuSO4=Cu+FeSO4.。
7.解析:
由题意知氢化物必须是由两种元素组成的,而硫酸是由三种元素组成的构成的二元酸。
8.解析:
考查有关概念的理解。
硫酸铜、氯化钠都属于盐类,因此符合题意。
9.解析:
先仔细分析每组中各物质在元素组成、化合价上的特点,找出其相似性,即可找出那一种不同的物质。
⑴只有NaClO3不是氯化物,它是钠盐,其中的氯元素的化合价也不同于其它物质。
⑵只有Cl2中的氯的化合价为0价,其它物质中的均为+5价。
⑶只有盐酸为无氧酸。
⑷只有空气为混合物,其它物质均为纯净物。
10.答案:
⑴3Fe+2O2
Fe3O4C+O2
2COC+O2
Fe+H2SO4===FeSO4+H2↑H2SO4+2NaOH===Na2SO4+2H2O
H2SO4+Na2CO3===Na2SO4+CO2↑+H2O
⑵树状分类法分类:
纯净物可分为单质、化合物。
单质可分为:
金属(Fe);
非金属(C、O2)
化合物可分为:
氧化物(CO2、CO、H2O、Fe3O4);
酸(H2SO4);
碱(NaOH);
盐(FeSO4、Na2CO3、Na2SO4)
交叉分类法分类:
盐可以分为:
硫酸盐、碳酸盐、亚铁盐、钠盐。
题型一、分散系的分类
【例题1】用特殊方法把固体物质加工到纳米级(1~100nm)的超细粉末粒子,然后得到纳米材料。
下列分散系中的分散质微粒直径
和这种粒子具有相同数量级的是()。
A.溶液B.悬浊液C.胶体D.乳浊液
胶体与溶液、浊液本质的区别在于分散质微粒大小不同,溶液中的溶质粒子通常小于1nm,浊液中的粒子通常大于100nm,而胶体粒子大小介于1nm~100nm之间。
选项C正确。
【变式训练】根据中央电视台报道,近年来,我国的一些沿江或沿海城市多次出现大雾天气,致使高速公路关闭,航班停飞,雾属于下列分散系中的( )
A.溶液 B.悬浊液 C.乳浊液 D.胶体
雾、云、烟都是分散剂为气体的胶体,即气溶胶。
故应选择答案D。
题型二、胶体
【例题2】FeCl3溶液和Fe(OH)3胶体具有的共同性质是( )
A.都能透过滤纸 B.都呈红褐色C.具有相同的颗粒直径 D.都比浊液稳定
溶液和胶体粒子都能透过滤纸。
FeCl3溶液呈棕黄色,Fe(OH)3胶体呈红褐色。
FeCl3溶液中,Fe3+和C1-直径都小于1nm,而Fe(OH)3胶粒是由许多分子组成的,直径在1nm~100nm之间。
AD。
【体验4】区别溶液和胶体的最简单的方法是( )
A.观察外观 B.丁达尔效应C.看能否透过滤纸 D.加热
利用丁达尔效应鉴别胶体和溶液是最简单易行的方法,故本题答案应选B。
B。
【例题】胶体区别于其他分散系的本质特征是(
)。
A、比较稳定B、产生丁达尔现象C、胶体微粒不能穿透半透膜D、分散质直径在10-7~10-9m之间
胶体的本质特征是胶体颗粒的大小,其他的性质都是由此而决定的,因此本题答案应选D。
1.下列分散系最稳定的是()
A、悬浊液B、乳浊液C、胶体D、溶液
2.下列分散系属于溶液的是()
A、牛奶B、豆浆C、白糖水D、肉汤
3.下列分散系能产生丁达尔效应的是()新课标第一网
A.食盐水B.酒精溶液C.淀粉溶液D.Fe(OH)3溶胶
4.下列关于胶体的说法正确的是()
A.胶体外观不均匀B.胶粒不能透过滤纸C.胶体一定是混合物D.胶体一定是液体。
5.NaCl溶于水形成溶液,如果NaCl分散在汽油中,形成的分散系是()
A.溶液B.胶体C.悬浊液D.乳浊液
1.用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是()
A.FeCl3溶液滴入蒸馏水中即可
B.将FeCl3溶液滴入热水中,生成棕黄色液体即可
C.将FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色液体即可
D.将FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可。
2.关于胶体的叙述,不正确的是()
A.有色玻璃是固溶胶
B.雾、云、烟都是气溶胶
C.用滤纸能把胶体中的分散质与分散剂分离
D.胶粒大小在1~100nm之间。
3.关于胶体和溶液的区别,下列叙述中正确的是( )
A.溶液呈电中性,胶体带有电荷
B.溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
C.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明显光带
D.溶液稳定,放置后不会生成沉淀;
胶体不稳定,放置会生成沉淀
4..下列实验可以制备胶体的是()
A.把1gKCl加入到10g沸腾的水中,充分振荡
B.把0.1g植物油加入到10g水中,充分振荡
C.把1mL饱和FeCl3溶液逐滴加入20mL沸水中,充分振荡
D.把1gCaCO3粉末加入到100g水,充分振荡
5.“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀
A.①④⑤ B.②③④ C.②③⑤ D.①③④⑥
6.向胶体中加入电解质(溶于水或受热熔化时能电离的化合物),能使胶体聚沉。
使一定量的胶体在规定的时间内开始凝聚所需的电解质的浓度(mmol·
L-1)称作“聚沉值”。
电解质的聚沉值越小,则表示其凝聚能力越大,实验证明,凝聚主要取决于与胶体粒子带相反电荷的离子所带的电荷数,电荷数越大,凝聚能力越大,则向Fe(OH)3胶体中加入下列物质时,其“聚沉值”最小的为()
A.NaOHB.AgNO3C.BaCl2D.Na3PO4
7.半透膜与滤纸一样有许多小孔,但孔径比滤纸小,只能通过较小的离子和分子,胶体分散质不能通过半透膜。
现把10mL淀粉胶体和5mLKCl溶液的混合液体加入用半透膜制成的袋内,将此袋浸入蒸馏水中。
2min后,用两支试管各取5mL烧杯中的液体,并做如下实验。
(1)向其中一支试管里滴加少量AgNO3溶液,其现象是。
(2)向另一支试管里滴加少量碘水,其现象是。
(3)由上述实验得出的结论是。
8.在制取Fe(OH)3胶体的实验中,为何不能搅拌或长时间加热?
9.如何鉴别溶液、胶体和浊液等分散系?
10.教材中在介绍胶体的应用时,有“用明矾净水”的说法。
如何证明明矾溶于水时生成了胶体?
参考答案达标体验
考查三种分散系的稳定性。
牛奶和豆浆属于胶体;
肉汤属于浊液。
胶体能产生丁达尔效应,而溶液不能。
A、B属于溶液,C、D属于胶体。
C、D。
胶体是均一的,故A不对;
胶粒能够透过滤纸,故B不对;
胶体是分散系的一种,而分散系都是混合物,故C正确;
胶体可以是液溶胶,也可以是气溶胶、固溶胶,故D不对。
C。
NaCl溶于水,但不溶于汽油,所以NaCl分散到汽油中形成的分散系为悬浊液。
Fe(OH)3胶体制备的要点是“向沸水中滴入饱和氯化铁溶液,并继续煮沸至溶液呈红褐色。
胶体中的分散质和分散剂都能通过滤纸。
分散系都是电中性的;
胶体与溶液都可以透过滤纸;
胶体比较稳定。
A形成的是溶液;
B形成的是乳浊液;
D形成的是悬浊液。
由于纳米碳的粒子直径为1~100nm,因此属于胶体,应该具备胶体的性质。
本题中的关键信息是“电解质的聚沉值越小,则表示其凝聚能力越大,实验证明,凝聚主要取决于与胶体粒子带相反电荷的离子所带的电荷数,电荷数越大,凝聚能力越大”,又知,Fe(OH)3胶体粒子带正电荷,起聚沉作用的是选项中的阴离子,所带电荷最大的是PO43-,带三个负电荷。
点评:
信息题的解题关键是把握好题给的信息,从中提取出有用的信息加以利用。
半透膜有非常细小的孔,只允许较小的离子、分子透过,胶体分散质的粒不能透过半透膜,故在烧杯中的液体中有k+、Cl-,不存在淀粉胶体。
(1)出现白色沉淀;
(2)无明显变化;
(3)Cl-能透过半透膜,淀粉胶体粒子不能透过半透膜。
胶体聚沉的方法通常有三种:
加热、搅拌、中和胶体粒子所带的电荷。
长时间加热和搅拌都会使胶体发生聚沉。
溶液、胶体和浊液都是一种(或多种)物质(分散质)分散在另一种(或多种)物质(分散剂)中所得到的体系,即分散系。
但它们也有许多不同之处。
从稳定性来看,溶液很稳定,浊液最不稳定,胶体则介于二者之间。
另外,只有胶体会出现“丁达尔效应”。
静置,分散质和分散剂很快分离的是浊液;
用一束光照射另两种分散系,出现一条明亮“光路”的为胶体,另一种为溶液。
10.解析:
当光束通过胶体时,可以看到一条光亮的通路,而光束通过其它分散系时,则看不到此现象,这是胶体区别于其它分散系的特征性质,可以用聚光束仪做丁达尔效应实验,如有丁达尔效应发生,就证明明矾溶于水时生成了胶体。
用聚光束仪做丁达尔效应实验,如有丁达尔效应发生,就证明明矾溶于水时生成了胶体。
题型一、电解质和非电解质
【题例1】下列说法正确的是()
A.凡是能导电的物质都是电解质
B.电解质溶液能导电的原因是溶液中有自由移动的离子
C.盐酸能导电的原因是在电流作用下电离产生了自由移动的离子的缘故
D.凡是能电离的物质一定能导电
本题包含的知识是电解质和非电解质两概念,以及溶液的导电性。
解题时要抓住概念中的“或”、“和”、“化合物”等关键词以及电解质电离的条件。
对答案A可以用熟知的金属单质和石墨等能导电的单质来判断;
C和D需抓住电解质电离的条件:
溶于水或熔融状态时发生电离,与通电与否无关。
选B。
本题关键是对电离、电解质和非电解质等几个基本概念的考查,要求同学们要从细微处把握概念的内涵和外延。
【变式训练】下列化合物中,只有在溶液中才能导电的电解质是()
A.NaClB.C2H5OHC.H2SO4D.NH4HCO3
注意两个限定条件:
(1)是电解质;
(2)只有在溶液中;
B是非电解质,而D在溶液中能导电但受热时会分解,即在熔融状态下不能实现导电,本题选C、D。
CD。
题型二、电离和电离方程式
【例题2】下列物质中,导电性能最差的是( )
A.熔融的氢氧化钠 B.石墨棒C.盐酸溶液 D.固态氯化钾
固态氯化钾不导电,因为无自由移动的离子。
【变式训练】把0.05molNaOH晶体分别加入到下列100mL液体中,溶液导电性变化较大的是( )
A.自来水 B.0.5mol·
L-1盐酸C.0.5mol·
L-1H2SO4 D.0.5mol·
L-1NaNO3
电解质溶液的导电能力取决于溶液中的离子浓度。
离子浓度大则导电能力强。
题中B、C反应后离子浓度变化不大,所以导电性变化不大,A、D中加入NaOH没有化学反应发生,但离子浓度变化较大。
AD
【例题】下列可用来区分离子化合物和共价化合物的是()
A.化合物在水中的溶解性B.水溶液的导电性C.熔融状态时的导电性D.常温时的状态
选项A、B、C是两类化合物都可能具有的性质,只有C是离子化合物独有,而大多数共价化合物不具有的性质。
1.下列物质属于电解质的是()
A.氨B.氯化氢C.硫酸钡D.铜
2.下列物质中,不能电离出酸根离子的是()
A.Na2SB.Ba(OH)2C.KMnO4D.KCl
3.关于酸、碱、盐的下列各种说法中,正确的是()
A.化合物电离时,生成的阳离子是氢离子的是酸
B.化合物电离时,生成的阴离子是氢氧根离子的是碱
C.化合物电离时,生成金属阳离子和酸根离子的是盐
D.NH4Cl电离的电离方程式是:
NH4Cl=NH4++Cl-,所以NH4Cl是盐
4.下列电离方程式不正确的是
A.H2SO4=2H++SO42- B. NH4NO3=NH4++NO3-C. Na2CO3=Na2+ +CO32-D.Ba(OH)2=Ba2++2OH-
5.下列物质哪些是电解质?
哪些是非电解质?
哪些能导电?
①金属铜②固态NaCl③O2④H2SO4⑤碳棒⑥酒精水溶液⑦KOH水溶液⑧熔融状态的KNO3 ⑨葡萄糖
1.对电解质的叙述正确的是( )
A.溶于水后得到的溶液能导电的物质 B.熔融态能导电的物质
C.不是电解质就是非电解质 D.在水溶液中或熔融状态下能导电的化合物
2.下列物质既能导电又是强电解质的是()
A.氯化钠溶液 B.氢氧化钠晶体C.熔融的硝酸钾 D.液态氯化氢
3.下面的说法正确的是()
A.硫酸钡不溶于水,所以硫酸钡是非电解质
B.二氧化碳溶于水可以导电,所以,二氧化碳是电解质
C.硫酸是电解质,所以硫酸在熔化时或溶于水时都能导电
D.液态氯化氢不能导电,但氯化氢是电解质
4.下列电离方程式错误的是()
ANaHCO3====Na++H++CO32―BNaHSO4====Na++H++SO42―
CMgCl2====Mg2++2Cl―DBa(OH)2=====Ba2++2OH―
5.NaHSO4在水溶液中能够电离出H+、Na+、和SO42-。
对于NaHSO4的分类不正确的是()
A.NaHSO4是盐B.NaHSO4是酸式盐C.NaHSO4是钠盐D.NaHSO4是酸
6.今有一种固体化合物X,X本身不导电,但熔化状态或溶于水中能够电离,下列关于该化合物X的说法中正确的是()
A.X是一定为电解质B.X可能为非电解质C.X只能是盐D.X可以是任何化合物
7.下面关于电解质的叙述中错误的是()
A.在水溶液中或熔融状态下均不导电的化合物叫非电解质
B.电解质、非电解质都指化合物而言,单质不属于此范畴
C.电解质在水中一定能导电,在水中导电的化合物一定是电解质
D.纯水的导电性很差,所以水不是电解质
8.在电解质溶液中,下列叙述正确的是()
A.阳离子和阴离子数目一定相等
B.阳离子带的正电荷总数一定和阴离子带的负电荷总数相等
C.除阴、阳离子外,溶液中不会再有其它粒子
D.电解质溶液的导电性一定很强
9.下列物质容易导电的是()
A、熔融的氯化钠B、硝酸钾溶液C、硫酸铜晶体D、无水乙醇
10.(选做)实验表明,氯化氢在水中完全电离,醋酸在水中部分电离。
相同体积的的0.1mol·
L-1的盐酸和醋酸溶液所含有的H+多少不同。
因此当这两种酸分别与金属镁反应时产生氢气的速率不同,两种溶液的导电能力也不一样。
人们把在水溶液中能完全电离的电解质称为强电解质,如强酸(H2SO4、HNO3、HCl)、强碱[NaOH、KOH、Ba(OH)2]、盐(NaCl、KNO3、CuSO4)等。
在水溶液中只部分电离的电解质称为弱电解质,如弱酸(H2CO3、CH3COOH)、弱碱(NH3H2O)等。
水是一种极弱的电解质。
读后有思:
下列物质中:
①NaCl溶液②氢氧化钠③二氧化碳④氯化氢⑤水⑥酒精⑦CaCO3,属于电解质的是______________;
非电解质是_____________;
强电解质是__________________;
弱电解质是__________________。
此题考查电解质的概念。
因发生化学反应生成物导电的是非电解质,因此A中NH3不符合题意,即要求电解质须本身电离;
单质既不是电解质也不是非电解质。
因此D中铜不符合题意。
BC。
Ba(OH)2属于碱,电离出的阴离子是氢氧根离子,而不是酸根离子。
A说法不符合酸的概念,生成的阳离子不一定全部是H+,如NaHSO4电离出的阳离子中有H+,还有Na+,其不是酸,而是一种盐——酸式盐;
B的说法与A一致,可从碱式盐,如Cu2(OH)2CO3;
对于D要注意NH4+的性质与金属离子相似,所以
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 胶体 离子 习题 教师版
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
