 还没修改Word格式文档下载.docx
还没修改Word格式文档下载.docx
- 文档编号:22591767
- 上传时间:2023-02-04
- 格式:DOCX
- 页数:9
- 大小:60.62KB
还没修改Word格式文档下载.docx
《还没修改Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《还没修改Word格式文档下载.docx(9页珍藏版)》请在冰豆网上搜索。
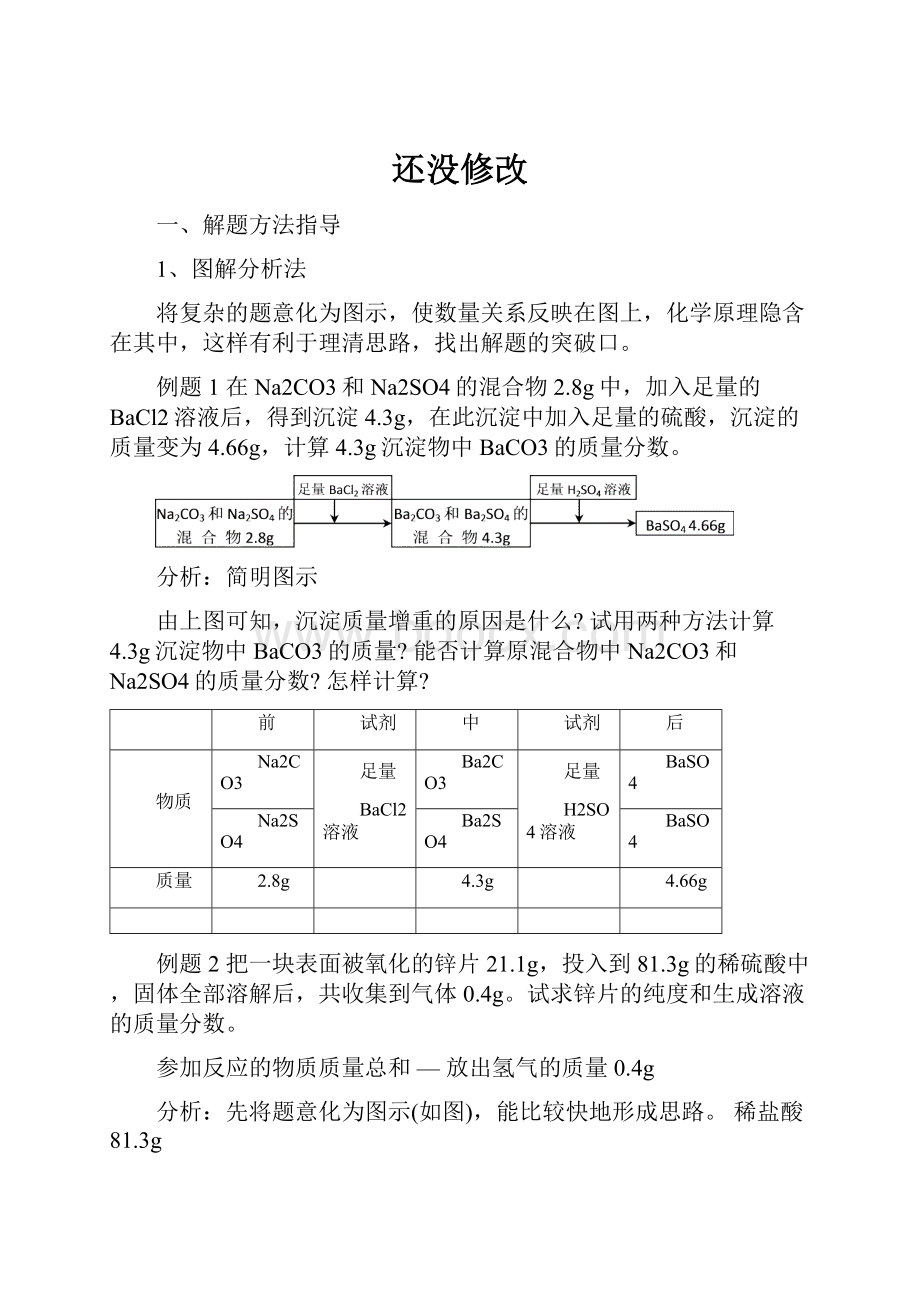
Ba2CO3
H2SO4溶液
BaSO4
Na2SO4
Ba2SO4
质量
2.8g
4.3g
4.66g
例题2把一块表面被氧化的锌片21.1g,投入到81.3g的稀硫酸中,固体全部溶解后,共收集到气体0.4g。
试求锌片的纯度和生成溶液的质量分数。
参加反应的物质质量总和—放出氢气的质量0.4g
先将题意化为图示(如图),能比较快地形成思路。
稀盐酸81.3g
21.1g
锌
氧化锌
81.3g+21.1g-0.4g
恰好完全反应反应后溶液的质量
2、分层解析法
有些计算题比较复杂,条件又多,条件之间虽有联系,却各有其独立性,此时可用分层解析法。
将试题剖析为几个层次,层层分析,分层突破,然后抓住各层题意间的内在联系,形成完整的解法。
例题373g溶质质量分数为10%的盐酸溶液,跟80g一定溶质质量分数的氢氧化钠溶液恰好完全反应,将反后的溶液蒸发掉108.8g水后,冷却至20℃,溶液正好达到饱和。
求:
①20℃时此反应后所得溶液中溶质的溶解度。
②氢氧化钠溶液的溶质质量分数。
此题应综合运用根据化学方程式的计算,溶解度计算,溶质质量分数的计算等多种计算方法,逐步展开解题思路。
第一步:
由盐酸和氢氧化钠溶液的反应确定生成物及其质量。
同时可计算出NaOH溶液的溶质质量分数。
(根据化学方程式的计算)。
第二步:
先由题意“恰好”完全反应,可知最后所得溶液的溶质只有。
再计算所得溶液的质量(在此应注意什么?
)
第三步:
由题意再计算出最后所得饱和溶液的质量,进一步计算出生成物的溶解度(有关溶解度的计算)。
例题4将NaOH和Na2CO3的混合物,放入45.1g盐酸中,恰好完全反应,测得反应后溶液的密度为1.175g/cm3。
将所得溶液分成两等份。
从一份中取出4mL,加入硝酸银溶液,直到不能继续产生沉淀为止,得到14.35g沉淀物,另一份蒸发掉10g水后,其溶质质量分数为29.25%,试计算原混合物中NaOH的质量分数。
一般综合性强,难度大的综合性题目,都是由基础题组成演变而成的。
如果抓住综合题的组合演变特点,将其分解成若干个从基本题目扩展的习题组,解题就会“柳暗花明又一村”。
本题可分解成以下3个基本题:
(1)取密度为1.175g/cm3的NaCl溶液4mL,加入硝酸银溶液,到不能继续产生沉淀为止,得到14.35g沉淀物,求该溶液的溶质质量分数。
(答:
23.4%)
(2)将一定量的23.4%NaCl溶液蒸发掉10g水后,溶液浓缩为29.25%,试计算原溶液的质量。
50g)
(3)将一定量的NaOH和Na2CO3的混合物,放入45.1g盐酸中,待恰好完全反应后,所得溶液的质量为50g,溶质质量分数为23.4%。
试计算NaOH和Na2CO3各多少克?
NaOH:
4g、Na2CO3:
5.3g)
二、题型分类指导
1.评价型计算题
例1.景色秀丽的洪泽湖畔,矿产资源十分丰富,本地所产优质元明粉供不应求。
元明粉的主要成分是Na2SO4,广泛用于洗涤、玻璃、造纸等行业,下表为元明粉的主要质量标准:
质检人员为确定某批产品的质量等级,进行了下列实验:
称取元明粉样品28.6g(杂质为可溶性氯化物),加适量的水使其完全溶解,再向其中加入20%的BaCl2溶液至不再产生沉淀,过滤、洗涤、干燥,得白色沉淀46.6g。
(1)通过计算确定该产品的质量等级最高可定为哪一级?
(2)反应中共消耗20%的BaCl2溶液多少克?
解析:
本题是一道有关产品等级评价的考题。
解题的关键是求得样品中Na2SO4的质量分数,再与所给标准比较,便可得出答案。
解:
设样品中所含Na2SO4的质量为x,反应中共消耗20%的BaCl2溶液的质量为y。
根据题意得:
142208233
x46.6g
样品中Na2SO4的质量分数为:
,因此该产品属于特等品。
答:
(1)该产品属于特等品。
(2)反应中共消耗20%的BaCl2溶液的质量为208g。
2.表格数据分析型计算题
例2.某同学去我市的道场山风景区游玩时,取回了若干块矿石样品,它采用了以下的方法对样品中碳酸钙的质量分数进行检测:
取这种石灰石样品6g,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中的杂质不溶于水,不与盐酸反应)。
求:
(1)6g石灰石样品中含有的杂质为_____________;
(2)m=____________;
(3)样品中CaCO3的质量分数;
(4)所用稀盐酸的质量分数。
解答本题的关键是分析表中所给数据之间的关系,并做出正确的判断。
(1)通过表中次序3和次序4的数据比较,可判断此时的石灰石中CaCO3已完全反应,且其中所含杂质的质量为0.6g,所含CaCO3的质量为:
6g-0.6g=5.4g;
(2)第一次加入10g盐酸,反应后剩余固体的质量为4.0g,说明10g盐酸消耗了2gCaCO3,因此第二次加入10g盐酸后所消耗CaCO3的质量可以最多为4g,;
(3)样品中CaCO3的质量分数为:
5.4g/6g×
100%=90%。
(4)设所用稀盐酸的质量分数为x。
10073
2g10g·
x
(提示:
计算稀盐酸的溶质质量分数时,只能用前两次所用盐酸中的任一次,不能根据第三次或第四次盐酸的质量计算,因为这两次盐酸有剩余。
(1)6g石灰石样品中含有的杂质为0.6g;
(2)m=2g;
(3)样品中CaCO3的质量分数为90%;
(4)所用稀盐酸的质量分数为14.6%。
3.图像型计算题
例3.研究性学习课题:
探究实验室中久置NaOH的变质程度。
研究方案:
先称取13.3gNaOH样品(杂质为Na2CO3),配制成溶液,然后向溶液中逐滴加入溶质质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度。
解决问题:
实验测得加入稀盐酸的质量与产生CO2气体的质量关系如下图所示:
填写下表:
(计算结果保留一位小数)
继续探究:
计算实验过程中与NaOH反应消耗盐酸的质量。
发现问题:
根据求得的与NaOH反应消耗盐酸的质量,对照图像,你发现了什么问题?
此题为一道研究型考题,解题的关键是正确分析图像中有关数据的涵义。
13.3gNaOH样品与足量盐酸反应,最多可生成2.2gCO2,设其中所含Na2CO3的质量为x。
10644
x2.2g
则样品中NaOH的质量为:
设生成5.3gNa2CO3需NaOH的质量为y。
80106
y5.3g
y=4g 未发生变质时NaOH的总质量为:
8g+4g=12g
所以NaOH的变质程度为:
设与8gNaOH反应消耗盐酸的质量为z。
4036.5
8g
比较图像中的横轴数据便会发现问题:
NaOH被盐酸中和后,继续滴加盐酸,为什么没有立即产生CO2气体等。
4.信息型计算题
例4.为测定混有少量氯化钠的碳酸氢钠(NaHCO3)固体的质量分数,现进行如下实验:
向盛有13.6g该混合物的烧杯中加入109.5g稀盐酸,恰好完全反应。
反应的化学方程式为:
。
反应过程中用精密仪器测得烧杯和药品的质量与反应时间的数据记录如下:
(1)混合物中NaHCO3的质量分数是__________,计算步骤为_________。
(2)反应后所得溶液中溶质的质量分数为___________,计算步骤为__________。
本题是一道信息型计算考题,其信息为碳酸氢钠(NaHCO3)与盐酸反应的化学方程式:
,由此可知,反应后所得溶液中的溶质为NaCl,分析表中数据可知:
完全反应后产生CO2的质量为:
(1)设混合物中NaHCO3的质量为x,该NaHCO3与盐酸反应时生成NaCl的质量为y。
8458.544
xy6.6g
混合物中NaHCO3的质量分数为:
混合物中NaCl的质量为:
反应后所得溶液中NaCl的质量为:
;
反应后溶液的质量为:
所得溶液中溶质的质量分数为:
5.实验型计算题
例5.某课外活动小组在研究“氧气对生物体生命活动的影响”时,需要制取一定量的氧气。
(1)下列是该小组的同学设计的几种制取氧气的装置及选用的试剂,其中错误的是()
ABCD
(2)他们在实验中需要制取氧气的质量为0.96g,若让你选择,你会选择上图中的哪种实验方法?
所需试剂的质量是多少?
(1)用加热高锰酸钾制取氧气时,试管口应略向下倾斜,因此选项B是错误的。
(2)本题是一道开放性试题,方案有以下几种情况。
方案一:
选择高锰酸钾作为制取氧气的试剂
设需高锰酸钾的质量为x。
31632
x0.96g
方案二:
选择15%的过氧化氢溶液作为制取氧气的试剂
设需要15%的过氧化氢溶液的质量为x。
6832
0.96g
需要15%的过氧化氢溶液13.6g。
方案三:
选择5%的过氧化氢溶液作为制取氧气的试剂(解法与方案二相似,答案为40.8g,解题过程略)
综上所述,综合计算题情境较复杂,同学们一定要注意把定性思考和定量计算结合起来,要善于透过现象来抓反应的本质,对于信息题及联系实际的计算题,解题关键在于审题,从题目所给信息分析利用哪部分知识可以解决问题。
图像型和表格型的计算题中已知数据大部分以图像或表格数据的形式出现,具有一定的隐蔽性,解答这类题的关键是通过分析图像涵义以及对表格中的数据做横向、纵向比较等方法,挖掘出隐含在图像或表格中的已知条件,再进行解答。
另外,要注意解题过程的完整性。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 修改
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
