 药物临床试验英文缩写.docx
药物临床试验英文缩写.docx
- 文档编号:26050656
- 上传时间:2023-06-17
- 格式:DOCX
- 页数:16
- 大小:21.11KB
药物临床试验英文缩写.docx
《药物临床试验英文缩写.docx》由会员分享,可在线阅读,更多相关《药物临床试验英文缩写.docx(16页珍藏版)》请在冰豆网上搜索。
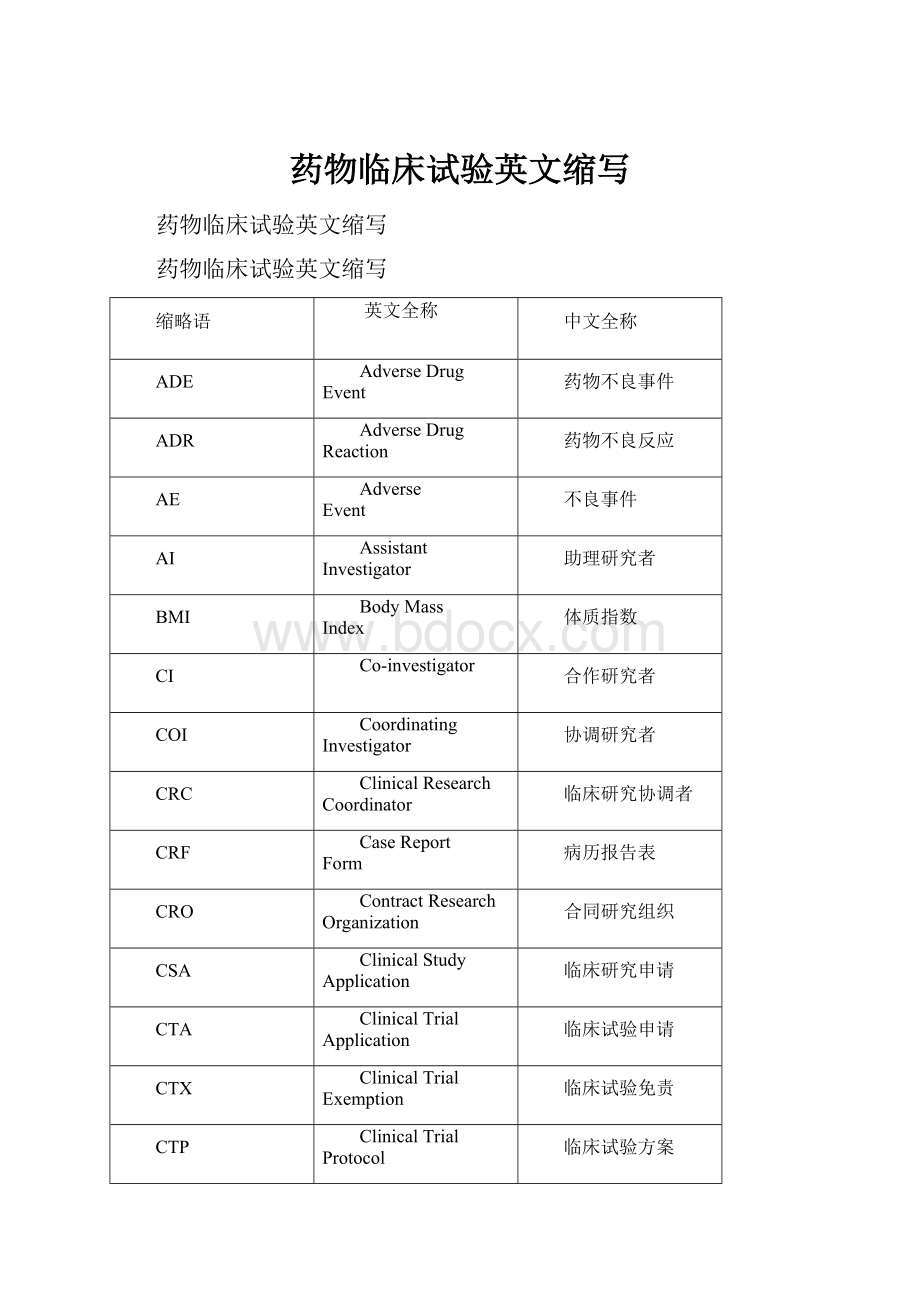
药物临床试验英文缩写
药物临床试验英文缩写
药物临床试验英文缩写
缩略语
英文全称
中文全称
ADE
AdverseDrugEvent
药物不良事件
ADR
AdverseDrugReaction
药物不良反应
AE
AdverseEvent
不良事件
AI
AssistantInvestigator
助理研究者
BMI
BodyMassIndex
体质指数
CI
Co-investigator
合作研究者
COI
CoordinatingInvestigator
协调研究者
CRC
ClinicalResearchCoordinator
临床研究协调者
CRF
CaseReportForm
病历报告表
CRO
ContractResearchOrganization
合同研究组织
CSA
ClinicalStudyApplication
临床研究申请
CTA
ClinicalTrialApplication
临床试验申请
CTX
ClinicalTrialExemption
临床试验免责
CTP
ClinicalTrialProtocol
临床试验方案
CTR
ClinicalTrialReport
临床试验报告
DSMB
DataSafetyandmonitoringBoard
数据安全及监控委员会
EDC
ElectronicDataCapture
电子数据采集系统
EDP
ElectronicDataProcessing
电子数据处理系统
FDA
FoodandDrugAdministration
美国食品与药品管理局
FR
FinalReport
总结报告
GCP
GoodClinicalPractice
药物临床试验质量管理规范
GCP
GoodLaboratoryPractice
药物非临床试验质量管理规范
GMP
GoodManufacturingPractice
药品生产质量管理规范
IB
Investigator’sBrochure
研究者手册
IC
InformedConsent
知情同意
ICF
InformedConsentForm
知情同意书
ICH
InternationalConferenceonHarmonization
国际协调会议
IDM
IndependentDataMonitoring
独立数据监察
IDMC
IndependentDataMonitoringCommittee
独立数据监察委员会
IEC
IndependentEthicsCommittee
独立伦理委员会
IND
InvestigationalNewDrug
新药临床研究
IRB
InstitutionalReviewBoard
机构审查委员会
IVD
InVitroDiagnostic
体外诊断
IVRS
InteractiveVoiceResponseSystem
互动语音应答系统
MA
MarketingApproval/Authorization
上市许可证
MCA
MedicinesControlAgency
英国药品监督局
MHW
MinistryofHealthandWelfare
日本卫生福利部
NDA
NewDrugApplication
新药申请
NEC
NewDrugEntity
新化学实体
NIH
NationalInstitutesofHealth
国家卫生研究所(美国)
PI
PrincipalInvestigator
主要研究者
PL
ProductLicense
产品许可证
PMA
Pre-marketApproval(Application)
上市前许可(申请)
PSI
StatisticiansinthePharmaceuticalIndustry
制药业统计学家协会
QA
QualityAssurance
质量保证
QC
QualityControl
质量控制
RA
RegulatoryAuthorities
监督管理部门
SA
SiteAssessment
现场评估
SAE
SeriousAdverseEvent
严重不良事件
SAP
StatisticalAnalysisPlan
统计分析计划
SAR
SeriousAdverseReaction
严重不良反应
SD
SourceData/Document
原始数据/文件
SD
SubjectDiary
受试者日记
SFDA
StateFoodandDrugAdministration
国家食品药品监督管理局
SDV
SourceDataVerification
原始数据核准
SEL
SubjectEnrollmentLog
受试者入选表
SI
Sub-investigator
助理研究者
SI
Sponsor-Investigator
申办研究者
SIC
SubjectIdentificationCode
受试者识别代码
SOP
StandardOperatingProcedure
标准操作规程
SPL
StudyPersonnelList
研究人员名单
SSL
SubjectScreeningLog
受试者筛选表
T&R
TestandReferenceProduct
受试和参比试剂
UAE
UnexpectedAdverseEvent
预料外不良事件
WHO
WorldHealthOrganization
世界卫生组织
WHO-ICDRA
WHOInternationalConferenceof
Drug RegulatoryAuthorities
WHO国际药品管理当局会议
英文全称
中文全称
Accuracy
准确度
Activecontrol,AC
阳性对照活性对照
Adversedrugreaction(ADR)
药物不良反应
Adverseevent(AE)
不良事件
Adversemedicalevents
不良医学事件
Adversereaction
药物不良反应
Alb
白蛋白
ALD(ApproximateLethalDose)
近似致死剂量
ALP
碱性磷酸酶
Alphaspendingfunction
消耗函数
ALT
丙氨酸氨基转换酶
Analysissets
统计分析的数据集
Approval
批准
Assistantinvestigator
助理研究者
AST
天门冬酸氨基转换酶
ATR
衰减全反射法
AUCss
稳态血药浓度-时间曲线下面积
Audit
稽查
Auditorinspection
稽查/视察
Auditreport
稽查报告
Auditor
稽查员
Bias
偏性偏倚
Bioequivalence
生物等效应
Blankcontrol
空白对照
Blindcodes
编制盲底
Blindreview
盲态审核
Blindreview
盲态检查
Blindingmethod
盲法
Blinding/masking
盲法/设盲
Block
层
Blocksize
每段的长度
Carryovereffect
延滞效应
Casehistory
病历
Casereportform/caserecordform(CRF)
病例报告表病例记录表
Categoricalvariable
分类变量
Cav
平均浓度
CD
圆二色谱
CL
清除率
Clinicalequivalence
临床等效应
Clinicalstudy
临床研究
Clinicalstudyreport
临床试验的总结报告
Clinicaltrial
临床试验
Clinicaltrialapplication (CTA)
临床试验申请
Clinicaltrialexemption (CTX)
临床试验免责
Clinicaltrialprotocol(CTP)
临床试验方案
Clinicaltrial/studyreport
临床试验报告
Cmax
峰浓度
Co-investigator
合作研究者
Comparison
对照
Compliance
依从性
Compositevariable
复合变量
Computer-assistedtrialdesign(CATD)
计算机辅助试验设计
Confidenceinterval
可信区间
Confidencelevel
置信水平
Consistencytest
一致性检验
Contractresearchorganization(CRO)
合同研究组织
Contract/agreement
协议/合同
Controlgroup
对照组
Coordinatingcommittee
协调委员会
Crea
肌酐
CRF(casereportform)
病例报告表
Crossoverdesign
交叉设计
Cross-overStudy
交叉研究
Css
稳浓度
Cure
痊愈
Datamanagement
数据管理
Database
建立数据库
Descriptivestatisticalanalysis
描述性统计分析
DF
波动系统
Dichotomies
二分类
Diviation
偏差
Documentation
记录/文件
Dose-reactionrelation
剂量-反应关系
Doubledummy
双模拟
Doubledummytechnique
双盲双模拟技术
Dropout
脱落
DSC
差示扫描热量计
Effectiveness
疗效
Electronicdatacapture(EDC)
电子数据采集系统
Electronicdataprocessing(EDP)
电子数据处理系统
Emergencyenvelope
应急信件
Endpoint
终点
EndpointCriteria
终点指标
Endpointcriteria/measurement
终点指标
Equivalence
等效性
EssentialDocumentation
必需文件
Ethicscommittee
伦理委员会
Excellent
显效
Exclusioncriteria
排除标准
Factorialdesign
析因设计
Failure
无效失败
Finalpoint
终点
Fixed-doseprocedure
固定剂量法
Forcedtitration
强制滴定
Fullanalysisset
全分析集
GC-FTIR
气相色谱-傅利叶红外联用
GC-MS
气相色谱-质谱联用
Genericdrug
通用名药
Globalassessmentvariable
全局评价变量
GLU
血糖
Goodclinicalpractice(GCP)
药物临床试验质量管理规范
Goodmanufacturepractice (GMP)
药品生产质量管理规范
Goodnon-clinicallaboratorypractice(GLP)
药物非临床研究质量管理规范
Groupsequentialdesign
成组序贯设计
Healtheconomicevaluation(HEV)
健康经济学评价
Hypothesistest
假设检验
Hypothesistesting
假设检验
Improvement
好转
InclusionCriteria
入选表准
Inclusioncriteria
入选标准
Independentethicscommittee (IEC)
独立伦理委员会
Informationconsentform (ICF)
知情同意书
InformationGathering
信息收集
InformedconsentIC
知情同意
Initialmeeting
启动会议
Inspection
检察/视察
Institutioninspection
机构检查
Institutionreviewboard(IBR)
机构审查委员会
Intention-to–treat (ITT)
意向性分析(-统计学)
Interactivevoiceresponsesystem (IVRS)
互动式语音应答系统
Interimanalysis
期中分析
InternationalConferenceofHarmonization (ICH)
人用药品注册技术要求国际技术协调会国际协调会议
InvestigationalProduct
试验药物
Investigator
研究者
Investigator’sbrochure(IB)
研究者手册
Lastobservationcarryforward(LOCF)
最接近一次观察的结转
LC-MS
液相色谱-质谱联用
LD50
板数致死剂量
Lastobservationcarryforward(LOCF)
最近一次观察的结转
Logiccheck
逻辑检查
LimitofQuantization(LOQ)
定量限
Lostoffollowup
失访
Marketingapproval/authorization
上市许可证
Matchedpair
匹配配对
Missingvalue
缺失值
Mixedeffectmodel
混合效应模式
Monitor
监察员
Monitoring
监查
MonitoringPlan
监察计划
MonitoringReport
监察报告
MRT
平均滞留时间
MS
质谱
MS-MS
质谱-质谱联用
MaximumToleratedDose(MTD)
最大耐受剂量
Multi-centerTrial
多中心试验
Newchemicalentity (NCE)
新化学实体
Newdrugapplication (NDA)
新药申请
NMR
核磁共振谱
Non-clinicalStudy
非临床研究
Non-inferiority
非劣效性
Non-parametricstatistics
非参数统计方法
Obedience
依从性
ODR
旋光光谱
Open-label
非盲
Optionaltitration
随意滴定
Originalmedicalrecord
原始医疗记录
Outcome
结果
OutcomeAssessment
结果评价
Outcomeassessment
结果指标评价
Outcomemeasurement
结果指标
Outlier
离群值
Parallelgroupdesign
平行组设计
Parameterestimation
参数估计
Parametricstatistics
参数统计方法
Patientfile
病人档案
Patienthistory
病历
Perprotocol (PP)
符合方案集
Placebo
安慰剂
Placebocontrol
安慰剂对照
Polytomies
多分类
Power
检验效能
Precision
精密度
Preclinicalstudy
临床前研究
Primaryendpoint
主要终点
Primaryvariable
主要变量
Principleinvestigator (PI)
主要研究者
Productlicense(PL)
产品许可证
Protocol
试验方案
ProtocolAmendments
修正案
Qualityassurance(QA)
质量保证
Qualityassuranceunit(QAU)
质量保证部门
Qualitycontrol(QC)
质量控制
Querylist queryform
应用疑问表
Randomization
随机
Rangecheck
范围检查
Ratingscale
量表
ReferenceProduct
参比制剂
Regulatoryauthorities (RA)
监督管理部门
Replication
可重复
RSD
日内和日间相对标准差
Runin
准备期
Safetyevaluation
安全性评价
Safetyset
安全性评价的数据集
Samplesize
样本量样本大小
Scaleoforderedcategoricalratings
有序分类指标
Secondaryvariable
次要变量
Sequence
试验次序
Seriousadverseevent(SAE)
严重不良事件
Seriousadversereaction(SAR)
严重不良反应
Seriousness
严重性
Severity
严重程度
Severity
严重程度
Significantlevel
检验水准
SimpleRandomization
简单随机
Singleblinding
单盲
Siteaudit
验机构稽查
SOP
试验室的标准操作规程
Sourcedata(SD)
原始数据
Sourcedataverification(SDV)
原始数据核准
Sourcedocument
原始文件
Specificity
特异性
Sponsor
申办者
Sponsor-investigator
申办研究者
Standardcurve
标准曲线
Standardoperatingprocedure (SOP)
标准操作规程
Statistic
统计量
Statisticalanalysisplan
统计分析计划
Statisticalmodel
统计模型
Statisticaltables
统计分析表
Stratified
分层
StudyAudit
研究稽查
Studyaudit
研究稽查
StudySite
研究中心
Subgroup
亚组
Sub-investigator
助理研究者
Subject
受试者
Subject
受试者
Subjectdiary
受试者日记
SubjectEnrollment
受试者入选
Subjectenrollmentlog
受试者入选表
Subjectidentificationcode (SIC)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 药物 临床试验 英文 缩写
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《爱和自由》读书心得15篇.docx
《爱和自由》读书心得15篇.docx
