 物质的量与阿伏伽德罗常数.docx
物质的量与阿伏伽德罗常数.docx
- 文档编号:26211255
- 上传时间:2023-06-17
- 格式:DOCX
- 页数:18
- 大小:133.98KB
物质的量与阿伏伽德罗常数.docx
《物质的量与阿伏伽德罗常数.docx》由会员分享,可在线阅读,更多相关《物质的量与阿伏伽德罗常数.docx(18页珍藏版)》请在冰豆网上搜索。
物质的量与阿伏伽德罗常数
物质的量及其阿伏伽德罗常数
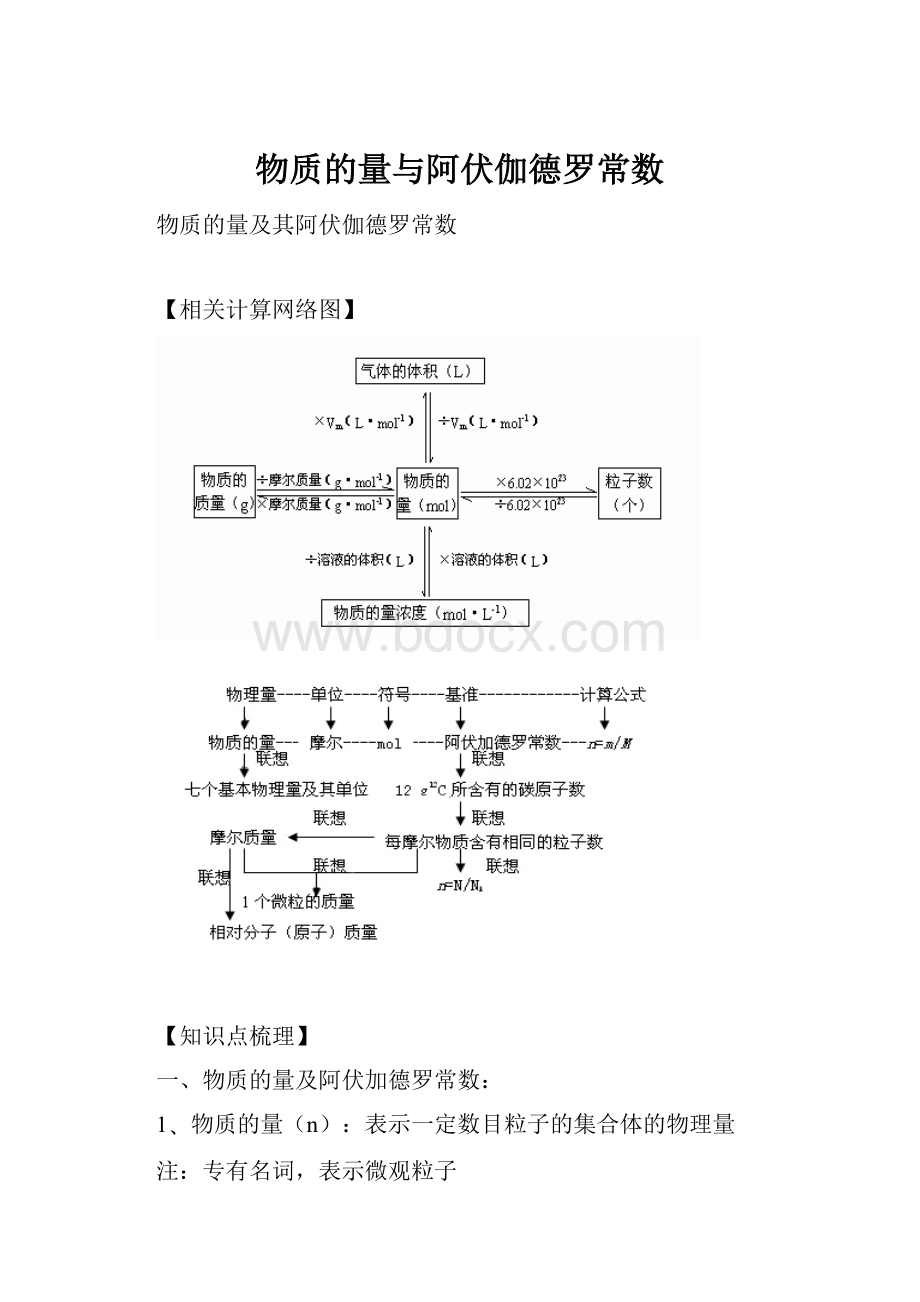
【相关计算网络图】
【知识点梳理】
一、物质的量及阿伏加德罗常数:
1﹑物质的量(n):
表示一定数目粒子的集合体的物理量
注:
专有名词,表示微观粒子
单位:
摩尔(mol),简称为摩规定0.012kg12C中所含碳原子数为1mol
阿伏加德罗常数NA≈6.02×1023mol-1
计算公式:
n=N/NA
2﹑摩尔质量(M):
单位物质的量的物质所具有的质量
单位:
g/mol或g﹒mol-1
计算公式:
M=m/n
3、阿伏加德罗常数(NA):
表示1mol任何粒子所含粒子数目的多少
计算公式:
NA=N/n
单位:
mol-1
易错点讲解:
1.阿伏加德罗常数
是一个物理量,符号为“NA”,单位是mol-1,是用来衡量物质中所含粒子的物质的量的标准。
(1)含义:
实验测定12g12C中碳原子的个数
(2)说明:
①NA的基准是12g碳-12中的原子个数
②12C不仅是摩尔的基准对象,而且还是相对原子质量的基准
③NA是一个实验值,现阶段常取6.02×1023作计算
④要注意NA与6.02×1023
的区别
2.阿伏加德罗常数常考知识点
(1)物质的状态:
水在标准状态下不是气态;SO3在标准状况下是固态,在常温常压下是液态;标准状况下含碳原子数大于4的烃不是气态。
(2)某些物质分子中原子的个数:
稀有气体为单原子分子、臭氧为三原子分子、而白磷分子中则含有4个磷原子。
(3)一些物质结构中化学键的数目:
SiO2中共价键的数目等于Si的数目的2倍;Si(或金刚石)中的共价键数目等于Si(或C)数目的2倍;CH4中共价键的数目等于C数目的4倍;1molP4分子中含有6mol共价键等。
(4)特殊物质的摩尔质量:
D2O的摩尔质量为20g·mol-1;18O2的摩尔质量为36g·mol-1。
(5)特殊物质在发生氧化还原反应得失电子数目的情况:
1molNa2O2只做
氧化剂时得到2mol电子。
若既做氧化剂又做还原剂则转移1mol电子。
1molFe与强氧化剂(Cl2、硝酸等)反应时,失去3mol电子,若与弱氧化剂反应则失去2mol电子。
(6)有关标况下物质的状态:
水、CCl4、C8H10等在标准状况下为液体或固体。
二﹑气体摩尔体积
1﹑物质体积大小取决于:
物质的量、微粒的大小、微粒的距离
气体体积大小的决定因素:
物质的量、微粒的距离
固体、液体体积大小的决定因素:
物质的量、微粒的大小
2﹑气体摩尔体积(Vm):
单位物质的量的气体所占的体积
单位:
L/mol或L﹒mol-1
标况下Vm=22.4L﹒mol-1,常温常压下Vm=24.8L﹒mol-1
计算公式:
Vm=V/n
3﹑等温等压下,物质的量相等的气体它们的体积相等
4﹑混合气体的平均摩尔质量:
M=m(总)/n(总)
1.影响物质体积大小的因素
(1)决定固体、液体体积大小的因素,主要是微粒的数量和微粒的大小,微粒间的距离可不考虑;决定气体体积的因素,主要是微粒的数量和微粒间平均距离的大小,微粒本身的大小可不考虑,因气体微粒间平均距离比微粒本身的直径约大十倍左右。
(2)外界条件如温度T、压强p对物质体积的影响:
对固态、液态物质来说,体
积V受T、p的影响较小;对一定量气体来说,T和p对气体分子间的平均距离有较大的影响。
易错点讲解:
(1)气体体积的大小受外界因素的影响
①温度:
对气体物质来说,温度升高,体积增大;温度降低,体积减小。
②压强:
对气体物质来说,压强增大,体积减小;压强减小,体积增大。
因此要比较一定量气体的体积,必须在同温同压下,否则就没有可比性,故在描述一定量气体的体积时,必须注明在某温度和某压强下,否则气体的体积是无意义的。
(2)标准状况
标准状况是指压强为101kPa和温度为0℃,即1标准大气压和0℃(标准状况时压强的准确值为101.325kPa)。
(3)气体摩尔体积的概念:
单位物质的量的气体所占的体积叫做气体摩尔体积。
①气体摩尔体积的符号Vm。
②意义及数学表达式:
气体摩尔体积就是气体体积与气体的物质的量之比。
即Vm=
④特例:
在标准状况下,气体的摩尔体积均为22.4L/mol,因此,我们可认为22.4L/mol是在特定条件下的气体摩尔体积(注意:
中学化学中主要是应用标准状况下的气体摩尔体积)。
⑤气体摩尔体积的四要素:
a.状态:
气体摩尔体积是指气态物质而言。
在一定的温度和压强下,气体分子的平均距离几乎都相等,与气体分子本身的构成和性质无关,气体的体积只随分子数目的多少而改变。
所以,在同温、同压下,含有相同数目分子的气体的体积尽然相等。
b.状况:
一定量的气体的体积是随着温度和压强等条件的改变而改变的。
只有在同温、同压的条件下,气体分子之间的平均距离才近似相等,这时含有相同分子数目的气体才会占有相同的体积。
标准状况是指温度为0℃、压强为101.325kPa时的状况,处在标准状况下的1mol任何气体,都含有相同数目的分子,因而也就占有相同的体积,且都约为
22.4L。
不处在标准状况下的1mol任何气体虽然体积也相等,但不一定是22.4L。
三、阿伏加德罗定律
(1)阿伏加德罗定律:
在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子
(2)注意:
①使用范围:
气体;②使用条件:
同温、同压、同体积;③特例:
气体摩尔体积
(3)推论:
用n表示物质的量,V表示体积,P表示压强,M表示摩尔质量(式量),ρ表示密度。
(注意语言表达)
①同温同压:
V1/V2=n1/n2=N1/N2
②同温同体积:
P1/P2=n1/n2=N1/N2
③同温同压:
ρ1/ρ2=M1/M2
④同温同压同质量:
V1/V2=M1/M2
⑤同温同压同体积:
m1/m2=M1/M2
四﹑物质的量浓度
1.概念:
以单位体积溶液里所含溶质的物质的量来表示溶液浓度的物理量。
2.符号:
c
单位:
摩/升(mol/L)或mol﹒L-1
3.计算公式
4.注意:
1)单位体积为溶液的体积,不是溶剂的体积。
2)溶质必须用物质的量来表示。
3)计算公式为概念中的单位体积一般指1升,溶质可以指单质或化合物,也可以指离子或其它特定组合。
4).溶质的质量分数(ω)
⑴定义:
溶质质量分数是溶质的质量和溶液质量的比值,数值上等于100g溶液中含有溶质的质量
⑵公式:
溶液的稀释与混合
1.溶液的稀释定律
由溶质的质量稀释前后不变有:
m=m浓×ω浓%=m稀×ω稀%
由溶质稀释前后物质的量不变有:
C=c浓×V浓=c稀×V稀
2.溶液在稀释或混合时,溶液的总体积不一定是二者混合的体积之和。
如给出溶液混合后的密度,应根据质量和密度求体积。
但若为稀溶液,体积可以加起来,进行近似计算
3.物质的量浓度C与溶质质量分数ω%的换算(ρ为该溶液的密度)
五、气体溶于水后溶液物质的量浓度的计算
1、在标准状况下,1L水中溶解某气体VL,所得溶液密度为ρg·mL-1,已知该气体的摩尔质量为Mg·mol-1,水的密度是1g·mL-1,则溶于水后溶质的物质的量浓度为:
c=
=
=
mol·L-1=m
ol·L-1
习题训练:
1、(2015全国I)NA为阿伏伽德罗常数的值。
下列说法正确的是()
A.18gD2O和18gH2O中含有的质子数均为10NA
B.2L0.5mol/L亚硫酸溶液中含有的H+两种数为2NA
C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
D.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
2、(2015全国II)NA代表阿伏加德
罗常数的值。
下列叙述正确的是
A.60g丙醇中存在的共价键总数为10NA
B.1L0.1mol·L-1的NaHCO3-溶液中HCO3-和CO32-离子数之和为0.1NA
C.钠在空气中燃烧可生成多种氧化物。
23g钠充分燃烧时转移电子数为1NA
D.235g核互
U发生裂变反应:
U+
n
Sr+
U+10
n净产生的中子(
n)数为10NA
3.(2015上海)工业上将Na2CO3和Na2S以1:
2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2。
在该反应中
A.硫元素既被氧化又被还原B.氧化剂与还原剂的物质的量之比为1:
2
C.每生成1molNa2S2O3,转移4mol电子
D.相同条件下,每吸收10m3SO2就会放出2.5m3CO2
4.(2015上海)将O2和NH3的混合气体448mL通过加热的三氧化二铬,充分反应后,再通过足量的水,最终收集到44.8mL气体。
原混合气体中O2的体积可能是(假设氨全部被氧化;气体体积均已换算成标准状况)
A.231.5mLB.268.8mLC.287.5mLD.313.6mL
1、(2014.大纲卷.7)NA表示阿伏加德罗常数,下列叙述正确的是()
A.lmolFeI2与足量氯气反应时转移的电子数为2NA
B.2L0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA
C.1molNa2O2固体中含离子总数为4NA
D.丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA
2、(2014.江苏。
6)NA表示阿伏加德罗常数,下列叙述正确的是()
A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
B、0.1mol丙烯酸中含有双键的数目为0.1NAmol
C、标准状况下,11.2L苯中含有分子的数目为0.5NA
D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为04NA
3、(2014.广东。
10)NA表示阿伏加德罗常数,下列叙述正确的是()
A、1mol甲苯中含有6NA个C—H键
B、18gH2O含有10NA个质子
C、标准状况下,22.4L氨水中含有NA个NH3分子
D、56g铁片投入足量浓H2SO4中生成NA个SO2分子
4、(2014.上海。
16)含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解生成单质砷和氢气。
若砷的质量为1.50mg,则()
A、被氧化的砒霜为1.98mgB、分解产生的氢气为0.672mL
C、和砒霜反应的锌为3.90mgD、转移的电子总数为6×10-5NA
5、(2014.大纲卷.13)已知:
将Cl2通人适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且
的值与温度高低有关。
当n(KOH)=amol时,下列有关说法错误的是()
A.若某温度下,反应后
=11,则溶液中
=
B、参加反应的氯气的物质的量等于
amol
C.改变温度,反应中转移电子的物质的量ne的范围:
amol≤ne≤
amol
D.改变温度,产物中KC1O3的最大理论产量为
amol
1.(2013·上海化学·15)NA代表阿伏伽德罗常数。
已知C2H4和C3H6的混合物的质量为ag,则该混合物()
A.所含公用电子对书目为(a/7+1)NAB.所含碳氢键数目为aNA/7
C.燃烧时消耗的O2一定是33.6a/14LD.所含原子总数为aNA/14
2.(2013·新课标卷Ⅱ·9)N0为阿伏伽德罗常数的值.下列叙述正确的是()
A.1.0L1.0mo1·L-1的NaAlO2水溶液中含有的氧原子数为2N0
B.12g石墨烯(单层石墨)中含有六元环的个数为0.5N0
C.25℃时pH=13的NaOH溶液中含有OH一的数目为0.1N0
D.1mol的羟基与1mot的氢氧根离子所含电子数均为9N0
3.(2013·广东理综·9)设nA为阿佛加德罗常数的数值,下列说法正确的是()
A.常温常压下,8gO2含有4nA个电子
B.1L0.1molL-1的氨水中有nA个NH4+
C.标准状况下,22.4L盐酸含有nA个HCl分子
D.1molNa被完全氧化生成Na2O2,失去个2nA电子
4.(2013·江苏化学·7)设NA为阿伏加德罗常数的值。
下列说法正确的是()
A.1L1mol·L-1的NaClO溶液中含有ClO-的数目为NA
B.78g苯含有C=C双键的数目为3NA
C.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6.72LNO2与水充分反应转移的电子数目为0.1NA
5、(2013·广西理综·8)下列关于同温同压下的两种气体12C18O和14N2的判断正确的是()
A.体积相等时密度相等B.原子数相等时具有的中子数相等
C.体积相等时具有的电子数相等D.质量相等时具有的质子数相等
2012
1.[2012·江苏化学卷8]设NA为阿伏伽德罗常数的值。
下列说法正确的是()
A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
B.常温常压下,18gH2O含有的原子总数为3NA
C.标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA
D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA
7.[2012·海南化学卷7]NA为阿伏加德罗常数的数值,下列说法中正确的是()
A.在密闭容器中加入l.5molH2和0.5molN2,充分反应后可得到NH3分子数为NA
B.一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA
C.1.0L的0.1mol·L-1Na2S溶液中含有的S2-离子数为0.1NA
D.标准状况下,22.4L的CCl4中含有的CCl4分子数为NA
8.[2012·四川理综化学卷7]设NA为阿伏加德罗常数的值,下列叙述正确的是()
A.标准状态下,33.6L氟化氢中含有氟原子的数目为1.5NA
B.常温常压下,7.0g乙烯与丙烯的混合物红含有氢原子的数目为NA
C.50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分支的数目为0.46NA。
D.某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA
24.[2012·广东理综化学卷11]设nA为阿伏伽德罗常数的数值,下列说法正确的是()
A.常温下,4gCH4含有nA个C-H共价键
B.1molFe与过量的稀HNO3反应,转移2nA个电子
C.1L0.1mol·
NaHCO3液含有0.1nA个HCO3—
D.常温常压下,22.4L的NO2和CO2合气体含有2nA个O原子
41.[2012·新课程理综化学卷9]用NA表示阿伏伽德罗常数的值,下列叙述中不正确的是
()
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气于足量的镁粉反应,转移的电子数为2NA
2011
1.(2011广东高考9)设nA为阿伏伽德罗常数的数值,下列说法正确的是()
A、常温下,23gNO2含有nA个氧原子
B、1L0.1mol•L-1的氨水含有0.1nA个OH―
C、常温常压下,22.4LCCl4含有个nA个CCl4分子
D、1molFe2+与足量的H2O2溶液反应,转移2nA个电子
2.(2011新课标全国)下列叙述正确的是()
A.1.00molNaCl中含有6.02×1023个NaCl分子
B.1.00molNaCl中,所有Na+的最外层电子总数为8×6.02×1023
C.欲配置1.00L,1.00mol.L-1的NaCl溶液,可将58.5gNaCl溶于1.00L水中
D.电解58.5g熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠
3.(2011海南)设NA是阿伏加德罗常数的数值,下列说法正确的是()
A.1molAl3+离子含有的核外电子数为3NA
B.1molCl2与足量的铁反应,转移的电子数为3NA[来
C.10LpH=1的硫酸溶液中含有的H+离子数为2NA
D.10LpH=13的NaOH溶液中含有的OH-离子数为NA[来源:
学科网ZXXK]
4.(2011全国II卷12)NA为阿伏伽德罗常数,下列叙述错误的是()
A.18gH2O中含的质子数为10NA
B.12g金刚石含有的共价键数为4NA
C.46gNO2和N2O4混合气体中含有原子总数为3NA
D.1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
5.(2011江苏高考8)设NA为阿伏伽德罗常数的值。
下列叙述正确的是()
A.1mol甲醇中含有C—H键的数目为4NA
B.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
C.标准状况下,2.24L已烷含有分子的数目为0.1NA
D.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA
6.(2011上海20)过氧化钠可作为氧气的来源。
常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)()
二氧化碳
碳酸钠
转移的电子
A
1mol
NA
B
22.4L
1mol
C
106g
1mol
D
106g
2NA
2010
1.(10广东理综卷8.)设
为阿伏加德罗常数的数值,下列说法正确的是()
A.16g
中含有4
个C-H键
B.1mol·
溶液含有
个
C.1molCu和足量稀硝酸反应产生
个NO分子
D.常温常压下,22.4L
中含有
个
分子
2.(2010山东卷9).
和
是氧元素的两种核素,
表示阿伏伽德罗常数,下列说法正确的是()
A.
与
互为同分异构体
B.
与
核外电子排布方式不同
C.通过化学变化可以实现
与
间的相互转化
D.标准状况下,1.12L
和1.12L
均含有0.1
个氧原子
3.(2010福建卷7).
表示阿伏伽德罗常数,下列判断正确的是()
A.在18
中含有
个氧原子
B.标准状况下,22.4L空气含有
个单质分子
C.1molCl2参加反应转移电子数一定为2
D.含
个
的
溶解于1L水中,
的物质的量浓度为
4.(2010上海卷7).NA表示阿伏加德罗常数,下列叙述正确的是()
A.等物质的量的N2和CO所含分子数均为NA
B.1.7gH2O2中含有的电子数为0.9NA
C.1molNa2O2固体中含离子总数为4NA
D.标准状况下,2.24L戊烷所含分子数为0.1NA
5.(2010江苏卷5).设
为阿伏加德罗常数的值,下列叙述正确的是()
A.常温下,
的
溶液中氮原子数为0.2
B.1mol羟基中电子数为10
C.在反应中,每生成3mol
转移的电子数为6
D.常温常压下WWWKS5U.COM
,22.4L乙烯中
键数为4
6.(2010四川理综卷7.)
表示阿伏加德罗常数的值,下列说法正确的是()
A.标准状况下,22.4L二氯甲烷的分子数约为
个
B.盛有
的密闭容器中含有
个氧原子,则
的物质的量为0.5mol
C.17.6g丙烷中所含的极性共价键为
个
D.电解精炼铜时,若阴极得到电子数为
个,则阳极质量减少64g
7.(2010四川理综卷12.)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为pg/ml,质量分数为ω,物质浓度为cmol/L,则下列关系中不正确的是()
A.
B.
C.
D.C=1000Vρ/(17V+22400)
(注:
可编辑下载,若有不当之处,请指正,谢谢!
)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 物质 阿伏伽德罗 常数
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《初级会计实务》试题题库大全及答案详解.docx
《初级会计实务》试题题库大全及答案详解.docx
