 高中化学镁铝铁知识归纳培训讲学.docx
高中化学镁铝铁知识归纳培训讲学.docx
- 文档编号:11936653
- 上传时间:2023-04-16
- 格式:DOCX
- 页数:11
- 大小:125.11KB
高中化学镁铝铁知识归纳培训讲学.docx
《高中化学镁铝铁知识归纳培训讲学.docx》由会员分享,可在线阅读,更多相关《高中化学镁铝铁知识归纳培训讲学.docx(11页珍藏版)》请在冰豆网上搜索。
高中化学镁铝铁知识归纳培训讲学
3、竞争对手分析高中化学镁铝铁知识归纳
情感性手工艺品。
不少人把自制的手机挂坠作为礼物送给亲人朋友,不仅特别,还很有心思。
每逢情人节、母亲节等节假日,顾客特别多。
【知识网络】
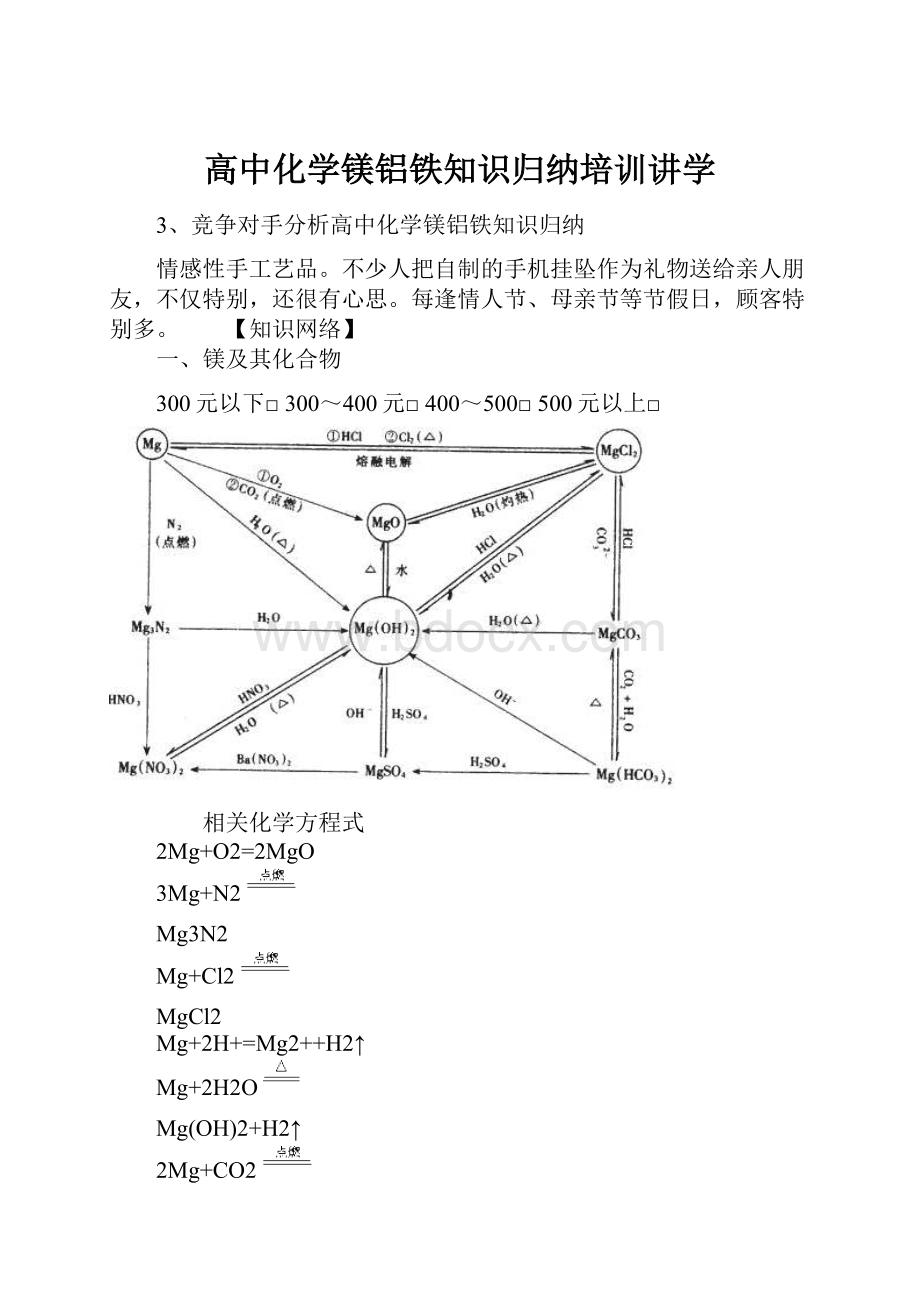
一、镁及其化合物
300元以下□300~400元□400~500□500元以上□
相关化学方程式
2Mg+O2=2MgO
3Mg+N2
Mg3N2
Mg+Cl2
MgCl2
Mg+2H+=Mg2++H2↑
Mg+2H2O
Mg(OH)2+H2↑
2Mg+CO2
2MgO+C
MgO+H2O=Mg(OH)2
MgO+2HCl=MgCl2+H2O
MgCl2(熔融)
Mg+Cl2↑
Mg2++CO32-=MgCO3↓
MgCO3+2H+=Mg2++CO2↑+H2O
MgCO3+CO2+H2O=Mg(HCO3)2
MgCO3+H2O
Mg(OH)2+CO2↑
Mg(OH)2+2H+=Mg2++H2O
Mg(OH)2
MgO+H2O
Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
二、铝及其化合物
随着社会经济、文化的飞跃发展,人们正从温饱型步入小康型,崇尚人性和时尚,不断塑造个性和魅力的现代文化价值观念,已成为人们的追求目标。
因此,顺应时代的饰品文化显示出强大的发展势头和越来越广的市场,从事饰品销售是有着广阔的市场空间。
相关化学方程式
4Al+3O2=2Al2O3
3S+2Al
Al2S3
2Al+3Cl2
2AlCl3
2Al+6HCl=2AlCl3+3H2↑
2Al+6H2O
2Al(OH)3+3H2↑
2Al+Fe2O3
Al2O3+2Fe
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
Al2O3+6HCl=2AlCl3+3H2O
Al2O3+2NaOH=2NaAlO2+2H2O
2Al2O3(熔融)
4Al+3O2↑
Al3++3H2O=Al(OH)3+3H+
Al3++3NH3·H2O=Al(OH)3↓+3NH4+
Al3++3OH-=Al(OH)3↓
Al3++4OH-=AlO2-+2H2O
Al2S3+6H2O=2Al(OH)3↓+3H2S↑
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+OH-=AlO2-+2H2O
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+H++H2O=Al(OH)3↓
AlO2-+4H+=Al3++2H2O
3AlO2-+Al3++6H2O=4Al(OH)3↓
三、铁及其化合物
创新是时下非常流行的一个词,确实创新能力是相当重要的特别是对我们这种经营时尚饰品的小店,更应该勇于创新。
在这方面我们是很欠缺的,故我们在小店经营的时候会遇到些困难,不过我们会克服困难,努力创新,把我们的小店经营好。
(1)位置的优越性 相关化学方程式
3Fe+2O2(纯)
Fe3O4
Fe+S
FeS
2Fe+3Cl2
2FeCl3
Fe+2H+=Fe2++H2↑
3Fe+4H2O
Fe3O4+4H2↑
Fe+Cu2+=Cu+Fe2+
FeO+2HCl=FeCl2+H2O
Fe(OH)2+2HCl=FeCl2+2H2O
4Fe(OH)2+O2+2H2O=4Fe(OH)3
2FeCl2+Cl2=2FeCl3
FeS+2H+=Fe2++H2S↑
2Fe3++Fe=3Fe2+
4FeS2+11O2
2Fe2O3+8SO2
Fe2O3+6H+=2Fe3++3H2O
Fe2O3+3CO
2Fe+3CO2
Fe3++3H2O
Fe(OH)3+3H+
Fe3++SCN-=Fe(SCN)2+
Fe(OH)3+3H+=Fe3++3H2O
2Fe(OH)3
Fe2O3+3H2O
【各部分知识回顾】
一、镁
1.原子结构示意图:
而手工艺制品是一种价格适中,不仅能锻炼同学们的动手能力,同时在制作过程中也能体会一下我国传统工艺的文化。
无论是送给朋友还是亲人都能让人体会到一份浓厚的情谊。
它的价值是不用金钱去估价而是用你一颗真诚而又温暖的心去体会的。
更能让学生家长所接受。
2.单质
(1)在周期表中位置:
第三周期ⅡA族(碱土金属)
(2)物理性质:
银白色,质软,轻金属,硬度较小,熔沸点较低。
(3)化学性质
①与非金属反应
(发出耀眼白光),常温形成致密氧化膜
②与非金属氧化物反应
③与非氧化学性质酸反应
④与氧化学性质酸(如硝酸、浓硫酸)反应,不放出H2
⑤与水反应
(能使酚酞变红)
⑥与盐溶液反应,能置换出后面的金属
(4)冶炼:
(5)用途:
制轻合金、飞机、汽车部件、烟火、照明弹等。
3.化合物
(1)MgO
①物理性质:
白色粉末,密度小,熔点高,硬度大,难溶于水。
②化学性质:
碱性氧化物,
(缓慢)
③制法:
MgCO3
MgO+CO2↑
④用途:
耐火材料
(2)Mg(OH)2:
难溶性中强碱:
(3)MgCl2:
无色、味苦、易溶、易潮解的白色晶体,具有可溶性盐的通性。
(4)KCl·MgCl2·6H2O(光卤石):
从中可提取MgCl2·6H2O
二、铝
1.原子结构示意图:
1996年“碧芝自制饰品店”在迪美购物中心开张,这里地理位置十分优越,交通四通八达,由于位于市中心,汇集了来自各地的游客和时尚人群,不用担心客流量的问题。
迪美有300多家商铺,不包括柜台,现在这个商铺的位置还是比较合适的,位于中心地带,左边出口的自动扶梯直接通向地面,从正对着的旋转式楼梯阶而上就是人民广场中央,周边4、5条地下通道都交汇于此,从自家店铺门口经过的90%的顾客会因为好奇而进去看一下。
是□否□ 2.在周期表中位置:
第三周期ⅢA族
3.单质
(1)物理性质:
银白色,质软,轻金属。
(2)化学性质
①与金属反应
常温下被O2氧化,形成致密氧化膜,在O2中或高温下点燃生成Al2O3 4Al+3O2
2Al2O3
与Cl2、S等非金属反应 2Al+3Cl2
2AlCl3 2Al+3S
Al2S3
②与Fe3O4、WO3、MnO2等金属氧化物发生铝热反应
8Al+3Fe3O4
4Al2O3+9Fe
③与非氧化性酸发生置换反应
2Al+6H+=2Al3++3H2↑
注:
常温下在浓硫酸、浓硝酸中钝化。
④与沸水发生置换反应
2Al+6H2O
2Al(OH)3+3H2↑
⑤与强碱液液反应:
⑥与盐溶液反应,置换后面的金属
(3)冶炼:
(熔融电解)
(4)用途:
制轻合金、飞机、汽车、轮船部件,导线,炊具、还原剂,铝热剂。
4.化合物
(1)Al2O3
①物理性质:
白色难溶固体,熔点高,硬度大。
②化学性质:
两性氧化物
Al2O3+6H+=2Al3++3H2O
Al2O3+2OH-=2AlO2-+H2O
③制法:
④用途:
制铝、耐火材料。
刚玉可做仪器、手表轴承、磨料等。
(2)Al(OH)3:
两性氢氧化物,不溶于水的白色胶状物
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+OH-=AlO2-+2H2O
(3)AlCl3:
具有可溶性盐的通性,能水解而呈酸性,只存在于酸性溶液中。
(4)NaAlO2:
易水解而显碱性,只存在于强碱性溶液中
AlO2-+H++H2O=Al(OH)3↓
(5)KAl(SO4)2·12H2O(明矾):
属复盐,易水解生成胶状Al(OH)3,可做净水剂。
三、铁
1.原子结构示意图:
然而影响我们大学生消费的最主要的因素是我们的生活费还是有限,故也限制了我们一定的购买能力。
因此在价格方面要做适当考虑:
我们所推出的手工艺制品的价位绝大部分都是在50元以下。
一定会适合我们的学生朋友。
能失去最外层2个电子及第三层1个电子
2.在周期表中位置:
第四周期第Ⅷ族,属过渡元素
3.存在
①游离态:
少量存在于陨石中。
②化合态:
赤铁矿、磁铁矿、褐铁矿、黄铁矿、菱铁矿。
4.单质
(1)物理性质:
银白色,ρ=7.86g·cm-3,熔点1535℃;纯铁抗蚀能力较强,能被磁铁吸引和磁化。
(2)化学性质:
典型金属,有金属通性。
①与非金属反应
与O2:
常温干燥空气中不易与O2反应,但在潮湿空气中易形成原电池等形式被腐蚀;
铁粉能在纯氧中燃烧:
与卤素:
I2+Fe
FeI2
与硫:
②与酸反应
非氧化学性质酸:
与浓硝酸、浓硫酸:
常温下钝化,加热时反应
③与盐:
④与水:
↑
(3)冶炼:
5.化合物
(1)氧化物:
FeO、Fe2O3、Fe3O4
(2)氢氧化物:
Fe(OH)2、Fe(OH)3
(3)盐:
①亚铁盐:
FeSO4·7H2O(绿矾)
②铁盐:
FeCl3、Fe2(SO4)3
③络盐:
[Fe(SCN)n]3-n(n=1~6)
四、合金
(1)概念:
由两种或两种以上的金属(或金属跟非金属)熔合而成的具有金属特性的物质。
(2)特点:
合金性质不是各成分金属性质的总和;硬度一般比各成分金属大;多数合金的熔点一般比各成分金属低;化学性质与成分金属不同。
(3)常见合金:
镁铝合金、硬铝、合金钢、锰钢、黄铜、青铜、钛合金……
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 镁铝铁 知识 归纳 培训 讲学
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
