 药品质量管理规定新修订制度Word格式文档下载.docx
药品质量管理规定新修订制度Word格式文档下载.docx
- 文档编号:14389647
- 上传时间:2022-10-22
- 格式:DOCX
- 页数:76
- 大小:82.63KB
药品质量管理规定新修订制度Word格式文档下载.docx
《药品质量管理规定新修订制度Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《药品质量管理规定新修订制度Word格式文档下载.docx(76页珍藏版)》请在冰豆网上搜索。
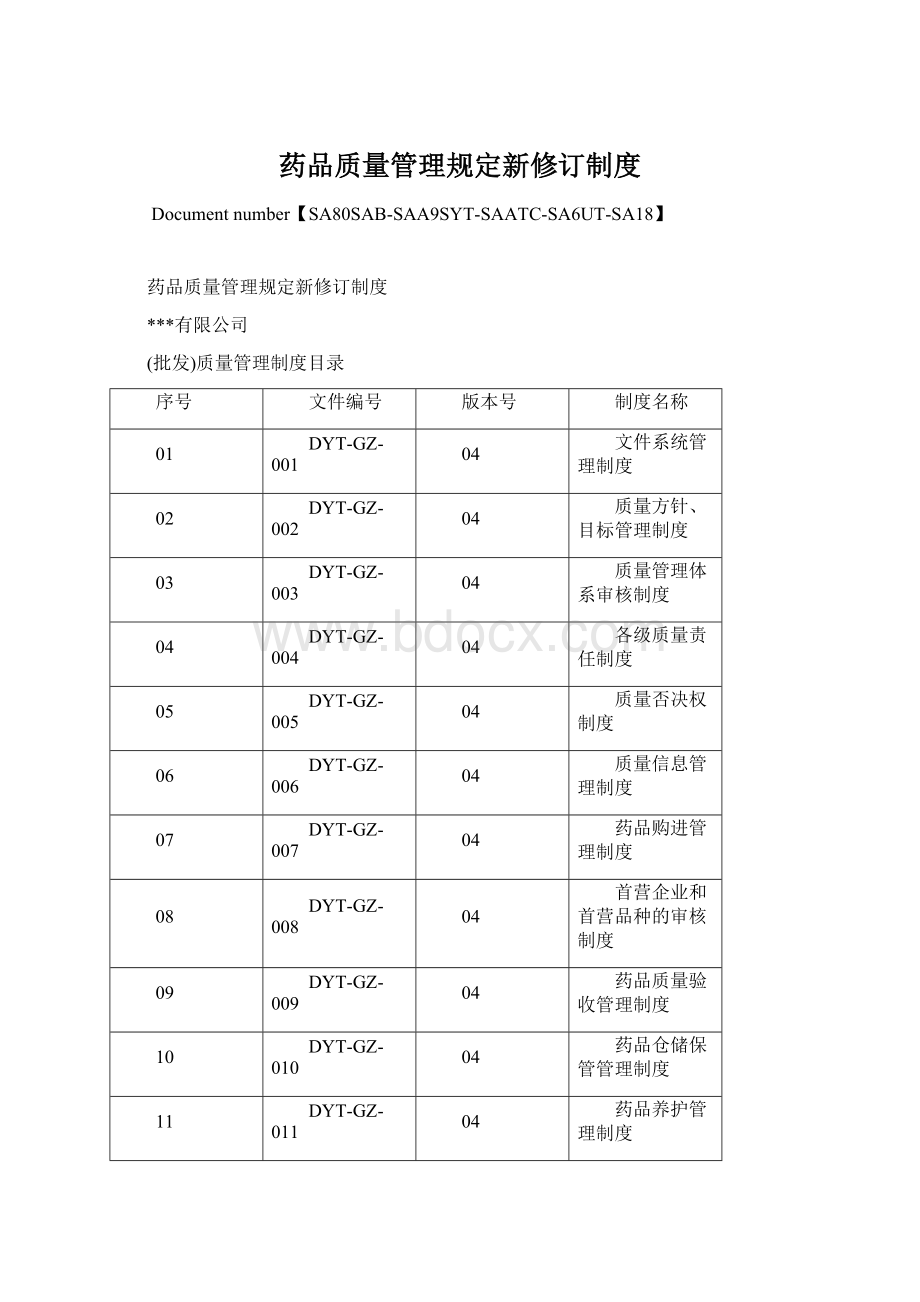
06
DYT-GZ-006
质量信息管理制度
07
DYT-GZ-007
药品购进管理制度
08
DYT-GZ-008
首营企业和首营品种的审核制度
09
DYT-GZ-009
药品质量验收管理制度
10
DYT-GZ-010
药品仓储保管管理制度
11
DYT-GZ-011
药品养护管理制度
12
DYT-GZ-012
药品销售管理制度
13
DYT-GZ-013
药品出库复核管理制度
14
DYT-GZ-014
有关记录和凭证的管理制度
15
DYT-GZ-015
近效期药品管理制度
16
DYT-GZ-016
不合格药品管理制度
17
DYT-GZ-017
退货药品管理制度
18
DYT-GZ-018
质量事故管理制度
19
DYT-GZ-019
质量查询和质量投拆管理制度
20
DYT-GZ-020
药品不良反应报告管理制度
21
DYT-GZ-021
卫生和人员健康状况管理制度
22
DYT-GZ-022
质量教育培训及考核管理制度
23
DYT-GZ-023
药品质量档案管理制度
24
DYT-GZ-024
药品进货合同管理制度
25
DYT-GZ-025
00
特殊管理药品的管理制度
26
DYT-GZ-026
进口药品管理制度
27
DYT-GZ-027
计算机系统管理制度
28
DYT-GZ-028
设施设备保管和维护管理制度
29
DYT-GZ-029
药品电子监管管理制度
30
DYT-GZ-030
药品召回管理制度
31
DYT-GZ-031
药品运输管理制度
题目
种类
制度
制定人
审核人
批准人
制定日期
审核日期
批准日期
颁发部门
质量部
执行日期
分发部门
办公室、质量部
第1页共2页
目的:
规范质量管理文件的起草、审核、批准、执行、修订、存档等环节的管理。
依据:
《药品经营质量管理规范》及其实施细则。
适用范围:
适用于质量管理过程中的质量管理制度、质量管理工作程序、质量记录等文件的管理。
内容:
1、文件管理
质量管理文件系统主要由质量管理制度、质量管理工作程序、质量记录三部分组成。
企业编制的质量管理制度、质量管理工作程序应有统一的格式:
题目、文件编号、版本号、颁发部门、起草人、审核人、批准人及日期、执行日期等内容。
质量管理文件由质量部起草,质量部部长审核,质量负责人批准执行。
质量记录由主要使用部门起草,质量部审核,质量负责人批准使用。
质量部组织相关岗位人员学习文件,负责指导、监督和检查文件的执行。
各部门填写质量记录、凭证应真实、完整、规范,无内容项目用“/”表示,填错的地方不能随意涂改,划一横线,注明原因、日期并签名以示负责,写错的地方要仍然可以辩认。
各部门自查本部门文件的执行情况,发现不足,及时整改。
各部门使用的文件应保存完整。
如发现文件破损、丢失、影响使用时,应到质量部申请更换。
质量部应定期对现行文件进行复查,做出确认或修订意见,质量管理文件由质量部提出修订申请,填写《文件修订申请》。
新文件起草后,经质量部门负责人审核,质量负责人批准后方可执行。
新文件颁发执行之时,旧文件同时撤销、收回。
质量部对质量管理文件进行统一管理,各部门借阅、复制文件,应填写《文
题目:
编号:
版本号:
共2页
第2页
件借
阅、复制记录》,经相关负责人签字批准后方可借阅、复制文件。
破损文件、撤销文件由质量部收回,填写《文件销毁申请》,统一销毁。
2、管理文件编号系统
文件分为两类:
管理制度和工作程序。
文件编号由二组字母加一组数字组成,表示如下:
DYT—***(DaYaoTang)汉语拼音分别取第一个大写字母组成。
GZ—管理制度(GuanLiZhiDu)汉语拼音缩写,分别取第一和第三个字母组成。
GC—管理程序(GuanLiChengXu)汉语拼音缩写,分别取第一和第三个字母组成。
001—表示文件流水号
版本—2位数字表示文件修订次数
文件编号举例:
DYT—GZ—001表示大药房管理制度第一个文件
DYT-GZ-002
总经理、物料部、质量部、销售部、办公室
共2页第1页
确定质量方针,制定质量目标,促使质量管理体系不断完善。
《药品管理法》、《药品经营质量管理规范》及其实施细则和《药品流通监督管理办法》。
适用于质量方针的确定和质量目标的制定,以及对质量方针和目标的管理。
1、质量方针是由企业总经理正式发布本企业总的质量宗旨和方向。
2、质量目标是企业一定时期在质量方面所追求的目的,与质量方针保持一致。
3、本公司的质量方针为“药品质量第一,人民健康至上”。
4、本公司的质量目标为:
严格执行药品经营质量管理规范,确保药品质量,服务人民群众健康。
物料部:
保证全年购进药品的药品生产企业的资质合法,并提供供货单位的有效证件;
与供货单位签订购货合同必须以书面形式确立,内容必须含有质量条款的相关规定,并与供货单位签订有期限的质量保证协议。
购进产品的验收合格率不低于98%;
相关记录准确、完整、及时,随时做到药品储存帐、货相符;
在质量部的指导下,药品仓储合理,全年无人为质量事故发生。
药品养护率不低于98%,重点养护品种养护率100%。
药品出库复核准确无误,复核率100%,准确率100%。
近效期品种催销率100%,不合格产品无出库,过效期产品无出库。
确保首营企业及首营品种审核的审核率100%;
药品入库验收率100%;
指导在库产品的养护,保证在库药品养护率不低于98%,重点养护品种养护率100%。
不合格药品处理及时,处理率100%。
因质量问题退货比例不高于1%;
药品质量档案建档率100%。
质量查询、投诉或事故处理及时,处理率100%。
不良反应报告及时性100%。
办公室
员工继续教育和培训档案建档率100%。
质量员省级继续教育培训率100%。
直接接触药品岗位人员每年组织健康检查,检查率100%、建档率100%。
销售部
保证全年经销我单位药品的企业的资质合法,并提供销售单位的有效证件;
与销售货单位签订购货合同内容必须含有质量条款的相关规定,并与供货单位签订有期限的质量保证协议。
销售产品的质量退货率不高于2%;
收集药品不良反应信息准确、反馈及时。
5、企业在各个相关部门将质量目标逐级分解和展开,质量部每年第四季度对各部门质量目标予以奖惩。
6、企业经理每年十二月召开质量领导小组成员会议,根据国家有关法律、法规和政策方针以及企业发展规划、经营目标、上年度计划完成情况,重新审核质量方针,修订年度质量目标。
DYT-GZ-003
共1页第1页
建立质量管理体系的评审机构,促进企业质量管理体系不断完善。
企业质量方针目标、组织机构、质量管理文件、人员配备、硬件条件及质量活动状态的审核。
1、各相关部门负责提供与本部门工作有关的审核资料。
2、审核工作按年度进行,于每年的年末组织实施。
3、质量体系审核的内容:
质量方针、目标;
质量管理文件;
组织机构的设置;
人力资源的配置;
硬件设施、设备;
质量活动过程控制;
客户服务及外部环境评价;
4、纠正与预防措施的实施与跟踪
质量体系审核应对存在的缺陷提出纠正与预防措施;
各部门根据评审结果落实改进措施;
质量管理机构负责对纠正与预防措施的具体实施情况及有效性进行跟踪检查。
5、质量体系审核应按规范的格式记录,记录由质量部归档。
DYT-GZ-004
总经理、副总经理、公司各相关部门
共16页第1页
质量领导小组职责
共16页
第1页
1、岗位职能
建立公司的质量管理体系,实施企业质量方针,保证企业质量管理工作人员行使职权。
2、工作内容
组织并监督公司员工实施《药品管理法》等药品管理的法律、法规和行政规章。
建立公司的质量管理体系。
制定公司的质量方针和质量目标,组织并监督实施。
负责拟定公司质量管理部门的设置方案,制定各部门的质量管理职能。
审定企业质量管理制度。
研究和确定公司质量管理工作的重大问题。
制定公司质量奖罚措施。
3、领导责任
在公司质量方针与目标的确定、质量管理体系的有效运行、公司质量管理工作的研究确定等工作中负领导责任。
4、主要权利
审核公司的质量管理体系运行情况。
根据公司情况修订企业的质量方针和质量目标。
调整各部门岗位的质量管理职能。
审定公司质量管理制度。
对各部门岗位质量管理执行情况有奖罚权。
5、主要考核内容
公司质量方针与目标实施情况
质量管理体系运行情况。
6、人员组成
公司负责人、公司质量负责人、质量部长、物料部长、销售部长。
质量部职责
第3页
1、
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 药品 质量管理 规定 修订 制度
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
