 常见的类别异构精品资料.docx
常见的类别异构精品资料.docx
- 文档编号:1481511
- 上传时间:2022-10-22
- 格式:DOCX
- 页数:16
- 大小:110.17KB
常见的类别异构精品资料.docx
《常见的类别异构精品资料.docx》由会员分享,可在线阅读,更多相关《常见的类别异构精品资料.docx(16页珍藏版)》请在冰豆网上搜索。
常见的类别异构精品资料
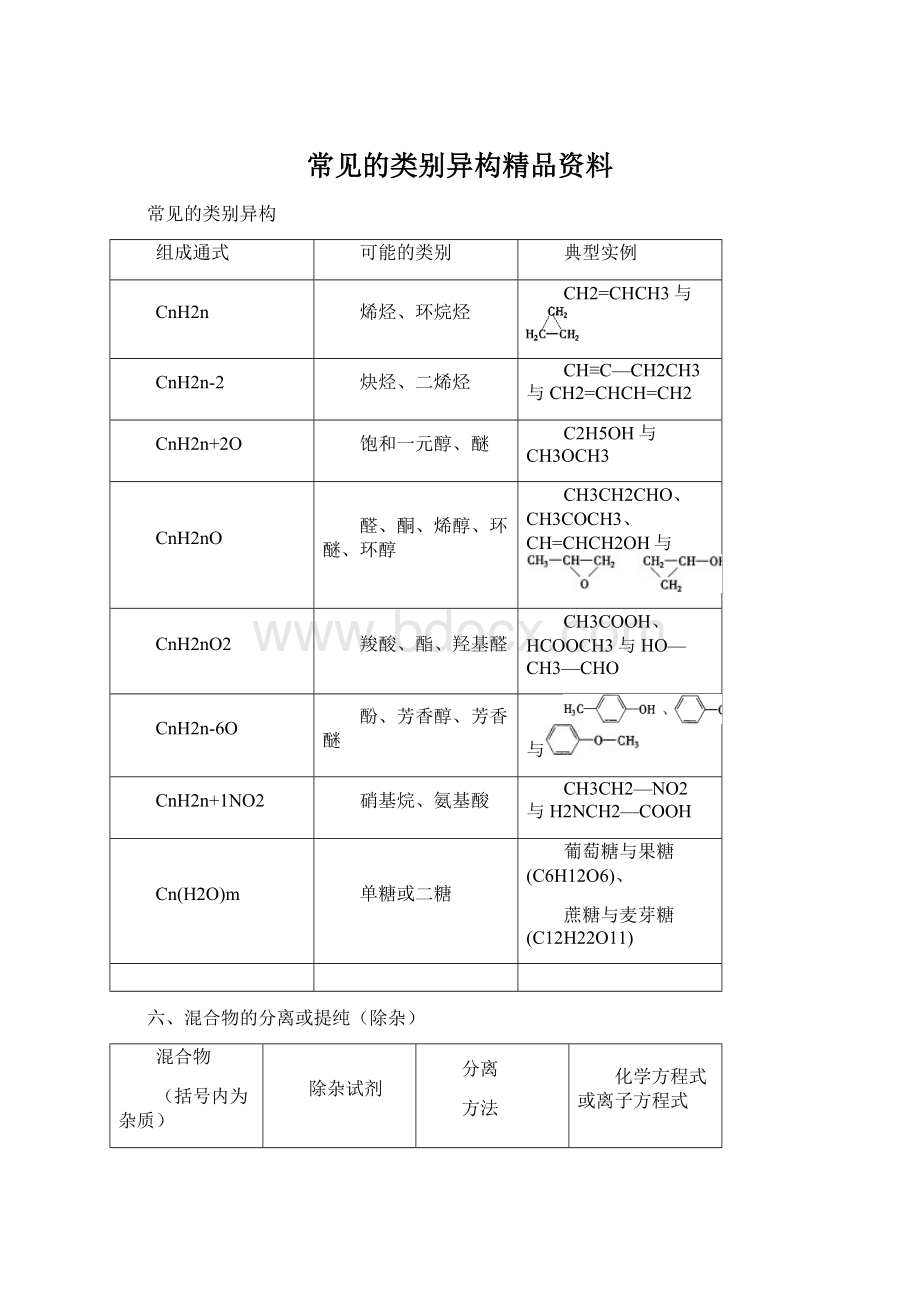
常见的类别异构
组成通式
可能的类别
典型实例
CnH2n
烯烃、环烷烃
CH2=CHCH3与
CnH2n-2
炔烃、二烯烃
CH≡C—CH2CH3与CH2=CHCH=CH2
CnH2n+2O
饱和一元醇、醚
C2H5OH与CH3OCH3
CnH2nO
醛、酮、烯醇、环醚、环醇
CH3CH2CHO、CH3COCH3、CH=CHCH2OH与
CnH2nO2
羧酸、酯、羟基醛
CH3COOH、HCOOCH3与HO—CH3—CHO
CnH2n-6O
酚、芳香醇、芳香醚
与
CnH2n+1NO2
硝基烷、氨基酸
CH3CH2—NO2与H2NCH2—COOH
Cn(H2O)m
单糖或二糖
葡萄糖与果糖(C6H12O6)、
蔗糖与麦芽糖(C12H22O11)
六、混合物的分离或提纯(除杂)
混合物
(括号内为杂质)
除杂试剂
分离
方法
化学方程式或离子方程式
乙烷(乙烯)
溴水、NaOH溶液
(除去挥发出的Br2蒸气)
洗气
CH2=CH2+Br2→CH2BrCH2Br
Br2+2NaOH=NaBr+NaBrO+H2O
乙烯(SO2、CO2)
NaOH溶液
洗气
SO2+2NaOH=Na2SO3+H2O
CO2+2NaOH=Na2CO3+H2O
乙炔(H2S、PH3)
饱和CuSO4溶液
洗气
H2S+CuSO4=CuS↓+H2SO4
11PH3+24CuSO4+12H2O=8Cu3P↓+3H3PO4+24H2SO4
提取白酒中的酒精
——————
蒸馏
——————————————
从95%的酒精中提取无水酒精
新制的生石灰
蒸馏
CaO+H2O=Ca(OH)2
从无水酒精中提取绝对酒精
镁粉
蒸馏
Mg+2C2H5OH→(C2H5O)2Mg+H2↑
(C2H5O)2Mg+2H2O→2C2H5OH+Mg(OH)2↓
提取碘水中的碘
汽油或苯或
四氯化碳
萃取
分液蒸馏
——————————————
溴化钠溶液
(碘化钠)
溴的四氯化碳
溶液
洗涤萃取分液
Br2+2I-==I2+2Br-
苯
(苯酚)
NaOH溶液或
饱和Na2CO3溶液
洗涤
分液
C6H5OH+NaOH→C6H5ONa+H2O
C6H5OH+Na2CO3→C6H5ONa+NaHCO3
乙醇
(乙酸)
NaOH、Na2CO3、NaHCO3溶液均可
洗涤
蒸馏
CH3COOH+NaOH→CH3COONa+H2O
2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
CH3COOH+NaHCO3→CH3COONa+CO2↑+H2O
乙酸
(乙醇)
NaOH溶液
稀H2SO4
蒸发
蒸馏
CH3COOH+NaOH→CH3COONa+H2O
2CH3COONa+H2SO4→Na2SO4+2CH3COOH
溴乙烷(溴)
NaHSO3溶液
洗涤
分液
Br2+NaHSO3+H2O==2HBr+NaHSO4
溴苯
(FeBr3、Br2、苯)
蒸馏水
NaOH溶液
洗涤
分液
蒸馏
FeBr3溶于水
Br2+2NaOH=NaBr+NaBrO+H2O
硝基苯
(苯、酸)
蒸馏水
NaOH溶液
洗涤
分液
蒸馏
先用水洗去大部分酸,再用NaOH溶液洗去少量溶解在有机层的酸H++OH-=H2O
提纯苯甲酸
蒸馏水
重结晶
常温下,苯甲酸为固体,溶解度受温度影响变化较大。
提纯蛋白质
蒸馏水
渗析
——————————————
浓轻金属盐溶液
盐析
——————————————
高级脂肪酸钠溶液
(甘油)
食盐
盐析
——————————————
1.常用的试剂及某些可鉴别物质种类和实验现象归纳如下:
试剂
名称
酸性高锰
酸钾溶液
溴水
银氨
溶液
新制
Cu(OH)2
FeCl3
溶液
碘水
酸碱
指示剂
NaHCO3
少量
过量
饱和
被鉴别物质种类
含碳碳双键、三键的物质、烷基苯。
但醇、醛有干扰。
含碳碳双键、三键的物质。
但醛有干扰。
苯酚
溶液
含醛基化合物及葡萄糖、果糖、麦芽糖
含醛基化合物及葡萄糖、果糖、麦芽糖
苯酚
溶液
淀粉
羧酸
(酚不能使酸碱指示剂变色)
羧酸
现象
酸性高锰酸钾紫红色褪色
溴水褪色且分层
出现白色沉淀
出现银镜
出现红
色沉淀
呈现
紫色
呈现蓝色
使石蕊或甲基橙变红
放出无色无味气体
四、烃的衍生物的重要类别和各类衍生物的重要化学性质
类别
通式
官能团
代表物
分子结构结点
主要化学性质
卤代烃
一卤代烃:
R—X
多元饱和卤代烃:
CnH2n+2-mXm
卤原子
—X
C2H5Br
(Mr:
109)
卤素原子直接与烃基结合
β-碳上要有氢原子才能发生消去反应
1.与NaOH水溶液共热发生取代反应生成醇
2.与NaOH醇溶液共热发生消去反应生成烯
醇
一元醇:
R—OH
饱和多元醇:
CnH2n+2Om
醇羟基
—OH
CH3OH
(Mr:
32)
C2H5OH
(Mr:
46)
羟基直接与链烃基结合,O—H及C—O均有极性。
β-碳上有氢原子才能发生消去反应。
α-碳上有氢原子才能被催化氧化,伯醇氧化为醛,仲醇氧化为酮,叔醇不能被催化氧化。
1.跟活泼金属反应产生H2
2.跟卤化氢或浓氢卤酸反应生成卤代烃
3.脱水反应:
乙醇
140℃分子间脱水成醚
170℃分子内脱水生成烯
4.催化氧化为醛或酮
5.一般断O—H键与羧酸及无机含氧酸反应生成酯
醚
R—O—R′
醚键
C2H5OC2H5
(Mr:
74)
C—O键有极性
性质稳定,一般不与酸、碱、氧化剂反应
酚
酚羟基
—OH
(Mr:
94)
—OH直接与苯环上的碳相连,受苯环影响能微弱电离。
1.弱酸性
2.与浓溴水发生取代反应生成沉淀
3.遇FeCl3呈紫色
4.易被氧化
醛
醛基
HCHO
(Mr:
30)
(Mr:
44)
HCHO相当于两个
—CHO
有极性、能加成。
1.与H2、HCN等加成为醇
2.被氧化剂(O2、多伦试剂、斐林试剂、酸性高锰酸钾等)氧化为羧酸
酮
羰基
(Mr:
58)
有极性、能加成
与H2、HCN加成为醇
不能被氧化剂氧化为羧酸
羧酸
羧基
(Mr:
60)
受羰基影响,O—H能电离出H+,受羟基影响不能被加成。
1.具有酸的通性
2.酯化反应时一般断羧基中的碳氧单键,不能被H2加成
3.能与含—NH2物质缩去水生成酰胺(肽键)
酯
酯基
HCOOCH3
(Mr:
60)
(Mr:
88)
酯基中的碳氧单键易断裂
1.发生水解反应生成羧酸和醇
2.也可发生醇解反应生成新酯和新醇
硝酸酯
RONO2
硝酸酯基
—ONO2
不稳定
易爆炸
硝基化合物
R—NO2
硝基—NO2
一硝基化合物较稳定
一般不易被氧化剂氧化,但多硝基化合物易爆炸
氨基酸
RCH(NH2)COOH
氨基—NH2
羧基—COOH
H2NCH2COOH
(Mr:
75)
—NH2能以配位键结合H+;—COOH能部分电离出H+
两性化合物
能形成肽键
蛋白质
结构复杂
不可用通式表示
肽键
氨基—NH2
羧基—COOH
酶
多肽链间有四级结构
1.两性
2.水解
3.变性
4.颜色反应
(生物催化剂)
5.灼烧分解
糖
多数可用下列通式表示:
Cn(H2O)m
羟基—OH
醛基—CHO
羰基
葡萄糖
CH2OH(CHOH)4CHO
淀粉(C6H10O5)n
纤维素
[C6H7O2(OH)3]n
多羟基醛或多羟基酮或它们的缩合物
1.氧化反应
(还原性糖)
2.加氢还原
3.酯化反应
4.多糖水解
5.葡萄糖发酵分解生成乙醇
油脂
酯基
可能有碳碳双键
酯基中的碳氧单键易断裂
烃基中碳碳双键能加成
1.水解反应
(皂化反应)
2.硬化反应
1.能使溴水(Br2/H2O)褪色的物质
(1)有机物
①通过加成反应使之褪色:
含有、—C≡C—的不饱和化合物
②通过取代反应使之褪色:
酚类
注意:
苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀。
③通过氧化反应使之褪色:
含有—CHO(醛基)的有机物(有水参加反应)
注意:
纯净的只含有—CHO(醛基)的有机物不能使溴的四氯化碳溶液褪色
④通过萃取使之褪色:
液态烷烃、环烷烃、苯及其同系物、饱和卤代烃、饱和酯
(2)无机物
①通过与碱发生歧化反应
3Br2+6OH-==5Br-+BrO3-+3H2O或Br2+2OH-==Br-+BrO-+H2O
②与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、I-、Fe2+
2.能使酸性高锰酸钾溶液KMnO4/H+褪色的物质
(1)有机物:
含有、—C≡C—、—OH(较慢)、—CHO的物质
与苯环相连的侧链碳碳上有氢原子的苯的同系物(与苯不反应)
(2)无机物:
与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、Br-、I-、Fe2+
3.与Na反应的有机物:
含有—OH、—COOH的有机物
与NaOH反应的有机物:
常温下,易与含有酚羟基、—COOH的有机物反应
加热时,能与卤代烃、酯反应(取代反应)
与Na2CO3反应的有机物:
含有酚羟基的有机物反应生成酚钠和NaHCO3;
含有—COOH的有机物反应生成羧酸钠,并放出CO2气体;
含有—SO3H的有机物反应生成磺酸钠并放出CO2气体。
与NaHCO3反应的有机物:
含有—COOH、—SO3H的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO2气体。
(四)、同分异构体数目的判断方法
1.记忆法记住已掌握的常见的异构体数。
例如:
(1)凡只含一个碳原子的分子均无异构;
(2)丁烷、丁炔、丙基、丙醇有2种;
(3)戊烷、戊炔有3种;
(4)丁基、丁烯(包括顺反异构)、C8H10(芳烃)有4种;
(5)己烷、C7H8O(含苯环)有5种;
(6)C8H8O2的芳香酯有6种;
(7)戊基、C9H12(芳烃)有8种。
2.基元法例如:
丁基有4种,丁醇、戊醛、戊酸都有4种
3.替代法例如:
二氯苯C6H4Cl2有3种,四氯苯也为3种(将H替代Cl);又如:
CH4的一氯代物只有一种,新戊烷C(CH3)4的一氯代物也只有一种。
4.对称法(又称等效氢法)等效氢法的判断可按下列三点进行:
(1)同一碳原子上的氢原子是等效的;
(2)同一碳原子所连甲基上的氢原子是等效的;
(3)处于镜面对称位置上的氢原子是等效的(相当于平面成像时,物与像的关系)。
具有特定碳、氢比的常见有机物
牢牢记住:
在烃及其含氧衍生物中,氢原子数目一定为偶数,若有机物中含有奇数个卤原子或氮原子,则氢原子个数亦为奇数。
①当n(C)︰n(H)=1︰
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 常见 类别 精品 资料
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
