 河南省郑州市中原区教师招聘考试高中化学教师试卷AB及答案.doc
河南省郑州市中原区教师招聘考试高中化学教师试卷AB及答案.doc
- 文档编号:204899
- 上传时间:2022-10-06
- 格式:DOC
- 页数:10
- 大小:465.50KB
河南省郑州市中原区教师招聘考试高中化学教师试卷AB及答案.doc
《河南省郑州市中原区教师招聘考试高中化学教师试卷AB及答案.doc》由会员分享,可在线阅读,更多相关《河南省郑州市中原区教师招聘考试高中化学教师试卷AB及答案.doc(10页珍藏版)》请在冰豆网上搜索。
姓名________学科________准考证号_____________考场_________座号________
························密············封············线···························
···
···
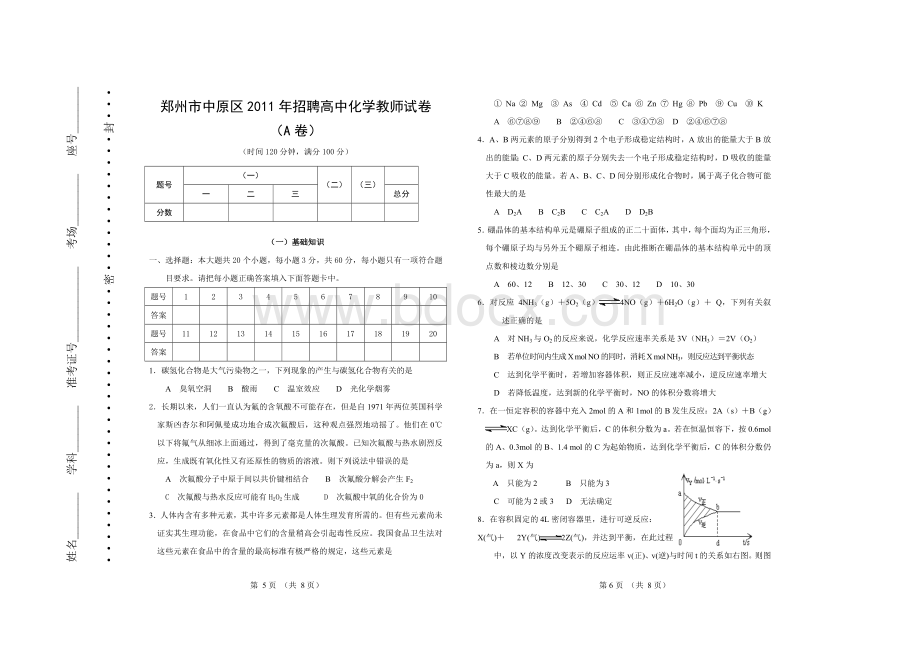
郑州市中原区2011年招聘高中化学教师试卷
(A卷)
(时间120分钟,满分100分)
(一)基础知识
题号
(一)
(二)
(三)
一
二
三
总分
分数
一、选择题:
本大题共20个小题,每小题3分,共60分,每小题只有一项符合题目要求。
请把每小题正确答案填入下面答题卡中。
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
1.碳氢化合物是大气污染物之一,下列现象的产生与碳氢化合物有关的是
A臭氧空洞B酸雨C温室效应D光化学烟雾
2.长期以来,人们一直认为氟的含氧酸不可能存在,但是自1971年两位英国科学家斯凶杏尔和阿佩曼成功地合成次氟酸后,这种观点强烈地动摇了。
他们在0℃以下将氟气从细冰上面通过,得到了毫克量的次氟酸。
已知次氟酸与热水剧烈反应,生成既有氧化性又有还原性的物质的溶液。
则下列说法中错误的是
A次氟酸分子中原于间以共价键相结合B次氟酸分解会产生F2
C次氟酸与热水反应可能有H2O2生成D次氟酸中氧的化合价为0
3.人体内含有多种元素,其中许多元素都是人体生理发育所需的。
但有些元素尚未证实其生理功能,在食品中它们的含量稍高会引起毒性反应。
我国食品卫生法对这些元素在食品中的含量的最高标准有极严格的规定,这些元素是
①Na②Mg③As④Cd⑤Ca⑥Zn⑦Hg⑧Pb⑨Cu⑩K
A⑥⑦⑧⑨B②④⑥⑧C③④⑦⑧D②④⑥⑦⑧
4.A、B两元素的原子分别得到2个电子形成稳定结构时,A放出的能量大于B放出的能量;C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量。
若A、B、C、D间分别形成化合物时,属于离子化合物可能性最大的是
AD2ABC2BCC2ADD2B
5.硼晶体的基本结构单元是硼原子组成的正二十面体,其中,每个面均为正三角形,每个硼原子均与另外五个硼原子相连。
由此推断在硼晶体的基本结构单元中的顶点数和棱边数分别是
A60、12B12、30C30、12D10、30
6.对反应4NH3(g)+5O2(g)4NO(g)+6H2O(g)+Q,下列有关叙述正确的是
A对NH3与O2的反应来说,化学反应速率关系是3V(NH3)=2V(O2)
B若单位时间内生成XmolNO的同时,消耗XmolNH3,则反应达到平衡状态
C达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D若降低温度,达到新的化学平衡时,NO的体积分数将增大
7.在一恒定容积的容器中充入2mol的A和1mol的B发生反应:
2A(s)+B(g)XC(g)。
达到化学平衡后,C的体积分数为a。
若在恒温恒容下,按0.6mol的A、0.3mol的B、1.4mol的C为起始物质,达到化学平衡后,C的体积分数仍为a,则X为
A只能为2B只能为3
C可能为2或3D无法确定
8.在容积固定的4L密闭容器里,进行可逆反应:
X(气)+2Y(气)2Z(气),并达到平衡,在此过程中,以Y的浓度改变表示的反应运率v(正)、v(逆)与时间t的关系如右图。
则图中阴影部分面积表示
AX的浓度减少BY的物质的量减少
CZ的浓度增加DX的物质的量减少
9.镍镉充电电池,电极材料是Cd和NiO(OH),电解质是KOH,电极反应分别是:
Cd+2OH---2e-=Cd(OH)2
2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH--
下列说法不正确的是
A电池放电时,负极周围溶液的pH不断增大
B电池的总反应是Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2
C电池充电时,镉元素被还原
D电池充电时,电池的正极和电源的正极相连接
10.在25℃时,纯水的电离度为a1,pH=11的氨水中水的电离度为a2,pH=3的盐酸中水的电离度为a3。
若将上述氨水与盐酸等体积混合,所得溶液中水的电离度为a4,则下列关系式正确的是
Aa1<a2<a3<a4Ba3<a2<a1<a4
Ca2<a3<a1<a4Da2<a3<a4<a1
11.广义水解观认为,无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,再两两重新组合成新物质。
根据上述观点,下列说法不正确的是
A.CaO2的水解产物是Ca(OH)2和H2O2 B.NaClO的水解产物之一是HClO
C.PCl3的水解产物是PH3和HClO D.Mg3N2水解生成NH3和Mg(OH)2
12.用铁酸钠(Na2FeO4)对未来河湖的淡水消毒是城市饮用水处理的一种新技术,下列对Na2FeO4用于饮用水消毒处理的分析正确的是
ANa2FeO4在溶液中显强酸性,能消毒杀菌
B在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌
CNa2FeO4的氧化产物Fe3+水解为Fe(OH)3胶体,可使水中悬浮物凝聚沉降
DNa2FeO4的还原产物Fe2+水解为Pe(OH)2胶体,可使水中悬浮物凝聚沉降
13.将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀,则通入的气体可能是下列中的
ACO2BNH3CNO2DH2S
14.已知C—C单键可以绕键轴自由旋转,结构简式为的烃,含一个苯环且处于同一平面的碳原子个数至少有
A8个B9个C10个D11个
15.在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”,凡是有一个手性碳原子的物质一定具有光学活性。
例如,有机化合物:
有光学活性,分别发生下列反应①与甲酸发生酯化反应,②与NaOH水溶液共热,③与银氨溶液作用,④在催化剂存在下与H2作用后,生成的有机物无光学活性的是
A①②B②③C②④D③④
16.环己烷可表示为:
,篮烷可表示为:
,则篮烷的一溴代物所具有的同分异构体有
A.2种B.3种C.4种D.5种
17.下列化学实验的方法和结果都正确的是
ACH3COONa·3H2O与碱石灰混合并热可以很快制得大量的CH4
B向碘水中通入H2S气体至反应完全,过滤可得氢碘酸
C将稀硫酸和乙醇的混合物加热,迅速升温至170℃,则可制得乙烯
D将甲烷气体与溴蒸气混合光照后,可制得纯净的二溴甲烷
18.已知在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。
工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。
欲除去溶液中的杂质离子,下述方法中可行的是
A加入纯Cu将Fe2+还原为Fe
B向溶液中通入H2S使Fe2+沉淀
C向溶液中通入Cl2,再通入NH3,调节pH值为4~5
D向溶液中通入Cl2,再加入纯净的CuO粉末调节pH值为4~5
19.取100mL18.3mol/L的H2SO4与Zn反应,当Zn完全溶解时,生成的气体在标准状况下占有的体积为11.2L。
将所得的溶液稀释成1L,测得溶液中H+浓度为1mol/L,则所生成的气体中SO2和H2的体积比约为
A1︰2B2︰1C1︰4D4︰1
20.NaCl溶液中可能混有杂质NaOH、NaHCO3、Na2CO3中的一种或二种,为测定溶液中混有的杂质成分,可进行如下实验操作:
分别取二份等体积混合液,用盐酸的标准液(0.10mol·L-1)滴定,以酚酞或甲基橙为指示剂,达到终点时消耗盐酸的体积分别为V1和V2,且V2>V1。
则NaCl溶液中混有的杂质可能为
ANaOHBNa2CO3CNa2CO3、NaHCO3DNaOH、Na2CO3
二.实验题
21.(9分)某学生试用电解法根据电报上析出的物质的质量来验证阿伏加德罗常数值,其实验方案的要点为:
(1)用直流电源电解CuCl2溶液,所用仪器如右图:
(2)在电流强度为1安培,通电时间为t秒时,精确测得某电极上析出的Cu的质量为mg。
回答:
(1)连接这些仪器的正确顿序为E接,C接,接F。
实验线路中的电流方向为→→→→→,
(2)写出B极上发生反应的离子方程式,
G试管中淀粉K1溶液变化的现象为,
相应的离子方程式为,
(3)为精确测定电极上析出Cu的质量,所必需的实验步骤的先后顺序应是(选填下列操作步骤的编号),
①称量电解前电极质量②刮下电解后电极上的Cu,并清洗③用蒸馏水清洗电解后电极④低温烘干电极后称量⑤低温烘干刮下的Cu后称量⑥再次低温烘干后称量到恒重。
(4)已知电子的电量为1.6×10—19C,试列出阿伏加德罗常数的计算表达式
NA=。
22.(8分)实验室里用加热正丁醇、溴化钠和浓H2SO4的混合物的方法来制备1一溴丁烷时,还会有烯、醚和溴等产物生成。
反应结束后将反应混合物蒸馏,分离得到1一溴丁烷,已知有关的有机物的性质如下:
熔点(℃)
沸点(℃)
密度(g/cm3)
正丁醇
–89.53
117.25
0.81
1–溴丁烷
–112.4
101.6
1.28
丁醚
95.3
142
0.76
1–丁烯
–185.3
–6.5
0.59
(1)生成1一溴丁烷的反应化学方程式是,
(2)反应中由于发生副反应而生成副产物的反应类型有,
(3)生成1一溴丁烷的反应装置应选用上图中的(填序号),反应加热时的温度t,应控制在100℃(填<、>或=),
(4)反应结束后,将反应混合物中1一溴丁烷分离出,应选用的装置是,
该操作应控制的温度t2范围是。
(5)在最后得到1一溴丁烷的产物中,可能含有的杂质主要是,将其
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 河南省 郑州市 中原 教师 招聘 考试 高中化学 试卷 AB 答案 精品 文档
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
 新办个体工商户.ppt
新办个体工商户.ppt
