 九年级化学中考常见化学式和化学方程式.docx
九年级化学中考常见化学式和化学方程式.docx
- 文档编号:24131137
- 上传时间:2023-05-24
- 格式:DOCX
- 页数:14
- 大小:40.74KB
九年级化学中考常见化学式和化学方程式.docx
《九年级化学中考常见化学式和化学方程式.docx》由会员分享,可在线阅读,更多相关《九年级化学中考常见化学式和化学方程式.docx(14页珍藏版)》请在冰豆网上搜索。
九年级化学中考常见化学式和化学方程式
九年级化学常见化学式和化学方程式
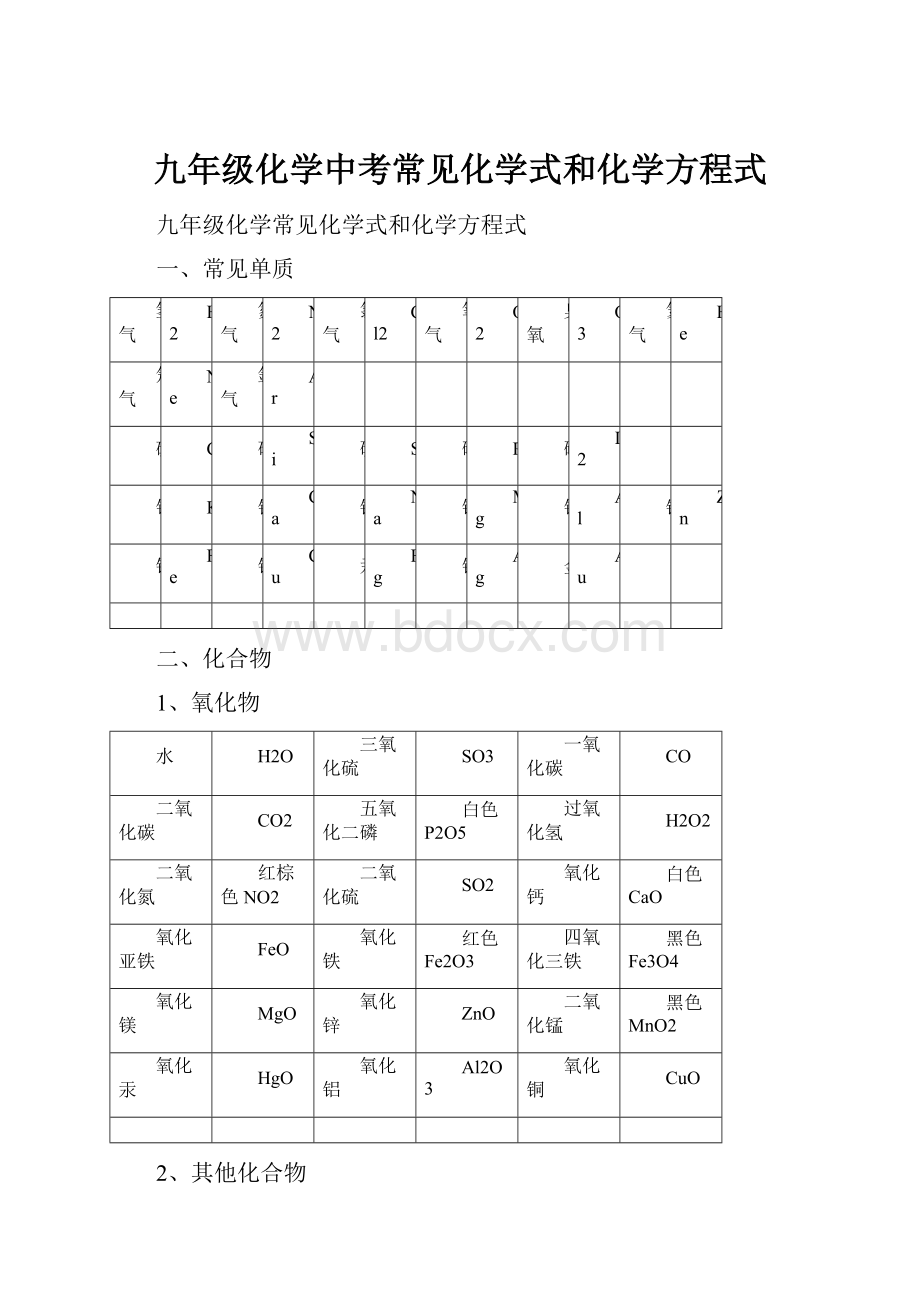
一、常见单质
氢气
H2
氮气
N2
氯气
Cl2
氧气
O2
臭氧
O3
氦气
He
氖气
Ne
氩气
Ar
碳
C
硅
Si
硫
S
磷
P
碘
I2
钾
K
钙
Ca
钠
Na
镁
Mg
铝
Al
锌
Zn
铁
Fe
铜
Cu
汞
Hg
银
Ag
金
Au
二、化合物
1、氧化物
水
H2O
三氧化硫
SO3
一氧化碳
CO
二氧化碳
CO2
五氧化二磷
白色P2O5
过氧化氢
H2O2
二氧化氮
红棕色NO2
二氧化硫
SO2
氧化钙
白色CaO
氧化亚铁
FeO
氧化铁
红色Fe2O3
四氧化三铁
黑色Fe3O4
氧化镁
MgO
氧化锌
ZnO
二氧化锰
黑色MnO2
氧化汞
HgO
氧化铝
Al2O3
氧化铜
CuO
2、其他化合物
硝酸
HNO3
硫酸
H2SO4
盐酸
HCl
碳酸
H2CO3
硫化氢
H2S
氢氧化钠
NaOH
氢氧化钾
KOH
氢氧化钙
Ca(OH)2
氢氧化镁
Mg(OH)2
氢氧化铝
Al(OH)3
氢氧化锌
Zn(OH)2
氢氧化铁
红褐色Fe(OH)3
氢氧化亚铁
Fe(OH)2
氢氧化铜
兰色Cu(OH)2
氢氧化钡
Ba(OH)2
氨水
NH3·H2O
氯化钠
NaCl
氯化铜
CuCl2
氯化铝
AlCl3
氯化钾
KCl
氯化亚铁
FeCl2
氯化铁
FeCl3
氯化银
AgCl
氯化钙
CaCl2
氯化镁
MgCl2
氯化钡
BaCl2
氯化锌
ZnCl2
硫酸铜
CuSO4
高锰酸钾
暗紫色KMnO4
锰酸钾
K2MnO4
氯酸钾
白色KClO3
碳酸钙
CaCO3
硝酸钾
KNO3
硝酸钠
NaNO3
硝酸铁
Fe(NO3)3
硝酸亚铁
Fe(NO3)2
硝酸铝
Al(NO3)3
碳酸钠
Na2CO3
碳酸钙
CaCO3
碳酸铵
(NH4)2CO3
碳酸氢钠
NaHCO3
硫酸铁
Fe2(SO4)3
硫酸亚铁
FeSO4
硝酸银
AgNO3
硝酸钡
Ba(NO3)2
硝酸铵
NH4NO3
硫酸钡
BaSO4
3、常见有机化合物
甲烷
CH4
乙醇〔酒精〕
C2H5OH
葡萄糖
C6H12O6
写出以下反响的化学方程式〔加下划线的方程式请掌握反响的现象〕
一、化合反响
1、红磷在空气〔或氧气〕中燃烧:
4P+5O22P2O5
2、氢气在空气中燃烧生成水:
2H2+O22H2O
3、硫磺在空气〔或氧气〕中燃烧:
S+O2SO2
4、镁条在空气〔或氧气〕中燃烧:
2Mg+O22MgO
5、铁丝在氧气中燃烧:
3Fe+2O2Fe3O4
6、木炭在空气〔或氧气〕中完全燃烧:
C+O2CO2
7、木炭不充分燃烧:
2C+O22CO
8、一氧化碳燃烧:
2CO+O22CO2
9、二氧化碳、二氧化硫三氧化硫分别和水反响生成相应的酸:
CO2+H2O==H2CO3
SO2+H2O==H2SO3〔亚硫酸〕SO3+H2O==H2SO4
10、二氧化碳通过灼热的炭层:
CO2+C2CO
11、生石灰与水反响:
CaO+H2O==Ca(OH)2
二、分解反响
12、高锰酸钾制氧气:
2KMnO4K2MnO4+MnO2+O2↑
13、氯酸钾制氧气:
2KClO32KCl+3O2↑
14、双氧水制氧气:
2H2O22H2O+O2↑
15、电解水:
2H2O2H2↑+O2↑
16、碳酸分解:
H2CO3H2O+CO2↑
17、高温煅烧石灰石:
CaCO3CaO+CO2↑
三、置换反响
18、铜和硝酸银溶液反响:
Cu+2AgNO3==2Ag+Cu(NO3)2
19、铁和硫酸铜溶液反响:
Fe+CuSO4==Cu+FeSO4
20、锌、铁、镁、铝分别和硫酸反响:
Zn+H2SO4==ZnSO4+H2↑
Fe+H2SO4==FeSO4+H2↑Mg+H2SO4==MgSO4+H2↑
2Al+3H2SO4==Al2(SO4)3+3H2↑
21、锌、铁、镁、铝分别和盐酸反响:
Zn+2HCl==ZnCl2+H2↑
Fe+2HCl==FeCl2+H2↑Mg+2HCl==MgCl2+H2↑
2Al+6HCl==2AlCl3+3H2↑
22、木炭复原氧化铁:
3C+2Fe2O34Fe+3CO2↑
木炭复原氧化铜:
C+2CuO2Cu+CO2↑
四、复分解反响
〔一〕酸+碱→盐+水
23、氢氧化钠分别与盐酸、硫酸反响:
NaOH+HCl==NaCl+H2O
2NaOH+H2SO4==Na2SO4+2H2O
24、氢氧化铜分别与盐酸、硫酸反响:
Cu(OH)2+2HCl==CuCl2+2H2O
Cu(OH)2+H2SO4==CuSO4+2H2O
25、氢氧化铝治疗胃酸过多:
Al(OH)3+3HCl==AlCl3+3H2O
26、氢氧化镁分别与盐酸、硫酸反响:
Mg(OH)2+2HCl==MgCl2+2H2O
Mg(OH)2+H2SO4==MgSO4+2H2O
27、氢氧化铁分别与盐酸、硫酸反响:
Fe(OH)3+3HCl==FeCl3+3H2O
Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O
28、氢氧化钙分别与盐酸、硫酸反响:
Ca(OH)2+2HCl==CaCl2+2H2O
Ca(OH)2+H2SO4==CaSO4+2H2O
〔二〕酸+盐→另一种酸+另一种盐
29、盐酸与硝酸银溶液反响:
HCl+AgNO3==AgCl↓+HNO3
30、氯化钡溶液与硫酸溶液反响:
BaCl2+H2SO4==BaSO4↓+2HCl
31、碳酸钠与稀盐酸:
Na2CO3+2HCl==2NaCl+H2O+CO2↑
32、石灰石与稀盐酸反响制取二氧化碳:
CaCO3+2HCl=CaCl2+H2O+CO2↑
33、碳酸氢钠用于治疗胃酸过多:
NaHCO3+HCl==NaCl+H2O+CO2↑
34、碳酸钡与盐酸反响:
BaCO3+2HCl=BaCl2+H2O+CO2↑
〔三〕碱溶液+盐溶液→另一种碱+另一种盐
35、硫酸铜溶液和氢氧化钠溶液反响:
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
36、氯化铁溶液和氢氧化钠溶液反响:
FeCl3+3NaOH==Fe(OH)3↓+3NaCl
37、碳酸钠溶液和石灰水反响:
Na2CO3+Ca(OH)2==CaCO3↓+2NaOH
〔四〕盐溶液+盐溶液→两种新盐
38、硝酸银溶液与氯化钠溶液反响:
AgNO3+NaCl==AgCl↓+NaNO3
39、氯化钡溶液与碳酸钠溶液反响:
BaCl2+Na2CO3=BaCO3↓+2NaCl
40、氯化钡溶液与硫酸钠溶液反响:
BaCl2+Na2SO4=BaSO4↓+2NaCl
〔五〕金属氧化物+酸→盐+水
41、稀盐酸或稀硫酸清洗铁锈:
6HCl+Fe2O3==2FeCl3+3H2O
Fe2O3+3H2SO4==Fe2(SO4)3+3H2O
42、氧化铜分别与稀硫酸、稀盐酸反响:
CuO+H2SO4==CuSO4+H2O
CuO+2HCl==CuCl2+2H2O
五、其他反响类型
43、二氧化碳通入澄清石灰水中:
CO2+Ca(OH)2==CaCO3↓+H2O〔验证二氧化碳〕
44、二氧化碳与氢氧化钡反响:
CO2+Ba(OH)2==BaCO3↓+H2O
45、氢氧化钠在空气中变质:
CO2+2NaOH=Na2CO3+H2O〔吸收二氧化碳〕
46、氢氧化钠溶液吸收二氧化硫:
SO2+2NaOH==Na2SO3+H2O〔用于吸收二氧化硫〕
〔亚硫酸钠〕
47、氢氧化钠溶液吸收三氧化硫:
SO3+2NaOH==Na2SO4+H2O
48、三氧化硫与氢氧化钡反响:
SO3+Ba(OH)2==BaSO4↓+H2O
49、一氧化碳复原氧化铜:
CO+CuOCu+CO2
50、一氧化碳复原氧化铁:
3CO+Fe2O32Fe+3CO2
51、酒精燃烧:
C2H5OH+3O22CO2+3H2O
52、甲烷燃烧:
CH4+2O2CO2+2H2O
一、初中化学常见物质的颜色
〔一〕、固体的颜色
1、红色固体:
铜,氧化铁
2、绿色固体:
碱式碳酸铜
3、蓝色固体:
氢氧化铜,硫酸铜晶体
4、紫黑色固体:
高锰酸钾
5、淡黄色固体:
硫磺
6、无色固体:
冰,干冰,金刚石
7、银白色固体:
银,铁,镁,铝,汞等金属
8、黑色固体:
铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,〔碳黑,活性炭〕
9、红褐色固体:
氢氧化铁
10、白色固体:
氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁
〔二〕、液体的颜色
11、无色液体:
水,双氧水
12、蓝色溶液:
硫酸铜溶液,氯化铜溶液,硝酸铜溶液
13、浅绿色溶液:
硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液
14、黄色溶液:
硫酸铁溶液,氯化铁溶液,硝酸铁溶液
15、紫红色溶液:
高锰酸钾溶液
16、紫色溶液:
石蕊溶液
〔三〕、气体的颜色
17、红棕色气体:
二氧化氮
18、黄绿色气体:
氯气
19、无色气体:
氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体
二、初中化学溶液的酸碱性
1、显酸性的溶液:
酸溶液和某些盐溶液〔硫酸氢钠、硫酸氢钾等〕
2、显碱性的溶液:
碱溶液和某些盐溶液〔碳酸钠、碳酸氢钠、碳酸钾等〕
3、显中性的溶液:
水和大多数的盐溶液
三、初中化学敞口置于空气中质量改变的
〔一〕质量增加的
1、由于吸水而增加的:
氢氧化钠固体,氯化钙,氯化镁,浓硫酸
2、由于跟水反响而增加的:
氧化钙、氧化钡、氧化钾、氧化钠,硫酸铜
3、由于跟二氧化碳反响而增加的:
氢氧化钠,氢氧化钾,氢氧化钡,氢氧化钙
〔二〕质量减少的
1、由于挥发而减少的:
浓盐酸,浓硝酸,酒精,汽油,浓氨水
2、由于风化而减少的:
碳酸钠晶体
四、初中化学物质的检验
〔一〕 、气体的检验
1、氧气:
带火星的木条放入瓶中,假设木条复燃,那么是氧气.
2、氢气:
在玻璃尖嘴点燃气体,罩一干冷小烧杯,观察杯壁是否有水滴,往烧杯中倒入澄清的石灰水,假设不变浑浊,那么是氢气.
3、二氧化碳:
通入澄清的石灰水,假设变浑浊那么是二氧化碳.
4、氨气:
湿润的紫红色石蕊试纸,假设试纸变蓝,那么是氨气.
5、水蒸气:
通过无水硫酸铜,假设白色固体变蓝,那么含水蒸气.
〔二〕、离子的检验.
6、氢离子:
滴加紫色石蕊试液/参加锌粒
7、氢氧根离子:
酚酞试液/硫酸铜溶液
8、碳酸根离子:
稀盐酸和澄清的石灰水
9、氯离子:
硝酸银溶液和稀硝酸,假设产生白色沉淀,那么是氯离子
10、硫酸根离子:
硝酸钡溶液和稀硝酸/先滴加稀盐酸再滴入氯化钡
11、铵根离子:
氢氧化钠溶液并加热,把湿润的红色石蕊试纸放在试管口
12、铜离子:
滴加氢氧化钠溶液,假设产生蓝色沉淀那么是铜离子
13、铁离子:
滴加氢氧化钠溶液,假设产生红褐色沉淀那么是铁离子
〔三〕、相关例题
14、如何检验NaOH是否变质:
滴加稀盐酸,假设产生气泡那么变质
15、检验生石灰中是否含有石灰石:
滴加稀盐酸,假设产生气泡那么含有石灰石
16、检验NaOH中是否含有NaCl:
先滴加足量稀硝酸,再滴加AgNO3溶液,假设产生白色沉淀,那么含有NaCl
17、检验三瓶试液分别是稀HNO3,稀HCl,稀H2SO4"
向三只试管中分别滴加Ba(NO3)2 溶液,假设产生白色沉淀,那么是稀H2SO4;再分别滴加AgNO3溶液,假设产生白色沉淀那么是稀HCl,剩下的是稀HNO3
18、淀粉:
参加碘溶液,假设变蓝那么含淀粉
19、葡萄糖:
参加新制的氢氧化铜,假设生成砖红色的氧化亚铜沉淀,就含葡萄糖
五、初中化学之三
1、我国古代三大化学工艺:
造纸,制火药,烧瓷器。
2、氧化反响的三种类型:
爆炸,燃烧,缓慢氧化。
3、构成物质的三种微粒:
分子,原子,离子。
4、不带电的三种微粒:
分子,原子,中子。
5、物质组成与构成的三种说法:
〔1〕二氧化碳是由碳元素和氧元素组成的;
(2)二氧化碳分子由碳原子和氧原子构成;
〔3〕一个二氧化碳分子由一个碳原子和两个氧原子构成
5、氢氧化钙(Ca(OH)2):
熟石灰,消石灰
6、二氧化碳固体(CO2):
干冰
7、氢氯酸(HCl):
盐酸
8、碱式碳酸铜(Cu2(OH)2CO3):
铜绿
9、硫酸铜晶体(CuSO4 .5H2O):
蓝矾,胆矾
10、甲烷 (CH4):
沼气
11、乙醇(C2H5OH):
酒精
12、乙酸(CH3COOH):
醋酸
13、过氧化氢(H2O2):
双氧水
14、汞(Hg):
水银
15、碳酸氢钠〔NaHCO3〕:
小苏打
八、物质的除杂
1、CO2〔CO〕:
把气体通过灼热的氧化铜,
2、CO〔CO2〕:
通过足量的氢氧化钠溶液
3、H2〔水蒸气〕:
通过浓硫酸/通过氢氧化钠固体
九、化学之最
1、未来最理想的燃料是 H2
2、最简单的有机物是 CH4
3、密度最小的气体是 H2
4、相对分子质量最小的物质是 H2
5、相对分子质量最小的氧化物是H2O
6、化学变化中最小的粒子是原子
7、PH=0时,酸性最强 ,碱性最弱
PH=14时,碱性最强 ,酸性最弱
8、土壤里最缺乏的是 N,K,P 三种元素,肥效最高的氮肥是尿素
9、天然存在最硬的物质是 金刚石
10、最早利用天然气的国家是 中国
11、地壳中含量最多的元素是 氧
12、地壳中含量最多的金属元素是 铝
13、空气里含量最多的气体是 氮气
14、空气里含量最多的元素是 氮
15、当今世界上最重要的三大化石燃料是 煤,石油,天然气
16、形成化合物种类最多的元素:
碳
十、有关不同
1、金刚石和石墨的物理性质不同:
是因为 碳原子排列不同
2、生铁和钢的性能不同:
是因为 含碳量不同
3、一氧化碳和二氧化碳的化学性质不同:
是因为 分子构成不同
〔氧气和臭氧的化学性质不同是因为分子构成不同;水和双氧水的化学性质不同是因为分子构成不同〕
4、元素种类不同:
是因为质子数不同
5、元素化合价不同:
是因为最外层电子数不同
6、钠原子和钠离子的化学性质不同:
是因为最外层电子数不
7、原子与分子的不同:
在化学变化中分子可以再分,而原子不可再分
8、原子与离子的不同:
原子呈电中性,质子数=电子总数;离子带有电荷,质子数不等于电子数
十一、有关一样
碱具有相似化学性质的原因:
不同的碱溶液具有一样的OH–
酸具有相似化学性质的原因:
不同的酸溶液具有一样的H+
十一、一定和不一定
十二:
有毒的物质
1、 有毒的固体:
亚硝酸钠〔NaNO2〕,乙酸铅等
2、 有毒的液体:
汞,硫酸铜溶液,甲醇,含Ba2+的溶液(除BaSO4) 、甲醛
3、 有毒的气体:
CO,氮的氧化物,硫的氧化物
十三:
实验室制法
1、实验室氧气
KMnO4=====
KClO3======
H2O2====
2、实验室制氢气
Zn+H2SO4===
4、 实验室制CO2:
CaCO3+HCl==
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 九年级 化学 中考 常见 化学式 化学方程式
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《当代世界政治与经济》.docx
《当代世界政治与经济》.docx
