 新课标1高考压轴卷 理科综合.docx
新课标1高考压轴卷 理科综合.docx
- 文档编号:2928338
- 上传时间:2022-11-16
- 格式:DOCX
- 页数:23
- 大小:335.85KB
新课标1高考压轴卷 理科综合.docx
《新课标1高考压轴卷 理科综合.docx》由会员分享,可在线阅读,更多相关《新课标1高考压轴卷 理科综合.docx(23页珍藏版)》请在冰豆网上搜索。
新课标1高考压轴卷理科综合
新课标I高考压轴卷
理科综合化学
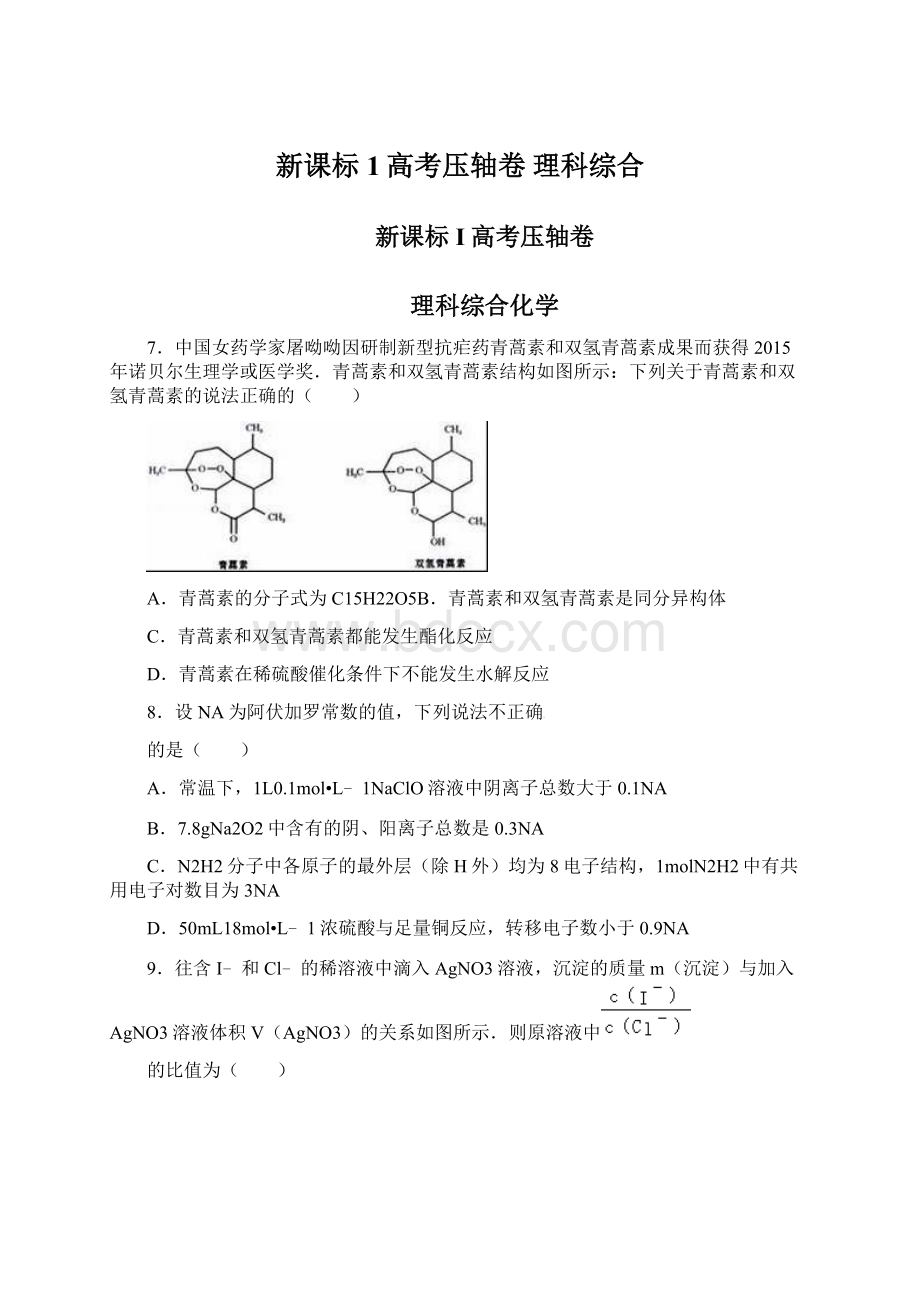
7.中国女药学家屠呦呦因研制新型抗疟药青蒿素和双氢青蒿素成果而获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素结构如图所示:
下列关于青蒿素和双氢青蒿素的说法正确的( )
A.青蒿素的分子式为C15H22O5B.青蒿素和双氢青蒿素是同分异构体
C.青蒿素和双氢青蒿素都能发生酯化反应
D.青蒿素在稀硫酸催化条件下不能发生水解反应
8.设NA为阿伏加罗常数的值,下列说法不正确
的是( )
A.常温下,1L0.1mol•L﹣1NaClO溶液中阴离子总数大于0.1NA
B.7.8gNa2O2中含有的阴、阳离子总数是0.3NA
C.N2H2分子中各原子的最外层(除H外)均为8电子结构,1molN2H2中有共用电子对数目为3NA
D.50mL18mol•L﹣1浓硫酸与足量铜反应,转移电子数小于0.9NA
9.往含I﹣和Cl﹣的稀溶液中滴入AgNO3溶液,沉淀的质量m(沉淀)与加入AgNO3溶液体积V(AgNO3)的关系如图所示.则原溶液中
的比值为( )
A.
B.
C.
D.
10.X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是( )
A.五种元素中,原子半径最大的是W
B.Y与Z形成的化合物都可以和盐酸反应
C.Y的简单阴离子比W的简单阴离子还原性强
D.Z与Q形成的化合物水溶液一定显酸性
11.已知高能锂电池的总反应式为:
2Li+FeS═Fe+Li2S[LiPF6.SO(CH3)2为电解质],用该电池为电源进行如图的电解实验,电解一段时间测得甲池产生标准状况下H24.48L.下列有关叙述不正确的是( )
A.从隔膜中通过的离子数目为0.4NA
B.若电解过程体积变化忽略不计,则电解后甲池中溶液浓度为4mol/L
C.A电极为阳极
D.电源正极反应式为:
FeS+2Li++2e﹣═Fe+Li2S
12.下列实验“操
作和现象”与“结论”都正确的是( )
选项
操作和现象
结论
A
向盛有2mL0
.1mol/LAgNO3溶液的试管中,先滴几滴0.1mol/LKCl溶液,再滴加0.1mol/LKI溶液。
试管中先出现白色沉淀,后出现淡黄色沉淀
Ksp(AgCl) B 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变 Fe(NO3)2与H2SO4不反应 C 在分液 漏斗中加入碘水后再加入CCl4,充分振荡,分层,下层溶液呈紫色 CCl4可作为碘的萃取剂 D 测定饱和NaClO溶液、CH3COONa溶液的pH,pH(NaClO)>pH(CH3COONa) 弱酸的酸性: HClO 13.25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ,滴定曲线如图所示。 下列说法正确的是 A.在相同温度下,同浓度的三种酸溶液的导电能力顺序: HZ<HY<HX B.根据滴定曲线,可得Ka(HY)≈10-5 C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时: c(X-)>c(Y-)>c(OH-)>c(H+) D.HY与HZ混合,达到平衡时: c(H+)= +c(Z-)+c(OH-) 26.(14分)铁触媒(铁的某氧化物)是工业合成氨的催化剂。 某同学设计了以下两种方案研究铁触媒的组成。 方案一: 用下列流程测定铁触媒的含铁量,确定其组成。 (1)步骤④后面需用(填仪器名称)取25.00mL稀释后溶液。 (2)因为通入Cl2不足量,“溶液B”中还含有会影响测定结果。 (3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2。 请设计实验方案检验Cl2,完成下列实验报告。 限选试剂: 0.1mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL·L-1KSCN溶液 实验操作 实验现象与结论 方案二: 用下列实验方法测定铁触媒的含铁量,确定其组成。 (4)“干燥管C”的作用是。 (5)称取15.2g铁触媒进行上述实验。 充分反应后,测得“干燥管B”增重11.0g,则该铁触媒的化学式可表示为。 27.(14分)某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁.其生产工艺流程如下: 已知: ①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42﹣; ②TiOSO4水解的反应为: TiOSO4+(x+1)H2O→TiO2·xH2O↓+H2SO4. 请回答: (1)步骤①所得滤渣的主要成分为,分离硫酸亚铁溶液和滤渣的操作中所用的玻璃仪器是;步骤②中得到硫酸亚铁晶体的操作为蒸发浓缩、. (2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为. (3)步骤④的离子方程式是. (4)已知: FeCO3(S) Fe2+(aq)+CO32﹣(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因. (5)实验室中常用KMnO4滴定法测定晶体中FeSO4·7H2O的质量分数,取步骤②中所得FeSO4·7H2O晶体样品ag,配成500.00mL溶液,取出25.00mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应).若消耗0.1000mol·L﹣1KMnO4溶液25.00mL,则所得晶体中FeSO4·7H2O的质量分数为(用a表示)。 28.(15分)研究发现,含pm2.5的雾霾主要成分有SO2、NOx、CxHy及可吸入颗粒等. (1)雾霾中能形成酸雨的物质是 (2)为消除NOx对环境的污染,可利用NH3在一定条件下与NO反应生成无污染的气体. 已知: 4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)△H=﹣905.48kJ•mol﹣1 N2(g)+O2(g)⇌2NO(g)△H=+180.50kJ•mol﹣1 ①下列表示NH3(g)与NO(g)在一定条件下反应,生成无污染气体的能量转化关系示意图1正确的是: (填字母) ②图2是反应4NH3(g)+6NO(g)⇌5N2(g)+6H2O(g) 过程中NH3的体积分数随X变化的示意图2,X代表的物理量可能是 ,原因是 . (3)图3电解装置可将雾霾中的SO2、NO转化为(NH4)2SO4,①阴极的电极反应式是 . ②物质A是 (填化学式),理由是 . (4)为减少雾霾、降低大气中有害气体含量,研究机动车尾气中CO、NOx及CxHy的排放量意义重大.机动车尾气污染物的含量与空/燃比(空气与燃油气的体积比)的变化关系示意图如图4: 请解释: ①随空/燃比增大,CO和CxHy的含量减少的原因是 . ②当空/燃比达到15后,NOx减少的原因可能是 . 38.【选修5《有机化学基础》(15分)】化合F是一种重要的有机合成中间体,它的合成路线如下: 请认真分析和推理回答下列问题: (1)由B生成C的化学反应类型是;化合物F中含氧官能团的名称是_____________________________________; (2)写出化合物C与乙酸反应生成酯的化学方程式: ____________________________________________________________________。 (3)写出化合物B的结构简式: _______________________________。 同时满足下列条件的B的同分异构体(不包括B)共有___________种: ①苯环上只有两个取代基②能与FeCl3溶液显紫色, (4)工业上以苯酚()和烃W为主要原料制备有机物3-乙基-1,6-已二酸的合成路线 流程图如下: 提示: 3-乙基-1,6-已二酸的结构简如下图: ①写出X、Z的结构简式: X: __________________________,Z: _________________________; ②写出苯酚与W反应的化学方程式: _______________________________________________________________。 KS5U2016新课标高考压轴卷化学答案及解析 7.A解: A.由结构简式可知青蒿素的分子式为C15H22O5,故A正确; B.青蒿素的分子式为C15H22O5,双氢青蒿素的分子式为C15H24O5,二者分子式不同,不是同分异构体,故B错误; C.青蒿素不含羟基或羧基,不能发生酯化反应,故C错误; D.青蒿素含有酯基,可水解,故D错误. 8.C解: A、根据电荷守恒可知,溶液中存在: n(ClO﹣)+n(OH﹣)=n(Na+)+n(H+),由于溶液中n(Na+)=1mol/L×1L=1mol,故溶液中的阴离子的物质的量大于1mol,个数大于NA个,故A正确; B、7.8g过氧化钠的物质的量为0.1mol,而1mol过氧化钠中含2mol钠离子和1mol过氧根,故0.1mol过氧化钠中含0.3NA个离子,故B正确; C、N2H2分子中各原子的最外层(除H外)均为8电子结构,可知N2H2的结构式为H﹣N=N﹣H,故1mol中含4mol共用电子对即4NA对,故C错误; D、铜只能与浓硫酸反应,与稀硫酸不反应,故浓硫酸变稀后反应即停止,即硫酸不能反应完全,则转移的电子数小于0.9NA个,故D错误. 故选C. 9.C解: 因为I﹣+Ag+=AgI↓,Cl﹣+Ag+=AgCl↓,可以看出I﹣、Cl﹣跟Ag+反应都是1: 1的关系,由图中可知: AgI的沉淀量为V1(黄色沉淀是AgI),而AgCl的沉淀量为V2﹣V1,所以c(I﹣): c(Cl﹣)= .故选C. 10.B解: 短周期主族元素.W的单质是黄色固体,则W为S,由X、Y、W在周期表中的相对位置可知,Y为O,X为C,X、Y、Z、W、Q是原子序数依次增大,所以Q为Cl,其中只有Z是金属,则Z可能为Na、Mg、Al中的一种, A.五种元素中,原子半径最大的是Z,故A错误; B.Y与Z形成的化合物为金属氧化物,都可以和盐酸反应,故B正确; C.氧气的氧化性比硫单质强,单质的氧化性越弱对应离子的还原性强,所以Y的简单阴离子比W的简单阴离子还原性弱,故C错误; D.若Z为Na,则Z与Q形成的化合物NaCl的水溶液为中性,故D错误; 故选B. 11. C解: A、由反应FeS+2Li=Fe+Li2S可知,Li被氧化,应为原电池的负极,FeS被还原生成Fe,为正极反应,正极方程式为FeS+2e﹣=Fe+S2﹣,甲连接原电池负极,A为阴极,生成氢气,电极方程式为2H++2e﹣=H2↑,n(H2)= =0.2mol,转移0.4mol电子,生成0.4molOH﹣,则隔膜H中通过的K+离子数为0.4mol,通过的离子数目为0.4NA,故A正确; B、甲连接原电池负极,为阴极,生成氢气,电极方程式为2H++2e﹣=H2↑,n(H2)=0.2mol,转移0.4mol电子,生成0.4molOH﹣,则隔膜H中通过的K+离子数为0.4mol,c(OH﹣)= =4mol/L,即电解后甲池中溶液浓度为4mol/L,故B正确; C、A电极为阴极,故C错误; D、FeS被还原生成Fe,为正极反应,正极方程式为Fe
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 新课标1高考压轴卷 理科综合 新课 高考 压轴 理科 综合
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
