 化学平衡图像题目补充.docx
化学平衡图像题目补充.docx
- 文档编号:3953157
- 上传时间:2022-11-26
- 格式:DOCX
- 页数:6
- 大小:360.38KB
化学平衡图像题目补充.docx
《化学平衡图像题目补充.docx》由会员分享,可在线阅读,更多相关《化学平衡图像题目补充.docx(6页珍藏版)》请在冰豆网上搜索。
化学平衡图像题目补充
化学平衡图像题目补充
1.光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性碳催化下合成。
(1)实验室中常用来制备氯气的化学方程式为_________;
答案:
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为-890.3kJ·mol-1、-285.8kJ·mol-1和-283.0kJ·mol-1,则生成1m3(标准状况)CO所需热量为___________;
答案:
5.52×103kJ
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为___________;
答案:
CHCl3+H2O2=HCl+H2O+COCl2
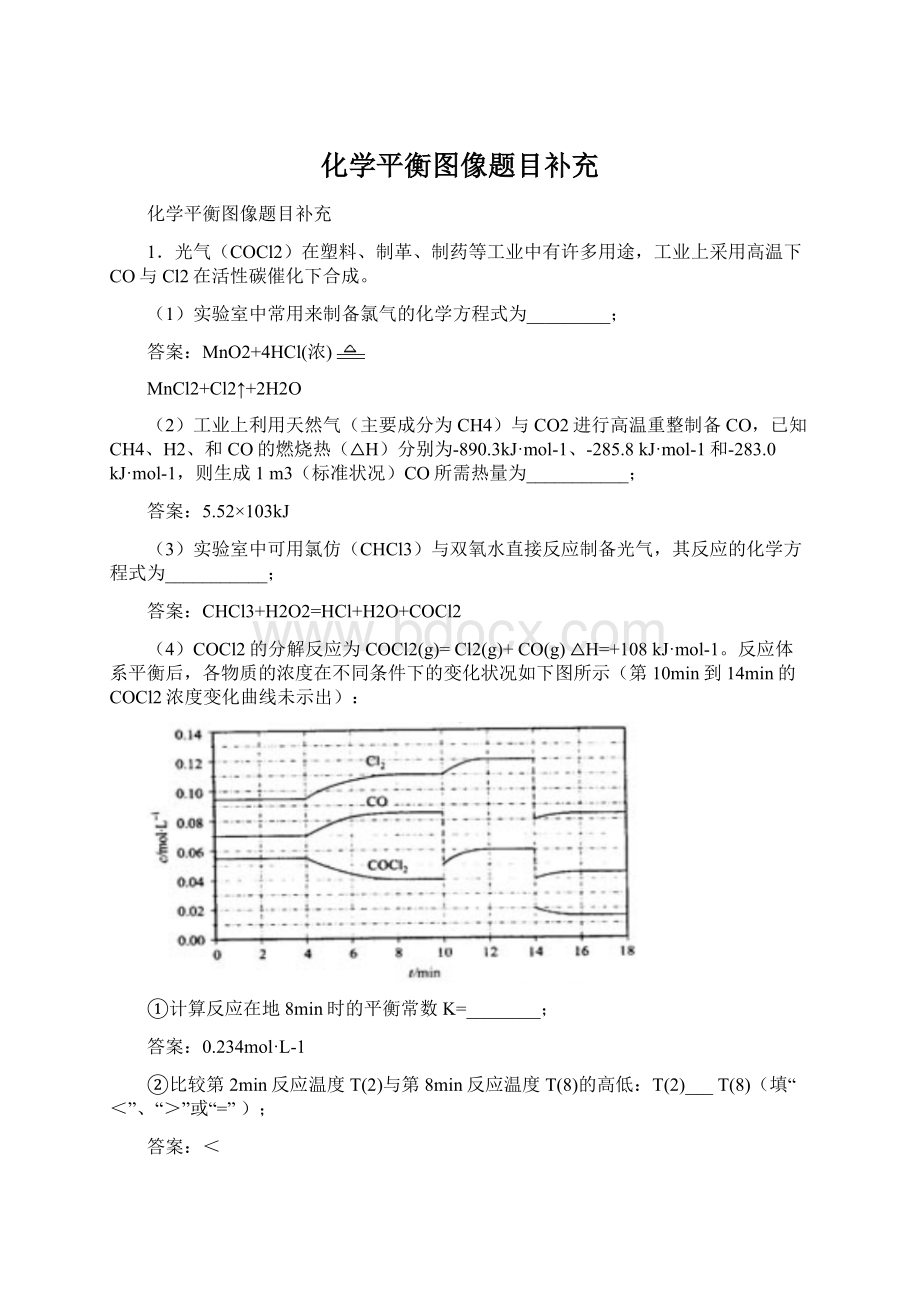
(4)COCl2的分解反应为COCl2(g)=Cl2(g)+CO(g)△H=+108kJ·mol-1。
反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出):
①计算反应在地8min时的平衡常数K=________;
答案:
0.234mol·L-1
②比较第2min反应温度T
(2)与第8min反应温度T(8)的高低:
T
(2)___T(8)(填“<”、“>”或“=”);
答案:
<
③若12min时反应与温度T(8)下重新达到平衡,则此时c(COCl2)=__mol·L-1
答案:
0.031
④比较产物CO在2-3min、5-6min和12-13min时平均反应速率[平均反应速率分别以v(2-3)、v(5-6)、v(12-13)表示]的大小________;
答案:
v(5-6)>v(2-3)=v(12-13)
⑤比较反应物COCl2在5-6min和15-16min时平均反应速率的大小:
v(5-6)___v(15-16)(填“<”、“>”或“=”),原因是_______
答案:
>;在相同温度时,该反应的反应物浓度越高,反应速率越大
反应aA(g)+bB(g)
cC(g)(ΔH<0)在等容条件下进行。
改变其他反应条件,
在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
(1)反应的化学方程式中,a:
b:
c为_______;
(2)A的平均反应速率vI(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为_______;
(3)B的平衡转化率αI(B)、αⅡ(B)、αⅢ(B)中最小的是_____,其值是_______;
(4)由第一次平衡到第二次平衡,平衡移动的方向是_____,采取的措施是__________;
(5)比较第II阶段反应温度(T2)和第III阶段反应速度(T3)的高低:
T2T3(填“>、=、<”)
判断的理由是;
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示
IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C)。
【解析】⑴依据图示第一次达到平衡时,A、B、C三种物质的物质的量的变化分别为1mol、3mol、2mol,故a∶b∶c=1∶3∶2。
⑵vⅠ(A)=(2.0-1.00)mol·L-1/20.0min=0.05mol·L-1·min-1、vⅡ(A)=(1.00-0.62)/15.0min=0.025mol·L-1·min-1、vⅢ(A)=(0.62-0.50)mol·L-1/10min=0.012mol·L-1·min-1。
故大小顺序为vⅠ(A)>vⅡ(A)>vⅢ(A)。
⑶由图可知αⅠ(B)=0.5、αⅡ(B)=1.14/3.00=0.38、αⅢ(B)=0.36/1.86=0.19,则B的平衡转化率最小的是αⅢ(B),其值为0.19。
⑷第一次平衡后,A、B的浓度从平衡点开始降低,而C的物质的量浓度突然变为0,则平衡向右移动,此时采取的措施是将C从平衡混合物中液化分离出去。
⑸因为生成物的浓度增大,反应向正方向进行,该反应为放热反应,故恒容下的措施应为降低温度,故T2﹥T3。
⑹容积加倍,体系压强减小,平衡向逆反应方向移动,作图要点:
①容积加倍的瞬间,各组分浓度都变为原来的1/2;②A、B的新平衡浓度比原来的1/2要大,而C的浓度比原浓度的1/2要小。
【答案】
(1)1:
3:
2
(2)vⅠ(A)>vⅡ(A)>vⅢ(A)
(3)αⅢ(B)0.19(4)向右移动将C从平衡混合物中液化分离出去(5)>由于平衡正向移动,且反应放热,在恒容条件下只能降低温度,故T2>T3
27.(15分)在溶液中,反应A+2B
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L及c(C)=0mol/L。
反应物A的浓度随时间的变化如下图所示。
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。
所改变的条件和判断的理由是:
②___________________________________________________________________
③___________________________________________________________________
(2)实验②平衡时B的转化率为_______;实验③平衡时C的浓度为___________;
(3)该反应的
H______0,其判断理由是___________________________________________
(4)该反应进行到4.0min时的平均反应速率:
实验②:
=_____________________________________________________________
实验③:
=______________________________________________________________
28.(15分)(注意:
在试题卷上作答无效)
有A,B,C,D,E和F六瓶无色溶液,它们都是中学化学中常用的无机试剂。
纯E为无色油状液体;B,C,D和F是盐溶液,且它们的阴离子均不同。
现进行如下实验:
1A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
2将A分别加入其它物种溶液中,只有D,F中有沉淀生成;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
3将B分别加入C,D,E,F中,C,D,F中产生沉淀,E中有无色,无味气体溢出;
4将C分别加入D,E,F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1)能确定的溶液是(写出溶液标号与相应溶质的化学式):
____________________________________________________
____________________________________________________
(2)不能确定的溶液,写出其标号,溶质可能的化学式及进一步鉴别的方法:
____________________________________________________
____________________________________________________
28.(15分)(注意:
在试题卷上作答无效)
反应aA(g)+bB(g)
cC(g)(
H<0)在等容条件下进行。
改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)反应的化学方程式中,a:
b:
c为;
(2)A的平均反应速率
(A)、
(A)、
(A)从大到小排列次序为;
(3)B的平衡转化率
中最小的是,其值是;
(4)由第一次平衡到第二次平衡,平衡移动的方向是,采取的措施是;
(5)比较第II阶段反应温度(
)和第III阶段反应速度(
)的高低:
填“>、=、<”判断的理由是;
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学平衡 图像 题目 补充
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
