 08年高考试题分析.docx
08年高考试题分析.docx
- 文档编号:10251714
- 上传时间:2023-02-09
- 格式:DOCX
- 页数:13
- 大小:132.14KB
08年高考试题分析.docx
《08年高考试题分析.docx》由会员分享,可在线阅读,更多相关《08年高考试题分析.docx(13页珍藏版)》请在冰豆网上搜索。
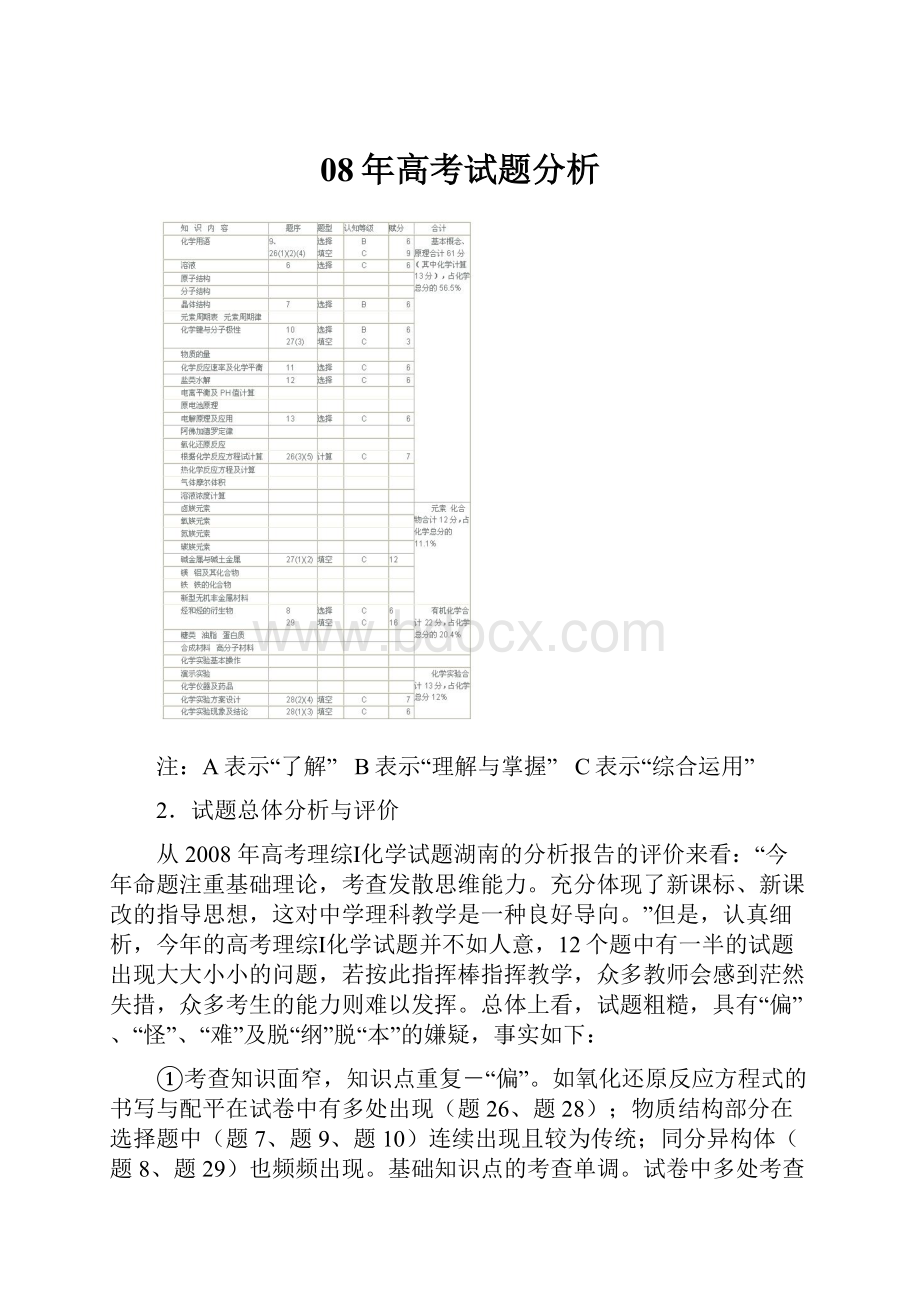
08年高考试题分析
注:
A表示“了解” B表示“理解与掌握” C表示“综合运用”
2.试题总体分析与评价
从2008年高考理综Ⅰ化学试题湖南的分析报告的评价来看:
“今年命题注重基础理论,考查发散思维能力。
充分体现了新课标、新课改的指导思想,这对中学理科教学是一种良好导向。
”但是,认真细析,今年的高考理综Ⅰ化学试题并不如人意,12个题中有一半的试题出现大大小小的问题,若按此指挥棒指挥教学,众多教师会感到茫然失措,众多考生的能力则难以发挥。
总体上看,试题粗糙,具有“偏”、“怪”、“难”及脱“纲”脱“本”的嫌疑,事实如下:
①考查知识面窄,知识点重复-“偏”。
如氧化还原反应方程式的书写与配平在试卷中有多处出现(题26、题28);物质结构部分在选择题中(题7、题9、题10)连续出现且较为传统;同分异构体(题8、题29)也频频出现。
基础知识点的考查单调。
试卷中多处考查基础知识的试题缺乏新意,命题角度陈旧,如题7物质熔点高低的比较、题9化合物的判断等。
没有体现选择题的功能之一:
考查基础知识覆盖面广。
②能力考查题基于创新,脱“纲”、脱“本”-“怪”。
试卷中许多能力考查题远远超出常规,走出中学化学教材,低起高落,如题8的同分异构体的判断,题27的碳化钙燃烧、题28的黄色粉未MZ等。
③试题语言描述似是而非,计算设计简单运算繁-“难”。
试卷中有好多地方语言描述不规范,让考生无所适从,难以动笔,如题12中的甲、乙酸的表述,题27中V与水反应的生成物的描述、题29中苯环上一溴代物的描述,题26的计算等。
6.在溶液中加入足量的Na2O2后仍能大量共存的离子组是
A.NH4+、Ba2+、Cl—、NO3—B.K+、AlO2—、Cl—、SO42—
C.Ca2+、Mg2+、NO3—、HCO3—D.Na+、Cl—、CO32—、SO32—
答案:
B。
解析:
考查知识点:
附加条件下的离子共存问题,过氧化钠的性质。
过氧化钠有强氧化性,溶于水生成氢氧化钠和氧气,由此可得A中,NH4++OH-=NH3·H2O;
B中的离子之间不发生反应,与过氧化钠也不反应,故可以大量共存。
C中,HCO3—+OH—=CO32—+H2O,Ca2++CO3—=CaCO3↓,Mg2++CO32—=MgCO3↓;
D中的SO32—具有较强的还原性,过氧化钠会将其氧化成SO42-。
点评:
关于附加条件下的离子共存问题是近年来高考化学的热点,但今年考查的附加条件为在溶液中加入足量的Na2O2,在中学教材内所学的知识为Na2O2转化为NaOH和O2,而Na2O2在碱性环境氧化SO32—是中学化学没有要求的,有超“纲”之嫌,也易误导考生选D,因此,这样的高考试题对于考生来说并不能真正的考查出其能力,有误导中学教学的作用。
7.下列化合物,按其晶体的熔点由高到低排列正确的是
A.SiO2CsClCBr4CF4B.SiO2CsClCF4CBr4
C.CsClSiO2CBr4CF4D.CF4CBr4CsClSiO2
答案:
A。
解析:
考查知识点:
物质结构中不同类型的晶体的判断、物质熔点高低比较的方法。
比较固体物质的熔点时,首先是区分各晶体的类型:
SiO2为原子晶体,CsCl为离子晶体,CBr4、CF4分别为分子晶体。
这几类晶体的熔点高低一般为:
原子晶体>离子晶体>分子晶体。
在结构相似的分子晶体中,分子的相对分子质量越大,熔点越高:
CBr4>CF4(注意:
若有氢键,应注意氢键的影响)
点评:
该题考查知识点基础,试题覆盖面窄、选项单调,没有体现能力立意的观点,不符合高考试题的选拔功能。
8.下列各组物质不属于同分异构体的是
A.2,2-二甲基丙醇和2-甲基丁醇B.邻氯甲苯和对氯甲苯
C.2-甲基丁烷和戊烷D.甲基丙烯酸和甲酸丙酯
答案:
D。
解析:
考查知识点:
同分异构体的判断、根据有机物名称写出其结构简式。
根据有机物的名称,知道各选项中有机物的碳原子数是一样多的。
D选项中的甲基丙烯酸中有两个双键(碳碳双键和碳氧双键),而甲酸丙酯中只有一个碳氧双键,故这两种物质不是同分异构体。
点评:
该题虽是考同分异构体的判断,不如说是考根据有机物名称写出其结构简式的问题,而命名在中学化学教材中仅仅详细的学习了烷烃,其它有机物未作要求,而选项A、D明显超出教材和高考大纲的基本要求。
9.下列各组给定原子序数的元素,不能形成原子数之比为1:
1稳定化合物的是
A.3和17B.1和8C.1和6D.7和12
答案:
D。
解析:
考查知识点:
元素周期律、原子序数、原子结构与物质构成的关系。
依据原子序数得:
A.锂和氯,LiCl;B项中,H和O,H2O2;C项中,H和C,C6H6、C2H2等;D项中,N和Mg,Mg3N2。
点评:
本题是依据原子序数书写原子间可能形成的化合物,属于较基础的题目,但命题的角度陈旧,因此,此题虽注重基础,但能力考核平平,有引导教死书之嫌。
在课改的今天出现这样的题在理综试题中,是不应该的。
10.下列叙述中正确的是
A.NH3、CO、CO2都是极性分子B.CH4、CCl4都是含有极性键的非极性分子
C.HF、HCl、HBr、HI的稳定性一次增强D.CS2、H2O、C2H2都是直线型分子
答案:
B。
解析:
考查知识点:
分子的空间构型、化学键的极性、分子的极性、氢化物的稳定性判断。
A中CO2分子中含有极性键但分子为直线型,为非极性分子;B中分子为正四面体型,说法正确;C按照此顺序,F、Cl、Br、I非金属性依次减弱,各物质的稳定性依次减小;D水分子不是直线型的,是V形结构。
点评:
该试题基础性、综合性较强,覆盖知识点为中学化学教学内容,考生普片认可。
11.已知:
4NH3(g)+5O2(g)=4NO(g)+6H2O(g),△H=—1025kJ/mol,该反应是一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是
答案:
C。
解析:
考查知识点:
温度、压强、催化剂如何影响化学反应的速率及它们对化学平衡移动的影响;会分析化学平衡的有关图像问题。
4NH3(g)+5O2(g)=4NO(g)+6H2(g).△H=-1025KJ/mol。
该反应是一个可逆反应。
正反应是一个气体体积缩小的放热反应。
因此,温度越高,反应速率越快,达到平衡的时间越短;升高温度时,平衡向逆反应方向移动,NO的含量降低,故A是正确的,C是错误的。
增大压强,反应速率加快,达到平衡的时间缩短,平衡向逆反应方向移动,NO的含量降低,故B是正确的。
加入催化剂,反应速率加快,达到平衡式的时间缩短,但NO的含量不变,故D是正确的。
点评:
本题是借助图象考查化学平衡的试题,该题呈现方式传统,图象简单明了,考生几乎不要读题即可找到答案,作为理综试题是否能在考查基础的同时,强化能力的考查。
12.已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1mol/L的NaA和NaB混合溶液中,下列排列正确的是
A.c(OH—)>c(HA)>c(HB)>c(H+)B.c(OH—)>c(A—)>c(B—)>c(H+)
C.c(OH—)>c(B—)>c(A—)>c(H+)D.c(OH—)>c(HB)>c(HA)>c(H+)
答案:
A。
解析:
考查知识点:
电解质溶液中盐类的水解、酸的电离、溶液中离子浓度大小比较等知识。
在一般情况下,酸越弱,对应的盐的水解程度越大,故同浓度的NaA和NaB,前者水解程度更大,因此其溶液中HA的浓度更大一些。
盐类的水解一般来说是一些比较弱的反应,盐溶液中水解生成的分子的浓度要远小于原来的盐电离出的离子的浓度。
又因为盐类水解的实质是阴离子或阳离子结合了水电离出的氢离子或氢氧根离子,使得其相应浓度剧烈减小,一般的,要小于生成的弱电解质分子的浓度。
点评:
该题语言描述模糊不清,试题中甲酸、乙酸为HCOOH、CH3COOH还是未知的以字母代替的甲乙等物质,如为HCOOH、CH3COOH,答案选A还有一定的道理,若为未知的以字母代替的甲乙等物质,乙酸(HA)的酸性比甲酸(HB)弱,甲酸(HB)是否也是弱酸?
显然不一定!
当甲酸为强酸时,如盐酸,此时NaA和NaB混合溶液中,结论“c(HB)>c(H+)”显然错误!
因为溶液中显然无盐酸物质,选项A则不正确。
在高考试题中出现语言描述不清问题,易使优秀生无所适从!
13.电解100mL含c(H+)=0.30mol/L的下列溶液。
当电路中通过0.04mol电子时,理论上析出金属质量最大的是
A.0.10mol/LAg+B.0.20mol/LZn2+
C.0.20mol/LCu2+D.0.20mol/LPb2+
答案:
C。
解析:
考查知识点:
电解的基本原理、离子的放电顺序、电子守恒的应用及计算。
题目中涉及到了五种阳离子,当电解时,其放电的先后顺序一般情况是:
Ag+、Cu2+、H+、Pb2+、Zn2+,当电路中通过0.04mol电子时,理论上析出金属质量依次是:
Ag:
0.10mol/L×0.1L×108g/mol=1.08g;Cu:
0.2mol/L×0.1L×64g/mol=1.28g;
Pb:
(0.04mol-0.03mol)÷2×207g/mol=1.05(化学教材中一般也认为H2O中H+继续放电,无金属铅析出);Zn:
(0.04mol-0.03mol)÷2×65g/mol=0.325g(中学化学教材一般也认为H2O中H+继续放电,无金属锌析出)。
点评:
溶液中离子放电的先后顺序不仅与金属活动顺序有关,还与电压、离子的浓度等有关,该题在电解时,若0.020molPb2+完全放电,则理论上析出金属质量为0.2mol/L×0.1L×207g/mol===4.14g,选项D为正确答案,在溶液中关于Pb2+放电问题在过去高考试题中曾多次 出现采用信息给与题的方式对铅蓄电池的考查中就涉及到了(如06年重庆高考理综题27)。
当铅蓄电池充电时,就是在酸性条件下电解PbSO4,此时为Pb2+离子放电,这样针对该题,难道就不需要考虑Pb2+离子首先放电吗?
另外,考生还经常遇到电镀锌的问题,这难道不是锌离子放电吗?
我们认为命题者要科学、严谨,不能闭门造车,要回避中学化学中难以讲清晰的知识点,这样才有利于对学生进行知识能力的考查,也有利于中学化学的教学。
(二)非选择题
26.(16分)
实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:
软锰矿和过量的固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩溶液,结晶得到深紫色的针状KMnO4。
试回答:
(1)软锰矿制备K2MnO4的化学方程式是;
(2)K2MnO4制备KMnO4的离子方程式是;
(3)若用2.5g软锰矿(含MnO280%)进行上述实验,计算KMnO4的理论产量:
(4)KMnO4能与热的经硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的化学方程式是;
(5)上述制得的KMnO4产品0.165g,恰好与0.335g纯Na2C2O4反应。
计算该KMnO4的纯度。
解析:
考查知识点:
氧化还原反应方程式的书写与配平、离子方程式的书写、化学计算等。
(1)反应中的变价元素是锰和氯,锰元素由+4价升高为+6价,氯元素由+5价降低到-1价,根据化合价升降总数相等,参加反应的二氧化锰和氯酸钾的物质的量之比为3:
1。
故该反应的化学方程式是:
3MnO2+KClO3+6KOH
3K2MnO4+KCl+3H2O.
(2)根据化合价变化和电荷守恒可写出并配平该离子方程式:
3MnO42—+4H+=MnO2↓+2MnO4—+2H2O
(3)根据
(1)和
(2)中的两个方程式可以得到关系式:
3MnO2——————2KMnO4
3×872×158
2.5g×80%m(KMnO4)
m(KMnO4)=2×158×2.5g×80%/(3×87)=2.4g。
(4)2KMnO4+8H2SO4+5Na2C2O42MnSO4+K2SO4+10CO2↑+5Na2SO4+8H2O
(5)根据(4)中的化学方程式:
2KMnO4————————5Na2C2O4
2×1585×134
m(KMnO4)0.335g
m(KMnO4)=2×158×0.335g/(5×134)=0.158g
KMnO4纯度=(0.158g/0.165g)×100%=95.8%.
答案:
见[解析]。
点评:
该试题为信息给予题,它能够较好的考查学生的自学能力与逻辑推理能力,试题立意较好,尊重了化学研究的实践性,但是题中出现了两个计算题,并在计算过程中所涉及到的物质式量是中学化学中不常见的,而所给的数据又来自于实验数据,我们认为,在高考有限的黄金时间内,让考生去做原理简单但计算繁琐的两个计算试题,是不妥当的。
这有无意浪费考生的时间和精力之嫌。
27.(15分)V、W、X、Y、Z是由周期表中1~20号部分元素组成的5种化合物,其中V、W、X、Z均为两种元素组成,上述5种化合物涉及的所有元素的原子序数之和等于35。
它们之间的反应关系如下图:
(1)5种化合物分别是V 、W 、X 、Y 、Z :
(填化学式)
(2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是 :
(3)V的电子式是 。
解析:
考查知识点:
元素及其化合物推断及相关知识点。
V与O2反应生成W与X,而W与X为两种元素组成,故W、X为氧化物,再由框图中W与X的物理性质,可初步猜测W为CaO,X为CO2,运用逆向推理,可知V应该为CaC2,再由CaC2与H2O反应正向推理,生成白色固体Y应为Ca(OH)2,无色气体Z应为C2H2,由此可得答案。
答案:
(1)CaC2、CaO、CO2、Ca(OH)2、C2H2;
(2)2CO2+Ca(OH)2===Ca(HCO3)2
(3)CaC2电子式
点评:
框图式推断题是历年来高考的热点试题,综合性较强,它能较好地考查考生对中学化学中的元素化合物知识掌握的情况,并考查考生分析问题和处理问题的能力。
但是今年该试题有如下遗憾:
1、语言描述上欠妥当,如20号以内的元素组成的化合物与水反应生成白色沉淀与气体的物质常见的有 CaC2、Mg3N2、Al2S3,这些考生均易考虑到,但今年命题时却说成为化合物与水反应生成白色固体与气体,这显然说法不常规、不科学,物质在水中一般说是沉淀、浑浊或是溶液;2、该试题中所涉及到的CaC2与O2反应在中学化学中未出现,在《无机化学反应方程式手册》也没出现,这是命题者闭门造车的反应,因为此反应是一个脱离现实的反应(用较大代价获的物质,一般来说是不会去烧掉的。
),再燃烧的产物X一定是CO2?
不能是CO?
如果是CO2,它能与CaO反应吗?
,这让考生如何能够顺利向下思考呢?
3、关于CaC2电子式的考查也有点偏僻、怪异,因为CaC2电子式的书写在中学化学教材中不作要求。
28:
(13分) 取化学式为MZ的黄色粉末状化合物进行如下实验。
将MZ和足量的碳粉充分混合物,平铺在反应管a中,在b瓶中盛足量澄清石灰水。
按图连接仪器。
实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成,同时,b瓶的溶液出现白色浑浊。
待反应完全后,停止加热,仍继续通氮气,直至反应管冷却,此时,管中的熔融物凝固城银白色金属。
根据以上叙述回答:
(1)元素Z是;
(2)停止加热前是否需要先断开a和b的连接处?
为什么?
;
(3)反应管a中发生的所有反应的化学方程式是
;
(4)本实验的尾气是否需处理?
如需处理,请回答如何处理;如不需处理,请说明理由。
。
解析:
本题重点考查考生的化学实验基本操作能力及判断、推理等思维能力。
(1):
反应管a中放有黄色粉末状化合物MZ和足量的碳粉,反应生成的气体能使澄清石灰水变浑浊,说明该气体中含有二氧化碳,逆向推理可得MZ中Z元素应该是氧。
(2):
停止加热若不通入氮气,则反应管a因温度降低,反应管内气压必减小,这从而引起液体倒吸现象,所以一般的实验操作是将导气管从液体中取出,而该试题走出常规,反应完全后虽停止加热但仍继续通氮气,管内压强不会减少从而产生倒吸现象。
(3):
该问题是众多考生感到困惑的知识点,因为确定不了MZ是什么物质,由题已知MZ为黄色化合物,而中学化学中遇到的黄色化合物不是很多,常见的有过氧化钠、溴化银、二硫化亚铁等(PbO、HgO等不常见,大纲也是没有要求的,学生难以想到),它们在化学课本中均未出现相关反应,所以许多考生思维受到障碍,无从下手。
其实,确定不了MZ是什么物质,我们若能走出思维定势,同样也不会影响解答该题,可直接用M代替元素符号书写反应方程式,可能的反应有:
(4):
尾气中可能含有有毒的CO气体,必需进行尾气处理,处理CO可利用化学课本所学知识将其在导管口点燃,或者用气球收集,或接一个加热的装有CuO的玻璃管等。
答案:
(1)氧
(2)不需要,因为一直通入氮气,b中溶液不会倒吸到a管中。
(3)
(4)需处理,因为一氧化碳有毒,应该进行尾气处理,处理的方法可以将其在导管口点燃,或者用气球收集,或接一个加热的装有CuO的玻璃管。
点评:
该试题是今年最让考生困惑、迷茫的试题,也是让中学一线教师感到失望、遗憾的试题,过去遇到类似的高考试题,均是先推断出具体的物质,然后以此为依据,顺藤摸瓜,寻求答案,而该题首先困惑考生的是黄色粉末状化合物MZ是何物质?
从中学化学中常见的物质中去寻找,难以得出黄色粉末状化合物MZ的答案,得不出黄色粉末状化合物MZ的答案,如何能完成MN与C反应的化学方程式?
!
此题是一道不负责任的试题,所设陷阱使考生误入歧途,使教师对以后的复习课,无依所从(脱离考试大纲)。
29.(16分)A、B、C、D、E、F和G都是有机化合物,它们的关系如下图所示:
(1)化合物C的分子式是C7H8O,C遇到FeCl3溶液显示紫色,C与溴水反应生成的一溴代物只有两种,则C的结构简式为;
(2)D为一直链化合物,其相对分子质量比化合物C的小20,它能跟NaHCO3反应放出CO2,则D分子式为,D具有的官能团是;
(3)反应①的化学方程式是;
(4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成E和F,F可能的结构简式是;
(5)E可能的结构简式是。
解析:
本题借助有机框图重点考查有机推断及有机化学中的酯化反应和酯的水解等重要的反应和同分异构体等知识点。
(1)由可C遇FeCl3溶液显紫色可知C分子中含有酚羟基,又由C的分子式C7H8O及C与溴水反应生成的一溴代物只有两种,可以判断出C是对甲基苯酚(
)。
(2)因为C的相对分子质量是108,所以D的相对分子质量为108-20=88,从框图转化关系知,A水解所得D中含有一个羧基,其式量是45,剩余部分的式量是43,应该是一个丙基,则D的分子式是C4H8O2,是正丁酸。
具有的官能团为羧基。
(3)由C、D的结构可逆向推理得化合物A是丁酸对甲基苯酚酯(
),故A在酸性条件下水解的化学方程式为:
(4)根据G的分子式,借助D采用逆向推理知F的分子式是C3H8O,其结构有两种,分别是丙醇(CH3CH2CH2OH)和异丙醇(CH3CHOHCH3)。
(5)B与A互为同分异构体,B水解所得E由框图可得是芳香酸,其分子式是C8H8O2.符合题意的结构有四种,分别是苯乙酸、邻甲基苯甲酸、间甲基苯甲酸、对甲基苯甲酸。
答案:
见解析部分,此处略。
点评:
该试题立意较好,但试题表述欠科学、欠规范。
化合物C的分子式是C7H8O,且C遇到FeCl3溶液显示紫色,显然该物质是甲基苯酚,到底是对甲基苯酚还是邻甲基苯酚呢?
众所周知,因酚羟基的影响,C与溴水反应时溴主要取代邻、对位,间位常被忽略,大学化学教材也是如此描述,这样以来,当C与溴水反应生成的一溴代物只有两种,则C的结构简式应该为邻甲基苯酚更符合题意!
若要考虑间位的存在,命题者应该指明C苯环上的H被溴取代只有两种!
!
如不指明,这会让众多考生无所适从。
总之,高考是一项严肃的工作,它不仅关系到千家万户,而且有着教学指挥棒的功能.但今年的高考题出现这样多的问题,想赞美你,我真难以出口。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 08 年高 考试题 分析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《Java程序设计》考试大纲及样题试行.docx
《Java程序设计》考试大纲及样题试行.docx
