 全国大联考河北新课标Ⅰ河北省石家庄市届高三下学期一模考试理综化学试题解析版.docx
全国大联考河北新课标Ⅰ河北省石家庄市届高三下学期一模考试理综化学试题解析版.docx
- 文档编号:10535102
- 上传时间:2023-02-21
- 格式:DOCX
- 页数:21
- 大小:1.06MB
全国大联考河北新课标Ⅰ河北省石家庄市届高三下学期一模考试理综化学试题解析版.docx
《全国大联考河北新课标Ⅰ河北省石家庄市届高三下学期一模考试理综化学试题解析版.docx》由会员分享,可在线阅读,更多相关《全国大联考河北新课标Ⅰ河北省石家庄市届高三下学期一模考试理综化学试题解析版.docx(21页珍藏版)》请在冰豆网上搜索。
全国大联考河北新课标Ⅰ河北省石家庄市届高三下学期一模考试理综化学试题解析版
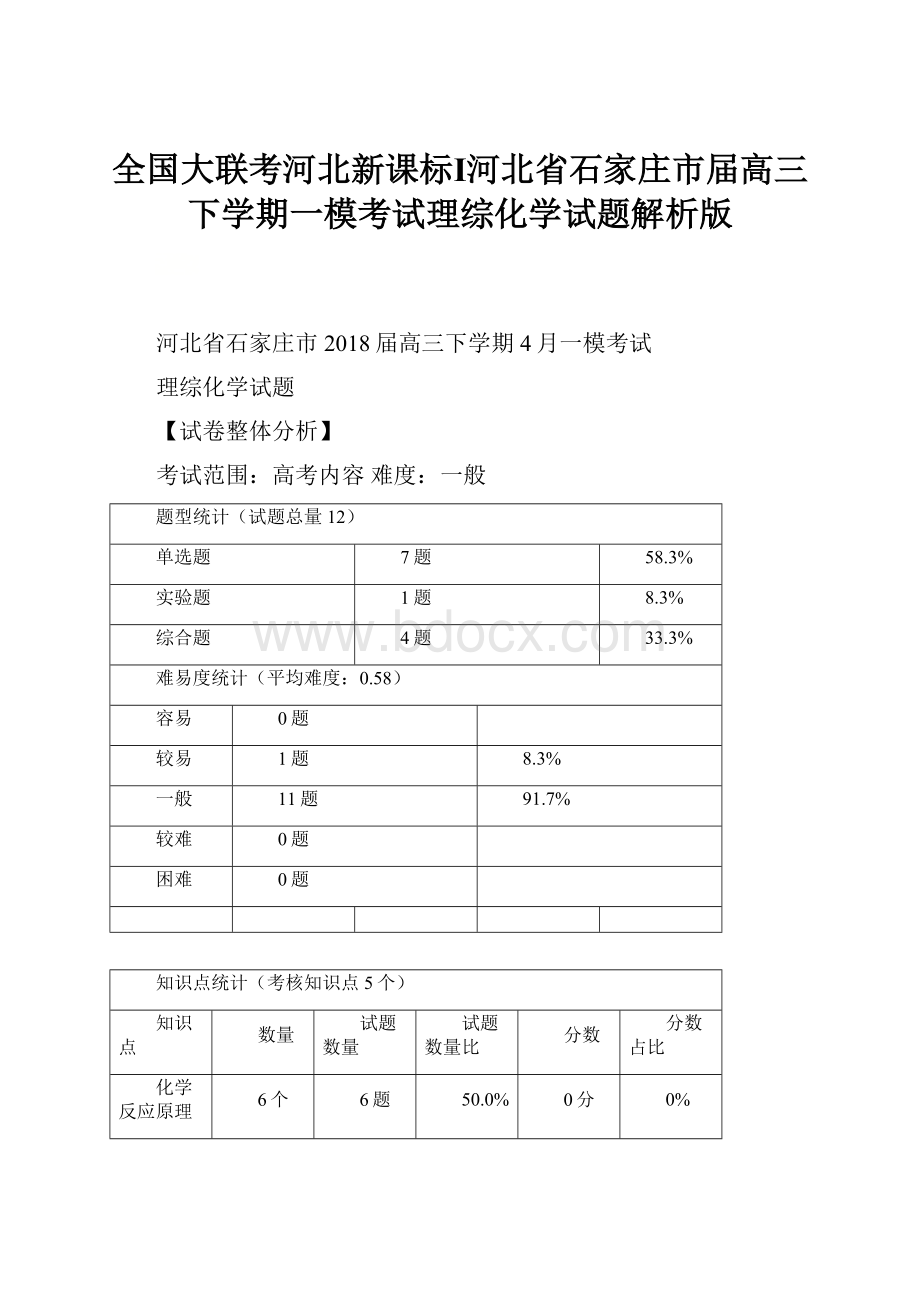
河北省石家庄市2018届高三下学期4月一模考试
理综化学试题
【试卷整体分析】
考试范围:
高考内容难度:
一般
题型统计(试题总量12)
单选题
7题
58.3%
实验题
1题
8.3%
综合题
4题
33.3%
难易度统计(平均难度:
0.58)
容易
0题
较易
1题
8.3%
一般
11题
91.7%
较难
0题
困难
0题
知识点统计(考核知识点5个)
知识点
数量
试题数量
试题数量比
分数
分数占比
化学反应原理
6个
6题
50.0%
0分
0%
有机化学基础
2个
2题
16.7%
0分
0%
化学实验基础
2个
2题
16.7%
0分
0%
认识化学科学
1个
1题
8.3%
0分
0%
物质结构与性质
1个
1题
8.3%
0分
0%
【题型考点分析】
题号
题型
知识点
1
综合题
氧化还原反应方程式的配平
2
综合题
盖斯定律的应用
3
单选题
有机化合物中碳的成键特征
4
综合题
物质结构与性质综合考查
5
综合题
有机合成综合考查
6
单选题
物质性质的探究
7
单选题
电解原理
8
单选题
盐类水解的原理
9
单选题
焓变产生原因及表示
10
单选题
盐类水解在生活、生产中的应用
11
实验题
物质性质的探究
12
单选题
电离平衡常数及影响因素
河北省石家庄市2018届高三下学期4月一模考试
理综化学试题
第I卷(选择题)
1.下列各项中,对所描述内容的相关分析不正确的是
选项
描述
分析
A
“青蒿一握,以水二升渍,绞取计”
其中涉及到了萃取过程
B
炼丹家制硫酸时用“炼石胆(胆矾)取其精华”
其中利用了分解反应
C
古代染坊常用某种碱剂来精炼丝绸
碱剂不可能为烧碱
D
“古剑‘沈卢’,以剂钢为刃”
剂钢的成分为纯铁
【答案】D
【解析】A、以水二升渍,绞取计,此过程为萃取过程,故A说法正确;B、胆矾为CuSO4·5H2O,炼胆矾涉及胆矾的分解,故B说法正确;C、碱剂为K2CO3,故C说法正确;D、济钢为合金,故D说法错误。
2.2SO2(g)十O2(g)=2SO3(g)△H=-198kJ·mol-1,在V2O3存在时,该反应机理为:
V2O3+SO2-→+2VO3+SO3(快)4VO2+O2→2V2O3(慢)。
下列说法正确的是
A.反应速率主要取决于V2O3的质量B.VO2是该反应的催化剂
C.该反应逆反应的活化能大于198kJ/molD.升高温度,该反应的△H增大
【答案】C
【解析】A、V2O5是固体,因此该反应取决于第二步反应,故A错误;B、两式相加,V2O3为催化剂,故B错误;C、活化能与反应热之间的关系,如图
,E1为正反应的活化能,E2为逆反应活化能,SO2与O2反应是放热反应,因此该反应的活化能大于198kJ·mol-1,故C正确;D、△H只与始态和终态有关,因此升高温度,△H不变,故D错误。
x@k#w
3.UrolithinA是一种含氧杂环化合物,在合成有机材料和药品中有重要应用、其结构如图所示。
下列关于该有机物的说法正确的是
A.分子式为C13H6O4
B.所有原子一定处于同一平面上
C.苯环上的一氯代物有3种
D.1mol该有机物与H2反应时,最多消耗6molH2
【答案】D
4.短周期主族元素W、X、Y、Z的原子序数依次增大,W与X形成的某种化合物可用作水果的催熟剂,Y的氧化物为碱性氧化物,X、Y、Z三种元素的最外层电子数之和为11。
下列说法正确的是
A.原子半径:
W
B.简单氢化物的稳定性:
X
C.W、X形成的某种化合物常用作萃取剂
D.Y和Z形成的含氧酸盐均可使酚酞溶液变红
【答案】C
【解析】W与X形成某种化合物可用作水果的催熟剂,即此化合物为C2H4,因为原子序数依次增大,因此W为H,X为C,Y的氧化物为碱性氧化物,则Y可能为Na或Mg,三种元素的最外层电子数之和为11,如果Y为Na,则Z为S,如果Y为Mg,则Z为P,A、电子层数越多,半径越大,同周期从左向右半径减小,因此原子半径大小顺序是Y>Z>X>W,故A错误;B、如果Z为S,C的非金属性小于S,因此H2S的稳定性比CH4稳定性强,如果Z为P,C的非金属性强于P,即CH4的稳定性强于PH3,故B说法错误;C、C和H形成的化合物为C6H6,即为苯,苯常用作萃取剂,故C正确;D、如果形成的含氧酸盐为Na2SO4,溶液显中性,不能使酚酞变红,故D错误。
5.已知:
2FeSO4·7H2O
Fe2O3+SO2↑+SO3↑+14H2O↑,用下图所示装置检验FeSO4·7H2O的所有分解产物,下列说法不正确的是
A.乙、丙、丁中可依次盛装无水CuSO4、Ba(NO3)2溶液、品红溶液
B.实验时应先打开K,缓缓通入N2,再点燃酒精喷灯
C.甲中残留固体加稀硫酸溶解,再滴加KSCN,溶液变红
D.还应在丁装置后面连接盛有NaOH溶液的洗气瓶
【答案】A
【解析】A、丙装置验证的是SO3,因为NO3-在酸性条件下具有强氧化性,能把SO2氧化成SO42-,对SO3的检验产生干扰,丙装置应换成BaCl2溶液,故A说法错误;B、先通N2,排除装置中空气,防止Fe2+被氧化,故B说法正确;C、残留固体加稀硫酸溶解,再滴加KSCN溶液,溶液变红说明溶液中含有Fe3+,反之不含有,故C说法正确;D、SO2有毒,为防止污染空气,因此在丁装置后面再加一尾气处理装置,即添加盛有NaOH溶液的洗气瓶,故D说法正确。
6.工业上通过电化学原理在铝表面形成氧化膜来提高其抗腐蚀能力,工作原理如图所示。
下列说法不正确的是
A.碳棒可用铜棒代替,其作用是传递电流
B.通电一段时间后,溶液的pH减小
C.通电后电子被强制从碳棒流向铝片使铝表面形成氧化膜
D.可通过调节滑动变阻器来控制氧化膜的形成速度
【答案】C
【解析】A、根据电解原理,碳棒为阴极,铜棒能够代替碳棒,作用是传递电流,故A说法正确;B、阳极反应式为2Al-6e-+3H2O=Al2O3+6H+,阴极反应式为2H++2e-=H2↑,总电解反应式为2Al+3H2O
Al2O3+3H2↑,硫酸浓度增大,c(H+)增大,即pH减小,故B说法正确;C、电子移动方向是从电源的负极→碳棒,铝片→电源的正极,电解质溶液中没有电子通过,故C说法错误;D、滑动变阻器调节电路中电流的强度,即可以控制氧化膜的形成速度,故D说法正确。
7.常温下。
向20.00mL0.1mol/LHA溶液中滴入0.1mol/LNaOH溶液,溶液中由水电离出的氢离子浓度的负对数[-lgc水(H+)]与所加NaOH溶液体积的关系如图所示,下列说法不正确的是
A.常温下,Ka(HA)约为10-5
B.M、P两点溶液对应的pH=7
C.b=20.00
D.M点后溶液中均存在c(Na+)>c(A-)
【答案】B
【解析】A、-lgc水(H+)=11,推出c水(H+)=c水(OH-)=10-11mol·L-1,根据水的离子积求出溶液中c(H+)=Kw/c(OH-)=10-3mol·L-1,HA
H++A-,c(H+)=c(A-)=10-3mol·L-1,Ka=
=10-5,故A说法正确;B、N点水电离出H+最大,说明HA与NaOH恰好完全反应生成NaA,P点溶质为NaOH和NaA,溶液显碱性,即P点pH不等于7,故B说法错误;C、0-b点水的电离程度增大,当达到b点时水的电离程度达到最大,即溶质为NaA,说明HA和NaOH恰好完全反应,b=20.00mL,故C说法正确;D、M点pH=7,根据溶液电中性,存在c(Na+)=c(A-),M点后,c(Na+)>c(A-),故D说法正确。
第II卷(非选择题)
8.AgNO3是中学化学常用试剂,某兴趣小组设计如下实验探究其性质。
I.AgNO3的热稳定性
AgNO3受热易分解,用下图装置加热AgNO3固体,试管内有红棕色气体生成,一段时间后,在末端导管口可收集到无色气体a。
(1)实验室检验气体a的方法为_______________________________________。
(2)已知B中只生成一一种盐,据此判断AgNO3受热分解的化学方程式为______________。
(3)从安全角度考虑,上述实验装置存在一处明显缺陷,改进措施为______________________。
II.AgNO3与盐溶液的反应
(4)甲同学认为试管②中产生银镜是Fe2+所致,其离子方程式为_____________________;
乙同学认为要判断该观点正确,需增加如下实验,取2 mL0.5mol/LAgNO3溶液于试营中,向其中满加几滴____________,若只产生白色远淀,证明甲同学观点正确。
(5)已知:
AgSCN为白色沉淀。
试管③中红色褪去的原因为__________________________(请从平衡移动的角度解释)。
(6)设计实验证明Ksp(AgI) 限选试剂: 0.1 mol/LAgNO3溶液、0.1mol/LKI溶液、0.1mol/LKSCN 溶液___________________________________________________________。 【答案】将带火星的木条放至导管口,木条复燃2AgNO3 2Ag+2NO2↑+O2↑A、B装置之间连接一个防倒吸的安全瓶Ag++Fe2+=Ag+Fe3+0.5mol/L(NH4)2SO4溶液溶液中发生Fe3++3SCN- Fe(SCN)3使局部变红;振荡试管时,过量的Ag+与SCN-反应生成AgSCN沉淀,降低了c(SCN-),平衡逆向移动,溶液褪色方案一: 向盛有0.1mol/LAgNO3溶液的试管中滴加0.1mol/LKSCN溶液至不再有白色沉淀生成,向其中滴加0.1mol/LKI溶液,白色沉淀转化为黄色沉淀,则证明Ksp(AgI)﹤Ksp(AgSCN)。 方案二: 将等体积的0.1mol/LKSCN溶液和0.1mol/LKI溶液混合,向混合液中滴加0.1mol/LAgNO3溶液,若生成黄色沉淀,则证明Ksp(AgI)﹤Ksp(AgSCN)。 【解析】考查实验方案设计与评价,I. (1)根据实验,加热硝酸银,有红棕色气体产生,说明产生NO2,通过装置B后,在末端导管口可收集到无色气体,无色气体可能为氧气,检验氧气的方法是将带火星的木条放至导管口,木条复燃; (2)NO2与NaOH反应: 2NO2+2NaOH=NaNO2+NaNO3+H2O,氧气能把NaNO2氧化成NaNO3,根据信息,B中只生成一种盐,说明氧气过量,根据得失电子数目守恒,Ag的化合价降低,推断出硝酸银受热分解的方程式为: 2AgNO3 2Ag+2NO2↑+O2↑;(3)NO2能与NaOH发生反应,容易造成导管内的气体压强减小,容易引起倒吸,因此A、B装置之间连接一个防倒吸的安全瓶;(4)Ag+的氧化性比Fe3+强,因此发生Ag++Fe2+=Fe3++Ag;根据②的实验现象以及若只产生白色沉淀,证明甲同学观点正确,推出所加溶液为0.5mol·L-1(NH4)2SO4;(5)溶液中发生Fe3++3SCN- Fe(SCN)3使局部变红;振荡试管时,过量的Ag+与SCN-反应生成AgSCN沉淀,降低了c(SCN-),平衡逆向移动,溶液褪色;(6)方案一: 向盛有0.1mol·L-1AgNO3溶液的试管中滴加0.1mol·L-1KSCN溶液至不再有白色沉淀生成,向其中滴加0.1mol·L-1KI溶液,白色沉淀转化为黄色沉淀,则证明Ksp(AgI)﹤Ksp(AgSCN)。 方案二: 将等体积的0.1mol·L-1KSCN溶液和0.1mol·L-1KI溶液混合,向混合液中滴加0.1mol·L-1AgNO3溶液,若生成黄色沉淀,则证明Ksp(AgI)﹤Ksp(AgSCN)。 9.铋(Bi)与氮同族,氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色、生产金属铋等。 一种用火法炼铜过程产生的铜转炉烟尘(除含铋的化合物之外,还有CuSO4、ZnSO4、CuS、Fe2O3、PbSO4及As2O3)制备高纯氯氧化铋的工艺流程如下: 请回答: (1)Bi位于第六周期,其原子结构示意图为__________________________________。 (2)向“酸浸”所得浸液中加入Zn粉,充分反应后过滤,从溶液中获得ZnSO4·7H2O的操作为__________、过滤、洗涤、干燥。 (3)“浸铜”时,有单质硫生成,其离子方程式为____________________________。 (4)“浸铋”时,温度升高,铋的浸出率降低,其原因为____________________________。 (5)“除铅、砷”时,可以采用以下两种方法。 ①加入改性HAP。 浸液1与HAP的液固比(L/S)与铅、砷去除率以及后续沉铋量的关系如下表: L/S 125: 1 50: 1 25: 1 15: 1 Pb2+去除率/% 84.86 94.15 95.40 96.83 As3+去除率/% 98.79 98.92 98.34 99.05 m(沉铋)/g 2.34 2.33 2.05 1.98 实验中应采用的L/S=_________________________。 ②铁盐氧化法,向浸液1中加入Fe2(SO4)3,并调节pH,生成FeAsO4沉淀。 欲使溶液中c(AsO42-)<10-9mol/L且不产生Fe(OH)3沉淀,应控制pH的范围为__________。 已知: 1g2=0.3: ;FeAsO4、Fe(OH)3的Ksp分别为5×10-23、4×10-38。 (6)“沉铋“时需控制溶液的pH=3.0,此时BiCl3发生反应的化学方程式为___________________。 【答案】 蒸发浓缩、冷却结晶CuS+MnO2+4H+=Cu2++Mn2++S+2H2O温度升高,盐酸挥发,反应物浓度降低50︰1pH<5.3BiCl3+Na2CO3=BiOCl↓+2NaCl+CO2↑ 不大,因此为了节省能源以及原料,L/S控制在50: 1;②c(AsO43-)=10-9mol·L-1,此时c(Fe3+)=Ksp(FeAsO4)/c(AsO43-)=5×10-21/10-9mol·L-1=5×10-12mol·L-1,此时c(OH-)= =2×10-9mol·L-1,此时的pH=5.3,即pH<5.3;(6)沉铋时,加入的物质是Na2CO3,生成的BiOCl,因此有BCl3+Na2CO3→BiOCl,根据反应特点,产物还有NaCl和CO2,化学方程式为BiCl3+Na2CO3=BiOCl↓+2NaCl+CO2↑。 点睛: 本题难点是(6),根据流程图,加入物质是BCl3和Na2CO3,生成物质为BOCl,可以理解为Na2CO3中一个氧原子,替代BCl3中两个Cl原子,替代下Cl原子与Na结合生成NaCl,CO32-去掉一个氧原子后,转化成CO2,因此方程式为BiCl3+Na2CO3=BiOCl↓+2NaCl+CO2↑。 10.氨气在工农业生产和国防科技中有着重要应用,科研工作者对其进行着广泛研究。 请回答: (1)某课题组实现了在常温常压下,以氮气和液态水为原料制备氨气,同时有氧气生成。 已知,在一定温度和压强下,由最稳定的单质生成1mol纯物质的热效应,称为该物质的生成热(△H)。 常温常压下、相关物质的生成热如下表所示: 物质 NH3(g) H2O(l) △H/kJ·mol-1 -46 -242 上述合成氨反应的热化学方程式为______________________________________。 (2)利用生物电池,以H2、N2为原料合成氨的装置如下图所示。 Q、R均为能化剂,据图示判断,负极反应的催化剂为______(填“Q”或“R”);正极的电极反应式为_________________________________________。 (3)氨气是工业制硝酸的主要原料之一,催化氧化步骤中发生的主要反应如下: I.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H=-906kJ/mol II.4NH3(g)+3O2(g) 2N2(g)+6H2O(g)△H=-1266kJ/mol 将固定比例NH3和O2 的混合气体以一定流速通过填充有催化剂的反应器,反应产率与温度的关系如图1所示。 ①催化氧化步骤中,最适宜的温度为_________________(填“T1”或“T2”)。 ②低于T1℃时,NO的产率较低的原因为_____________________________________。 ③高于T2℃时,NO的产率降低的可能原因为______________(填选项字母) A.催化剂活性降低B.平衡常数减小 C.反应活化能增大D.氨气溶于水 ④T2℃(T1>T2)时,向20L恒容密闭容器中充人2molNH3和2.75molO2,发生反应 I.反应过程中各物质的物质的量的随时间(t)变化关系如图2所示。 T2℃时,该反应的平衡常数K=________________;5min时,改变了某一外界条件,所改变的条件可能为_________________________________________。 【答案】2N2(g)+6H2O(l) 3O2(g)+4NH3(g)ΔH=+1268kJ·mol-1QN2+6H++6e-=2NH3T2温度较低时,反应速率慢,同时部分反应物生成N2AB0.075升高温度或缩小容器容积 【解析】 (1)考查热化学反应方程式的书写,N2与H2O之间的反应是2N2+6H2O=3O2=4NH3,N2(g)+3H2(g)=2NH3(g),此时热效应是(-46×2)kJ·mol-1,2H2(g)+O2(g)=2H2O(l),此时的热效应是(-242×6)kJ·mol-1,两式变形得到此方法合成氨的热化学反应方程式为2N2(g)+6H2O(l) 3O2(g)+4NH3(g)△H=[-46×4-(-242×6)]kJ·mol-1=+1268kJ·mol-1,即为2N2(g)+6H2O(l) 3O2(g)+4NH3(g)ΔH=+1268kJ·mol-1; (2)考查原电池工作原理和电极反应式的书写,根据原电池工作原理,负极上失去电子,化合价升高,因此通氢气一极为负极,根据装置图,Q为催化剂;通氮气一极为正极,根据工作原理,正极反应式为N2+6H++6e-=2NH3;(3)考查化学反应条件的控制、化学平衡常数的计算、勒夏特列原理,①制取硝酸,NH3与氧气反应生成NO,NO与O2反应生成NO2,NO2与水反应生成HNO3,T2时NO的产率最高,因此最适宜的温度是T2;②低于T1℃时,反应速率慢,同时部分反应物转化成N2,造成NO的产率降低;③A、催化剂活性受温度影响,在一定温度时,催化剂催化效率最高,超过此温度,降低催化剂的催化效率,故A正确;B、根据反应方程式,生成NO的反应是放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,故B正确;C、活化能的大小不影响平衡的移动,故C错误;D、这里的水为气态水,故D错误;④根据图2,4min时达到平衡,c(NH3)=c(NO)=1/20mol·L-1,c(O2)=c(H2O)=1.5/20mol·L-1,根据化学平衡常数的表达式,K= =0.075;根据NH3和O2的物质的量减小,NO和H2O的物质的量增大,说明改变的这一因素,平衡向逆反应方向移动,即升高温度或缩小容器的容积。 点睛: 本题的难点是热化学反应方程式的书写,学生不清楚生成热的定义,应根据生成热的定义,书写出1/2N2(g)+3/2H2(g)=NH3(g)△H=-46kJ·mol-1,然后写出生成H2O的生成热: H2(g)+1/2O2(g)=H2O(l)△H=-242kJ·mol-1,然后根据目标方程式以及盖斯定律,写出2N2(g)+6H2O(l) 3O2(g)+4NH3(g)ΔH=+1268kJ·mol-1;或者根据单质的生成热为0,以及反应热等于反应物生成热总和-生成物生成热总和,写出问题即可。 11.【化学一选修3: 物质结构与性质】铜及其化合物在化工生产中有着广泛的应用。 回答下列问题: (1)铜元素在元素周期表中的位置为_________________,基态Cu原子核外电子占据的原子轨道数为____________________。 (2)向硫酸铜溶液中加入乙二胺(H2N-CH2-CH2-NH3)溶液后,每个Cu2+可与两个乙二胺分子形成四配位离子,导致溶液由蓝色变为紫色。 ①乙二胺分子中C、N原子的杂化轨道类型分别为_______________、_________________。 ②与硫酸根离子互为等电子体的分子为___________(任写一种)。 ③四配位离子的结构式为_____________________,该离子中所有元素的电负性由大到小的顺序为____________________________。 (3)硫化亚铜和氧化亚铜均为离子晶体,其中熔点较高的为___________(填化学式),原因为________________________________________________。 (4)下图为铜与氧(O)、钇(Y)、钡(Ba)形成的一种超导体材料的长方体晶胞结构,其晶胞参数如图(i)所示,该结构中有平面正方形(CuO4)和四方锥(CuO6)结构单元如图(ii)所示。 x/k**w ①该超导体材料的化学式为____________________________。 ②已知该化合物的摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,其密度为____g·cm-3(列出表达式即可)。 【答案】第四周期第ⅠB族15sp3sp3CCl4CBr4SiCl4SiF4Cl2O3(答案合理即可) N>C>H>CuCu2O因为氧离子半径小于硫离子半径,所以氧化亚铜的晶格能大于硫化亚铜的晶格能,熔点也高于硫化亚铜YBa2Cu3O7 结构式为 ;(3)考查晶体熔沸点高低的判断,两者属于离子晶体,判断熔沸点高低需要从晶格能的角度思考,因此有因为氧离子半径小于硫离子半径,所以氧化亚铜的晶格能大于硫化亚铜的晶格能,熔点也高于硫化亚铜;(4)考查晶胞的计算,①根据图i,Cu位于顶点和棱上,Ba、Y位于内部,根据图ii,O位于棱上,共有14个,根据均摊法,求出化学式为YBa2Cu3O7;晶胞的质量为 ,晶胞的体积为(a×10-10×a×10-10×b×10-10)cm3,根据密度的定义,晶胞的密度为 g/cm3。 点睛: 本题难度是(4),关键是O原子位置的确定,观看图ii,会发现氧原子位于棱上,共有28个氧原子,然后用均摊法,求出化学式,晶胞密度的计算中晶胞质量的计算是难点,可以认为此晶胞中有1个YBa2Cu3O7,则晶胞质量为 ,最后根据密度的定义求出密度。 12.[化学-选修5: 有机化学基础]2017年治疗膀胱癌的有机小分子药物Aminolevulinic
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 全国 联考 河北 新课 河北省 石家庄市 届高三 下学 期一模 考试 化学试题 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《城市规划基本知识》深刻复习要点.docx
《城市规划基本知识》深刻复习要点.docx
