 防腐蚀讲义f第四章金属在自然环境中的腐蚀与防护Word文档格式.docx
防腐蚀讲义f第四章金属在自然环境中的腐蚀与防护Word文档格式.docx
- 文档编号:15212487
- 上传时间:2022-10-28
- 格式:DOCX
- 页数:13
- 大小:50.18KB
防腐蚀讲义f第四章金属在自然环境中的腐蚀与防护Word文档格式.docx
《防腐蚀讲义f第四章金属在自然环境中的腐蚀与防护Word文档格式.docx》由会员分享,可在线阅读,更多相关《防腐蚀讲义f第四章金属在自然环境中的腐蚀与防护Word文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
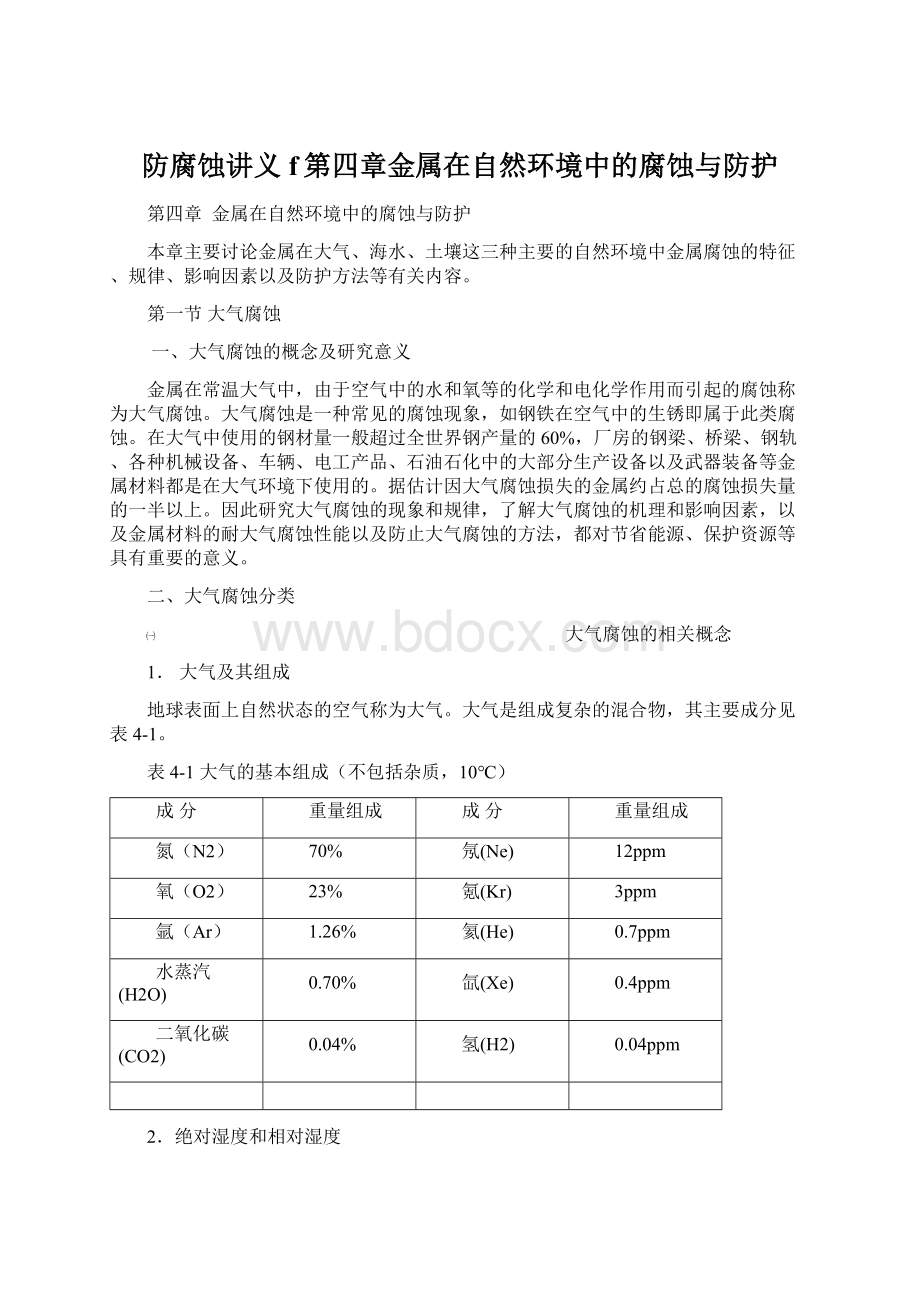
氮(N2)
70%
氖(Ne)
12ppm
氧(O2)
23%
氪(Kr)
3ppm
氩(Ar)
1.26%
氦(He)
0.7ppm
水蒸汽(H2O)
0.70%
氙(Xe)
0.4ppm
二氧化碳(CO2)
0.04%
氢(H2)
0.04ppm
2.绝对湿度和相对湿度
参与金属大气腐蚀过程的主要组成是氧和水蒸汽。
二氧化碳虽参与锌和铁等某些金属的腐蚀过程,形成腐蚀产物的碳酸盐,但它的作用是次要的。
氧在大气腐蚀中主要是参与电化学腐蚀过程。
空气中的氧溶于金属表面存在的电解液薄层中作为阴极去极化剂,而金属表面的电解液层由大气中的水蒸汽所形成。
大气中的水分常用湿度来表示:
绝对湿度:
一立方米大气中的水汽含量(g/m3);
一定温度下大气的最高绝对湿度叫做大气的饱和水蒸汽量。
相对湿度(RH):
大气中的绝对湿度与同温度下的饱和水蒸汽量之比。
大气腐蚀的分类
按照金属表面的潮湿度不同,也就是按照电解液膜层的存在和状态不同,可把大气腐蚀分为三类:
1.干大气腐蚀
在干燥大气中(通常RH<
60%--80%)金属表面不存在液膜时的腐蚀,这种腐蚀属于化学腐蚀中的常温氧化。
其特点是金属表面形成不可见的保护膜。
某些金属,如铜、银等非铁金属,在被硫化物所污染了的空气中产生的失泽作用就是一个例子。
2.潮大气腐蚀
在相对湿度足够高,60%—80%<
RH<
100%,金属表面存在肉眼看不见的极薄水膜时发生的大气腐蚀。
例如铁在没有雨雪淋到时的生锈即属于此。
3.湿大气腐蚀
当金属表面存在肉眼可见的凝结水膜时发生的大气腐蚀。
也就是说,当空气湿度接近100%,以及当水分以雨、雪、水沫等形式直接落在金属表面上时所发生的腐蚀。
大气腐蚀速度与液膜厚度的关系
可以定性地用图4-1来表示大气腐蚀速度与金属表面上膜层厚度之间的关系。
图4-1大气腐蚀速度与金属表面上膜层厚度之间的关系
区域:
在大气湿度特别低的情况下,金属表面只有薄薄的吸水薄膜,最多只有几个水分子厚度(10~100),还不能认为是连续的电解液。
此区相当于干大气腐蚀,腐蚀速度很低。
随大气湿度增加,金属表面液膜层厚度也逐渐增加,水膜厚度可达几十或几百个水分子层厚,形成连续的电解液薄层,开始了电化学腐蚀过程。
此区域腐蚀速度急剧增加,相当于潮大气腐蚀。
当金属表面水膜层厚继续增加到几十微米厚时,进入到湿大气腐蚀区。
由于氧通过液膜扩散到金属表面困难了,所以此区腐蚀速度有所下降。
当金属水膜层变得更厚,如大于1mm时已相当于全浸在电解液中的腐蚀情况,腐蚀速度已基本不变。
应当指出,在实际大气腐蚀情况下,由于环境条件变化,各种腐蚀形式可以相互转换。
而通常所说的大气腐蚀,是指在常温下潮湿空气中的腐蚀,也就是只考虑潮和湿大气腐蚀这两种主要腐蚀形式。
三、大气腐蚀机理
讨论大气腐蚀的机理时,首先应认识到大气腐蚀是金属处于表面薄层电解液下的腐蚀过程,因此既可以应用电化学腐蚀的一般规律,又要注意到大气腐蚀电极过程的特点。
金属表面上水膜的形成
大气腐蚀之所以发生,首先由于金属表面上有水膜形成。
湿大气腐蚀是水膜的形成比较容易理解,而在潮大气腐蚀时金属表面水膜的形成一般有以下几种情况:
1.毛细凝聚
研究表明:
液面的曲率半径越小,饱和蒸汽压的值越小,水蒸汽就越易凝聚。
因此在金属表面上的微细裂纹、结构间隙、氧化膜或涂镀层的孔隙及表面尘埃微粒等处,会形成许多曲率半径很小的毛细管凹面,水蒸汽就会在这些部位优先凝聚,此即为毛细凝聚。
2.吸附凝聚
在RH<
100%,未发生纯粹的物理凝聚之前,由于金属表面的不饱和键力对水分子的吸附作用,也能形成很薄的水分子层。
表面越粗糙,相对湿度越高,吸附效应越强。
3.化学凝聚
金属表面落上或生成吸水性化合物,如NaCl、NH4NO3、手汗等,这些物质会吸收水分并与水发生化学反应,促进水蒸汽在金属表面上优先凝聚。
上述三种优先凝聚作用使得金属表面在相对湿度未达100%,大气中水汽含量并未达到饱和蒸汽压时就会形成水膜,水膜的形成便为金属发生电化学腐蚀创造了条件,因此在大气条件下金属所发生腐蚀的机理主要是电化学腐蚀。
大气腐蚀初期的腐蚀机理
当金属表面一旦形成连续的水膜,就会溶解一定数量的CO2、SO2等而形成电解质溶液,并且溶入大气中的氧。
由于金属表面的电化学不均匀性,就会构成各种腐蚀电池,开始电化学腐蚀过程。
1.阴极过程
金属表面主要是依靠氧的去极化作用,通常的反应为:
即使是电位极负的金属,如镁及其合金,当它从全浸于电解液的腐蚀转变为大气腐蚀时,阴极过程由氢去极化为主转变到氧去极化为主。
在强酸性的溶液中,象铁、锌、铝这些金属在全浸时主要依靠氢去极化进行腐蚀;
但是在城市污染大气所形成的酸性水膜下,这些金属的腐蚀主要依靠氧的去极化作用。
这是因为在液膜较薄的情况下,氧的扩散比全浸状态更为容易。
2.阳极过程
腐蚀的阳极过程是金属失去电子的氧化溶解反应:
在薄的液膜条件下,大气腐蚀阳极过程会受到较大的阻碍。
一是容易生成氧化膜或氧的吸附膜,使阳极钝化;
二是阳极反应使液膜中的金属离子浓度增大,导致阳极极化。
同时腐蚀生成的金属离子水化困难,易于形成固态腐蚀产物。
所有这些都阻碍阳极反应的顺利进行,使得整个过程为阳极过程所控制。
湿的大气腐蚀,腐蚀过程主要受阴极控制,但其阴极控制的程度和全部浸没于电解质溶液中的腐蚀情况相比,已经大为减弱。
对潮大气腐蚀,腐蚀过程主要是阳极过程控制。
可见随着水膜层厚度变化,不仅表面潮湿程度不同,而且彼此的电极过程控制特征也不同。
大气腐蚀在金属表层形成锈层后的腐蚀机理
一般认为:
存在锈层时,它对锈层下基体钢的离子化将起强氧化剂的作用。
在一定的条件下,腐蚀产物会影响大气腐蚀的电极反应。
Evans认为大气腐蚀的铁锈层处在湿润条件下,可以作为强烈的氧化剂而作用。
在锈层内,Evans模型如图4-2所示。
图4-2Evans模型
阳极反应发生在金属/Fe3O4的界面上:
阴极反应发生在Fe3O4/FeOOH界面上:
即锈层内发生的还原反应,可见锈层参与了阴极过程。
当锈层干燥时,即外部气体相对湿度下降时,锈层和底部基体钢的局部电池成为开路,在大气中氧的作用下锈层重新氧化成Fe3+的氧化物,可见在干湿交替的条件下带有锈层的钢能加速腐蚀的进行。
但是一般说来,在大气中长期暴露的钢,其腐蚀速度还是逐渐减慢的。
原因之一是锈层的增厚会导致锈层电阻的增加和氧渗入的困难,这就使阴极去极化作用减弱;
其二是附着性好的锈层内层将减小活性的阳极面积,增加了阳极极化,使大气腐蚀速度减慢。
四、大气腐蚀的特点
1.液膜表积比极大,具有极好的溶氧条件,使之一方面始终为氧饱和,另一方面氧极易达到金属表面,所以大气腐蚀具有吸氧腐蚀的优越条件。
2.由于液膜的高含氧特征及金属离子水化过程的困难,容易促成阳极极化乃至阳极钝化。
3.腐蚀产物残留沉积于金属表面,它们的特性对腐蚀影响极大,有的具有保护作用能够抑制腐蚀的发展,有的可能进一步加速腐蚀过程产生不良后果。
4.大气腐蚀的电极过程特征随大气条件的不同而变化。
五、影响大气腐蚀的主要因素
影响大气腐蚀的因素很多,季节、风向、气候区类、大气成分等都对大气腐蚀有显著的影响,主要影响因素有以下几各方面。
1.相对湿度
相对湿度决定了金属表面的水膜厚度,也就决定了大气腐蚀的类型、腐蚀控制因素及腐蚀速度。
所以它是影响大气腐蚀的首要因素。
一般说来,在临界相对湿度以下,水膜极薄,发生的是干大气腐蚀,腐蚀速度极慢。
而高于临界相对湿度,水膜显著增厚,腐蚀速度剧增。
2.温度
温度的影响有两重性,一般情况下,温度升高不会改变大气腐蚀的类型,则由于阴、阳极反应速度加快使腐蚀速度增大。
但是若绝对湿度不变,升温将降低相对湿度,使水膜减薄。
如果温升使相对湿度跨越临界相对湿度,将潮大气腐蚀变为干大气腐蚀,则会急剧降低腐蚀速度。
3.大气类型及成分
按照大气中所含有害物质,大气可分为乡村大气、城市大气、海洋大气、工业大气等,它们所含腐蚀物质的种类、含量各不相同,从而使水膜电解液的成分、腐蚀特性不同。
总的看来,气相污染物中最为有害的是H2S和SO2,它们既直接参与阴极反应,加速阴极过程,还会破坏钝化膜,加速阳极反应。
4.固体尘粒
工业大气和城市大气中固态尘粒含量较高,它们对大气腐蚀也有明显的促进效果。
尘粒种类不同,促进大气腐蚀的机理也不相同。
首先,落于金属表面的尘粒成为毛细凝聚的核心,加速了水膜的形成。
其次,有的尘粒本身就有腐蚀性,如盐类颗粒。
另外,有的本身虽无腐蚀性,但能吸附腐蚀性气体,如碳粒吸附SO2等。
对于较大、较多的固体颗粒,还可能与金属表面形成缝隙,造成缝隙腐蚀。
5.金属的表面状态
金属制品的加工方法、粗糙程度、表面附着物、有无氧化膜或防护涂层以及腐蚀产物等都对大气腐蚀有明显的影响。
六、大气腐蚀的防护措施
1.提高材料的耐大气腐蚀性
通过在钢中加入Cu、P、Cr等元素使之合金化的方法,可以改善材料的耐大气腐蚀性能。
2.表面保护
采用表面保护层隔绝潮湿空气与金属直接接触是防止大气腐蚀的有效手段。
3.降低相对湿度
采用加热空气、干燥剂、冷冻除水等方法将相对湿度控制在临界值以下,使大气腐蚀控制在干大气腐蚀的低速率之内。
4.缓蚀剂
采用多种缓蚀剂制成保护材料,可有效地抑制或减缓大气腐蚀的发生和发展。
5.其它
净化空气、清除金属表面附着物等方法也有助于减轻大气腐蚀的危害。
第二节海水腐蚀
海洋约占地球表面积的十分之七。
海水是自然界量最大,而且还具有很强腐蚀性的天然电解质。
近年来海洋开发受到普遍的重视,各种海上运输工具,各类的舰船,海上的采油平台,开采和水下输送及储存设备,海岸设施等不断增加。
工业的发展使沿岸污染增加,腐蚀问题也更加突出。
我国的海岸线长达一万八千公里,海洋天然资源十分丰富,所以研究和解决金属材料的海水腐蚀问题,对于发展我国的海运和海洋开发,以及海军现代化建设具有重要意义。
一、海水的性质
海水作为腐蚀性介质,其特性首先在于它的含盐量相当大。
世界性的大洋中,水的成分和含盐度是颇为恒定的。
内海里的含盐量差别较大,因地区的条件不同而异。
例如,地中海的总盐度高达3.7~3.9%,而里海则低到1.0~1.5%,且所含的硫酸根离子高。
海水中的主要盐类的含量见表4-2。
成分
100海水中的盐的克数
占总盐度的百分数
NaCl
2.7213
77.8
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 腐蚀 讲义 第四 金属 自然环境 中的 防护
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
