 第八章镁铝Word下载.docx
第八章镁铝Word下载.docx
- 文档编号:15315683
- 上传时间:2022-10-29
- 格式:DOCX
- 页数:16
- 大小:75.98KB
第八章镁铝Word下载.docx
《第八章镁铝Word下载.docx》由会员分享,可在线阅读,更多相关《第八章镁铝Word下载.docx(16页珍藏版)》请在冰豆网上搜索。
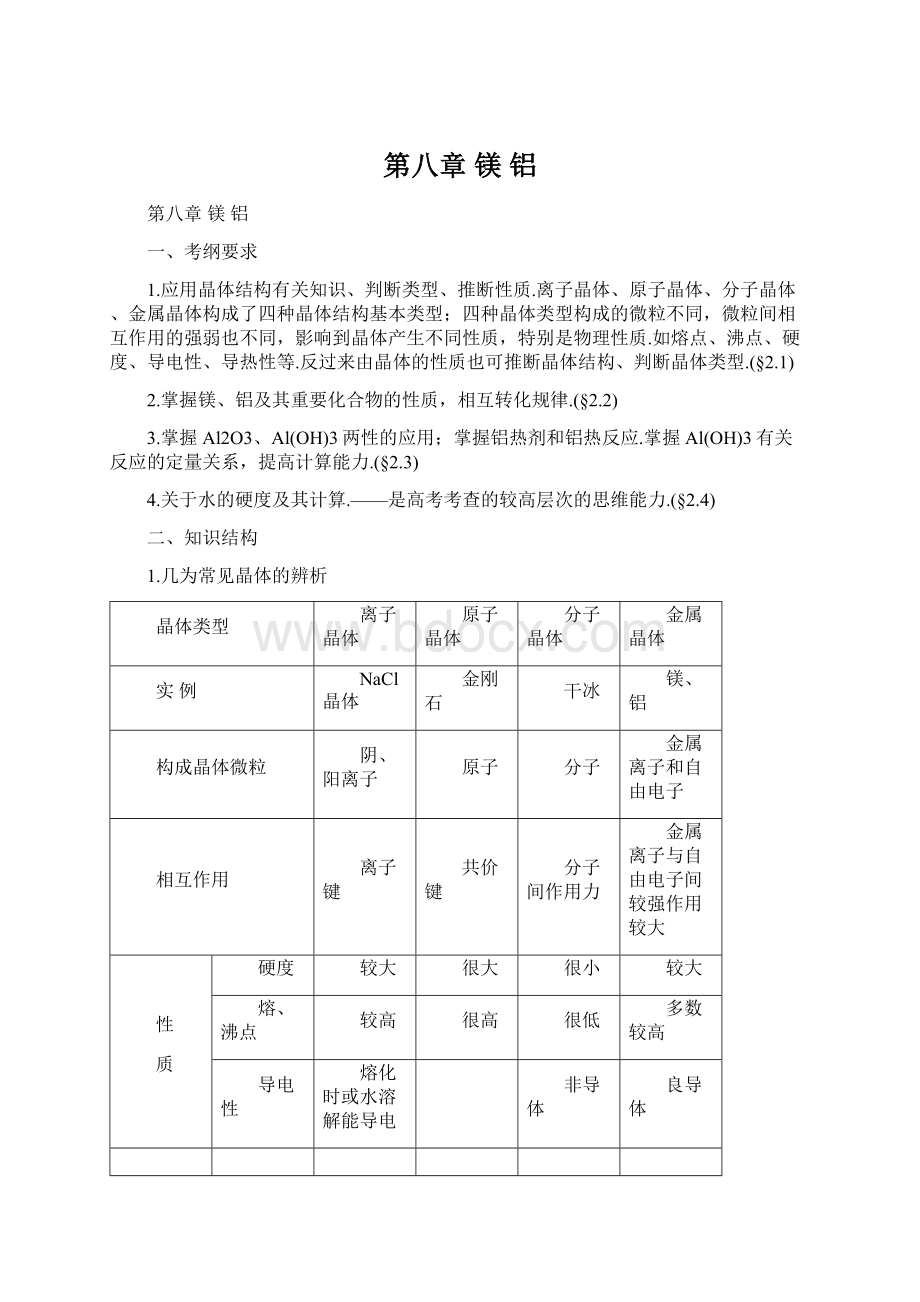
镁、铝
构成晶体微粒
阴、阳离子
原子
分子
金属离子和自由电子
相互作用
离子键
共价键
分子间作用力
金属离子与自由电子间较强作用较大
性
质
硬度
较大
很大
很小
熔、沸点
较高
很高
很低
多数较高
导电性
熔化时或水溶解能导电
非导体
良导体
2.镁和铝的性质
物理性质
共性:
密度小熔点较低,硬度较小银白色金属.
不同点:
Al的上述性质都比镁略高.
化学性质
1.跟O2及其它非金属反应
常温下,在空气中都因生成氧化膜,具有抗腐蚀能力.
Mg+O22MgO
4Al+3O22Al2O3
3Mg+N2Mg3N2
Mg+Br2MgBr2
2Al+3SAl2S3
2.跟某些氧化物
2Mg+CO22MgO+C
2Al+Fe2O32Fe+Al2O3(铝热反应)
3.跟水反应
Mg+2H2OMg(OH)2+H2↑(冷水慢,沸水快)
2Al+6H2O2Al(OH)30+3H2↑(一般不反应,只有氧化膜被破坏后反应)
4.跟酸的反应
Mg+2H+Mg2++H2↑
2Al+6H+3Al3++3H2↑(常温下,在浓H2SO4、浓HNO3中钝化)
5.跟碱反应
2Al+2NaOH+2H2O2NaAlO2+3H2↑
3.镁和铝的氧化物的主要性质
MgO(碱性氧化物)Al2O3(两性氧化物)
物理性质
白色粉末、熔点高白色固体、熔点高
1.跟水的反应
MgO+H2O=Mg(OH)2↓(反应缓慢进行)
2.跟酸反应
MgO+2H+Mg2++H2O
Al2O3+6H+2Al3++3H2O
3.跟碱反应
Al2O3+2OH-AlO-2+2H2O
4.镁和铝的氢氧化物的主要性质
Mg(OH)2(中强碱)Al(OH)3(两性氢氧化物)
物理性质
白色粉末难溶于水白色固体,难溶于水
1.跟酸反应
Mg(OH)2+2H+Mg2++2H2O(可溶于NH4Cl等强酸弱碱盐)
Al(OH)3+3H+Al3++3H2O
2.跟碱反应
Al(OH)3+OH-AlO-2+2H2O
3.受热分解
Mg(OH)2MgO+H2O
2Al(OH)3Al2O3+3H2O
实验室制法
可溶性镁盐加NaOH溶液Mg2++2OH-Mg(OH)2↓
可溶性铝盐加氨水Al3++3NH3·
H2OAl(OH)3↓+3NH+4
三、知识点、能力点提示
1.铝与强碱溶液反应的实质
反应过程:
2×
3e
2Al+6H2O2Al(OH)3↓+3H2↑
2Al(OH)3+2NaOH2NaAlO2+4H2O
总反应式:
2Al+2H2O+2NaOH2NaAlO2+3H2↑
Al与水很难反应,且生成的Al(OH)3附在Al的表面,阻止了Al继续反应,但强碱NaOH能溶解Al(OH)3,故可促使Al与强碱液反应,而弱碱如氨水,不溶解Al(OH)3,故Al在弱碱溶液中不反应.
2.Al(OH)3的两性
在溶液中同时发生酸式电离和碱式电离.
Al(OH)3H3AlO3HAlO2+H2O
碱式电离
Al3++3OH-AlO-2+H+
若向此溶液中加入酸,因H+与OH-结合生成水,反应向碱式电离方向进行,此时Al(OH)3是碱性,若加入碱,因OH-与H+结合生成水,故向酸式电离方向进行,这时Al(OH)3显酸性.
Al(OH)3溶解度很小,无论酸式或碱式电离的程度都很小,其碱性略强于酸性,故仍属于弱碱.
3.铝盐溶液与强碱溶液的反应.
(1)向AlCl3溶液中滴加NaOH溶液
①现象:
白色沉淀沉淀增加减少消失
②有关反应:
Al3++3OH-Al(OH)3↓
Al(OH)3+OH-AlO-2+2H2O
(2)向NaOH溶液中滴加AlCl3溶液
沉淀立刻消失,沉淀沉淀增加沉淀量不变
Al3++3OH-Al(OH)3↓
Al3++3AlO-2+6H2O4Al(OH)3↓
四、能力训练
1.今有四种处于固态的物质:
钠、硅、氖、氯化钠.问下列四项性质的叙述各属于哪种物质?
(1)由分子间力结合而成,熔点很低.
(2)电的良导体,熔点在1000℃左右.
(3)由共价键组成的网状原子晶体.
(4)非导体、但熔融后可以导电.
知识点:
晶体类型与物理性质间的关系.
能力点:
概括能力、判断能力.
2.已发现的一百多种元素里,大约有是金属元素,其中:
(1)自然界中,最活泼的金属元素是;
(2)熔沸点最低的金属元素是;
(3)质量相同时,与足量的酸反应,放出H2的量最多的金属是;
(4)第三周期氧化性最强的离子是
从不同角度分析金属有关性质.
综合能力
3.向一个铝制易拉罐充满CO2气,然后往罐内注入足量的NaOH溶液,立即用胶布严封罐口,不多会儿听到罐内“卡卡”作响,发现易拉罐变瘪,再过一会易拉罐又鼓起来.
①易拉罐变瘪的原因,反应的离子反应式;
②易拉罐又鼓起来的原因,离子反应式
铝与碱液的反应
将理论知识运用于实际生活的能力.
4.不另加固体或液体物质,如何使含有amolAl3+的A溶液中的铝元素和含有bmolAlO2-的B溶液中的铝元素全部转化为Al(OH)3沉淀?
NH3与Al3+,CO2与AlO2-的反应。
分解发散能力。
5.有一不纯的Mg条0.8g(杂质不能燃烧,且不溶于盐酸),在空气中充分燃烧,然后将生成物溶于50ml、1.8mol/L盐酸中,当往此溶液中加入0.2mol/L的NaOH溶液90ml时,正好中和多余的盐酸,如再加入碱液360ml并加热,不但Mg2+完全沉淀,且放出134.4mlNH3(标准状况)
求:
(1)写出有关反应式或离子反应式(7个)
(2)NH3多少摩?
(3)Mg3N2多少摩?
(4)MgO多少摩?
(5)Mg条中Mg的质量分数
镁及其化合物的一系列反应
阶梯发散思维.
6.氢化钠(NaH)是一种离子晶体,它与水反应生成碱和H2,现有NaH和Al粉混合物m(g),与足量的水充分反应放出n(g)气体.
求下列条件下混合物中Al的质量
(1)x≥y(设NaHxmol,Alymol)
(2)x<y
Al粉与其他混合物的反应
信息迁移能力
7.可能含有下列离子:
K+、H+、Mg2+、OH-、CO2+3、Cl-、NO-3的某无色透明溶液,能与Al反应放出H2.
①若反应时Al转变成Al3+并放出H2,则该溶液中无离子,一定有离子,可能有离子.
②若与Al反应后,向所得溶液中滴加盐酸,发现仅有白色沉淀生成,则该无色溶液中,一定有离子,一定无离子,可能存在的离子有.
Al与强酸或强碱液反应
8.下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)不正确的是()
(A)向1L浓度均为0.1mol/L的Ba(OH)2、NaAlO2混合液加入0.1mol/L稀H2SO4
(B)向含有0.1mol/LAlCl3和0.3mol/LNH4Cl的混合液1L中加入0.1mol/LNaOH溶液
(C)向烧碱溶液滴加明矾溶液
(D)向AlCl3溶液滴加过量氨水
反应在图像中如何体现
数学与化学知识的有机结合
9.下列图示中,E是不溶于水的白色胶状物质。
则:
(A)化学式:
ABC
DE
(B)反应式或离子反应式.
①②③
④⑤⑥
框图,信息的运用
善于找突破口,展开逆向发散.
10.右图是向MgCl2、AlCl3混合溶液中,开始滴加6ml试剂A,之后改滴试剂B,所得沉淀ymol与试剂体积V(ml)间的关系.以下结论不正确的是()
(A)A是盐酸,B是NaOH,且[B]=2[A]
(B)原混合液中,[Al3+]∶[Mg2+]∶[Cl-]=1∶1∶5
(C)A是NaOH,B是盐酸,且[NaOH]∶[HCl]=2∶1
(D)从6到9,相应离子反应式H++OH-H2O
Mg2+和Al3+与碱NaOH反应的差异
判断识图能力
11.关于ⅠA族和ⅡA族元素的下列说法中正确的是()
A.在同一周期中,ⅠA族单质的熔点比ⅡA族高
B.浓度都是0.01mol/L时,KOH溶液的pH比Ba(OH)2的小
C.氧化钠的熔点比氧化镁高
D.加热时,碳酸钠比碳酸镁易分解
对各主族元素性质的熟练掌握程度。
学会归纳比较的能力。
12.下列叙述中,一定是金属元素的是()
A.原子的最外层只有一个电子的元素
B.易失去电子的物质
C.原子的最外层有两个电子的主族元素
D.单质具有金属光泽的元素
金属元素的有关性质
13.已知工业上真空炼铷的反应方程式为:
2RbCl+MgMgCl2+2Rb(g),对于此反应,能够进行正确解释的是()
A.Rb比Mg金属性强
B.铷的沸点比镁的低,当把铷蒸气抽走时,平衡向正反应方向移动
C.MgCl2对热的稳定性比RbCl弱
D.高温下,Mg2+离子得电子的能力比Rb+离子弱
金属的还原性以及化学平衡方程。
比较迁移能力。
14.有关Al与NaOH溶液的反应的说法中,正确的是()
A.铝是还原剂,其氧化产物是Al(OH)3
B.NaOH是氧化剂,其还原产物是H2
C.铝是还原剂,H2O和NaOH都是氧化剂
D.H2O是氧化剂,Al被氧化
Al与NaOH溶液反应的实质
追溯求源的能力
15.向某溶液中投入铝片后有大量H2放出,则溶液中不可能大量存在的离子是()
A.Cl-B.H+
C.OH-D.HCO-3
Al的化学性质及离子共存条件
16.据报道:
高温超导材料中,铊(Tl)是组成成分之一.
下列关于铊的性质判断,一定错误的是()
A.铊是银白色质软的金属B.Tl(OH)3是两性氢氧化物
C.Tl与Cl2化合能生成TlCl3D.Tl的密度大于Al
新型材料铊的有关性质及元素周期律的知识.
类推能力
17.甲、乙两烧杯中各盛有100mL3mol/L的盐酸和氢氧
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第八章 第八
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
