 专题无机推断Word下载.docx
专题无机推断Word下载.docx
- 文档编号:17509162
- 上传时间:2022-12-06
- 格式:DOCX
- 页数:13
- 大小:151KB
专题无机推断Word下载.docx
《专题无机推断Word下载.docx》由会员分享,可在线阅读,更多相关《专题无机推断Word下载.docx(13页珍藏版)》请在冰豆网上搜索。
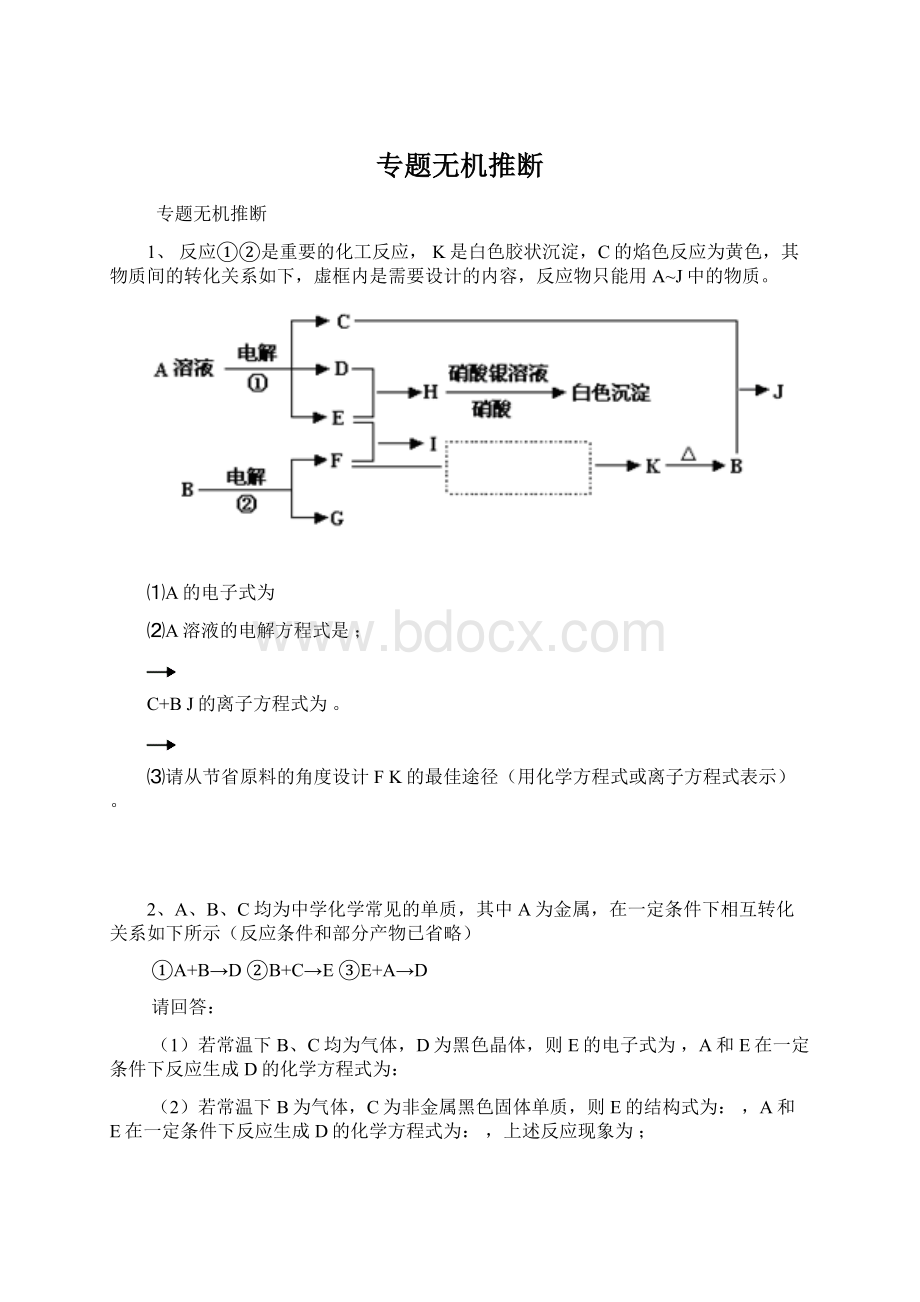
。
3、已知A是应用最为广泛的金属,x、y为同一主族的元素的单质,B和C是两种黑色化合物。
A、B、C与有关物质之间的相互转化关系如下图所示,其中每一方格内的字母表示一种反应物或生成物,反应加入或生成的水已略去。
填写下列空白:
(1)物质的化学式:
A_____________,B_______________,C_______________。
(2)写出反应的化学方程式:
B+M:
_____________________________________________________
C+M:
(3)写出E与G反应的离子方程式:
___________________________________________
4、以海水中常见物质A为原料可以发展很多工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题。
(1)C和D、C和G反应都可以制取消毒剂。
C和D反应制取的消毒剂中有效成分的化学式为__________。
(2)电解A溶液反应的离子方程式为_________________________________。
(3)将F和J通入A的饱和溶液中,反应的化学方程式为:
________________________________。
(4)J的空间构型为___________形,
J和G反应的工业名称___________
(5)空气分离出H后剩余气体的最主要成分是 ,有可以将其与B及D组成燃料电池,则该电池的负极反应式:
;
正极反应式:
。
5、物质之间的转化关系如下图所示:
A可作为工业生产J的原料,B、C、H、I为非金属,X的水溶液为一种常见的医用消毒液,F为常见的红棕色油漆颜料的主要成分,O是常见有机氮肥,分子内所有原子皆达到稳定结构且氢原子只有一种空间位置;
反应⑦中L与M的物质的量这比为1:
2,A、E、J、N中含有同一种元素。
回答下列问题:
(1)A、E、J、N中所含元素的名称是,X的化学式为,O的结构简式为。
(2)考虑到综合经济效益,工业生产M时,可采取的措施有(填序号)。
a.使用催化剂b.适当降低温度c.选择合适的温度d.适度增大压强e.及时分离出产物f.对原料进行循环利用g.充分利用反应本身放出的热量h.工厂地址尽可能选择在交通发达的城市
(3)反应①②④⑦中,属于转换反应的是(填序号)
⑦的方程式为
(4)现有1mol纯净物A参加反应,假设各步均完全反应,生成N的质量为1165g,生成K的质量为224g,则反应①化学反应方程式为。
6.已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。
现用A与石墨作电极,B的浓溶液作电解质,构成原电池。
有关物质之间的转化关系如下图:
(注意:
其中有些反应的条件及部分生成物被略去)
请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为
(2)从D溶液制备D的无水晶体的“操作a”为。
(3)反应②的化学方程式为 。
(4)反应⑤的化学方程式为 。
(5)原电池反应①中正极的电极反应式为。
7.A~K各物质间存在如下转化关系。
其中:
①E和K为无色气体单质,F为常见的金属,它在高温下与某些金属氧化物反应是工业上冶炼金属的方法之一。
②A为无色气体,B为淡黄色固体,C为无色液体。
(1)写出以下物质的化学式:
A,H,I
(2)写出B的电子式,固态G属于晶体。
(3)写出F+G+C→J+K的化学方程式:
8.已知B是常见金属单质,E为常见非金属单质,H常温下为无色液体。
根据下列关系,试回答:
(1)L的化学式:
F的电子式:
。
(2)反应①的离子方程式:
(3)反应②,工业上采取的反应条件:
。
(4)每生成1molK,反应放出98.3kJ热量,该反应的热化学方程式为:
。
9物质A、B、C、D为中学常见单质,其组成元素的原子序数依次减小,且其中只有三种是短周期元素,B为黄绿色气体;
物质A、E、F、G、J中含相同元素X。
试根据下图中物质的相互转化关系回答下列问题。
(1)X为_________元素(填“金属”或“非金属”);
(2)在
的转化中,A的作用是;
在①~⑥的反应中,不属于氧化还原反应的是。
(多填或少填无分)
(3)A在高温下与H反应产生产生E和D,每产生0.4molD至少消耗物质A
mol。
(4)写出反应⑥的化学反应方程式
______________________________________________________________。
(5)已知在101kPa条件下,2molD的完全燃烧生成气态H放出483.6kJ热量;
1molH(液态)汽化时吸热44kJ。
请书写表示D燃烧热的热化学方程式:
______________________________________________________________。
10.已知A为酸式盐,B为某二价主族金属的化合物,C、D、F、G、I在常温常压下均呈气态,且D燃烧时产生的氧炔焰常用来焊接或切割金属。
等物质的量A、B与少量的水充分混合能恰好完全反应。
图中反应条件(除高温外)均已略去。
(1)写出B的电子式,D的结构简式。
(2)写出A与B反应的化学方程式。
(3)将I气体通入溶有饱和C气体的NaCl溶液,是侯氏制碱法的一步关键反应,该反应的化学方程式为。
(4)写出下列反应的离子方程式:
①在A溶液中加入M。
②在A溶液中加入过量NaOH溶液,并加热:
③已知Fe3O4能溶于M溶液并产生F气体,该离子反应为:
11.已知:
D、E、F为中学化学中常见的气体,A、C、G、H中含有同一元素R,C溶液的焰色反应为黄色,D为平面形分子,相对分子质量为28,M是有香味的有机物。
物质之间有如下转化关系(部分反应物和产物已略去):
试回答下列问题:
(1)B的化学式。
(2)若M的相对分子质量比I的相对分子质量大42,则M的结构简式为
(3)E的电子式为:
E可在空气中燃烧,其燃烧现象是,
(4)证明A中含有R元素的操作为:
取一支试管,滴入10滴~15滴A,再加入1mL5%的B溶液,充分振荡后静置,待液体分层后,用滴管小心吸取10滴上层溶液,转入另一盛有10mL稀HNO3溶液的试管中,然后加入2滴~3滴2%的AgNO3溶液,有浅黄色沉淀产生。
在上述操作中稀HNO3的作用是:
,能说明该反应中A已经作用完
全的实验现象是。
(5)写出下列反应的化学方程式:
①
⑥
12.下图涉及多种无机化工反应,其中R是一种新型无机材料,M是一种应用广泛的金属材料,F为尿素[CO(NH2)2],A、C、D、M均为常见元素的单质,“↑”表示该物质常温下是气体,反应G+J→F+H2O中G与J的最佳配比为2∶1,向Y溶液中通入足量的J气体时可得到一种白色胶状沉淀,将该白色胶状沉淀滤出洗净后加热分解可以得到B。
⑴试写出B的化学式:
_________________,J的电子式_____________。
⑵反应①的化学方程式为___________________________________________。
⑶反应④的离子方程式为___________________________________________。
⑷上述反应中属于非氧化还原反应的有_____________(填写相应反应的序号)。
13.有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成物从略)。
其中B、D、E、F均为无色气体,M、L为常见的金属单质,C为难溶于水的红褐色固体。
在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和M反应可放出大量的热。
请回答下列问题:
(1)B的电子式,B气体的检验方法为。
(2)画出元素L的原子结构示意图。
(3)电解混合液时阳极反应式为。
(4)按要求写出上述转化关系中有关反应的化学方程式:
①含有L元素的化合反应,
②含有L元素的置换反应。
(5)L与过量G的稀溶液反应的离子方程式为
(6)物质X的化学式。
(7)已知agE气体在D中完全燃烧生成稳定的化合物时,放出bkJ的热量,写出E燃烧热的热化学方程式。
14.下图所示的框图中,A-I都是由短周期元素组成的常见物质。
其中A是气体,它的水溶液呈碱性;
氧化物D和氧化物F都易与人体血液中的血红蛋白结合而使人中毒;
单质E可作半导体材料。
(1)化合物A的化学式是,氧化物G的电子式是。
(2)组成单质E的元素在元素周期表中的位置是;
单质H和单质E以及氧化物I均能形成(填“分子”、“原子”或“离子”)晶体,其中单质E的熔点(填“高于”、“低于”或“等于”)氧化物I的熔点。
(3)标准状况下,将2.24L氧化物F和1.68L单质B同时通入1L氧化物G中(反应前后溶液体积的变化忽略不计),发生的反应的化学方程式为,所得溶液的PH=。
此时再向溶液中通入2.24L化合物A,完全反应后所得溶液的PH(填“>7”、“<7”或“=7”),用离子方程式表示其原因:
(4)单质B和单质C在一定条件下可组成原电池(用KOH溶液作电解质),则该原电池负极的电极反应式为。
15.下图是无机物A-M在一定条件下的转化关系(部分产物及反应条件未列出)。
其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
(1)在周期表中,组成单质G的元素位于第周期第族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为。
(3)在反应②③⑥⑨中,既属于化合反应又属于非氧化还原反应的是:
(填序号)
(4)反应④的离子方程式是:
(5)将化合物D与KNO3、KOH共熔,可制得一种“绿色”环保高效净水剂高铁酸钾(K2FeO4),同时还生成KNO2和H2O。
该反应的化学方程式是:
16.下图是无机物A-M在一定条件下的转化关系(部分产物及反应条件未列出)。
17.(13分)下图所示的转化关系图中(部分反应物或生成物未列出),B、C为常见的两种金属单质,且B和C的摩尔质量之比为7:
8;
A为常见的非金属单质;
E为一种具有磁性的黑色粉末;
H为红褐色沉淀;
I为白色沉淀。
(1)A的化学式为,H的化学式为。
(2)反应①中阴极的电极反应式为。
(3)反应⑦的化学方程式为。
(4)单质C与G溶液反应的离子方程式为。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 专题 无机 推断
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
