 化学新导学笔记人教选修三讲义第二章第二节分子立体结构第1课时Word文件下载.docx
化学新导学笔记人教选修三讲义第二章第二节分子立体结构第1课时Word文件下载.docx
- 文档编号:18372740
- 上传时间:2022-12-15
- 格式:DOCX
- 页数:14
- 大小:64.91KB
化学新导学笔记人教选修三讲义第二章第二节分子立体结构第1课时Word文件下载.docx
《化学新导学笔记人教选修三讲义第二章第二节分子立体结构第1课时Word文件下载.docx》由会员分享,可在线阅读,更多相关《化学新导学笔记人教选修三讲义第二章第二节分子立体结构第1课时Word文件下载.docx(14页珍藏版)》请在冰豆网上搜索。
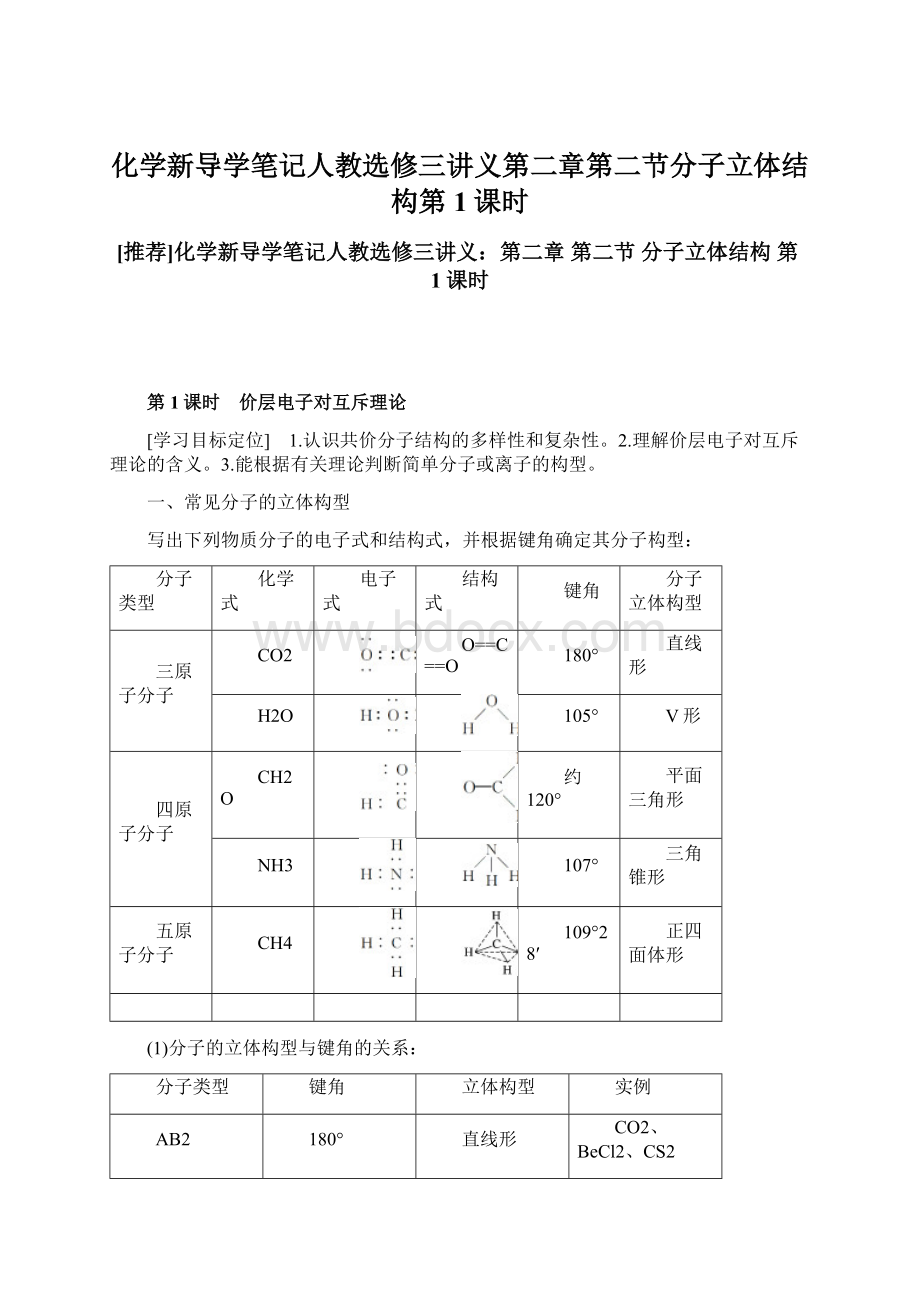
(1)分子的立体构型与键角的关系:
立体构型
实例
AB2
CO2、BeCl2、CS2
<
H2O、H2S
AB3
120°
BF3、BCl3
NH3、H3O+、PH3
AB4
CH4、NH
、CCl4
(2)典型有机物分子的立体结构:
C2H4、苯(C6H6)、CH2==CH—CH==CH2(1,3-丁二烯)、CH2==CH—C≡CH(乙烯基乙炔)等都是平面形分子;
C2H2为直线形分子。
例1 (2017·
衡水中学高二调考)下列有关键角与分子立体构型的说法不正确的是( )
A.键角为180°
的分子,立体构型是直线形
B.键角为120°
的分子,立体构型是平面三角形
C.键角为60°
的分子,立体构型可能是正四面体形
D.键角为90°
~109°
28′之间的分子,立体构型可能是V形
【考点】常见分子的立体构型
【题点】键角与分子立体构型的关系
答案 B
解析 键角为180°
的分子,立体构型是直线形,例如CO2分子是直线形分子,A正确;
苯分子的键角为120°
,但其立体构型是平面正六边形,B错误;
白磷分子的键角为60°
,立体构型为正四面体形,C正确;
水分子的键角为105°
,立体构型为V形,D正确。
例2 下列各组分子中所有原子都可能处于同一平面的是( )
A.CH4、CS2、BF3B.CO2、H2O、NH3
C.C2H4、C2H2、C6H6D.CCl4、BeCl2、PH3
【题点】常见分子立体构型的综合判断
答案 C
解析 题中的CH4和CCl4为正四面体形分子,NH3和PH3为三角锥形分子,这几种分子的所有原子不可能都在同一平面上。
CS2、CO2、C2H2和BeCl2为直线形分子,C2H4为平面形分子,C6H6为平面正六边形分子,这些分子都是平面形结构。
故选C项。
二、价层电子对互斥理论
1.价层电子对互斥理论
分子中的价层电子对包括σ键电子对和中心原子上的孤电子对,由于价层电子对相互排斥的作用,尽可能趋向彼此远离。
2.价层电子对的计算
(1)中心原子价层电子对数=σ键电子对数+孤电子对数。
(2)σ键电子对数的计算
由分子式确定,即中心原子形成几个σ键,就有几对σ键电子对。
如H2O分子中,O有2对σ键电子对。
NH3分子中,N有3对σ键电子对。
(3)中心原子上的孤电子对数的计算
中心原子上的孤电子对数=(a-xb)
①a表示中心原子的价电子数;
对主族元素:
a=最外层电子数;
对于阳离子:
a=价电子数-离子电荷数;
对于阴离子:
a=价电子数+离子电荷数。
②x表示与中心原子结合的原子数。
③b表示与中心原子结合的原子最多能接受的电子数,氢为1,其他原子=8-该原子的价电子数。
3.常见分子的VSEPR模型和立体构型
σ键电
子对数
孤电子
对数
价层电
电子对的排列方式
VSEPR模型
分子的立体构型
BeCl2、CO2
2
3
SO2
1
CH4、CCl4
4
四面体形
利用VSEPR模型确定分子或离子的立体构型的注意事项
(1)对于ABn型分子,成键电子对数等于配位原子的原子个数。
(2)若ABn型分子中,A与B之间通过两对或三对电子(即通过双键或三键)结合而成,则价层电子对互斥理论把双键或三键作为一对电子对看待。
(3)分子的中心原子的孤电子对数为0时,VSEPR模型与分子立体构型相同,分子均为空间对称性结构。
(4)分子的立体构型与分子类型有关,如AB2型分子只能为直线形或V形结构,AB3型分子只能为平面正三角形或三角锥形结构。
故由分子类型(ABn型)和孤电子对数能很快确定分子的立体构型。
例3 下列分子或离子的中心原子上未用于成键的价电子对最多的是( )
A.H2OB.HClC.NHD.PCl3
【考点】价层电子对互斥理论
【题点】价层电子对数目的计算与判断
答案 A
解析 A项,氧原子有两对未成键的价电子对;
B项,HCl分子属于AB型分子,没有中心原子;
C项,NH的中心原子的价电子全部参与成键;
D项,磷原子有一对未成键的价电子对。
例4 用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的立体构型,有时也能用来推测键角大小。
下列判断正确的是( )
A.SO2、CS2、HI都是直线形的分子
B.BF3键角为120°
,SnBr2键角大于120°
C.COCl2、BF3、SO3都是平面三角形的分子
D.PCl3、NH3、PCl5都是三角锥形的分子
【题点】价层电子对互斥理论的应用
解析 SO2是V形分子,CS2、HI是直线形的分子,A错误;
BF3键角为120°
,是平面三角形结构,而Sn原子价电子数是4,在SnBr2中两个价电子与Br形成共价键,还有一对孤对电子,对成键电子有排斥作用,使键角小于120°
,B错误;
COCl2、BF3、SO3都是平面三角形的分子,键角是120°
,C正确;
PCl3、NH3都是三角锥形的分子,而PCl5是三角双锥形结构,D错误。
分子立体构型的确定方法
中心原子价层电子对数n=σ键电子对数+(a-xb)
⇓
分子的立体构型——略去孤电子对在价层电子对互斥模型中占有的空间
注意
(1)价层电子对互斥构型是价层电子对的立体构型,而分子的立体构型指的是成键电子对的立体构型,不包括孤电子对。
两者是否一致取决于中心原子上有无孤电子对(未用于形成共价键的电子对),当中心原子上无孤电子对时,两者的构型一致;
当中心原子上有孤电子对时,两者的构型不一致。
(2)常见的分子立体构型:
直线形、V形、平面三角形、三角锥形、四面体形等。
1.下列有关价层电子对互斥理论的描述正确的是( )
A.价层电子对就是σ键电子对
B.孤电子对数由分子式来确定
C.分子的立体构型是价层电子对互斥的结果
D.孤电子对数等于π键数
【题点】价层电子对互斥理论的理解
解析 价层电子对数是σ键电子对数与孤电子对数之和,孤电子对数是指没有成键的价电子对数,其与中心原子价层电子总数、与中心原子结合的原子最多能接受的电子数及与中心原子结合的原子数有关,A、B、D项错误。
2.下列分子构型与分子中共价键键角对应正确的是( )
A.直线形分子:
B.平面正三角形:
C.三角锥形:
D.正四面体形:
解析 A项,HCl也是直线形分子,因只有一个共价键,故不存在键角,A项错误;
氨分子呈三角锥形,键角为107°
,C项错误;
甲烷与白磷分子均是正四面体形分子,但键角分别为109°
28′、60°
,D项错误。
3.下列分子或离子的中心原子,带有一对孤电子对的是( )
A.H2OB.BeCl2C.CH4D.PCl3
答案 D
解析 方法1:
选项中四种物质的电子式依次为。
H2O有2对孤电子对,BeCl2和CH4没有孤电子对,PCl3有一对孤电子对。
方法2:
将选项中各物质的未知数据代入公式:
中心原子上的孤电子对数=×
(a-xb),经计算知,选项中原子上的孤电子对数依次为2、0、0、1。
4.下列分子或离子中,中心原子价层电子对的立体构型为正四面体形且分子或离子的立体构型为V形的是( )
A.NHB.PH3
C.H3O+D.OF2
解析 中心原子价层电子对的立体构型为正四面体形,且分子或离子的立体构型为V形的只有3个原子构成的分子或离子,OF2为V形结构。
A选项NH是三角锥形的NH3结合了一个H+,呈正四面体形,B项中PH3为三角锥形,C中H3O+是V形的H2O结合了一个H+,呈三角锥形。
5.用价层电子对互斥理论完成下列问题(点“·
”的原子为中心原子)。
σ键电子对数
孤电子对数
H2S
Cl3
O2
O
答案
[对点训练]
题组一 常见分子的立体构型
1.下列分子的立体结构错误的是( )
A.SO2:
B.NH3:
C.CS2:
D.CH4:
2.判断BeCl2和H2O分子中化学键的键角的关系( )
A.前者大于后者B.前者小于后者
C.二者相等D.无法判断
3.下列分子构型为正四面体形的是( )
①P4 ②NH3 ③CCl4 ④CH4 ⑤H2S ⑥CO2
A.①③④⑤B.①③④⑤⑥
C.①③④D.④⑤
题组二 分子中价电子对数目的确定
4.下列微粒中,含有孤电子对的是( )
A.SiH4B.H2OC.CH4D.NH
解析 SiH4、H2O、CH4、NH的电子式分别为,只有H2O分子中的O原子上有2对孤电子对。
5.下列微粒的价电子对数正确的是(点“”的原子为中心原子)( )
A.H4 4B.O2 1
C.F3 2D.O3 2
解析 对ABm型分子中心原子价电子对数:
n=
H4中,n==4,A正确;
O2中,n==2,B不正确;
F3中,n==3,C不正确;
O3中,n==3,D不正确。
6.乙烷、乙炔分子中碳原子间的共用电子对数目分别是1、3,则C20H32分子中碳原子间的共用电子对数目可能为( )
A.20B.24C.25D.77
解析 烷烃中碳碳间共用电子对数为碳原子数减去1;
若每减少2个H原子,则相当于碳碳间增加一对共用电子对,利用减少的H原子数目,再除以2可知增加的碳碳间共用电子对数,烷烃C20H42分子中碳原子间的共用电子对数目为19,则C20H32分子中碳原子间的共用电子对数目为19+10×
=24。
题组三 价层电子对互斥理论及其应用
7.下列关于价层电子对互斥模型(VSEPR模型)的叙述中不正确的是( )
A.VSEPR模型可用来预测分子的立体构型
B.分子中价电子对相互排斥决定了分子的立体构型
C.中心原子上的孤电子对也要占据中心原子周围的空间并参与互相排斥
D.分子中键角越大,价电子对相互排斥力越大,分子越稳定
解析 VSEPR模型可用来预测分子的立体构型,注意实际立体构型要去掉孤电子对,A正确;
立体构型与价电子对相互排斥有关,所以分子中价电子对相互排斥决定了分子的立体构型,B正确;
中心原子上的孤电子对也要占据中心原子周围的空间并参与互相排斥,且孤电子对间的排斥力>孤电子对和成对电子对间的排斥力,C正确;
分子的稳定性与键角没有关系,D不正确。
8.下列分子的VSEPR模型与分子的立体构型相同的是( )
A.CCl4B.SOC.NH3D.H2O
【题点】价层电子对互斥(VSEPR)模型与分子立体构型的对比
9.根据VSEPR模型判断下列各组分子或离子结构相同的是( )
A.SO2和CO2B.BF3和NH3
C.PH3和H2SD.CCl4和NH
解析 A项中,SO2分子中S有一对孤电子对,而CO2分子中没有孤电子对,因此SO2为V形而CO2为直线形;
B项中,BF3中B无孤电子对,而NH3中有一对孤电子对,因此其构型分别为平面三角形和三角锥形;
C项中,其构型分别为三角锥形和V形;
D项中,中心原子的成键情况相同,故分子结构也相同,为正四面体形。
10.氯的含氧酸根离子有ClO-、ClO、ClO、ClO等,关于它们的说法中不正确的是( )
A.ClO-中Cl显+1价
B.ClO的立体构型为直线形
C.ClO的立体构型为三角锥形
D.ClO是SO的等电子体
【题点】分子立体构型的综合
解析 ClO立体构型为V形。
11.已知在CH4中,C—H键间的键角为109°
28′,NH3中,N—H键间的键角为107°
,H2O中O—H键间的键角为105°
,则下列说法中正确的是( )
A.孤电子对与成键电子对间的斥力大于成键电子对与成键电子对间的斥力
B.孤电子对与成键电子对间的斥力小于成键电子对与成键电子对间的斥力
C.孤电子对与成键电子对间的斥力等于成键电子对与成键电子对间的斥力
D.题干中的数据不能说明孤电子对与成键电子对间的斥力与成键电子对与成键电子对间的斥力之间的大小关系
12.短周期主族元素A、B可形成AB3分子,下列有关叙述正确的是( )
A.若A、B为同一周期元素,则AB3分子一定为平面正三角形
B.若AB3分子中的价电子个数为24个,则AB3分子可能为平面正三角形
C.若为A、B为同一主族元素,则AB3分子一定为三角锥形
D.若AB3分子为三角形锥形,则AB3分子一定为NH3
解析 A项,若为PCl3,则分子为三角锥形,错误;
B项,BCl3满足要求,其分子为平面正三角形,正确;
C项,若分子为SO3,则为平面正三角形,错误;
D项,分子不一定为NH3,也可能为NF3等。
[综合强化]
13.
(1)计算下列分子或离子中点“”原子的价电子对数。
①CCl4____________;
②BeCl2___________;
③BCl3____________;
④PCl3____________。
(2)计算下列微粒中点“”原子的孤电子对数。
①H2S_____________;
②PCl5____________;
③BF3_____________;
④NH3____________。
答案
(1)①4 ②2 ③3 ④4
(2)①2 ②0 ③0 ④1
解析
(1)根据ABm型分子中价电子对数目n的计算公式:
①CCl4中C原子的价电子对数为=4;
②BeCl2中Be原子的价电子对数为=2;
③BCl3中B原子的价电子对数为=3;
④PCl3中P原子的价电子对数为=4。
(2)根据ABm型分子中心原子的孤电子对数=(a-xb)的计算公式:
①H2S中的S原子的孤电子对数:
×
(6-2×
1)=2;
②PCl5中的P原子的孤电子对数:
(5-5×
1)=0;
③BF3中的B原子的孤电子对数:
(3-3×
④NH3中的N原子的孤电子对数:
(5-3×
1)=1。
14.为了解释和预测分子的立体构型,科学家在归纳了许多已知分子立体构型的基础上,提出了一种十分简单的理论模型——价层电子对互斥理论。
这种模型把分子分成两类:
一类是中心原子________(填“有孤电子对”或“无孤电子对”,下同);
另一类是中心原子____________________________。
BF3和NF3都是四个原子的分子,BF3分子的立体构型是平面三角形,而NF3分子的立体构型是三角锥形的原因是__________________________。
答案 无孤电子对 有孤电子对 BF3分子中B原子的3个价电子都与F原子形成共价键而形成平面三角形;
而NF3分子中N原子的3个价电子与F原子形成共价键,还有1对未成键的孤电子对,占据了N原子周围的空间,参与相互排斥,形成三角锥形
15.20世纪50年代科学家提出价层电子对互斥理论(简称VSEPR模型),用于预测简单分子立体构型。
其要点可以概括:
Ⅰ.用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤电子对),(n+m)称为价层电子对数。
分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间;
Ⅱ.分子的立体构型是指分子中的原子在空间中的排布,不包括中心原子未成键的孤电子对;
Ⅲ.分子中价层电子对之间的斥力主要顺序为ⅰ.孤电子对之间的斥力>
孤电子对与共用电子对之间的斥力>
共用电子对之间的斥力;
ⅱ.双键与双键之间的斥力>
双键与单键之间的斥力>
单键与单键之间的斥力;
ⅲ.X原子得电子能力越弱,A—X形成的共用电子对之间的斥力越强;
ⅳ.其它。
请仔细阅读上述材料,回答下列问题:
(1)根据要点Ⅰ可以画出AXnEm的VSEPR理想模型,请填写下表:
n+m
VSEPR理想模型
价层电子对之间的理想键角
(2)请用VSEPR模型解释CO2为直线形分子的原因:
________________________________________________________________________。
(3)H2O分子的立体构型为__________,请你预测水分子中∠H—O—H的大小范围并解释原因:
________________________________________________________________________
(4)SO2Cl2和SO2F2都属AX4E0型分子,S与O之间以双键结合,S与Cl、S与F之间以单键结合。
请你预测SO2Cl2和SO2F2分子的立体构型:
_____________________,SO2Cl2分子中∠Cl—S—Cl________(选填“<
”“>
”或“=”)SO2F2分子中∠F—S—F。
答案
(1)
(2)CO2属AX2E0,n+m=2,故为直线形
(3)V形 水分子属AX2E2,n+m=4,VSEPR理想模型为正四面体形,价层电子对之间的夹角均为109°
28′,根据Ⅲ中的ⅰ,应有∠H—O—H<
(4)四面体形 >
解析 VSEPR模型的判断方法:
在分子中当n+m=2为直线形分子;
当n+m=3时,如果没有孤电子对时为平面三角形,如果有孤电子对时为V形;
当n+m=4时,如果没有孤电子对时为正四面体形,如果有一对孤电子对时为三角锥形,如果有两对孤电子对时为V形。
所以水分子中n+m=4,且有两对孤电子对,所以是V形结构,又由于孤电子对的作用力强于成键的共用电子对,所以使其角度小于109°
28′。
再如SO2Cl2和SO2F2中的硫原子是中心原子,此时n+m=4且没有孤电子对,所以它应为正四面体形,但由于原子种类不同,所以不是正四面体形。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学 新导学 笔记 选修 讲义 第二 分子 立体 结构 课时
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
