 高一化学(必修2)第二学期期中考试试卷.doc
高一化学(必修2)第二学期期中考试试卷.doc
- 文档编号:1866721
- 上传时间:2022-10-24
- 格式:DOC
- 页数:4
- 大小:460.50KB
高一化学(必修2)第二学期期中考试试卷.doc
《高一化学(必修2)第二学期期中考试试卷.doc》由会员分享,可在线阅读,更多相关《高一化学(必修2)第二学期期中考试试卷.doc(4页珍藏版)》请在冰豆网上搜索。
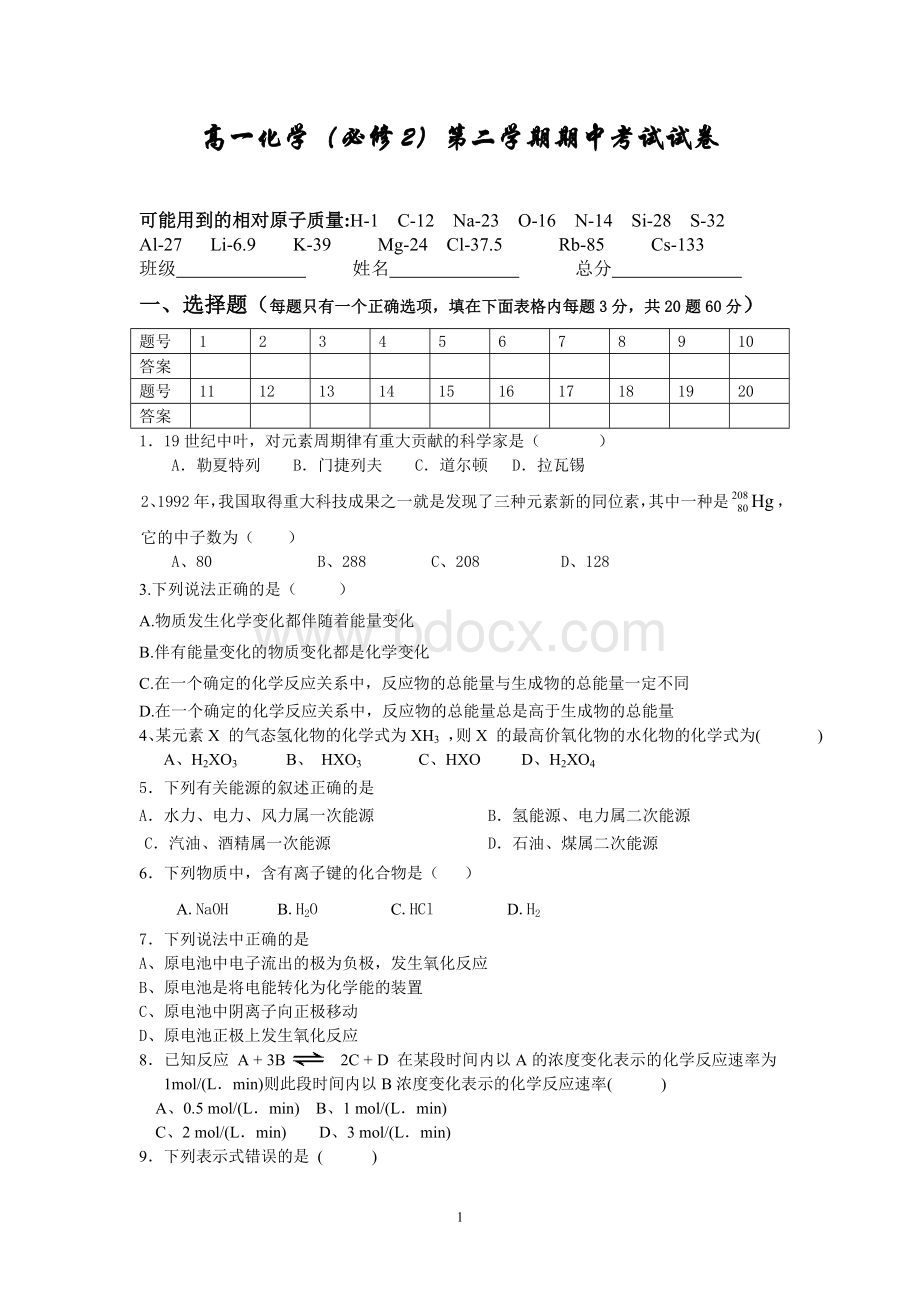
高一化学(必修2)第二学期期中考试试卷
可能用到的相对原子质量:
H-1C-12Na-23O-16N-14Si-28S-32
Al-27Li-6.9K-39Mg-24Cl-37.5Rb-85Cs-133
班级姓名总分
一、选择题(每题只有一个正确选项,填在下面表格内每题3分,共20题60分)
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
1.19世纪中叶,对元素周期律有重大贡献的科学家是()
A.勒夏特列B.门捷列夫C.道尔顿D.拉瓦锡
2、1992年,我国取得重大科技成果之一就是发现了三种元素新的同位素,其中一种是,它的中子数为()
A、80 B、288 C、208 D、128
3.下列说法正确的是()
A.物质发生化学变化都伴随着能量变化
B.伴有能量变化的物质变化都是化学变化
C.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同
D.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量
4、某元素X的气态氢化物的化学式为XH3,则X的最高价氧化物的水化物的化学式为()
A、H2XO3B、HXO3C、HXOD、H2XO4
5.下列有关能源的叙述正确的是
A.水力、电力、风力属一次能源 B.氢能源、电力属二次能源
C.汽油、酒精属一次能源 D.石油、煤属二次能源
6.下列物质中,含有离子键的化合物是()
A.NaOHB.H2OC.HClD.H2
7.下列说法中正确的是
A、原电池中电子流出的极为负极,发生氧化反应
B、原电池是将电能转化为化学能的装置
C、原电池中阴离子向正极移动
D、原电池正极上发生氧化反应
8.已知反应A+3B2C+D在某段时间内以A的浓度变化表示的化学反应速率为1mol/(L.min)则此段时间内以B浓度变化表示的化学反应速率()
A、0.5mol/(L.min)B、1mol/(L.min)
C、2mol/(L.min)D、3mol/(L.min)
9.下列表示式错误的是()
A、铝离子的结构示意图:
B、氯化钠的电子式:
Na+[]-
C、铝离子的电子式:
Al3+D、铝原子的结构示意图:
10.一学生欲通过实验判断X,Y,Z,W四块金属的活泼性,做了如下实验并得结论:
当X,Y组成原电池时,Y为负极;当Z,W组成原电池时,W为正极;W能将Y从其盐溶液中置换出来,据此可知它们的活泼性顺序是()
A.Z>W>X>YB、Z>W>Y>XC、X>Y>W>ZD、X>Y>Z>W
11.下列各装置能构成原电池的是()
G
Zn
C
G
Ag
Cu
G
Zn
Cu
G
G
稀硫酸)稀硫酸蔗糖稀硫酸
ABCD
12.、在相同条件下,下列气态氢化物的稳定性排列顺序正确的是()
A.HF>HCl>HBr>HIB.HCl>HBr>HI>HF
C.HBr>HI>HF>HClD.HI>HBr>HCl>HF
13.A、B、C均为短周期元素,它们在周期表中的位置如左图所示。
已知:
B、C两元素原子最外层电子数之和等于A元素原子最外层电子数的2倍;B、C两元素的核电荷数之和是A元素原子序数的4倍。
则A、B、C分别是
A.C、Al、PB.N、Si、S
C.0、P、ClD.F、S、Al
14.已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是()
A、X的能量一定低于M的,Y的能量一定低于N的
B、因为该反应为吸热反应,故一定要加热反应才能进行
C、破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D、X和Y的总能量一定低于M和N的总能量
15.下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是()
A.a电极是负极
B.b电极的电极反应为:
4OH--4e-=2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装
16.对化学反应限度的叙述,错误的是()
A.任何可逆反应都有一定的限度
B.化学反应达到限度时,正逆反应速率相等
C.化学反应的限度与时间的长短无关
D.化学反应的限度是不可改变的
17.
对于可逆反应M+3N2Q达到平衡时,下列说法正确的是
A.M、N、Q三种物质的浓度一定相等
B.M、N全部变成了Q
C.反应混合物各组分的浓度不再变化
D.反应已经停止
18.下列表示电子式的形成过程正确的是:
()
19.镭是元素周期表中第ⅡA族元素,下列关于镭的叙述不正确的是()
A.镭比钙的金属性更强B.在化合物中呈+2价
C.镭是一种放射性元素D.氢氧化镭呈两性
20.将ag块状碳酸钙跟足量的盐酸反应,反应物损失的质量随时间的变化曲线如图中的实线所示,在相同条件下,将bg(a>b)粉末状碳酸钙与同浓度的盐酸反应,则相应的曲线如图中的虚线所示。
其中正确的是()
损失质量
损失质量
损失质量
损失质量
、
ABCD
二、非选择题(共7题40分)
21.(5分)在原子中含有_____个质子,____个中子,____个电子。
在H、H、H、Mg、Mg和Cu中共有_______种原子,其中属于氢元素的同位素的是。
22.(5分)当一个反应进行到正反应速率与逆反应速率_____时,反应物和生成物的不再改变,就达到了平衡状态。
对于一定条件下的反应2SO2+O22SO3当有2molSO3生成同时也有____mol生成,则反应达到了平衡状态。
23.(4分)卤族元素的原子最外层都有个电子,在化学反应中容易电子,形成离子,它们都可以作剂。
24.(8分)下表标出的是元素周期表的一部分元素,回答下列问题:
(1)表中用字母标出的15种元素中,化学性质最不活泼的是(用元素符号表示,下同),金属性最强的是,非金属性最强的是,常温下单质为液态的非金属元素是,属于过渡元素的是(该空用字母表示)。
(2)B,F,C气态氢化物的化学式分别为,其中以最不稳定。
(3)第三周期中原子半径最小的是。
25.(9分)A、B、C、D均是短周期元素,A和B同周期,B和C同族,A元素族序数是周期数的三倍,B原子最外层电子数是内层电子数的二倍,B与A能生成化合物BA2,C与A生成化合物CA2,A的阴离子与D的阳离子电子层结构相同,都与氖原子的电子层结构相同,D的单质与A的单质在不同条件下反应,可生成D2A或D2A2。
请回答
(1)(2分)写出元素符号B:
C:
(2)(3分)BA2的电子式,BA2分子中化学键属于键.。
(3)(2分)D2A2的化学式,灼烧这化合物火焰呈色。
(4)(2分)C在元素周期表中的位置是第周期,族,其原子结构示意图
26.(3分)有①质子数②中子数③核外电子数④价电子数⑤最外层电子数⑥电子层数。
请用上述番号回答:
(1)元素种类由决定。
(2)原子的质量数由决定,元素在周期表中的位置由决定
27.(6)如下图,A、B、C、D为四种金属
装置
--------------
稀硫酸
B
A
--------------
CuSO4溶液
B
C
--------------
稀硫酸
A
D
现象
B棒有气泡
C棒有Cu析出
A棒有气泡
正极反应式:
①
②
四种金属活动性由强到弱的顺序:
③
4
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高一化学 必修 第二 学期 期中考试 试卷
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 保育笔记.doc
保育笔记.doc
 幼儿园日常安全检查记录表.xls
幼儿园日常安全检查记录表.xls
