 高中化学必修1第四章知识总结与习题练习含答案Word文档下载推荐.docx
高中化学必修1第四章知识总结与习题练习含答案Word文档下载推荐.docx
- 文档编号:18984028
- 上传时间:2023-01-02
- 格式:DOCX
- 页数:17
- 大小:127.61KB
高中化学必修1第四章知识总结与习题练习含答案Word文档下载推荐.docx
《高中化学必修1第四章知识总结与习题练习含答案Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《高中化学必修1第四章知识总结与习题练习含答案Word文档下载推荐.docx(17页珍藏版)》请在冰豆网上搜索。
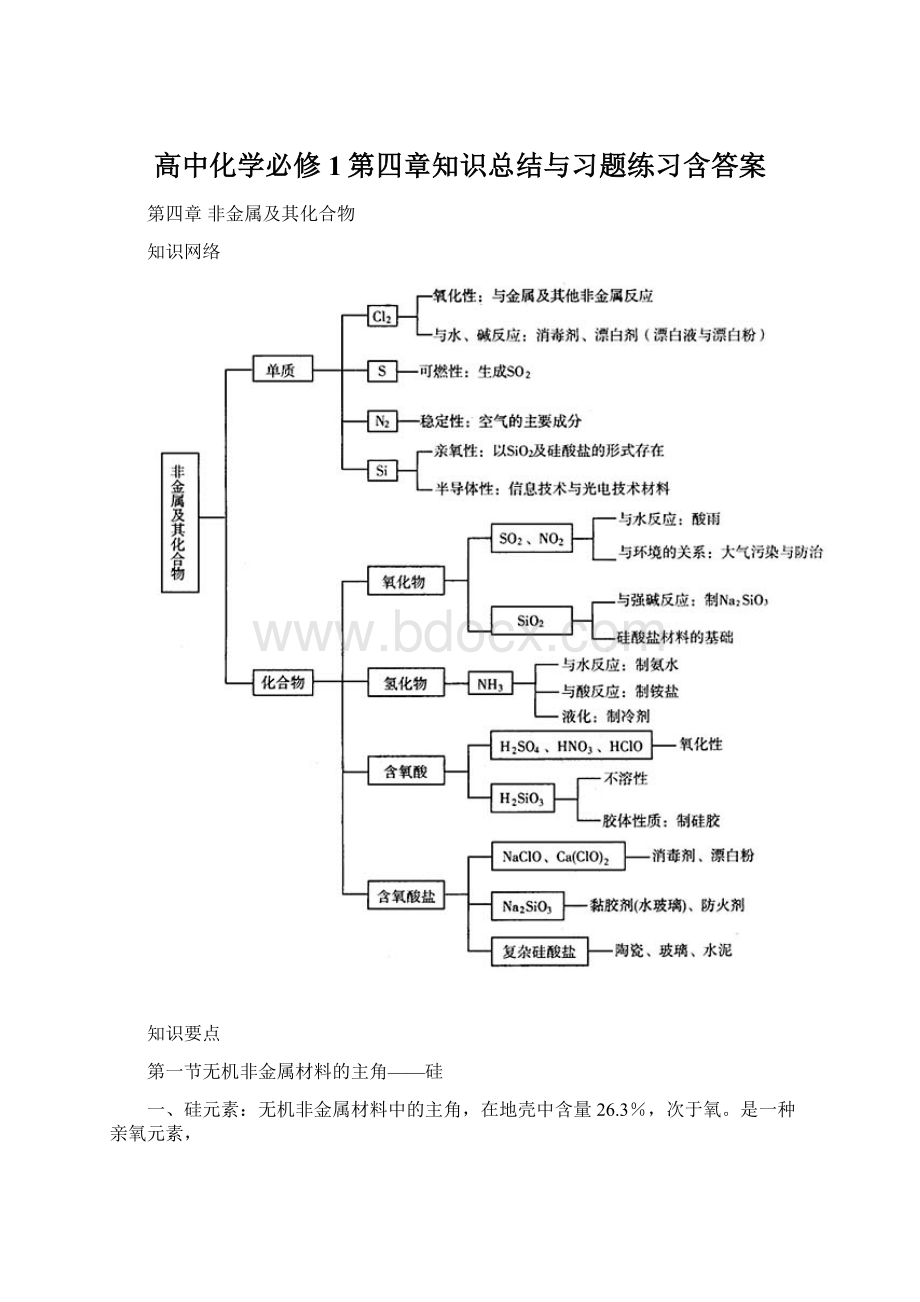
第二节富集在海水中的元素——氯
一、氯元素:
位于第三周期第ⅦA族,原子结构:
容易得到一个电子形成氯离子Cl-,为典型的非金属元素,在自然界中以化合态存在。
二、氯气
物理性质:
黄绿色气体,有刺激性气味、可溶于水、加压和降温条件下可变为液态(液氯)和固态。
(加热)
制法:
MnO2+4HCl(浓)=====MnCl2+2H2O+Cl2↑
闻法:
用手在瓶口轻轻扇动,使少量氯气进入鼻孔。
化学性质:
很活泼,有毒,有氧化性,能与大多数金属化合生成金属氯化物(盐)。
也能与非金属反应:
(点燃)(点燃)(点燃)
2Na+Cl2====2NaCl2Fe+3Cl2====2FeCl3Cu+Cl2====CuCl2
(点燃)
Cl2+H2====2HCl现象:
发出苍白色火焰,生成大量白雾。
认识:
燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧。
燃烧的本质是剧烈的氧化还原反应,所有发光放热的剧烈化学反应都称为燃烧。
Cl2的用途:
(光照)
①自来水杀菌消毒Cl2+H2O====HCl+HClO2HClO====2HCl+O2↑
氯气的水溶液称为氯水,其中次氯酸HClO有强氧化性和漂泊性,起主要的消毒漂白作用。
次氯酸有弱酸性,不稳定,光照或加热分解,因此久置氯水会失效。
②制漂白液、漂白粉和漂粉精
制漂白液Cl2+2NaOH====NaCl+NaClO+H2O,其有效成分NaClO比HClO稳定多
可长期存放制漂白粉(有效氯35%)和漂粉精(充分反应有效氯70%)
2Cl2+2Ca(OH)2====CaCl2+Ca(ClO)2+2H2O
③与有机物反应,是重要的化学工业物质。
④用于提纯Si、Ge、Ti等半导体和钛
⑤有机化工:
合成塑料、橡胶、人造纤维、农药、染料和药品
三、氯离子的检验
使用硝酸银溶液,并用稀硝酸排除干扰离子(CO32-、SO42-)
HCl+AgNO3====AgCl↓+HNO3
NaCl+AgNO3====AgCl↓+NaNO3
Na2CO3+2AgNO3====Ag2CO3↓+2NaNO3
Ag2CO3+2HNO3====2AgNO3+CO2↑+H2O
Clˉ+Ag+====AgCl↓
第三节硫和氮的氧化物
一、二氧化硫(点燃)
制法(形成):
硫黄或含硫的燃料燃烧得到(硫俗称硫磺,是黄色粉末)S+O2====SO2
无色、刺激性气味、容易液化,易溶于水
有毒,溶于水与水反应生成亚硫酸H2SO3,形成的溶液酸性,有漂白作用,遇热会变回原来颜色。
这是因为H2SO3不稳定,会分解回水和SO2
SO2+H2O→H2SO3因此这个化合和分解的过程可以同时进行,为可逆反应。
可逆反应——在同一条件下,既可以往正反应方向发生,又可以向逆反应方向发生的化学反应称作可逆反应,用可逆箭头符号连接。
二、一氧化氮和二氧化氮(高温或放电)
一氧化氮在自然界形成条件为高温或放电:
N2+O2========2NO,生成的一氧化氮很不稳定,在常温下遇氧气即化合生成二氧化氮:
2NO+O2==2NO2
一氧化氮的介绍:
无色气体,是空气中的污染物,少量NO可以治疗心血管疾病。
二氧化氮的介绍:
红棕色气体、刺激性气味、有毒、易液化、易溶于水,并与水反应:
3NO2+H2O==2HNO3+NO这是工业制硝酸的方法。
十、大气污染
SO2、NO2溶于雨水形成酸雨。
防治措施:
①从燃料燃烧入手。
②从立法管理入手。
③从能源利用和开发入手。
④从废气回收利用,化害为利入手。
(催化剂)
(2SO2+O2→2SO3SO3+H2O=H2SO4)
第四节硫酸、硝酸和氨
一、硫酸
无色粘稠油状液体,不挥发,沸点高,密度比水大。
具有酸的通性,浓硫酸具有脱水性、吸水性和强氧化性。
是强氧化剂。
(浓H2SO4)
C12H22O11========12C+11H2O放热
2H2SO4(浓)+C====CO2↑+2H2O+SO2↑
还能氧化排在氢后面的金属,但不放出氢气。
(附:
金属活动性顺序表K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au初中生应该掌握。
)
2H2SO4(浓)+Cu====CuSO4+2H2O+SO2↑
稀硫酸:
与活泼金属反应放出H2,使酸碱指示剂紫色石蕊变红,与某些盐反应,与碱性氧化物反应,与碱中和
二、硝酸
无色液体,易挥发,沸点较低,密度比水大。
具有一般酸的通性,浓硝酸和稀硝酸都是强氧化剂。
4HNO3(浓)+Cu====Cu(NO3)2+2NO2↑+4H2O
8HNO3(稀)+3Cu====3Cu(NO3)2+2NO↑+4H2O+4+3+2+10-3
反应条件不同,硝酸被还原得到的产物不同,可以生成:
NO2,HNO2,NO,N2O,N2,NH3
△硫酸和硝酸:
浓硫酸和浓硝酸都能钝化某些金属(如铁和铝)使表面生成一层致密的氧化保护膜,隔绝内层金属与酸,阻止反应进一步发生。
因此,铁铝容器可以盛装冷的浓硫酸和浓硝酸。
硝酸和硫酸都是重要的化工原料和实验室必备的重要试剂。
可用于制化肥、农药、炸药、染料、盐类等。
硫酸还用于精炼石油、金属加工前的酸洗及制取各种挥发性酸。
三、氨气及铵盐
氨气的性质:
无色气体,刺激性气味、密度小于空气、极易溶于水(且快)
溶于水发生以下反应使水溶液呈碱性:
NH3+H2O→NH3·
H2O→NH4++OHˉ可作红色喷泉实验。
生成的一水合氨NH3·
H2O是一种弱碱,能使酚酞溶液变红或使湿润红色石蕊试纸变蓝,很不稳定,会分解,受热更不稳定:
(△)
NH3·
H2O====NH3↑+H2O
浓氨水易挥发出氨气,有刺激难闻的气味。
氨气能跟酸反应生成铵盐:
NH3+HCl==NH4Cl(晶体)
氨是重要的化工产品,氮肥工业、有机合成工业及制造硝酸、铵盐和纯碱都离不开它。
氨气容易液化为液氨,液氨气化时吸收大量的热,因此还可以用作制冷剂。
铵盐的性质:
易溶于水(很多化肥都是铵盐),受热易分解,放出氨气:
NH4Cl====NH3↑+HCl↑
NH4HCO3====NH3↑+H2O↑+CO2↑
可以用于实验室制取氨气:
(干燥铵盐与和碱固体混合加热)
NH4NO3+NaOH====NaNO3+H2O+NH3↑
2NH4Cl+Ca(OH)2====CaCl2+2H2O+2NH3↑
用向下排空气法收集,红色石蕊试纸检验是否收集满。
单元测试
一、选择题
1.为迎接北京奥运,北京曾采用机动车按照单双号行驶的方案,该方案既保障了交通秩序,又大大减少了空气污染。
汽车尾气中所含污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有( ).
A.氮气 B.硫化氢
C.二氧化硫
D.氮的氧化物
2.某地发生了食用熟牛肉中毒事件,导致四个死亡、一百多人中毒。
经过对该牛肉的检测,发现其中某盐的含量比国家标准允许的含量高800多倍,则该盐可能是( ).
A.NaNO2
B.NaNO3
C.NaCl
D.BaSO4
3.下列现象或事实可用同一原理解释的是( ).
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色,其原理相同
C.漂白粉和水玻璃长期暴露在空气中变质
D.能使品红溶液褪色的气体不一定是SO2
4.绿色化学实验是在绿色化学思想指导下的实验新方法,以减少污染,防止浪费等。
下列符合绿色化学实验的是( ).
A.用铜与浓硫酸反应制取CuSO4,并用少量品红溶液吸收尾气
B.将CO还原Fe2O3后的尾气直接排入空气中
C.用CCl4完成萃取操作练习时,将溴水改成碘水
D.将Zn和稀硫酸制H2后的废液倒入水槽后再清洗玻璃仪器
5.烧瓶中放入铜片和稀硝酸,用酒精灯加热来制取较纯净的一氧化氮,反应开始后发现烧瓶中充满棕红色气体,这时的操作应是( ).
A.立即接收集容器,用向上排空气法收集
B.待烧瓶中红棕色气体消失后,用向上排空气法收集
C.待烧瓶中红棕色气体消失后,用排水法收集
D.立即用排水法收集
6.下列关于氨气的说法正确的是( ).
A.氨既能用浓硫酸干燥也能用无水CaCl2干燥
B.NH3是电解质,所以氨水能导电
C.沸点:
NH3<PH3<AsH3
D.用水吸收NH3用如图装置可防止倒吸
7.为了证明[(NH4)2Fe(SO4)2·
6H2O(硫酸亚铁铵晶体)]的成分中含有NH4+、Fe2+、SO42ˉ和H2O,下列实验叙述中不正确的是( ).
A.取少量硫酸亚铁铵晶体放入试管中,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水
B.硫酸亚铁铵晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+
C.硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42ˉ
D.取少量硫酸亚铁铵放入试管,加入少量稀NaOH溶液,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中含有NH4+
8.有a、b、c、d、e五种气体,进行下列实验:
(1)a和b混合
气体变红棕色
(2)c和d混合
产生白烟
(3)c和e分别通入少量溴水中
溴水都变成无色透明的液体
(4)b和e分别通入氢硫酸中
都产生淡黄色浑浊
a、b、c、d、e依次可能是( ).
A.O2、NO、HCl、NH3、CO2
B.O2、NO、NH3、HCl、SO3
C.NO、O2、NH3、HCl、SO2
D.HCl、CO2、NH3、H2S、CH4
9.下列对实验现象的预测不正确的是( ).
A.向Na2SiO3溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失
B.向氢氧化铁胶体中滴加盐酸至过量,开始有沉淀出现,后来沉淀又溶解
C.向Ca(ClO)2溶液中通入CO2,溶液变浑浊,再加入品红溶液,红色褪去
D.向Ca(OH)2溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入过量NaOH溶液,溶液又变浑浊
10.根据陈述的知识,类推得出的结论正确的是( ).
A.磷在足量氧气中燃烧生成一种相应氧化物,则碳在足量氧气中燃烧生成一种氧化物
B.稀硝酸能将木炭氧化成二氧化碳,同理稀硫酸也能将木炭氧化成二氧化碳
C.CO2与SiO2化学式相似,则CO2与SiO2的物理性质也相似
D.NaHCO3、(NH4)2CO3固体受热后均能生成气体,则Na2CO3固体受热后也能生成气体
11.奥运会会标是五环旗,假定奥运五环旗中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( ).
选项
蓝
黑
红
黄
绿
A
SiO2
CuSO4溶液
O2
NaOH
溶液
Ag
B
稀H2SO4
CO2
Fe
NaOH溶液
C
Al(OH)3
NH3
D
Mg
KOH溶液
Al
Fe2O3
12.有一瓶可能部分被氧化的Na2SO3溶液,某同学进行如下实验:
取少量此溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。
下述有关此实验的结论正确的是( ).
A.Na2SO3已部分被空气中的氧气氧化
B.加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4
C.加硝酸后的白色沉淀不一定是BaSO4
D.此实验不能确定Na2SO3是否部分被氧化
13.实验室有一瓶久置的白色K2SO3粉末,元素分析表明粉末中K和S元素的质量比为39∶16,下列结论正确的是( ).
A.根据元素分析结果推测该粉末为纯净物
B.将粉末溶于水,加入氯化钡,有白色沉淀生成,证明原粉末是K2SO4
C.将粉末加入盐酸中,产生气泡,证明原粉末是K2SO3
D.将粉末溶于水,加入氯化钡和过量的盐酸,有白色沉淀和气泡生成,证明原粉末是K2SO4和K2SO3的混合物
14.工业上以硫铁矿为原料制硫酸所产生的尾气中含有SO2,为便于监控,实施环境保护,下列适合测定硫酸尾气中SO2含量的试剂是( ).
A.品红溶液
B.氨水、酚酞试液
C.碘水、淀粉溶液
D.以上都可以
15.(2009·
吉林七校)向含有下列离子的溶液中,通入适量的氯气会引起离子浓度减少的是( ).
①HCO ②SO ③OH- ④Fe2+
A.①②
B.③④
C.①②③
D.①②③④
16.某化学教师为“氯气与金属钠反应”设计了如图装置与操作以替代相关的教材上的实验。
实验操作:
先给钠预热,当钠熔成圆球时,撤火、通入氯气,即可见钠着火燃烧,并产生大量白烟。
以下叙述错误的是( ).
A.钠着火燃烧产生苍白色火焰
B.反应生成的大量白烟是氯化钠晶体
C.管中部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
D.管右端棉球外颜色变化可判断氯气是否被碱液完全吸收
17.在氯水中存在多种分子和离子,可通过实验的方法加以确定,下列说法中可能错误的是( ).
A.加入含有NaOH的酚酞试液,红色褪去,说明有H+存在
B.加入有色布条后,有色布条褪色,说明有HClO分子存在
C.氯水呈浅黄色,且有刺激性气味,说明有Cl2分子存在
D.加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在
18.已知BrCl能发生下列反应:
nBrCl+2M===MCln+MBrn(M为+n价的金属元素),BrCl+H2O===HCl+HBrO,以下推论不正确的是( ).
A.BrCl具有和卤素单质相似的化学性质
B.BrCl和M反应时,BrCl只做氧化剂
C.BrCl和NaOH溶液反应生成NaCl、NaBrO两种盐
D.将BrCl跟FeSO4溶液反应,溶液会变成无色
二、非选择题
19.氰(CN)2的化学性质与卤素很相似(X2),称为拟卤素,氰能和氢气反应生成HCN,其水溶液是一种酸。
氰的氧化性比溴弱、比碘强。
(1)HCN分子中含有4个共价键,写出HCN的结构式:
____________。
(2)KCN溶液显碱性,原因是____________(用离子方程式表示)。
(3)下列有关方程式不正确的是____________。
A.(CN)2+2NaOH===NaCN+NaCNO+H2O
B.MnO2+4HCN===Mn(CN)2+(CN)2+2H2O
C.I2+2KCN===2KI+(CN)2
D.向NaBr(aq)和KCN(aq)中加入少量Cl2:
Cl2+2NaBr===2NaCl+Br2
(4)处理CN-的工业废水常用ClO-氧化处理生成CNO-,反应的离子方程式如下:
aCN-+bClO-+2cOH-===dCNO-+eN2+fCO+bCl-+cH2O
上述化学方程式可能的配平化学计量数有多组,回答下列问题。
①方程式中e∶f的值为____________;
A.1
B.1/2
C.2
D.不能确定
②若d=e=1,则b=____________。
20.饮用水质量是关系人类健康的重要问题。
(1)氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为____________,所生成的次氯酸的电子式为____________。
(2)写出工业上制取漂白粉的化学反应方程式:
(3)ClO2被称为“第四代”饮用水杀虫剂,因其高效率,无污染而被广泛使用。
制备ClO2是发达国家普遍重视的课题,我国北京永利科技有限公司已用电解法批量生产ClO2。
其反应原理为:
4ClO+4H+===4ClO2+O2↑+2H2O,试写出两电极反应式,阳极:
____________;
阴极:
(4)相同物质的量的氯气与二氧化氯消毒时转移电子数目之比是____________。
(5)采用氧的一种同素异形体给自来水消毒,既提高了消毒效率、安全无副作用,又因为该物质在自然界中存在,对地球生命体起保护伞作用,该物质和氯气溶于水以及SO2的漂白原理分别是____________;
若将氯气与SO2二者混合,若想使石蕊试液褪色则范围为____________。
21.硫酸具有以下A~F的性质:
A.酸性 B.高沸点难挥发 C.吸水性 D.脱水性 E.强氧化性 F.溶于水放出大量热
(1)浓硫酸与铜共热发生反应的化学方程式为____________。
实验中往往有大量白色固体析出,可见浓硫酸在该实验中表现了哪些性质:
(浓硫酸性质用A、B、C、D、E、F填空,下同)
(2)实验证明铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液。
铜屑在此状态下被溶解的化学方程式为__________________________________。
硫酸在该反应中表现了哪些性质:
__________________。
(3)在过氧化氢跟稀硫酸的混合溶液中加入铜片,常温下就生成蓝色溶液。
写出有关反应的化学方程式:
与
(2)中反应比较反应条件不同的原因是____________。
(4)蔗糖晶体中滴2~3滴水,再滴入适量的浓硫酸。
发现加水处立即变黑,黑色区不断扩大,最后变成一块疏松的焦炭,并伴有刺激性气味气体产生。
写出产生有刺激气味气体的化学方程式:
____________________________。
该实验中浓硫酸表现的性质有____________________。
(5)工业制备CuSO4溶液采用实验
(2)的原理而没有采用实验
(1)和(3)的原理,是因为
(1)和(3)有某些缺点,请你列举
(1)和(3)分别有哪此缺点:
实验
(1)____________________________;
实验(3)____________________________。
22.某课外兴趣小组对双氧水(H2O2水溶液)做了如下实验探究。
(1)将质量相同但聚集状态不同的MnO2分别加入5mL5%的双氧水中,并用带火星的木条试之。
测定结果如下:
①写出H2O2反应的化学方程式:
__________________;
②实验结果说明催化剂作用的大小与__________有关。
(2)取三份含有等量H2O2、但质量分数不同的双氧水,分别向其中加入1gMnO2粉末。
测定结果如下,请简要说明:
①反应完成所需的时间不同的原因:
________________;
②反应后液体温度不同的原因:
____________________;
③收集到气体体积不同的原因:
______________。
(3)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的双氧水,红色褪去。
①已知双氧水显弱酸性,试写出H2O2的电离方程式:
______________________;
②小组讨论红色褪去的原因时,甲同学认为是双氧水显酸性所致;
乙同学认为是双氧水有较强氧化性所致。
请你设计一个简单实验来说明是甲对还是乙对(简要文字说明):
____________________________________
。
参考答案
1.解析:
汽车的尾气中,除了含有碳氢化合物、可吸入颗粒物、一氧化碳外,还含有氮的氧化物,汽车尾气最主要的危害是形成光化学烟雾。
答案:
2.解析:
亚硝酸盐是工业用盐,它在外观上类似食盐,误食会引起中毒,国家标准中,肉制品的亚硝酸盐含量是被限制使用的;
由题意知,该盐为NaNO2,A项正确;
NaNO3、NaCl、BaSO4食用后,不会引起中毒现象,B、C、D项不正确。
3.解析:
浓硫酸浓度降低的原因是由于吸水,而浓盐酸浓度降低的原因是由于氯化氢气体的挥发,所以两者不能用同一原理解释,A项错误;
SO2漂白是利用其与有色物质化合,生成不稳定的无色物质,漂白粉、过氧化钠漂白是利用其强氧化性,破坏有色物质的结构,而活性炭使红墨水褪色,是由于活性炭具有吸附性,将有色物质吸附在活性炭的表面,故漂白原理不同,B项错误;
漂白粉在空气中变质是由于吸收CO2和水生成HClO,然后见光分解,而水玻璃的变质是由于与空气中的CO2反应生成了硅酸的缘故,两者也不能用同一原理解释,C项错误;
能使品红溶
液褪色的物质除SO2外,氯水、过氧化钠等也可使品红溶液褪色,D项正确。
4.解析:
品红溶液可以用来检验SO2气体,但不能用来吸收尾气,A项错误;
CO还原Fe2O3后的尾气中含有少量CO气体,直接排放到空气中造成污染,B项错误;
溴易挥发,而碘不易挥发,C项正确;
锌与稀硫酸制氢气后的废液倒入水槽会污染环境,D项错误。
5.解析:
在制取NO过程中,常常会混有NO2气体,要得到纯净的NO,需除去混有的NO2的气体。
直接用
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 必修 第四 知识 总结 习题 练习 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
