 化学综合测试1Word格式文档下载.docx
化学综合测试1Word格式文档下载.docx
- 文档编号:21122679
- 上传时间:2023-01-27
- 格式:DOCX
- 页数:12
- 大小:100.94KB
化学综合测试1Word格式文档下载.docx
《化学综合测试1Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《化学综合测试1Word格式文档下载.docx(12页珍藏版)》请在冰豆网上搜索。
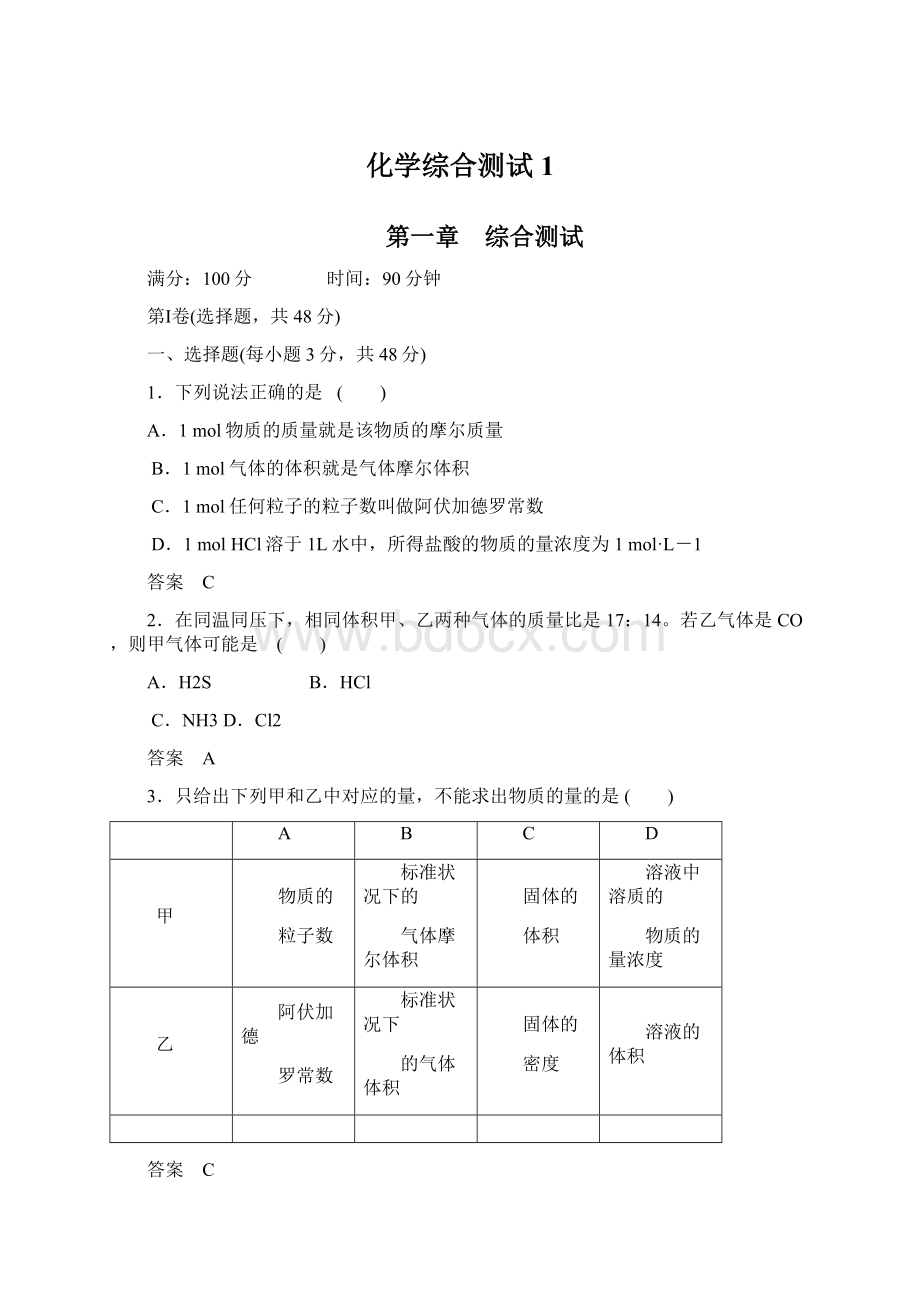
物质的量浓度
乙
阿伏加德
罗常数
标准状况下
的气体体积
密度
溶液的体积
解析 根据n=
、n=
、nB=cBV可知,A、B、D中都能求出物质的量。
4.O2、SO2、SO3三者的质量比为2∶4∶5时,它们的物质的量之比为
( )
A.2∶4∶5B.1∶2∶3
C.1∶1∶1D.2∶2∶3
5.300mLAl2(SO4)3溶液中,含Al3+为1.62g,在该溶液中加入0.1mol/LBa(OH)2溶液300mL,反应后溶液中SO
的物质的量浓度约为( )
A.0.4mol/LB.0.3mol/L
C.0.2mol/LD.0.1mol/L
答案 D
解析 n(Al3+)=1.62g/27g·
mol-1=0.06mol,n(SO
)=0.09mol。
加入Ba(OH)2溶液中含Ba2+0.03mol,剩余SO
0.06mol,此时溶液的体积为600mL,c(SO
)=0.1mol/L。
6.标准状况下,mgA气体与ngB气体分子数相等,下列说法不正确的是
A.标准状况下,同体积的气体A和气体B的质量比为m∶n
B.25℃时,1kg气体A与1kg气体B的分子数之比为n∶m
C.同温同压下,气体A与气体B的密度之比为m∶n
D.标准状况下,等质量的A与B的体积比为m∶n
7.把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;
另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。
则原混合溶液中钾离子的浓度为
A.
mol·
L-1B.
C.
L-1D.
解析 根据Mg2+~2OH-,则混合溶液中n(Mg2+)=
n(NaOH)=0.5amol;
根据SO
~Ba2+,则n(SO
)=n(BaCl2)=bmol;
根据电荷守恒:
2n(Mg2+)+n(K+)=2n(SO
),则n(K+)=(2b-a)mol,则原溶液中c(K+)=
=
mol/L,D项正确。
8.(2012·
河北质量监测)设NA为阿伏加德罗常数的数值,若等质量的H2O和D2O分别与一定质量的金属钾完全反应,转移的电子数均为
NA,则下列各化学量不相等的是( )
A.消耗H2O和D2O的物质的量
B.同温同压下生成气体的体积
C.反应后所得溶液中溶质的质量分数
D.参加反应的钾的质量
解析 由关系式2K~2H2O~H2~2e-和2K~2D2O~D2~2e-可知:
只要完全反应转移的电子数相等,消耗H2O和D2O的物质的量就相等,A项错误;
同温同压下,生成H2和D2的体积相等,B项错误;
参加反应的钾的质量相等,D项错误。
9.(2012·
江西四市联考)若NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.1molCl2参加反应转移电子数一定为2NA
B.将31gNa2O溶解于1L水中,所得溶液中Na+的物质的量浓度为1mol/L
C.22.4LNH3和16gCH4中所含有的电子数都是10NA
D.20g重水(2H
O)含有的电子数为10NA
解析 1molCl2与足量NaOH溶液反应时,转移电子数为NA,A项错;
B项中反应生成1molNaOH,但溶液的体积不是1L,故Na+的物质的量浓度不是1mol/L;
C项没有指明气体的状态,22.4LNH3的物质的量不一定是1mol;
重水的摩尔质量为20g/mol,20g重水即为1mol重水,含有的电子数为10NA。
10.(2012·
合肥一质检)设NA表示阿伏加德罗常数的数值,下列叙述中不正确的是( )
A.18gNH
中所含电子数为10NA
B.5.6g铁粉与硝酸反应失去的电子数一定为0.3NA
C.用惰性电极电解饱和食盐水,若产生2g氢气,则转移的电子数目为2NA
D.28gC3H6与C2H4的混合物完全燃烧可生成CO2分子数为2NA
答案 B
解析 铁与硝酸反应时,可能生成Fe2+,也可能生成Fe3+,所以5.6g铁失去的电子数可能是0.2NA,也可能是0.3NA,故B项错误。
11.(2012·
广东省重点中学联考)标准状况下,一个装满氯气的容器的质量为74.6g,若装满氮气时总质量为66g,则此容器的容积是( )
A.22.4LB.44.8L
C.11.2LD.4.48L
解析 22.4L(标准状况下)Cl2换成22.4L(标准状况下)N2的质量差是(71-28)g=43g,设氯气的体积为xL,则有
Cl2 ~ N2 Δm
22.4L 43g
xL74.6g-66g=8.6g
解得xL=4.48L。
12.把氯气通入浓氨水中,会立即发生下列反应:
3Cl2+8NH3·
H2O===6NH4Cl+N2+8H2O。
在标准状况下,把1.12LCl2、N2的混合气体(90%Cl2和10%N2,均为体积分数)通过浓氨水,实验测得逸出气体体积为0.672L(其中有50%Cl2和50%N2),此反应中被氧化的NH3的质量为( )
A.3.4g B.0.34g
C.1.36gD.4.48g
解析 由反应式可得出每3molCl2(反应气)生成1molN2(生成气)时,气体物质的量减少了2mol,即体积减小44.8L,这一量即为“理论差量”,而这一差量所对应的被氧化的氨气的物质的量为2mol(质量为34g),再从题中所给的数据可以求出“实际差量”为(1.12-0.672)L=0.448L。
即:
3Cl2~2NH3 ~ N2 ΔV
2mol×
17g·
mol-1 44.8L
m(被氧化的NH3)g(1.12-0.672)L
列出比例式:
(2mol×
mol-1)∶44.8L=m(被氧化的NH3)g∶(1.12-0.672)L,则m(被氧化的NH3)g=0.34g。
13.浓度不等的两种硫酸溶液等质量混合后,溶液的质量分数为a%,而等体积混合后,溶液的质量分数为b%;
浓度不等的两种氨水等质量混合时,其溶质的质量分数为a%,而等体积混合后,溶液的质量分数为c%,那么a、b、c数值的关系是( )
A.a>
b>
c B.b>
a>
c
C.c>
aD.c>
b
解析 由混合后溶质质量分数的判定规律知,硫酸溶液密度大于1g·
cm-3,故b>
a;
氨水密度小于1g·
cm-3,且浓度越大,密度越小,则c<
a。
故答案为B。
14.某结晶水合物的化学式为R·
nH2O,其相对分子质量为M。
25℃时,将ag该晶体溶于bg水中恰好可形成VmL饱和溶液。
下列关系中正确的是( )
A.饱和溶液的物质的量浓度为c=
B.饱和溶液中溶质的质量分数为w=
%
C.25℃时R的溶解度为S=
g
D.饱和溶液的密度为ρ=
g·
解析 A项,晶体的物质的量等于无水盐的物质的量。
c(R)=
L-1。
B项,w=
×
100%=
%。
C项,
,S=
g。
D项,ρ=
15.用NA表示阿伏加德罗常数的值。
下列正确的组合是( )
①2.3gNa和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA
②含0.2molH2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
③标准状况下,2.24LCl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA
④25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA
⑤100mL1mol·
L-1AlCl3溶液中含有的阳离子数大于0.1NA
⑥50mL12mol·
L-1浓盐酸与足量二氧化锰加热反应,转移电子数小于0.3NA
⑦13.0g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
A.①②⑥B.①⑤⑥⑦
C.②④⑥⑦D.③⑤⑥
解析 ①中0.1molNa失去电子为0.1mol;
②随着反应不断进行,浓硫酸变成稀硫酸而不能与Cu反应,即生成SO2的物质的量小于0.1mol;
③Cl2只有部分能与水反应,转移电子数小于0.1NA;
④pH=13,溶液中c(OH-)=0.1mol/L,即溶液中含有的OH-数目为0.1NA;
⑤由于Al3+水解,即Al3++3H2OAl(OH)3+3H+,而使溶液中阳离子数大于0.1NA;
⑥随着反应不断进行,盐酸浓度变稀,不再与MnO2反应生成Cl2,即转移电子数小于0.3NA;
Zn无论是与浓硫酸还是与稀硫酸反应,均是1molZn对应1mol气体;
综上本题答案为B。
16.将mg含氧化铁、氧化铜或氧化亚铁的样品投入物质的量浓度为1mol/L的2L盐酸中恰好完全反应,若向等质量的该样品中通入足量的氢气并加热,充分反应后所得金属的质量是( )
A.(m-16)gB.(m+16)g
C.(m-32)gD.16g
解析 把mg含氧化铁、氧化铜和氧化亚铁的样品投入稀盐酸中,发生的反应如下:
Fe2O3+6HCl===2FeCl3+3H2O,CuO+2HCl===CuCl2+H2O,FeO+2HCl===FeCl2+H2O。
向等量的该样品中通入足量的氢气并加热,发生的反应如下:
Fe2O3+3H2△,2Fe+3H2O,CuO+H2△,Cu+H2O,FeO+H2△,Fe+H2O。
比较以上化学方程式可得到关系式:
2HCl~H2O~O,而n(HCl)=1mol·
L-1×
2L=2mol,故失去的氧的质量为16g,所以得到金属的质量为(m-16)g,即A项正确。
第Ⅱ卷(非选择题,共52分)
二、非选择题(本题包括5小题,共52分)
17.(10分)
(1)将40gNaOH溶于水,配成250mL溶液甲,甲的浓度为________mol/L(将正确选项的标号填入空格,下同)。
将50mL甲加水稀释至100mL后,得溶液乙,乙的浓度为________mol/L。
将10mL乙溶液与质量分数为9%、密度为1.11g/cm3的NaOH溶液10mL混合,该混合溶液丙的溶度为________mol/L(忽略溶液体积变化)。
混合溶液丙能与________mL0.5mol/L的盐酸恰好完全中和。
选项
A4
B1
C2
D90
E45
F35
G4.25
H2.25
(2)若12.4gNa2X中含有0.4mol钠离子,Na2X的摩尔质量是________,X的相对原子质量是________。
答案
(1)A C H D
(2)62g/mol 16
解析
(1)n(NaOH)=
=1mol,
c(甲)=
=4mol/L;
c(乙)=
=2mol/L;
c(丙)=
=2.25mol/L,丙中NaOH的物质的量等于HCl的物质的量,n(HCl)=2.25mol/L×
0.02L=0.045mol,
V[HCl(aq)]=
=0.09L(即90mL)。
(2)n(Na2X)=
n(Na+)=
0.4mol=0.2mol,M(Na2X)=
=62g/mol,M(X)=62g/mol-2×
23g/mol=16g/mol。
因此,x的相对原子质量为16。
18.(12分)(2010·
临沂调研)下图是医院为病人输液时用的一瓶质量分数为5%的葡葡糖(C6H12O6)注射液标签。
请认真观察标签所列内容并填空:
·
葡萄糖注射液
规格:
250mL内含12.5g
生产批号:
0503203
有效期:
至2010年12月
(1)该溶液中含水________g;
(2)该溶液的密度约为________g/mL;
(3)该溶液的物质的量浓度为________;
(4)若用25%的葡萄糖注射液来配置该注射液250mL,需25%的葡萄糖注射液________g。
答案
(1)237.5
(2)1 (3)0.28mol/L (4)50
19.(12分)实验室需要0.1mol·
L-1NaOH溶液450mL和0.5mol·
L-1硫酸溶液500mL。
根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)
(2)下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的液体
E.量取一定体积的液体
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为________g。
在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1mol·
L-1(填“大于”“等于”或“小于”,下同)。
若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1mol·
(4)根据计算得知,所需质量分数为98%、密度为1.84g·
cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。
如果实验室有15mL、20mL、50mL量筒,应选用________mL量筒最好。
配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是_________________________________。
答案
(1)A、C 烧杯、玻璃棒
(2)B、C、E、F
(3)2.0 小于 小于
(4)13.6 15 将浓硫酸沿器壁缓缓倒入水中,并用玻璃棒不断搅拌
解析
(1)五种仪器分别为烧瓶、量筒、分液漏斗、胶头滴管、容量瓶,配制上述溶液肯定不需要烧瓶和分液漏斗,还需要烧杯、玻璃棒。
(2)容量瓶不能用于贮存、加热溶液,它只有一个刻度线,也不能测量容量瓶规格以下的任意体积的液体。
(3)因无480mL的容量瓶,配制NaOH溶液常用500mL的容量瓶,m(NaOH)=c·
V·
M=0.1mol/L×
0.5L×
40g/mol=2.0g,定容仰视刻度线,造成加水较多,浓度偏低,洒落溶液会造成溶液浓度偏低。
(4)由稀释前后物质的量相等,V(浓)=
L=
L=13.6mL,选用15mL量筒最好,误差小。
稀释时将浓硫酸沿器壁缓缓倒入水中,并用玻璃棒不断搅拌。
20.(6分)已知M(Mg)=24g·
mol-1,Vm=22.4L·
mol-1,今有0.48g金属镁与10mL盐酸反应,计算生成的H2在标准状况下的体积V(H2)。
(1)缺少的一个数据a是________(要求指出该数据的名称、符号和单位)。
(2)写出计算式:
①____________;
②____________。
答案
(1)盐酸的物质的量浓度amol/L
(2)①当c(HCl)≥4mol/L时,V(H2)=0.448L
②当c(HCl)<
4mol/L时,V(H2)=0.112aL
解析 根据化学方程式:
Mg + 2HCl===MgCl2+H2↑
1 2
0.010L×
amol/L
根据关系式:
1∶2=0.02∶0.01a,可确定a取何值时,Mg适量、HCl过量和HCl适量、Mg过量。
21.(12分)(2012·
保定调研)下图所示的实验装置可用来测定含两种元素的某种气体X的分子式。
在注射器A中装有240mL气体X并慢慢通过不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到以下实验结果:
实验前B管重20.32g,实验后B管重20.00g,B管中的黑色粉末变成红色粉末。
在C管中收集到的无色液体是水;
在注射器D中收集到的气体是氮气。
试回答下列问题:
(1)X气体是由________和________元素组成的。
(2)若240mLX气体完全反应后,收集到的氮气质量是0.28g。
根据实验时温度和压强计算1molX气体的体积是24000mL,则X的摩尔质量是________g·
mol-1。
(3)通过计算,确定X的分子式为________。
(4)写出B中发生反应的化学方程式(X在该条件下不发生分解反应)
____________________________。
答案
(1)氮 氢
(2)32 (3)N2H4 (4)N2H4+2CuO
N2+2H2O+2Cu
解析 在C管中收集到水、其中氧来源于CuO,则X中一定含有氢元素。
在D中收集到氮气,说明X中一定含有氮元素,即X中含有氮、氢两种元素。
B管中CuO含O:
20.32g-20.00g=0.32g。
n(O)=0.02mol,n(N2)=0.01mol,240mLX气体物质的量为0.01mol。
因此n(X)∶n(N)∶n(H)=0.01mol∶(0.01mol×
2)∶(0.02mol×
2)=1∶2∶4,所以化学式为N2H4,摩尔质量为32g·
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学 综合测试
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
