 环境监测期末考点总结Word格式文档下载.docx
环境监测期末考点总结Word格式文档下载.docx
- 文档编号:22515706
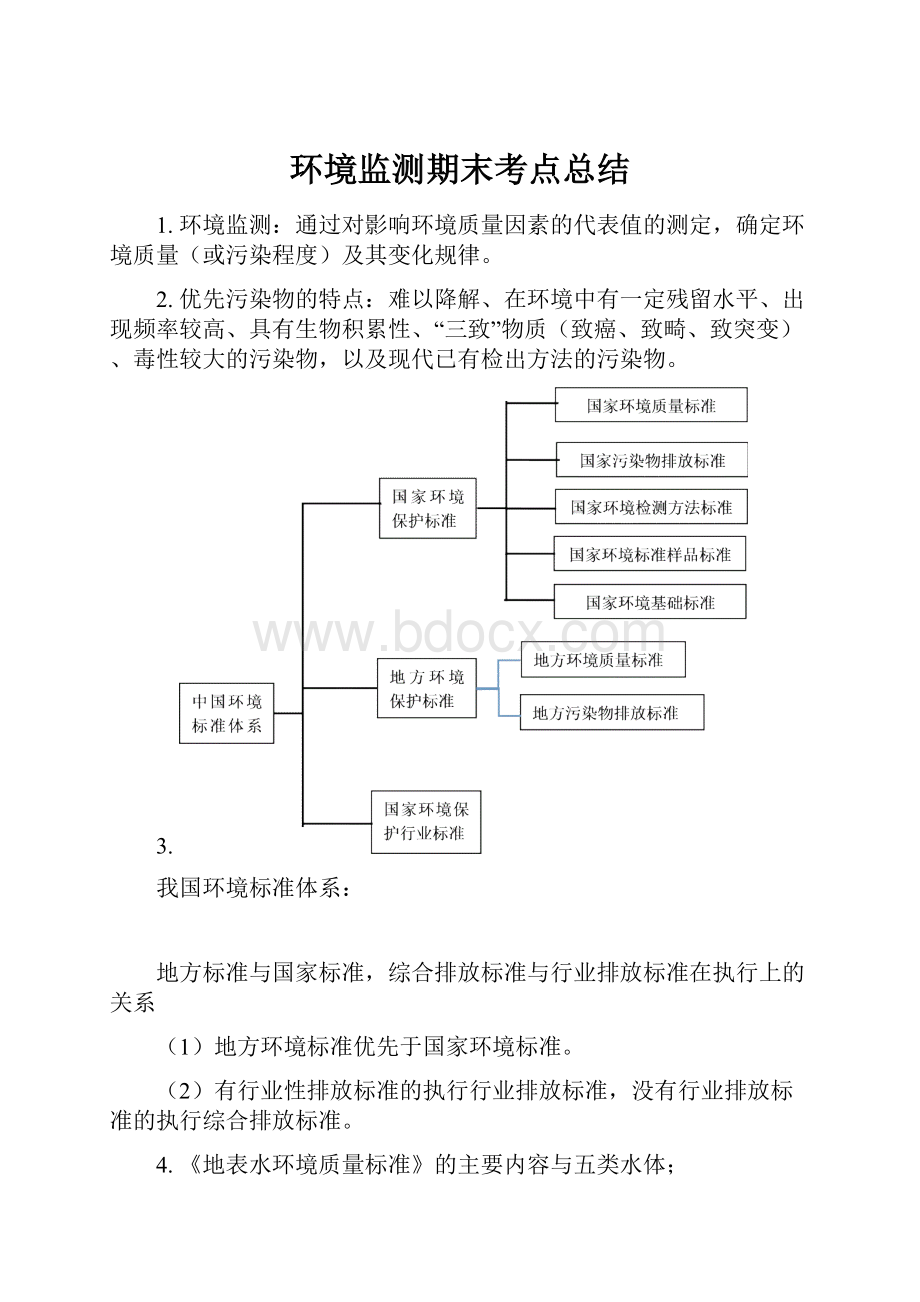
- 上传时间:2023-02-04
- 格式:DOCX
- 页数:27
- 大小:115.59KB
环境监测期末考点总结Word格式文档下载.docx
《环境监测期末考点总结Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《环境监测期末考点总结Word格式文档下载.docx(27页珍藏版)》请在冰豆网上搜索。
(1)有大量废水排入河流的主要居民区,工业区的上游和下游
;
(2)湖泊、水库、河口的主要入口和出口
(3)饮用水源区、水资源集中的水域,主要风景游览区;
(4)较大支流汇合进口上游;
(5)国际河流出入国境线的出入口处
Θ监测断面(采样断面)的类型:
a.背景断面:
设在未受人类活动影响的河段;
b.对照断面:
设在河流进入城市或工业区以前的地方
c.控制断面:
设在污染源排放口下游500-1000m处的点(因500m横断面上1/2宽度处重金属浓度出现峰值);
d.消减断面:
设在离最后一个排污口1500m以外的地方;
采样点位置的确定(根据河宽和回流决定)
水面宽≤50m,设一条中泓垂线
水面宽50~100m,设在两岸有明显水流处设两条垂线
水面宽>100m,设左、中、右三条垂线
水面宽>1500m,设至少五条等距离垂线
【采样点】
在垂线上,水深≤5m时
水面下(0.3~0.5m)设一点
水深<50m
一条垂线
水深5~10m
水面下(0.3~0.5m)底上0.5m处设点
水深50~100m
两条垂线
在明显水流处
水深>100m
三条垂线
水深>10
m
水面下0.5m
底上0.5m处
1/2水深处设点
7.水污染源监测的采样点位置如何确定
(1)工业废水
①在车间或车间处理设施的废水排放口布设采样点,监测第一类污染物;
在工厂废水总排放口布设采样点,监测第二类污染物;
②已有废水设施的工厂,在处理设施的总排放口布设采样点。
如需要了解废水处理效果和为调控处理工艺参数提供依据,应在处理设施进水口和部分单元处理设施进、出水口布设采样点。
(2)生活污水
对城市管网污水,采样点设在污水排放干管的不同位置和污水进入受纳水体的排放口。
对城市污水处理厂,在污水进口和处理后的总排放口及各单元处理设施进出口布设采样点。
8.水样的类型
(1)瞬时水样
(2)混合水样(同一采样点不同时间)(3)综合水样(不同点采样)
9.水样的保存方法
(1)冷藏或冷冻法:
减缓进行化学和生物化学反应的速度,抑制细菌增长。
(2)化学法:
测NH3-N、COD加入HgCl2,抑制生物氧化还原
①加入生物抑制剂
测酚:
用H3PO4调PH,加入CaSO4抑制苯酚分解
②调节PH值:
测金属离子,用HNO3酸化1~2小时,防止金属离子水解沉淀
汞测:
加入K2Cr2O7和HNO3,保持高价态
③加入氧化剂或还原剂
测硫化物:
加入坏血酸,防止被氧化(还原)
注:
加入的保存剂不能干扰以后的测定
参照标准《水质采样样品的保存和管理技术规定》(HJ493-2009)
10.水样预处理的原因及预处理方法消解富集和分离
环境水样所含组分复杂,并且多数污染物组分含量低,存在形态各异,所以在分析测定之前,往往需要进行预处理,以得到欲测组分适合适合测定方法要求的形态、浓度和消除共存组分干扰的试样体系。
(一)消化法(消解法、湿灰法)
一般用两种或两种以上酸进行消化。
把样品与一种或两种以上强酸混合煮沸,使有机物变为CO2、H2O
H2SO4+CSO2+CO2+H2O
消化体系中常加入催化剂加速消化过程。
1.HNO3消解法:
较清洁水样可用HNO3消解。
2.HNO3-H2SO4消化体系:
都有强氧化力,HNO3沸点低,H2SO4沸点高,二者结合可提高消解效果。
HNO3:
H2SO4=5:
2。
先加HNO3加热一会儿,在加H2SO4至冒白烟,冷却至溶液变清亮,如有渣子,应将渣子过滤再消化。
3.HNO3-HClO4(高氯酸)消化体系
两酸强氧化性,H2ClO4易与羟基化合物结合,形成高氯酸酯(爆炸),所以先加硝酸,当有机物基本上被破坏掉后在加H2ClO4。
4.HCl-HNO3体系 王水(HCl:
HNO3=3:
1) 镪水(浓HCl+ZnCl2)
为完全些,最后加入H2ClO4使消化结果更好。
5.H2SO4-H3PO4体系
两种酸沸点都高,其中H3PO4对无机元素(Fe3+)络合力强,可消除Fe3+等的干扰。
6.H2SO4-KMnO4体系
用在处理含汞的水样。
7.多元消解体系(含三元或三元以上组成体系)
如:
测土壤或废水中总铬,可用H2SO4-H3PO4-KMnO4
测生物样品中Hg用H2SO4-HNO3-KMnO4体系。
8.碱分解法
因酸解造成挥发组分损失,可用NaOH+H2O2,NH3·
HO2+H2O2
(二)干灰化法(灰化法,高温分解法)
水样白瓷或石英蒸发皿水浴上蒸干移入450~550℃(P197)马福炉中进行高温灰化(有些挥发性组分易损失)冷却加HNO3(或HCl)溶解样品,过滤(定容)测定。
(三)蒸馏消化法
废水、土壤、生物样品中易挥发成分的测定采用这种消化法。
如CN-、F2-、S2-、凯氏氮(游离氮+有机N)消化又可分离。
例如测F-,将样品放入蒸馏瓶中,加H2SO4和H3PO4,加热蒸馏(120~180℃)产生HF用NaOH吸收。
(四)用有机溶剂分解法
二.无机物样品提取方法:
不是含无机物(P280)无机物提取
酸溶法:
HCl、HNO3、H2SO4不加温
(一)溶解法
碱溶法:
重金属
(二)高温熔融法:
样品中加碱性(Na2CO3、K2CO3、Na2O2、NaOH、KOH)或酸性(K2S2O7焦硫酸钾)溶剂。
在高温(300~1000℃)下,使试样中的成分发生复分解反应,生成易溶解产物。
三.富集与分离
含义:
(1)富集—对预测成分进行浓缩。
浓缩达到分析方法要求的监测线以上
(2)分离—将样品中预测成分与其他干扰物质分开。
往往是伴生进行。
方法:
(一)挥发和蒸发浓缩
a.挥发:
利用不同物质的挥发度不同进行分离
测水样中的Hg吸收后比色
Hg2+SnCl2Hg用吹气法带出来测定
气体直接用冷原子吸收法测
b.蒸发浓缩:
在电直板上或水浴中加热蒸发浓度水样。
(二)蒸馏法:
利用不同物质的沸点不一样
例如:
水样中“挥发酚”蒸馏出酚,在测定
CN-
HCNNaOH吸收测定
S2-
H2S
ZnS+I2S+ZnI(I-)侧H2S先用Zn(AC)2吸收,加入过量I2,再用Na2S2O3标液滴定过量I2,淀粉(蓝色)无
(三)溶剂萃取法(液—液萃取,水相—有机相)
①原理
分配系数K=
分配比D=
萃取率E%=
E%100
E%=
当V水=V有机时
0D
D=∞E=100%一次萃取完全
D=99%E=99%需几次萃取
D=90%E=90%需连续萃取
D=50%E=50%很难萃取完全
②类型
a.有机物萃取分离—选择适当的溶剂,直接进行萃取。
如:
水中酚蒸馏出后,如浓度太低,需用CHCl3萃取后再测定水中的有机氯农药、油。
用石油醚萃取后测定。
b.无机物的萃取分离—首先必须将其转化为不带电荷的易溶于有机溶剂的物质。
一般用加入一种适当试剂(萃取剂)的方法,这样的一种萃取
体系:
水相+萃取剂+有机溶剂
1.生成螯合物萃取体系—广泛应用
NaDDC(双硫腙)—三氯甲烷—H2O(Hg2+、cd2+、Zn2+、Pb2+)
铜铁试剂—MLBK—H2O(Cu、Fe、Mn、Ni)
2.离子缔合物萃取体系—加入适当萃取剂,使被测离子生成疏水不带电的离子缔合物,用有机溶剂萃取。
Fe3++O-邻菲罗啉
3.生成三元络合物体系
Cu2++吡啶+水相酸
[Cu(Py)2Sa]
(四)离子交换法
①原理—利用离子交换剂中可交换基团与被测离子之间发生的交换反应来进行分离。
无机离子交换剂
②离子交换剂阳离子:
R-SO3H
离子交换树脂—应用广泛
阴离子:
R-N(CH3)3+OH-
交换能量—每一克干树脂能交换的离子的毫克当量数
③性能交换能力—被测离子与树脂之间的亲和力大小
(决定于被交换的那种离子大小和电荷数)
④分离操作程序
a.树脂处理和装柱,分离阳离子,用Hcl洗除杂志
b.交换和洗脂
c.树脂再生
(五)沉淀分离法(共沉淀法)
①用无机沉淀剂和有机沉淀剂分离
用NH3水将Fe3+、Al3+等与Co2+、Ni2+、Zn2+等分离。
S2-H2S吸收(加Zn(Ac)2ZnS)
②共沉淀分离法—水中Hg2+﹤0.02μg/l时加入Cu2+和S2-生成CuS沉淀可将Hg2+沉淀下来。
测Cr6+Zn(OH)2沉淀
a.利用吸附作用共沉淀
b.利用生成混晶共沉淀:
若具有相似的晶格,可形成混晶共同析出。
(六)吸附法(分离)
多孔吸附剂—活性碳、分子筛、网状树脂、氧化铝
固体阻留法采集大气样品
a.固体阻留法
b.用5
分子筛在-78℃富集大气中的CO
c.富集水中的微量
d.AD-20型树脂吸附富集海水中PPb级有机氯农药
XAD-2树脂富集饮水中36种有机化合物
(七)其他分离法
溶液吸收法、电泳分离法、低温冷凝法、电解分离法、层析分离法(柱层析、纸层析、薄层层析)
11.水质的外观指标是什么,其标准测定方法是什么
色度(铂钴标准比色法、稀释倍数法)
①铂钴比色法:
用氯铝酸钾与氯化钴配成标准色列,目视比色。
(水样要澄清,用离心法或孔径0.45μm滤膜过滤,不能用滤纸。
适于用天然水和饮用水。
)
②稀释倍数法:
适用于工业污染水和污染地下水。
(取一定量水样,用蒸馏水稀释到刚好看不见颜色,根据稀释倍数表示该水样的色度。
浊度(目视比浊法、分光光度法、浊度仪法)
①分光光度法
a.原理:
将一定量的硫酸肼(有机化合物一类,用来制药,也做火箭燃料)与6次甲基四胺聚合,生成白色高分子聚合物。
以此作为浊度标准溶液,在一定条件下与水样浊度比较。
—水样经稀释后的体积(ml)
—原水样体积(ml)
—经稀释的水样浊度。
②目视比浊法
原理:
将水样与用硅藻土(白陶土)配制的标准浊度溶液进行比较,以确定水样的浊度。
1度=1mg粒度的硅藻土/1L蒸馏水(P62)
③浊度计(仪器)法:
根据散射光强度(1度NTV—散射浊度单位)
透明度(铅字法、塞式盘法)
悬浮物(过滤后蒸干称量)
12.分光光度法(原理):
在光谱分析中,不同溶液对不同波长的单色光吸收能力不同,依据物质对光的选择性吸收的特点,根据朗伯-比尔定律,通过测定其对特征波长的吸光度,并与标准溶液的吸光度相比较实现定量测定的方法。
(主要组成部分)光源(常用氢灯或氘灯(紫外光区)、钨丝灯(可见光区))
分光系统(由棱镜(或光栅)与透镜、狭缝等组成)
比色皿(由石英材料(紫外光区)或光学玻璃(可见光区)制成)
检测器及放大装置(常用光电管或光电倍增管)
指示、记录系统(有微安表、数字电压表、记录仪、示波器等)
13.原子吸收光谱法定性与定量分析的原理
原子吸收分光光度计(主要结构):
光源原子化系统分光系统检测系统
(定量分析的方法及适用情况)
①标准曲线法(配制的标准溶液浓度应在吸光度与浓度成线性关系的范围内,整个过程操作条件保持不变)
②标准加入法(若样品基体组成复杂,且对滴定有明显干扰,则在标准曲线成线性关系的范围内,使用标准加入法)
14.铜、锌、铅、镉、铬等金属元素常用的分析测定方法有哪几种
(1)原子吸收光谱法
①火焰原子吸收光谱法;
②石墨炉原子吸收光谱法;
(二)双硫腙分光光度法
(三)阳极溶出伏安法
铅:
原子吸收分光光度法和双硫腙分光光度法,也可以用阳极溶出伏安法、示波极谱法和电感耦合等离子体发射光谱法(ICP-AES)。
铜:
有原子吸收分光光度法、二乙氨基二硫代甲酸钠萃取分光光度法和新亚铜灵萃取分光光度法,还可以用阳极溶出伏安法、示波极谱法、ICP-AES法。
锌:
原子吸收分光光度法测定锌,灵敏度较高,干扰少,适用于各种水体。
此外,还可选用双硫腙分光光度法、阳极溶出伏安法或示波极谱法、ICP-AES法。
对于锌含量较高的废(污)水,为了避免高倍稀释引入的误差,可选用双硫腙分光光度法;
对于高盐度的废水和海水中微量锌的测定,可选用阳极溶出伏安法或示波极谱法。
铬:
二苯碳酰二肼分光光度法、原子吸收分光光度法、等离子体发射光谱法和硫酸亚铁铵滴定法。
镉:
原子吸收分光光度法、双硫腙分光光度法、阳极溶出伏安法和电感耦合等离子体发射光谱法(ICP-AES法)
15.酸度:
指水中所含能与强碱发生中和作用的物质的总量,包括无机酸、有机酸、强酸弱碱盐等。
碱度:
指水中所含能与强酸发生中和作用的物质的总量,包括强碱、弱碱、强碱弱酸盐等。
ΘpH——水中酸碱性的强弱;
酸度或碱度——水中所含酸性或碱性物质的含量。
16.溶解氧的概念,其标准测定方法的名称与原理
溶解氧(DO):
溶解于水中的分子态氧。
(1)碘量法(清洁水)
水样中加入硫酸锰和碱性碘化钾,水中的溶解氧将
并生成氢氧化物沉淀。
加酸沉淀溶解
而释放出与DO相当游离
(2)修正碘量法(污、废水)
1.叠氮化钠修正法
水样中加入叠氮化钠(NaN3)将亚硝酸盐(NO2—)水解(干扰碘量法)再用碘量法测定。
2.高锰酸钾修正法
适用于亚铁盐含量高的水样,酸性KMnO4将亚铁盐、亚硝酸盐及有机物氧化,消除干扰。
过量KMnO4用草酸钠除去,并加氯化钾掩蔽高价铁离子,其他同碘量法。
(三)氧电极法
17.水中含氮化合物的存在形态;
含氮化合物的监测指标及其标准分析方法的名称与原理
(1)氨氮(NH3—N)
指以游离氮(NH3)和离子氮(NH4+)形式存在的氮。
NH3—N来源于生活污水中含氮有机物受了微生物作用的分解产物。
1.钠式试剂分光光度法
纳氏试剂(碘化汞和碘化钾的强碱溶液)与氨反应生成黄棕色胶态化合物,在410-425nm范围比色定量。
2.水杨酸-次氯酸盐分光光度法
在亚硝基铁氰化钠存在下,氨与水杨酸和次氯酸反应生成蓝色化合物,在697nm处比色定量。
3.气相分子吸收光谱法
4.离子选择电极法
氨气敏电极是一种复合电极。
(以阳玻璃电极为指示电极,银—氯化银电极为参比电极)置于NH4Cl液中,PH电极敏感膜贴聚四氟乙烯薄膜,PH调至11时,生成NH3通过半透膜NH4+使H+变化PH玻璃电极测定。
5.滴定法(氨氮较高时)
水样加入MgCl2呈微碱性
用硼酸吸收。
用酸滴定。
(二)亚硝酸盐氮(
1.N-(1-萘基)乙二胺分光光度法2.离子色谱法3.气相分子吸收光谱法
(三)硝酸盐氮(NO-2—N)
1.酚二磺酸分光光度法2.紫外分光光度法3.气相分子吸收光谱法
(四)凯式氮气相分子吸收光谱法
(五)总氮(各种形态的氮加和的方法求得)
18.水中含磷化合物的存在形态,其监测指标及标准分析方法的名称
(存在形式)各种磷酸盐、有机磷化物
1.钼酸铵分光光度法
2.钼锑抗分光光度法
3.孔雀绿-磷钼杂多酸分光光度法
19.水质有机污染物的保证指标
(综合指标)化学需氧量COD、生化需氧量BOD、总有机氮TOC……
(类别指标)挥发酚、石油类、硝基苯类……
20.COD的概念及其标准分析方法与原理
化学需氧量(COD):
指在一定条件下,氧化1L水样中还原性物质所消耗的氧化剂的量,以氧的质量浓度(以mg/L为单位)表示。
Θ重铬酸钾法
在强酸性溶液中,用K2Cr2O7氧化水样中的还原性物质,过量的重铬酸钾以试铁灵作指示剂,用硫酸亚铁胺标准溶液回滴,根据其用量计算水样中还原物质消耗的量。
21.高锰酸盐指数的概念及其测定方法的名称与原理
高锰酸盐指数(IMn):
以高锰酸钾为氧化剂测得的化学需氧量,以氧的质量浓度(以mg/L为单位)表示。
[高锰酸钾法测定比较快速,但是不能代表水中有机物质的全部含量,一般来说,适用于测定天然水或含容易被氧化的有机物的一般废水]
1.酸性高锰酸钾法(适用于Cl-含量不超过300mg/L的水样)
取水样100ml(原样或稀释)于锥形瓶中
(1+3)H2SO45ml
混匀
0.01mol/L高锰酸钾标液(1/5KMnO4)10.0ml
沸水浴30min
0.010mol/L草酸钠标液10.00ml
褪色
0.01mol/LKMnO4标液回滴V1
终点微红色
V1:
滴水样消耗KMnO4标液量(ml)
K:
校正系数(每mlKMnO4标液相当于草酸钠标液的ml数)
M:
草酸钠标液浓度(mol/L)
8:
1/2O摩尔质量
2.碱性高锰酸钾法
(过程与上述基本一致,只是在加热反应之前将溶液用NaOH溶液调至碱性,在加热反应之后加入H2SO4酸化,再按上法测定。
22.BOD的概念及其标准分析方法的名称与原理
生化需氧量(BOD):
指在有溶解氧条件下,好氧微生物在分解水中有机物的生物氧化过程中所消耗的溶解氧量。
Θ稀释与接种法(五日培养法,BOD5法)
水样稀释后,在20±
1℃条件下培养5天,求出培养前后水样中DO含量,二者的差值为BOD5,若BOD5<7mg/L,则不需稀释(如河水)
若①工业废水中不含或少含微生物,应接种;
②若水中有难降解有机物或剧毒物质时,应将驯化后的微生物接种入水中;
23.COD、BOD和高锰酸盐指数(IMn)之间的关系
生化需氧量(BOD)、化学需氧量(COD)和高锰酸盐指数(IMn)都是定量地反映水中有机物质数量的重要水质指标。
其原理都是测定氧化有机物质所消耗的溶解氧,后两者是化学物质作用,前者则是微生物的作用。
这三者之间有一定的比例关系。
一般说,COD>
BOD>
IMn。
生活污水的BOD5一般约为其IMn的2~4倍。
对于不易为微生物作用的物质,其COD可能比BOD大得多。
24.气相色谱分析方法(层析法):
使用气相色谱仪来实现对多组分混合物分离和分析的方法。
色谱仪的主要组成:
载气系统进样系统分离系统(色谱柱)
检测系统数据处理系统
气相色谱常用的检测器种类与适用条件:
热导检测器(均适用)火焰离子化检测器(均适用)
电子捕获检测器(分析痕量电负性(亲电子)有机化合物)
火焰光度检测器(分析含硫或磷的化合物)
色谱常用的定量分析方法:
标准曲线法(外标法)、内标法、归一法
气相色谱与液相色谱的异同。
基本理论及定性、定量方法在两种方法中均基本适用。
气相色谱的流动相是惰性气体,只起到运载作用,组分分离取决于各组分与固定相间的作用力;
液相色谱的流动相是液体,与组分之间有一定的亲和力,可通过改变流动相的各种条件来提高分析的选择性。
(应用条件)高效液相色谱适用于分离沸点高、极性强、热稳定性差、相对分子大和离子型的化合物。
气相色谱适用于分析气体试样,也可分析易挥发或可转化为易挥发的液体和固体。
25.空气中污染物的存在形态
①分子状态污染物②粒子状态污染物
26.空气中污染物浓度的表达方式
(1)质量浓度(适用任何气体)
指单位体积空气中所含污染物的质量数,常用mg/m3或ug/m3,表示。
(2)体积分数(适用气态或蒸气态物质)
指单位体积空气中含污染气体或蒸气的体积数,常用ml/m3和uL/m3表示
27.环境空气质量监测点位布设方法及常用的经验布点法
监测区域内的采样站(点)总数确定后,可采用经验法、统计法、模拟法等进行站(点)布设。
1.功能区布点法(按功能区划分布点法多用于区域性常规监测)
2.网格布点法(对于有多个污染源,且污染源分布较均匀的地区)
3.同心圆布点法(用于多个污染源构成污染群,且大污染源较集中的地区)
4.扇形布点法(扇形布点法适用于孤立的高架点源,且主导风向明显的地区)
28.空气样品的采集方法;
二氧化硫等气态污染物常用的采样方法;
颗粒物常用的采样方法
1、直接采样法
注射器采样塑料袋采样采气管采样真空瓶采样
2、富集(浓缩)采样法
(1)溶液采集法(采集气态、蒸气态及某些气溶胶态污染物)
(2)滤料阻留法(采集颗粒物)
29.空气样品的采样仪器及专用采样器
(采样仪器)收集器流量计采样动力
(专用采样器)空气采样器颗粒物采样器个体采样器
30.SO2的标准分析方法名称及原理
(1)分光光度法
1.甲醛吸收-副玫瑰苯胺分光光度法
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 环境监测 期末 考点 总结
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《Java程序设计》考试大纲及样题试行.docx
《Java程序设计》考试大纲及样题试行.docx
