 高中化学化学反应速率和化学反应限度专题训练新人教版必修1.docx
高中化学化学反应速率和化学反应限度专题训练新人教版必修1.docx
- 文档编号:23465808
- 上传时间:2023-05-17
- 格式:DOCX
- 页数:39
- 大小:482.30KB
高中化学化学反应速率和化学反应限度专题训练新人教版必修1.docx
《高中化学化学反应速率和化学反应限度专题训练新人教版必修1.docx》由会员分享,可在线阅读,更多相关《高中化学化学反应速率和化学反应限度专题训练新人教版必修1.docx(39页珍藏版)》请在冰豆网上搜索。
高中化学化学反应速率和化学反应限度专题训练新人教版必修1
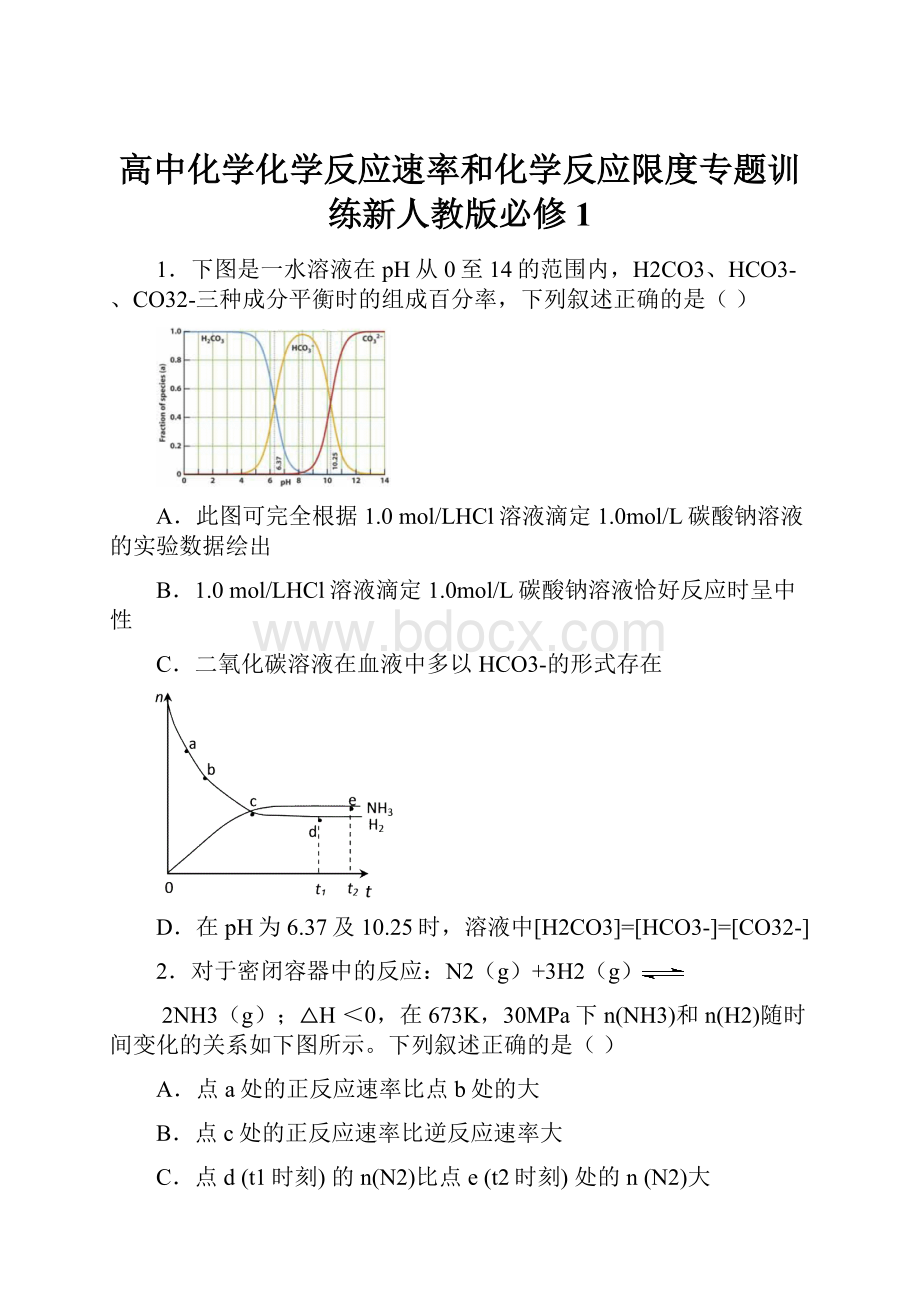
1.下图是一水溶液在pH从0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率,下列叙述正确的是()
A.此图可完全根据1.0mol/LHCl溶液滴定1.0mol/L碳酸钠溶液的实验数据绘出
B.1.0mol/LHCl溶液滴定1.0mol/L碳酸钠溶液恰好反应时呈中性
C.二氧化碳溶液在血液中多以HCO3-的形式存在
D.在pH为6.37及10.25时,溶液中[H2CO3]=[HCO3-]=[CO32-]
2.对于密闭容器中的反应:
N2(g)+3H2(g)
2NH3(g);△H<0,在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
下列叙述正确的是()
A.点a处的正反应速率比点b处的大
B.点c处的正反应速率比逆反应速率大
C.点d(t1时刻)的n(N2)比点e(t2时刻)处的n(N2)大
D.其他条件不变,773K下反应至t1时刻,此时画出的
两根平行线间的距离将要变大。
3.对于反应A(s)+2B(g)
3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列
结论正确的是()
A.Y表示温度,X表示压强,且Y3>Y2>Y1
B.Y表示压强,X表示温度,且Y3>Y2>Y1
C.X表示压强,Y表示温度,且Y1>Y2>Y3
D.X表示温度,Y表示压强,且Y1>Y2>Y3
4、如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应X(g)+Y(g)
2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法错误的是()
A.反应开始时,B容器中化学反应速率快
B.A容器中X的转化率为40%,且比B容器中X的转化率小
C.打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计)
D.打开K达新平衡后,升高B容器温度,A容器体积一定增大
8.将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)2C(g),若经2s后测得C的浓度为0.6mol·L-1,下列几种说法:
①用物质A表示的反应的平均速率为0.3mol·L-1·s-1 ②用物质B表示的反应的平均速率为0.6mol·L-1·s-1 ③2s时物质A的转化率为70%④2s时物质B的浓度为0.7mol·L-1,其中正确的()
A.①③B.①④C.②③D.③④
5.右图是恒温下某化学反应的反应速率随时间变化示意图。
下列说法不符合该示意图的是()
A.反应达到平衡时,正反应和逆反应速率相等
B.该反应达到平衡I以后,增大反应物的浓度,平衡发生移动,达到平衡态II
C.反应达到平衡I以后,减小反应物浓度,平衡发生移动,达到平衡态II
D.同一种反应物在平衡态Ⅰ和平衡态II时浓度不相等。
6.已知反应N2(g)+3H2(g)
2NH3(g);△H<0,向某体积恒定的密闭容器中按体积比1∶3充入N2和H2,在一定条件下发生反应,下图是某物理量Y随时间(t)变化的示意图,Y不可以是()
A.密闭容器的压强 B.混合气体的密度
C.N2的转化率 D.混合气体的平均摩尔质量
7.在1L的密闭容器中,充入1mo1CO和1mo1H2O(g),于850℃时进行化学反应:
CO(g)+H2O(g)
CO2(g)+H2(g)△H<0,达平衡时,有50%的CO转化为CO2。
在相同温度下,将1mo1CO和4mo1H2O(g)充入同样的容器中,记录0~8分钟内测得容器内各物质的物质的量如下表。
t分钟时为改变条件后达平衡时所测得的数据。
下列说法正确的是()
时间/min
n(CO)/mo1
n(H2O)/mo1
n(CO2)/mo1
n(H2)/mo1
0
1
4
0
0
4
0.25
3.25
0.75
0.75
6
n1
n2
n3
n4
8
n1
n2
n3
n4
t
0.15
3.15
0.85
0.85
A.前4min,用CO表示的化学反应速率为v(CO)=0.25mol/(L·min)B.反应在第4min时处于化学平衡状态
C.8分钟时,混合气体中CO2的体积分数为16%D.t分钟时,反应所处的温度高于850℃
9.在一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:
3A(g)+B(g)
xC(g)+2D(g)。
2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol·L-1。
下列判断错误的是( )
A.x=1B.2min内A的反应速率为0.3mol·(L·min)-1
C.B的转化率为40%D.若混合气体的密度不变则表明该反应达到平衡状态
10.已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是
A.该反应在T1、T3温度时达到过化学平衡
B.该反应在T2温度时达到化学平衡
C.升高温度,平衡会向正反应方向移动
D.该反应的正反应是放热反应过
11.对于平衡体系mA(g)+nB(g)
pC(g)+qD(g);△H<0.下列结论中不正确的是()
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n>p+q
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:
n
C.若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
D.若m+n=p+q,则往含有amol气体的平衡体系中再加入amol的B,达到新平衡时,气体的总物质的量等于2a
12.在容积固定的密闭容器中存在如下反应:
N2(g)+3H2(g)
2NH3(g);△H<0。
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图
下列判断正确的是()
A.图Ⅲ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较低
B.图Ⅱ研究的是温度对反应的影响;且甲的温度较高C.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
D.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
14.某温度下,将2molA和3molB充入一密闭容器中,发生反应:
aA(g)+B(g)
C(g)+D(g),5min后达到平衡。
该温度下其平衡常数K=1,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则()
A.a=1B.a=2C.B的转化率为40%D.B的转化率为60%
15.下列事实中,不能用勒夏特列原理加以解释的是( )。
A.夏天,打开啤酒瓶时会在瓶口逸出气体
B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体
C.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深
D.将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅
16.已知反应2A(g)
B(?
)+2C(?
)-Q (Q>O),满足如图所示的关系,则下列说法中正
确的是 ( )
A.B、C可能均为非气态B.若B是气态,则C一定也只能是气态
C.若B为固态,则C一定为气态D.B、C可能均是气态
二、填空题
1.二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。
综合治理其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g)
2SO3(g)。
某温度下,SO2的平衡转化率与体系总压强(p)的关系如图所示。
根据图示回答下列问题:
①将2.0molSO2和1.0molO2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。
该反应的平衡常数等于____________。
②平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。
例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);H=-574kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);H=-1160kJ/mol
若用标准状况下4.48LCH4还原NO2至N2,整个过程中转移的电子总数为_____________(阿伏加德罗常数的值用NA表示),放出的热量为_________kJ。
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。
转化流程如图所示:
请写出MFe2Ox分解SO2的化学方程式______________________________________(不必配平)。
3.在一个固定体积的密闭容器中,向容器中充入2molA和1molB,发生如下反应:
2A(g)+B(g)
3C(g)+D(s),反应达到平衡时C的浓度为1.2mol/L。
(1)若使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,则正反应为________(填“吸热”或“放热”)反应。
(2)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2mol/L的是_________
①4molA+2molB②3molC+1molD+lmolB③3molC+2molD④1.6molA+0.8molB+0.6molC
(3)某温度下,向容器中加入3molC和0.8mo1D,反应达到平衡时C的浓度仍为1.2mol/L,则容器的容积V应大于_________L,小于________L
4.I.恒温、恒压下,在一个可变容积的容器中发生如下发应:
A(g)+B(g)
C(g)
(1)若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为mol。
(3)若开始时放入xmolA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol,3amol,则x=mol,y=mol。
平衡时,B的物质的量(选填一个编号)。
(甲)大于2mol(乙)等于2mol(丙)小于2mol(丁)可能大于、等于或小于2mol
作出此判断的理由是。
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是。
II.若维持温度不变,在一个与
(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(5)开始时放入1molA和1molB到达平衡后生成bmolC。
将b与
(1)小题中的a进行比较
(选填一个编号)。
(甲)a<b.(乙)a>b.(丙)a=b.(丁)不能比较a和b的大小
作出此判断的理由是。
5.请你协助化学兴趣小组的同学完成如下实验,并回答相关问题。
实验目的:
比较等体积0.5mol/L硫酸、1mol/L盐酸、1mol/L醋酸分别与金属反应生成氢气的速率和体积。
实验原理:
(用离子方程式表示)。
实验用品:
仪器(略)、药品(除给定的三种酸溶液外,在Na、Mg、Fe三种金属中选择最合适的一种,并说明理由)。
选择的金属是,不选其它两种金属的理由是。
实验步骤:
(1)甲同学设计的实验装置:
(2)乙同学认为该装置不能控制三个反应在同一时间发生,并作了相应的改进。
你认为乙同学改进的措施是:
。
(3)按改进后的装置进行实验,观察现象并得出相关结论。
实验现象及结论:
(4)反应开始时的速率:
v(H2SO4)v(HCl)v(HAc)(用“=”、“<”、“>”填空,下同),反应进行一段时间后的速率:
v(H2SO4) < v(HCl)v(HAc);
(5)最终得到的氢气体积:
V(H2/H2SO4)V(H2/HCl)V(H2/HAc)。
问题讨论:
(6)量筒的规格由决定。
(7)对结论“⑷”、“⑸”中盐酸和醋酸的异同,你的解释是。
(8)根据现有知识,上述实验中硫酸和盐酸分别与金属反应的速率应始终相等,但反应一段时间后有v(H2SO4) < v(HCl)。
对此现象,你猜想可能的原因是。
大学无机化学对此问题将有科学的解释。
6.瑞典皇家科学院2007年10月10日宣布,将本年度诺贝尔化学奖授予德国马普学会弗里茨一哈勃研究所的格哈德·埃特尔教授,以表彰他在固体表面化学过程研究领域做出开拓性成就。
格哈德·埃特尔的重要贡献之一是对哈伯一博施法合氨反应催化机理的研究。
格哈德·埃特尔建立的某温度下合成氨反应机理的各步反应的能量变化如图所示,图中的能量单位为kJ·mol-1。
(注:
图中“吸”表示在催化剂表面的吸附)
请回答下列问题:
(1)在合成氨反应中,决定反应速率的最主要的步骤是(填字母)
A.氮分子解离为氢原子B.氮原子的解离吸附C.氢分子解离为氢原子D.氨的解离吸附
(2)合成氨反应的机理为(用化学方程式表示)
①;②N2
N2吸
2N吸;③;
④NH吸+H吸
NH3吸⑤NH2吸+H吸
NH3吸
NH3
(3)某温度下合成氨反应的热化学方程式为;
(4)某温度下,合成氨反应K=3.0×103(mol·L-1)-1,该温度下,在体积恒定为10L的四个密闭容器中分别充入:
(A)10mol、30molH2和20molNH3;(B)10molN2和30molH2;(C)20molN2和60molH2;(D)10molN2和28molH2;(E)0.1molN2、0.3molH2和20molNH3,则反应达到平衡后,N2的转化率最大的是(填字母)。
(5)合成氨工业生产中所用的α—Fe催化剂的主要成分是FeO、Fe2O3,当催化剂中Fe3+与Fe3+的物质的量之比为1︰2时,其催化剂活性最高,以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉。
发生如下反应:
2Fe2O3+C=4FeO+CO2,为制得该种活性最高的催化剂,应向480gFe2O3粉末加入炭粉的质量为g.
7.“碘钟”实验中,3I-+
→I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。
某探究性学习小组在20℃进行实验,得到的数据如下表:
实验编号
①
②
③
④
⑤
c(I-)/mol·L-1
0.040
0.080
0.080
0.160
0.120
c(
)/mol·L-1
0.040
0.040
0.080
0.020
0.040
t/s
88.0
44.0
22.0
44.0
t1
(1)该实验的目的是___________________________________________。
(2)显色时间t1=______________。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实
验,显色时间t2的范围为______(填字母)。
a.<22.0s b.22.0s~44.0s c.>44.0s d.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是___________________________________。
8.(10分)工业生产硝酸铵的流程图如下:
请回答下列问题:
(1)写出硝酸铵在工农业生产中的重要作用__________________(任写一条)
(2)已知N2(g)+3H2(g)
2NH3(g),ΔH=-92kJ·mol-1。
请回答:
①在500℃、200atm和铁催化条件下向一密闭容器中充入1molN2和3molH2,充分反应后,放出的热量______(填“<”“>”“=”)92.4kJ,理由是_________________
②为有效提高氢气的转化率,实际生产中宜采取的措施有____________
A.降低温度B.最适合催化剂活性的适当高温C.增大压强
D.降低压强E.循环利用和不断补充氮气F.及时移出氨
(3)已知铂铑合金网未预热也会发热。
写出氨催化氧化的化学方程式。
____________________________________________________________________
该反应的化学平衡常数表达式K=________________,当温度升高时,K值______(增大、减小、无影响),其原因是_____________________________________。
(4)在一定温度和压强的密闭容器中,将平均式量为8.5的H2和N2混合,当该反应达到平衡时,测出平衡混合气的平均式量为10,此时N2的转化率为_______________。
9.有如下化学反应:
2A(g)+B(g)2C(g),△H<0。
(1)若将4molA和2molB在2L的容器中混合,经2s后测得C的浓度为0.6mol·L-1,用物质A表示的平均反应速率为____________;2s时物质B的浓度为_______________;
(2)若把amolA和bmolB充入一密闭容器中,达到平衡时它们的物质的量满足:
n(A)+n(B)=n(C),则A的转化率为_________________;
(3)若将4molA和2molB加入体积可变的等压容器中,一定温度下达到平衡状态,测得气体总物质的量为4.2mol。
此时,混合气体中C的体积分数为_____________;若再通入少量B气体,体系中A的体积分数_____________(填“增大”、“减小”或“不变”),若要使A的体积分数再达到与原平衡状态相同,可采取的措施有________________________。
(4)下图是一定条件下该反应过程中,体系内各物质浓度的变化情况。
反应处于平衡状态的时间是________________,t2时曲线发生变化的原因是__________________________
,若在t4时将B的浓度增大0.lmol·L-1,请在上图中画出各物质浓度的变化情况。
10.(12分)氨是最重要的氮肥,是产量最大的化工产品之一。
课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,其合成原理为:
N2(g)+3H2(g)
2NH3(g);△H<0他因此获得了1918年诺贝尔化学奖。
工业上合成氨的部分工艺流程如下:
反应体系中各组分的部分性质见下表:
气体
氮气
氢气
氨
熔点(℃)
-210.01
-252.77
-77.74
沸点(℃)
-195.79
-259.23
-33.42
(1)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程。
即反应后通过把混合气体的温度降低到使混合气体分离出来产品;继续循环的气体是。
写出该反应的化学平衡常数表达式:
K=。
(2)运用化学反应速率和化学平衡的观点说明工业上采取用上述实际生产措施的理由:
。
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________。
(4)合成氨工业对国民经济和社会发展具有重要的意义。
对于密闭容器中的反应:
N2(g)+3H2(g)
2NH3(g),673K,30MPa下
n(NH3)和n(H2)随时间变化的关系如下图所示。
下列叙述正确的是()
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比上图
中d点的值大
(5)1998年希腊亚里斯多德大学的Marmellos和
Stoukides采用高质子导电性的SCY陶瓷(能传递
H+),实现了高温常压下高转化率的电化学合成氨。
其实验装置如图。
阴极的电极反应式:
。
测试题二
.X、Y、Z三种气体,取X和Y按1:
1的物质的量之比混合,放入密闭容器中发生如下反应:
X+2Y
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为
3:
2,则Y的转化率最接近于()
A.33%B.40%C.50%D.65%
.反应A(g)+B(g)
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是____________________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”“减小”“不变”),原因是____________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?
_______________,原因是_________。
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:
E1_________,E2________(填“增大”“减小、”“不变”)。
.等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V
的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能是()
A.4-3-2-1B.1-2-3-4C.3-4-2-1D.1-2-4-3
.在2L密闭容器中,800℃时反应2NO(g)+O2(g)
2NO2(g)体系中,n(NO)随时间变化如表:
(1)写出该反应的平衡常数表达式:
K=___________________。
已知:
K(300℃)>K(350℃),该反应是________热反应。
(2)下图中表示NO2的变化的曲线是____________。
用O2表示从0~2s内该反应的平均速率v=___________。
(3)能说明该反应已经达到平衡状态的是___________。
a、v(NO2)=2v(O2)b、容器内压强保持不变c、v逆(NO)=2v正(O2)d、容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a、及时分离出NO2气体b、适当升高温度c、增大O2的浓度d、选择高效的催化剂
.已知:
4NH3(g)+5O2(g)=4NO(g)+6H2(g).△H=-1025kJ/mol该反应是一个可逆反应。
若反应物
起始物质的量相同,下列关于该反应的示意图不正确的是()
.将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)
2HBr(g)
g平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)
的转化率为b。
a与b的关系是()
A.a>bB.a=bC.a<bD.无法确定
.碘钨灯比白
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 化学反应 速率 限度 专题 训练 新人 必修
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《公务员财产申报制度》.docx
《公务员财产申报制度》.docx
