 上海原电池和电解池专题习题解析LXdocx.docx
上海原电池和电解池专题习题解析LXdocx.docx
- 文档编号:25725019
- 上传时间:2023-06-11
- 格式:DOCX
- 页数:31
- 大小:582.77KB
上海原电池和电解池专题习题解析LXdocx.docx
《上海原电池和电解池专题习题解析LXdocx.docx》由会员分享,可在线阅读,更多相关《上海原电池和电解池专题习题解析LXdocx.docx(31页珍藏版)》请在冰豆网上搜索。
上海原电池和电解池专题习题解析LXdocx
原电池和电解池专题习题-LX
一.选择题(共18小题)
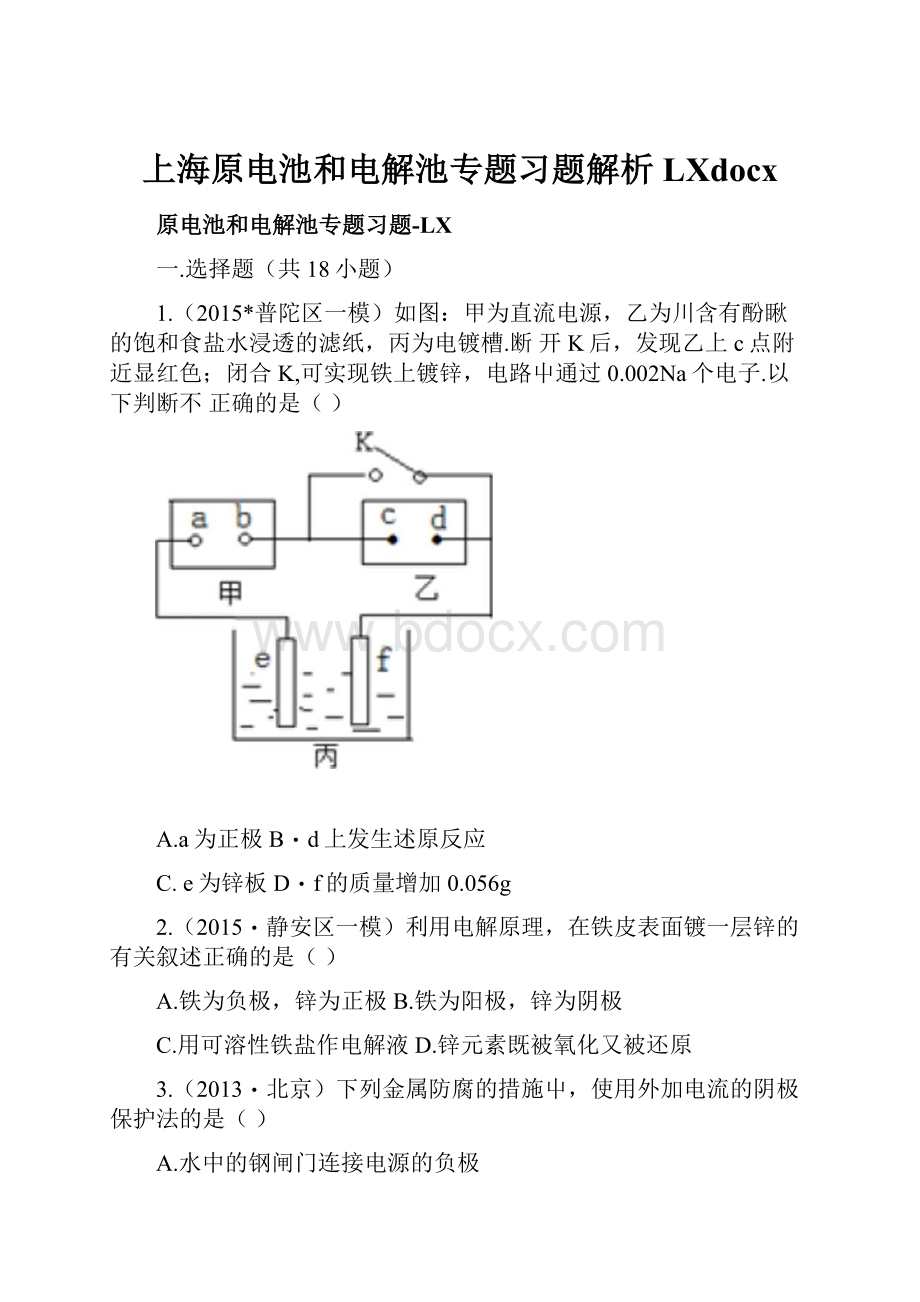
1.(2015*普陀区一模)如图:
甲为直流电源,乙为川含有酚瞅的饱和食盐水浸透的滤纸,丙为电镀槽.断开K后,发现乙上c点附近显红色;闭合K,可实现铁上镀锌,电路屮通过0.002Na个电子.以下判断不正确的是()
A.a为正极B・d上发生述原反应
C.e为锌板D・f的质量增加0.056g
2.(2015・静安区一模)利用电解原理,在铁皮表面镀一层锌的有关叙述正确的是()
A.铁为负极,锌为正极B.铁为阳极,锌为阴极
C.用可溶性铁盐作电解液D.锌元素既被氧化又被还原
3.(2013・北京)下列金属防腐的措施屮,使用外加电流的阴极保护法的是()
A.水中的钢闸门连接电源的负极
B.金属护拦表面涂漆
C.汽车底盘喷涂高分子膜
D.地下钢管连接镁块
4.
(2015・嘉定区一模)石墨作电极电解氯化铜溶液,(如图),下列分析正确的是()
A.a端是直流电源的负极
B.通电使氯化铜发生电离
C.阳极上发生的反应:
C『++2eTCu
D・通电一段时间,在阴极附近观察到有黄绿色气体产生
5.(2014秋•虹口区期末)下列有关电化学的图示,完全止确的是()
A.
——
稀h2so4
Cu-Zn原电池
粗铜楮炼
c.ZnCl2溶袤
铁片镀锌
溶袤
淙粉
碘化押
验证气体产物
6.
(2014秋•奉贤区期末)甲、乙、丙3个烧杯小分别装有稀H2SO4、CuCl2溶液、饱和食盐水,甲小电极为锌片和铜片,乙中电极为右黑棒Ci、C2,丙中电极为石墨棒C3、铁片,电极之间用导线相连.则下列叙述不正确的是()
B.C】、C2分别是阳极、阴极,锌片、C3上都发生氧化反应
C.C]和C3放出的气体相同,铜片和铁片放出的气体也相同
D.甲中溶液的pH逐渐升高,乙、丙中溶液的pH逐渐减小
7.
(2015・崇明县一模)如图所示,在毛玻璃片上放有一张浸有含酚駄的饱和氯化钠溶液的滤纸,滤纸上点有A、B、C、D四个点(指靠近电极的溶液).有关说法正确的是()
溶液的滤纸
A.A点比B点先出现红色B.B点比A点先出现红色C.A点比C点先岀现红色D・D点比C点先岀现红色
8.
(2015・青浦区一模)下列与金加腐蚀有关的说法止确的是()
图中,开关由M改置于N时,Cu・Zn合金的腐蚀速率减小
C.CL-TJ
图屮,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增人
图中,钢铁轮船外壳连接一块金属A(铜块)可以减缓船体外壳腐蚀速度
9.(2015*浦东新区一模)如图所示的方案可以降低铁闸门的腐蚀速率.下列判断正确的是()
电
A.若X为导线,Y可以是锌
B.若X为导线,铁闸门上的电极反应式为Fe-2e^Fe2+
C.若X为直流电源,铁闸门做负极
D.若X为直流电源,Y极上发生还原反应
10.(2015*宝山区二模)如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是()
®2H++2e^H2/r②O2+4e+2H2O^4OH③2C1・2eTCb个
A.①B.②C.①②D.①②③
11.(2015・杨浦区二模)下列有关钢铁腐蚀与防护的说法错误的是()
A.生铁比纯铁容易生锈
B.钢铁的腐蚀生成疏松氧化膜,不能保护内层金属
C.钢铁发生吸氧腐蚀吋,正极反应式为:
O2+2H2O+4eT4OH「
D.为保护地卜•钢管不受腐蚀,可使具与直流电源正极相连
12.
(2015*黄浦区二模)结合图判断,如卜-叙述正确的是()
13.
III
A.I和II中负极均能产生气泡
B.I和II中正极均能产生气泡
C.I和II中负极反应均是Fe-2e=Fe2+
D.I和II中正极反应均是2H++2e=H2
A.当a、b间用导体连接时,则X应发生氧化反应
B.当a、b间用导体连接时,则X可以是锌或石墨
C.当a、b与外接电源相连时,a应连接电源的正极
D.当a、b与外接电源相连时,阴极的电极反应式:
2C「-2eTC12T
15.(2015*浦东新区二模)实验室川图所示装置电解氯化铜溶液,实验屮观察到碳(I)电极质量增加,碳(II)电极有气体放出.下列说法正确的是()
A.a为电源正极B.电极II上发生还原反应
C.电子流向:
“TlTllTbD.该装置将电能转化为化学能
16.(2015*普陀区二模)在化学能与电能的转化小,下列叔述正确的是()
A.镀锌铁皮在食盐水屮发生析氢腐蚀
B.电解池的阴极材料一定比阳极材料活泼
C.将铁器与电源正极相连,可在其表面镀锌
D.原电池的负极和电解池的阳极均发生氧化反应
17.(2015*徐汇区二模)一定条件下,碳钢腐蚀与溶液pH的关系如下表•下列说法错误的是()
PH
2
4
6
6.5
8
13.5
14
腐蚀快慢
较快
慢
较快
主要产物
Fe2+
Fe3C>4
Fe2C)3
FeO?
4
A.当pH<4时,碳钢主要发牛析氢腐蚀
B.当pH>6时,碳钢主要发牛•吸氧腐蚀
C.当pH>14时,正极反应为Ch+4H++4e^2H2O
D.在煮沸除氧气后的碱性溶液屮,碳钢腐蚀速率会减缓
18.(2015*闵行区二模)如图可设计成多种用途的电化学装置.下列分析正确的是()
A.当a和b用导线连接时,溶液中的SO42-向铜片附近移动
B.将a打电源正极相连可以保护锌片,这叫牺牲阳极的阴极保护法
C.当a和b用导线连接时,铜片上发生的反应为:
2H++2eTH2T
D.a和b用导线连接后,电路中通过0.02mo1电子时,产牛:
0.02mol气体
原电池和电解池专题习题
参考答案与试题解析
一.选择题(共18小题)
1.(2015・普陀区一模)如图:
甲为总流电源,乙为用含有酚臥的饱和食盐水浸透的滤纸,丙为电镀槽・断开K后,发现乙上c点附近显红色;闭合K,可实现铁上镀锌,电路中通过0.002N八个电了.以下判断不正确的是()
丙
A.a为正极B.d上发生还原反应
C.e为锌板D.f的质量增加0.056g
【考点】原电池和电解池的工作原理.
【分析】甲为直流电源,乙为用含有酚瞅的饱和食盐水浸透的滤纸,丙为电镀槽.断开K后,发现乙上c点附近显红色,则c极为电解池阴极,d为阳极,c电极上氢离了放电生成氢气,d电极上氯离了放电生成氯气,则a是直流电源正极,b是直流电源负极;
为实现铁上镀锌,接通K后,使c、d两点愆路,e是电解池阳极,f是阴极,电镀吋,镀层作阳极,镀件作阴极,以此解答该题.
【解答】解:
甲为直流电源,乙为用含有酚駄的饱和食盐水浸透的滤纸,丙为电镀槽.断开K后,发现乙上c点附近显红色,贝Uc极为电解池阴极,d为阳极,c电极上氢离了放电生成氢气,d电极上氯离了放电牛成氯气,则a是直流电源正极,b是直流电源负极;
为实现铁上镀锌,接通K后,使c、d两点愆路,e是电解池阳极,f是阴极,电镀吋,镀层作阳极,镀件作阴极,
A.通过以上分析知,a是直流电源正极,故A正确;
B・d为阳极,该电极上发生氧化反应,故B错课;
C.为实现铁上镀锌,锌作阳极,铁作阴极,所以c电极为锌板,故C正确;
D.f极是阴极,阴极上得电子发生还原反应,Fe2++2e_=Fe,电路中通过0.002Na个即0.002mol电子,生成铁是0.001mol,质量是0.056g,故D正确.
故选B.
【点评】木题综合考杳原电池和电解池知识,侧重于学生的分析能力和电化学知识的综合应用的考杏,为高考常见题型和高频考点,难度中等,注意把握电极方程式的书写和判断.
2.(2015*静安区一模)利用电解原理,在铁皮表面镀一层锌的有关叙述正确的是()
A.铁为负极,锌为正极B.铁为阳极,锌为阴极
C.用可溶性铁盐作电解液D.锌元素既被氧化又被还原
【考点】电解原理.
【专题】电化学专题.
【分析】利川电解原理,在铁皮表面镀一层锌,那么金属锌作电解池的阳极,铁作阴极,阳极锌放电牛成锌离子进入溶液,溶液中的锌离子在阴极放电,从而在铁上镀上锌,据此解答即可.
【解答】解:
在铁皮表面镀一层锌,那么金属锌作电解池的阳极,发生氧化反应,铁作阴极,阳极锌放电生成锌离子进入溶液,溶液屮的锌离子在阴极放电,被还原,从而在铁上镀上锌,故锌既被氧化,又被还原,故选D.
【点评】本题主耍考查的是电解原理的应用,分清电极反应是解决本题的关键,难度不大.
3.(2013・北京)下列金属防腐的措施中,使用外加电流的阴极保护法的是()
A.水中的钢闸门连接电源的负极
B.金属护拦表面涂漆
C.汽车底盘喷涂高分子膜
D.地下钢管连接镁块
【考点】金属的电化学腐蚀与防护.
【专题】电化学专题.
【分析】使川外加电流的阴极保护法说明该该金属防腐的措施中连接外加电源,阴极连接电源负极.
【解答】解:
A.水屮的钢闸门连接电源负极,阴极上得电子被保护,所以属于使川外加电流的阴极保护法,故A正确;
B.对健身器材涂油漆使金属和空气、水等物质隔离而防止生锈,没冇连接外加电源,故B错误;
C.汽车底盘喷涂高分子膜阻止了铁与空气、水的接触,从而防止金加铁防锈,没有连接外加电源,故C错误;
D.镁的活泼性人于铁,川牺牲镁块的方法來保护船身而防止铁被腐蚀,屈丁•牺牲阳极的阴极保护法,故D错込
故选A.
【点评】木题考查了金属的腐蚀与防护,解答时要从钢铁生锈的条件方面进行分析、判断,从而找出科学的防锈方法.
4.(2()15・嘉定区一模)石墨作电极电解氯化铜溶液,(如图),下列分析正确的是()
ab
2+cr
A.a端是直流电源的负极
B.通电使氯化铜发牛电离
C.阳极上发生的反应:
C『++2eTCu
D.通电一段吋间,在阴极附近观察到有黄绿色气体产生
【考点】电解原理.
【分析】用石黑作电极电解氯化铜溶液,连接电源正极的为电解池的阳极,发生氧化反应:
2C「-2e=C12T,连接电源负极的为电解池的阴极,发生:
Cu2++2e'=Cu,电解池工作时,阴离了向阳极移动,阳离了向阴极移动,以此解答该题.
【解答】解:
A.铜离子向c端移动,说明c是电解池的阴极,则a端是肓流电源的负极,故A正确;
B.氯化铜的电离只需溶于水,不需通电,故B错i吴;
C・阴极发生:
Cu2++2e'=Cu,故C错误;
D.通电一段时间,在阳极发生氧化反应:
2C1'・2“=C12个,阳极附近观察到有黄绿色气体产生,故D错误.
故选A.
【点评】本题考查电解池知识,题口难度不人,注意把握电极的判断以及电极方程式的书写,为解答该题的关键.
5.
(2014秋•虹口区期末)下列有关电化学的图示,完全正确的是()
验证气体产物
【考点】化学实验方案的评价.
【专题】实验评价题.
【分析】A.原电池中较活泼的金属作负极,较不活泼的金属或导电的非金属作正极;
B.粗铜的精炼中,粗铜作阳极,纯铜作阴极;
C.电镀时,镀层作阳极,镀件作阴极;
D.电解时,电流流入的电极为阳极,期一电极为阴极,阳极上发生氧化反应,阴极上发生还原反应.
【解答】解:
A・原电池屮较活泼的金屈作负极,较不活泼的金属或导电的非金属作正极,所以铜-锌-稀硫酸原电池中,锌作负极,铜作正极,故A错误;
B.粗铜的精炼中,粗铜作阳极,纯铜作阴极,电解质溶液为含冇铜离了的盐,故B错误;
C.电镀时,镀层作阳极,镀件作阴极,所以铁片上镀锌,锌作阳极,铁作阴极,故C错谋;
D.电解时,电流流入的电极为阳极,另一电极为阴极,所以电解氯化钠溶液时,根据图片知,碳棒为阳极,铁棒为阴极,阳极上氯离子失电子生成氯气,氯气能置换碘化钾中的碘,碘遇淀粉变蓝色,所以阳极上用淀粉碘化钾溶液可检验氯气的存在;阴极上氢离了得电了生成氢气,利用氢气的燃烧实验检验阴极产物;溶液中冇氢氧化钠产生,无色酚臥试液遇碱变红色,所以可用无色酚駄检验氢氧化钠的生成,故D正确;
故选D.
【点评】本题考查了原电池原理、电解原理、电镀等知识点,难度不大,注意:
电镀时,镀层作阳极,镀件作阴极.
6.(2014秋•奉贤区期末)甲、乙、丙3个烧杯中分别装有稀H2SO4.CuC12溶液、饱和食盐水,甲中电极为锌片和铜片,乙中电极为石墨棒C]、C2,丙中电极为石墨棒C3、铁片,电极之间用导线相连.则下列叙述不正确的是()
1frifnir
■■■
■■OB4■■■■—■■■
•■■■■■■
■■■••■■■■■■■■■
乜二二二二―匕二二:
二二二二乜三W二二£二二芳
甲样弘酸乙缜化倒沛改»博和負益水
A.甲是化学能转变为电能,乙、内是电能转变为化学能
B.Ci、C2分别是阳极、阴极,锌片、C3上都发生氧化反应
C.©和C3放出的气体相同,铜片和恢片放出的气体也相同
D.甲屮溶液的pH逐渐升高,乙、丙屮溶液的pH逐渐减小
【考点】原电池和电解池的工作原理.
【专题】电化学专题.
【分析】A、甲中锌片和铜片、稀硫酸构成原电池,则乙、内为电解池;
B、根据甲中锌片和铜片、稀硫酸构成原电池,活泼金属锌为负极,铜为正极,所以C|、C2分别是阳极、阴极,C3、铁分别是阳极、阴极;
C、根据B的分析,C]、C3都是阳极,都为氯离子失电子放出氯气,铜片为正极放出蛍气、铁阴极氢离子得电子放出氢气;
D、甲屮锌片和铜片、稀硫酸构成原电池,氢离子得电子放出氢气,pH逐渐升高,乙电极氯化铜本身,pH基本不变,丙电极饱和氯化钠溶液生成氢氧化钠,pH逐渐升高.
【解答】解:
A、甲屮锌片和铜片、稀硫酸构成原电池,则乙、丙为电解池,所以甲是化学能转变为电能,乙、丙是电能转变为化学能,故A正确;
B、卬中锌片和铜片、稀硫酸构成原电池,活泼金属锌为负极发生氧化反应,铜为正极,所以0、C2分别是阳极、阴极,C3是阳极发生氧化反应,故B正确;
C、由B的分析,C]、C3都是阳极,都为氯离子失电子放出氯气,铜片为正极放出氢气、铁阴极氮离子得电子放出氢气,故C正确;
D、甲屮锌片和铜片、稀硫酸构成原电池,氢离了得电了放出氢气,pH逐渐升高,乙电极氯化铜木身,pH基本不变,丙电极饱和氯化钠溶液生成氢氧化钠,pH逐渐升高,故D错误.
故选D.
【点评】本题考査了原电池原理和电解池原理的应川,注意根据装登的原理分析反应,题口难度不人.
7.(2015・崇明县一模)如图所示,在毛玻璃片上放冇一张浸冇含酚駄的饱和氯化钠溶液的滤纸,滤纸上点有A、B、C、D四个点(指靠近电极的溶液).有关说法正确的是()
含酚猷的饱和氯化钠
溶液的滤纸
A.A点比B点先出现红色B.B点比A点先出现红色
C.A点比C点先出现红色D.D点比C点先出现红色
【考点】电解原理.
【专题】电化学专题.
【分析】冇外加电源的部分是电解池装置,没冇外加电源的金属诙和石墨构成原电池,左边的金属铁是阴极,右边的金属铁是负极,在电解池屮,阴极区域是氢离子得电子,生成氢气,碱性增强,在原电池中的石黑电极上氧气得电子牛成氢氧根离子,碱性增强,碱遇到酚瞅显示红色,电解池能让化学反应发牛的比原电池的更快.
【解答】解:
有外加电源的部分是电解池装置,没有外加电源的金属铁和石墨构成原电池,所以左边的金属诙是阴极,右边的金属铁是负极,
在电解池屮,阴极区域B极是氢离子得电子,生成氢气,碱性增强,遇到酚瞅显示红色,
A区域生成氯气,B点比A点先出现红色,并且氢氧根离子会移向A电极,
在原电池中的石墨电极上氧气得电子生成氢氧根离子,碱性增强,显示红色,D金属铁会溶解,
根据电解池能让化学反应发生的比原电池的更快,所以A点比C点先出现红色,故选BC.
【点评】本题考查学生原电池和电解池的工作原理以及电极反应的书写知识,属于综合知识的考查题,难度中等.
8.(2015•青浦区一模)下列与金属腐蚀有关的说法正确的是()
图中,插入海水中的铁棒,越靠近底端腐蚀越严重
图中,开关由M改置丁-N吋,Cu-Zn合金的腐蚀速率减小
C.
图屮,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增人
图中,钢铁轮船外壳连接一块金属A(铜块)可以减缓船体外壳腐蚀速度
【考点】金属的电化学腐蚀与防护.
【分析】A.越靠近底端,越不易腐蚀;
B.开关由M改置于N时,Zn为负极,合金为正极;
C.接通开关时,形成原电池,Zn为负极,pt为正极;
D.Fe、Cu形成原电池时,Fe为负极被腐蚀.
【解答】解:
A.越靠近底端,氧气的含量越少,越不易腐蚀,故A错误;
B.开关由M改置于N时,Zn为负极,合金为止极,则Cu-Zn合金的腐蚀速率减小,故B正确;
C.接通开关时,形成原电池,Zn为负极,负极上Zn的腐蚀速率加快,牛成氢气的速率减慢,Pt为正极,正极上生成氢气,故C错课;
D.Fc、Cu形成原电池时,Fc为负极被腐蚀,则钢铁轮船外壳连接一块金属A(铜块)不能减缓船体外壳腐蚀速度,故D错误.
故选B.
【点评】本题综合考查电化学知识,侧重于金属的腐蚀与防护以及原电池的工作原理的考查,题口难度不大,注意把握电极反应.
9.(2015*浦东新区一模)如图所示的方案可以降低铁闸门的腐蚀速率.下列判断正确的是()
电
A.若X为导线,Y可以是锌
B.若X为导线,铁闸门上的电极反应式为Fe-2e^Fe2+
C.若X为直流电源,铁闸门做负极
D.若X为直流电源,Y极上发生还原反应
【考点】金属的电化学腐蚀M防护.
【分析】作原电池的正极或电解池的阴极被保护,能降低铁闸门的腐蚀速率,据此分析.
【解答】解:
A.若X为导线,Y可以是锌,形成原电池,铁闸门作正极被保护,能降低铁闸门的腐蚀速率,故A正确;
B.若X为导线,铁闸门上的电极反应式为Fe-2e^Fe2+,则铁闸门作负极被腐蚀,所以不能降低铁闸门的腐蚀速率,故B错误:
C.若X为直流电源,铁闸门连接负极,作阴极,能降低铁闸门的腐蚀速率,故C错i吴;
D.若X为直流电源,诙闸门连接负极,作阴极,Y极为阳极,则Y极上发牛氧化反应,故D错误.故选A.
【点评】木题考杳了金属的腐蚀与防护,
侧重于原电池原理和电解池原理的应用的考查,题日难度不人,
注意把握原电池和电解池中电极的判断.
10.(2()15・宝山区二模)如图的装置,左为铁电极,右为石墨电极,3为水或某种溶液.若两电极肓接连接或外接电源,石墨上可能发生的反应是()
①2H++2e^H2^②O2+4C+2H2OT4OH-③2C1'・2e^C\2t
A.①B.②C.①②D.①②③
【考点】原电池和电解池的工作原理.
【分析】若两电极直接连接,则该装置是原电池,铁作负极,石墨作正极,负极上铁失电子发牛氧化反应,正极石墨上得电子发生还原反应;
若两电极外接电源,则该装置为电解池,石墨电极若与正极相连,则为阳极,溶液中的阴离了失电了发生氧化反应,据此分析;
【解答】解:
若两电极总接连接,则该装置是原电池,恢作负极,石墨作正极,弱电解质为酸性溶液则正极石墨上发生2HJ2cTH2T,若电解质为中性溶液,则正极石墨上发生O2+4e+2H2O^4OH_;若两电极外接电源,贝I」该装置为电解池,石墨电极若与正极相连,则为阳极,如果电解氯化钠溶液,则电解反应为2C「-2eTC12T,所以①②③都有可能发生,
故选:
D.
【点评】木题考查原电池和电解池原理,根据电极上得失电子來分析解答,切确原电池的工作原理及电解质溶液的性质是解答木题的关键,电解过程的反应原理应用,注意相关基础知识的积累,难度不大.
11.(2015*杨浦区二模)下列有关钢铁腐蚀与防护的说法错误的是()
A.主铁比纯铁容易生锈
B.钢铁的腐蚀生成疏松氧化膜,不能保护内层金属
C.钢铁发生吸氧腐蚀时,正极反应式为:
O2+2H2O+4e-^4OH
D.为保护地下钢管不受腐蚀,可便其与直流电源正极相连
【考点】金属的电化学腐蚀与防护.
【分析】A.作原电池负极的金属加速被腐蚀;
B.钢铁和空气、水能构成原电池导致钢铁被腐蚀,生成疏松的氧化铁;
C.钢铁发生吸氧腐蚀时,正极上氧气得电了发生还原反应;
D.作电解池阳极的金属加速被腐蚀,作阴极的金属被保护.
【解答】解:
A.生铁中含有C、Fe,生铁和电解质溶液构成原电池,Fe作负极而加速被腐蚀,纯铁不易构成原电池,所以生铁比纯铁易生•锈,故A正确;
B.钢恢和空气、水能构成原电池导致钢铁被腐蚀,钢铁的腐蚀牛成疏松氧化膜不能隔绝空气,所以不能保护内层金属,故B正确;
C.钢铁发生吸氧腐蚀时,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-40H,故C正确;
D.作电解池阳极的金属加速被腐蚀,作阴极的金属被保护,为保护地下钢管不受腐蚀,可使其与直流电源负极相连,故D错误;
故选D.
【点评】本题考查金属腐蚀与防护,明确原电池和电解池原理即可解答,知道钢铁发牛•析氢腐蚀、吸氧腐蚀发生的电极反应,知道如何采用化学方法保护金属,题目难度不人.
12.
(2015*黄浦区二模)结合图判断,如下叙述止确的是()
In
A.I和II屮负极均能产生气泡
B.1和II中正极均能产生气泡
C.I和II中负极反应均是Fe・2e=Fe2+
D.I和II中正极反应均是2H++2e=H2
【考点】原电池和电解池的工作原理.
【专题】电化学专题.
【分析】A.I、II中的负极均为Fc火去电子;
B.I中正极发生吸氧腐蚀的电极反应,II中正极发生析氢腐蚀的电极反应;
C.I和II中负极Fe失去2个电子;
D.【屮正极发生吸氧腐蚀的电极反应,II中正极发牛析氢腐蚀的电极反应.
【解答】解:
I中性环境中发生吸氧腐蚀,负极Fe失电子,正极氧气得电子,II酸性环境中发纶析氢腐蚀,负极Fc火电了,正极氢离子得电子生成氢气.
A.I和II中负极反应均是Fe・2e=Fe2+,I和II中负极均不产生气泡,故A错误;
B.I中正极发生O2+2H2O+4e=4OH_,II中正极反应发生2H*+2e二HqT,故B错误;
C.I和II中负极反应均是Fe-2e=Fe2+,故C正确;
D.【屮正极发4O2+2H2O+4e=4OH_,【I中正极反应发生2H++2e=H2T,故D错误;故选C.
【点评】本题考查吸氧腐蚀和析红腐蚀,注意电解质溶液的羌别判断出I为吸氧腐蚀、II为析氢腐蚀时解答本题的关键,明确发生的电极反应即可解答,题目难度不大.
13.(2015*嘉定区模拟)下列关于电化学的实验事实正确的是()
出现环境
实验事实
A
以稀H2SO4为电解质的Cu・Zn原电
池
Cu为正极,正极上发牛还原反应
B
电解CuCb溶液
电子经过负极T阴极
通过电解液阳
•H••••W•▼■•"
极9正极
C
弱酸性环境下钢铁腐蚀
负极处产生h2,正极处吸
收02
D
将钢闸门与外加电源负极相连
牺牲阳极阴极保护法,可防止钢闸门腐蚀
A.AB.BC.CD.D
【考点】原电池
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 上海 原电池 电解池 专题 习题 解析 LXdocx
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《初级会计实务》试题题库大全及答案详解.docx
《初级会计实务》试题题库大全及答案详解.docx
