 沪教版全国化学九年级下册第7单元《应用广泛的酸碱盐》测试题含答案.docx
沪教版全国化学九年级下册第7单元《应用广泛的酸碱盐》测试题含答案.docx
- 文档编号:29179190
- 上传时间:2023-07-21
- 格式:DOCX
- 页数:12
- 大小:156.08KB
沪教版全国化学九年级下册第7单元《应用广泛的酸碱盐》测试题含答案.docx
《沪教版全国化学九年级下册第7单元《应用广泛的酸碱盐》测试题含答案.docx》由会员分享,可在线阅读,更多相关《沪教版全国化学九年级下册第7单元《应用广泛的酸碱盐》测试题含答案.docx(12页珍藏版)》请在冰豆网上搜索。
沪教版全国化学九年级下册第7单元《应用广泛的酸碱盐》测试题含答案
第7单元《应用广泛的酸碱盐》测试题
一、单选题
1.除去下列物质中的余质所选用的试别及操作方法不正确的一组是()
物质
所含杂质
除去杂质的方法
A
N2
O2
将气体缓缓通过灼热的铜网
B
KCl
MnO2
溶解、过滤、蒸发
C
CuO
Cu
稀硫酸、过滤
D
KOH溶液
K2CO3
适量Ca(OH)2溶液、过滤
A.AB.BC.CD.D
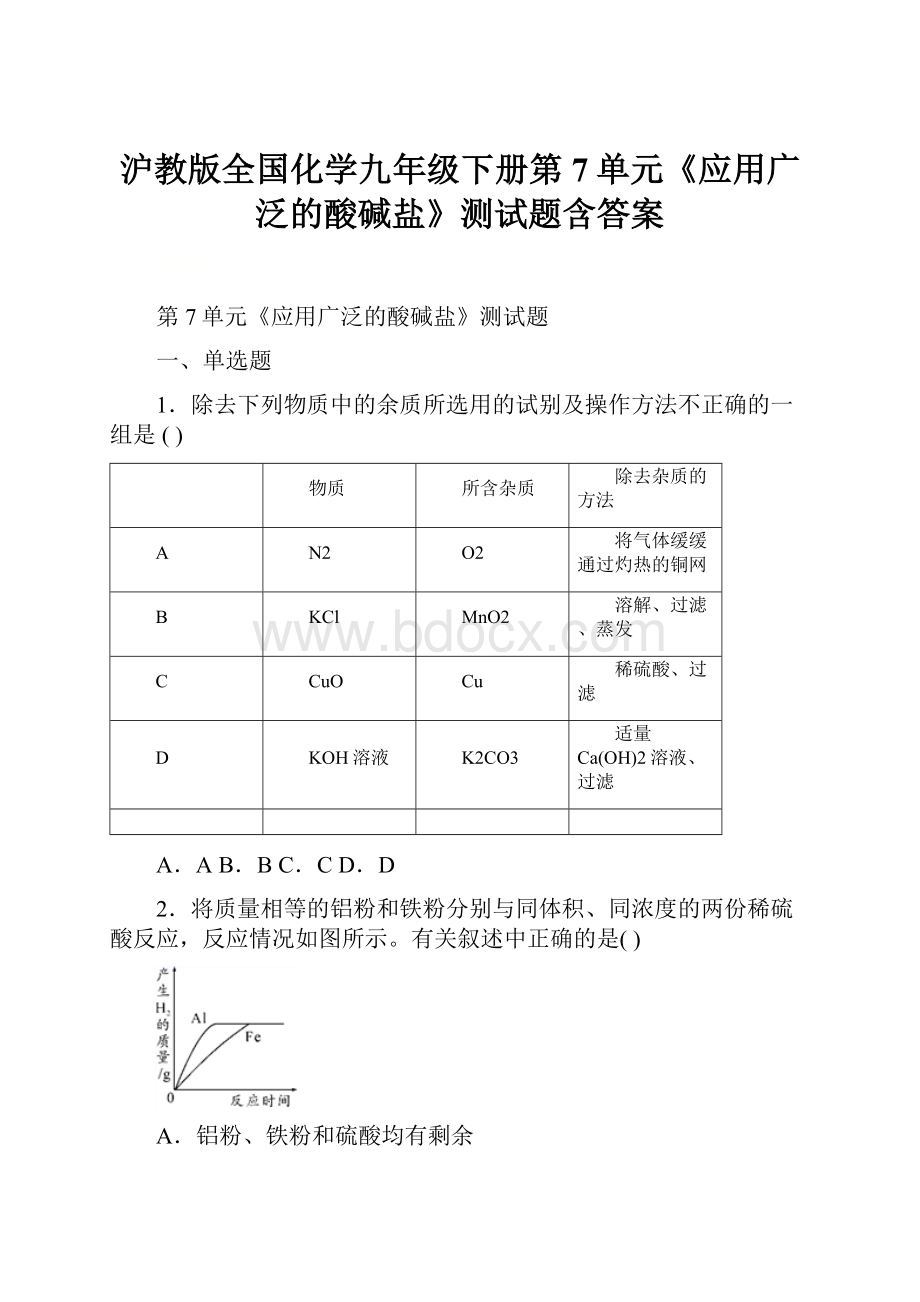
2.将质量相等的铝粉和铁粉分别与同体积、同浓度的两份稀硫酸反应,反应情况如图所示。
有关叙述中正确的是()
A.铝粉、铁粉和硫酸均有剩余
B.铝粉、铁粉均反应完,硫酸有剩余
C.硫酸、铝粉均反应完,铁粉有剩余
D.铁粉、硫酸均反应完,铝粉有剩余
3.“凤凰”号火星探测器测得火星北极的土壤呈弱碱性,如果火星具备作物生长的条件,下列作物较适宜在火星北极种植的是( )
植物
大豆
棉花
茶树
松树
pH
6.5﹣7.5
6.0﹣6.8
5.0﹣5.5
5.0﹣6.0
A.大豆B.棉花C.茶树D.松树
4.我国制碱工业的先驱,发明了联合制碱法的科学家是()
A.张青莲B.侯德榜C.屠呦呦D.道尔顿
5.焰色反应中火焰呈黄色的是()
A.K2SO4B.CaCl2C.Na2OD.ZnCl2
6.下列实验操作不正确的是()
A.用托盘天平称取2.3克氯化钠B.用10mL的量筒量取8mL的水
C.用50mL的烧杯盛放大约15mL的水D.用石蕊测定某溶液的pH值
7.下列说法不正确的是
A.金刚石、石墨和C60的结构中碳原子的排列方式不同
B.常喝碳酸饮料不可以治疗胃酸过多
C.食醋可以除去水壶中的水垢
D.酸雨就是指呈酸性的雨水
8.能治疗胃酸过多的物质是( )
A.氢氧化铝B.氢氧化钠C.生理盐水D.氢氧化钙
9.下列关于硝酸铵
的说法中,正确的是()
A.硝酸铵是一种常用的复合肥B.硝酸铵的相对分子质量为80g
C.硝酸铵能与氢氧化钾反应D.硝酸铵中氮元素和氢元素的质量比为1:
2
10.下列关于金属的说法正确的是
A.人类使用金属的年代早晚只取决于地壳中金属的含量
B.武德合金的熔点高,可用于制造保险丝
C.“真金不怕火炼”表明金(Au)在高温条件下也很难与氧气反应
D.除了银、铂、金以外,自然界中的金属一般都是以单质形式存在
11.下列实验基本操作不正确的是
A.称量氢氧化钠固体
B.过滤黄泥水
C.测定溶液的PH
D.蒸发结晶
12.质量相等的金属镁和铝分别加入质量相等、溶质质量分数相等的两份稀硫酸中,反应完毕后,金属均有剩余。
则反应两种溶液质量关系是( )
A.相等B.镁反应后的溶液质量大
C.铝反应后的气体质量大D.无法比较
13.鉴别CO、O2、CO2三种气体,最简便的方法是()
A.用燃着的木条分别接触导出的气体B.将气体分别通入澄清石灰水
C.将气体分别通入紫色石蕊溶液D.试验三种气体的溶解性
二、填空题
14.金属在生产生活中起着重要作用。
(1)铜可以做导线,主要利用了金属铜的延展性和______。
(2)赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的化学方程式为____。
(3)对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是_____。
①Fe、Ag、CuSO4溶液
②Cu、Ag、FeSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
(4)某化学小组在实验结束后,进行了如上图所示的废液处理:
①I中的操作名称是_____。
②写出Ⅱ中一定发生反应的化学方程式_____。
15.人体内胃酸的主要成分是盐酸,其酸性强于醋酸。
胃酸有两大主要作用:
一是杀死大部分随食物入胃的细菌,二是帮助消化。
胃酸过多,对胃壁有损害作用;胃酸过稀,容易造成消化不良。
(1)由于铝元素对人体健康有害,治疗胃酸过多的含铝止酸剂正被新药“胃舒乳”(主要成分是氢氧化镁)所代替,则服用胃舒乳治疗胃酸的化学方程式是:
___
;
(2)饭后不宜大量喝水,以免影响胃液的酸碱性。
某人在大量喝水时,其胃液的酸碱性变化符合下图所示的___(选填编号)。
16.肯德基套餐是我们大家比较喜欢的一种食物。
请回答下列问题
(1)可乐中糖份来自新鲜的甘蔗,甘蔗中所含蔗糖的化学式是____________,
其中鸡肉中富含的营养素的作用是____________的基本物质,是________及修补受损组织的主要原料,并提供能量。
(2)可乐又叫做碳酸饮料,喝可乐时先保存在冰雪冷藏一会引用口感较好,说明气体溶解度随温度______________________________________________,
(3)套餐中也含有一些蔬菜沙拉,为了提高蔬菜的抗寒和抗旱能力,使蔬菜叶色浓绿应施加的一种化肥是______________(填化学式)有些可乐是铝罐盛装的,铝制的可乐罐喷漆的作用为___________。
17.干粉灭火器的主要成分是碳酸氢钠,其受热易分解,化学方程式为:
2NaHCO3
Na2CO3+CO2↑+H2O。
一定量NaHCO3固体在密闭容器中受热分解(此过程Na2CO3不分解)。
下列图像表示此过程中容器内某些量的变化趋势,其中不正确的是
A.
B.
C.
D.
18.山西老陈醋选用优质高梁、大麦、豌豆等五谷,经蒸、酵、熏、淋、晒的过程酿造而成,是中国四大名醋之一,至今已有3000余年的历史,素有“天下第一醋”的盛誉,以色,香、醇、浓、酸五大特征著称于世。
(1)山西老陈醋的主要成分的化学式为_____。
(2)山西老陈醋和酱油颜色相近,鉴别这两种调味品,常用的方法有_____(填字母)。
A闻气味
B观察颜色
C分别加入少量苏打粉
三、推断题
19.有一包白色固体粉末,可能由Ca(OH)2、KNO3、Na2CO3、CuSO4、BaCl2中的一种或几种组成,现做实验得如下结果:
(1)将此固体粉末加入到水中,得到白色沉淀,上层清液呈蓝色;
(2)该白色沉淀不溶于稀硝酸.从实验可知,该粉末一定含有______,可能含有:
______,一定不含有______.
20.已知A~E为初中化学常见的五种不同物质,B、C、E为化合物,它们的转化关系如图:
(1)若A、D为单质,B溶液为浅绿色,则D为_________________。
(2)若A、D为化合物,B的俗名是苏打,请写出变化①的化学方程式:
_________________。
四、实验题
21.课外小组利用下图装置验证碳酸钠的性质。
(1)将注射器1的针头向瓶内推进,使针头下端进入瓶内液面下,抽取少量A中液体,此时注射器1中发生反应的化学方程式为_________。
(2)验证碳酸钠是碳酸盐,应进行的操作及观察到现象是__________。
22.
(1)天然碱可表示为aNa2CO3•bNaHCO3•cH2O,为测定其组成,称取一定质量的天然碱样品进行如下实验。
已知:
图中B处为两个单向阀:
推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭。
实验步骤①组装好装置,检查气密性②反复推拉注射器③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行⑤打开弹簧夹,再次反复缓缓推拉注射器⑥再次称量E、F的质量。
问题探究:
①E中的药品为_____,E的作用是_____。
C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是_____,F的作用是_____。
②若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数_____(填“偏大”“偏小”或“无影响”),
(2)实验室有一瓶硝酸铜溶液,其中可能混有硝酸银、硝酸钡两种物质,请你设计一个实验方案来证明硝酸铜溶液中确实含有硝酸银、硝酸钡。
限制试剂:
稀硫酸、碳酸钠溶液、稀盐酸、氢氧化钾溶液
(本实验条件下,微溶物以沉淀形式出现,Ag2SO4微溶于水)
实验操作
预期现象
结论
①取少量混合溶液于试管中,_____。
_____
_____
②_____
_____
_____
五、计算题
23.实验室用13g锌粒与足量的稀硫酸反应制取氢气。
计算:
(已知:
Zn+H2SO4=ZnSO4+H2↑)
(1)生成氢气的质量为多少克?
(2)这些氢气在标准状况下的体积是多少升?
(标准状况下,氢气密度为0.0899g/L)
24.医疗上常用硫酸钡作透视肠的内服剂.俗称“钡餐”。
一旦误将碳酸钡代替硫酸钡作“钡餐”,就会致人中毒,此时可服用硫酸镁溶液解毒。
某化学兴趣小组用如下实验模拟了碳酸钡在胃液中的变化,并验证了硫酸镁解番的原理:
I.取一定量碳酸钡固体于烧杯中,逐滴加入188g稀盐酸至过量,并不断搅拌至固体完全溶解。
II.再向该烧杯中逐滴加入硫酸镁溶液,并不析搅拌,烧杯内产生白色沉淀质量与加入硫酸镁溶液的质量关系如图所示。
请你结合图像和提供的数据进行分析与计算。
(1)请你设计实验方案证明步骤I反应后的溶液中盐酸过量(只写出试剂名称)_____;
(2)通过计算确定硫酸镁溶液的溶质质量分数_____。
(写出计算过程)
(3)请你计算M点所得溶液中氯化镁的溶质质量分数为_____。
参考答案
1.C2.D3.A4.B5.C6.D7.D8.A9.C10.C11.C12.B13.A
14.导电性3CO+Fe2O3
2Fe+3CO2②过滤Fe+H2SO4=FeSO4+H2
15.Mg(OH)2+2HCl=MgCl2+2H2OA
16.C12H22O11构成细胞的基本物质机体生长减小而增大NH4H2PO4或(NH4)2HPO4美观
17.C
18.CH3COOHAC
19.CuSO4、BaCl2KNO3Ca(OH)2、Na2CO3
20.Fe
21.Na2CO3+Ca(OH)2=2NaOH+CaCO3↓将注射器2中的稀硫酸推入瓶中,A中有气泡产生,B中澄清石灰水变浑浊
22.浓硫酸吸收水蒸气除去空气中的CO2、H2O吸收生成的CO2偏小滴加足量的稀盐酸,振荡,直至不再产生沉淀为止有白色沉淀生成证明有AgNO3将上述溶液静置后,取少量上层清液于另一支试管中,滴加少量的硫酸溶液,振荡.(或将以上液体进行过滤,取少量滤液于试管中,滴加少量的硫酸溶液,振荡)有白色沉淀生成证明有Ba(NO3)2
23.
(1)0.4g;
(2)4.48L
24.
(1)紫色石蕊试剂
(2)解:
设硫酸镁的质量为X,氯化镁的质量为Y。
;
硫酸镁溶液的溶质质量分数为:
答:
硫酸镁溶液的溶质质量分数为6%;故填:
6%
(3)M点时,硫酸镁和氯化钡完全反应,所得溶液中氯化镁的质量由
(2)已经求出等于9.5g;根据硫酸钡的质量推求出碳酸钡的质量及产生二氧化碳气体的质量为:
此时溶液的质量把所有加入的试剂全部加起来,以沉淀和其体形式脱离溶液体系的都减去。
得其质量为:
19.7g+188g+200g-23.3g-4.4g=380g
故M点所得溶液中氯化镁的溶质质量分数为:
答:
M点所得溶液中氯化镁的溶质质量分数为2.5%;故填:
2.5%
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 应用广泛的酸碱盐 沪教版 全国 化学 九年级 下册 单元 应用 广泛 酸碱 测试 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
