 人教版中考化学专题训练实验探究题.docx
人教版中考化学专题训练实验探究题.docx
- 文档编号:3165888
- 上传时间:2022-11-18
- 格式:DOCX
- 页数:16
- 大小:253.47KB
人教版中考化学专题训练实验探究题.docx
《人教版中考化学专题训练实验探究题.docx》由会员分享,可在线阅读,更多相关《人教版中考化学专题训练实验探究题.docx(16页珍藏版)》请在冰豆网上搜索。
人教版中考化学专题训练实验探究题
2020年中考化学专题训练:
实验探究题
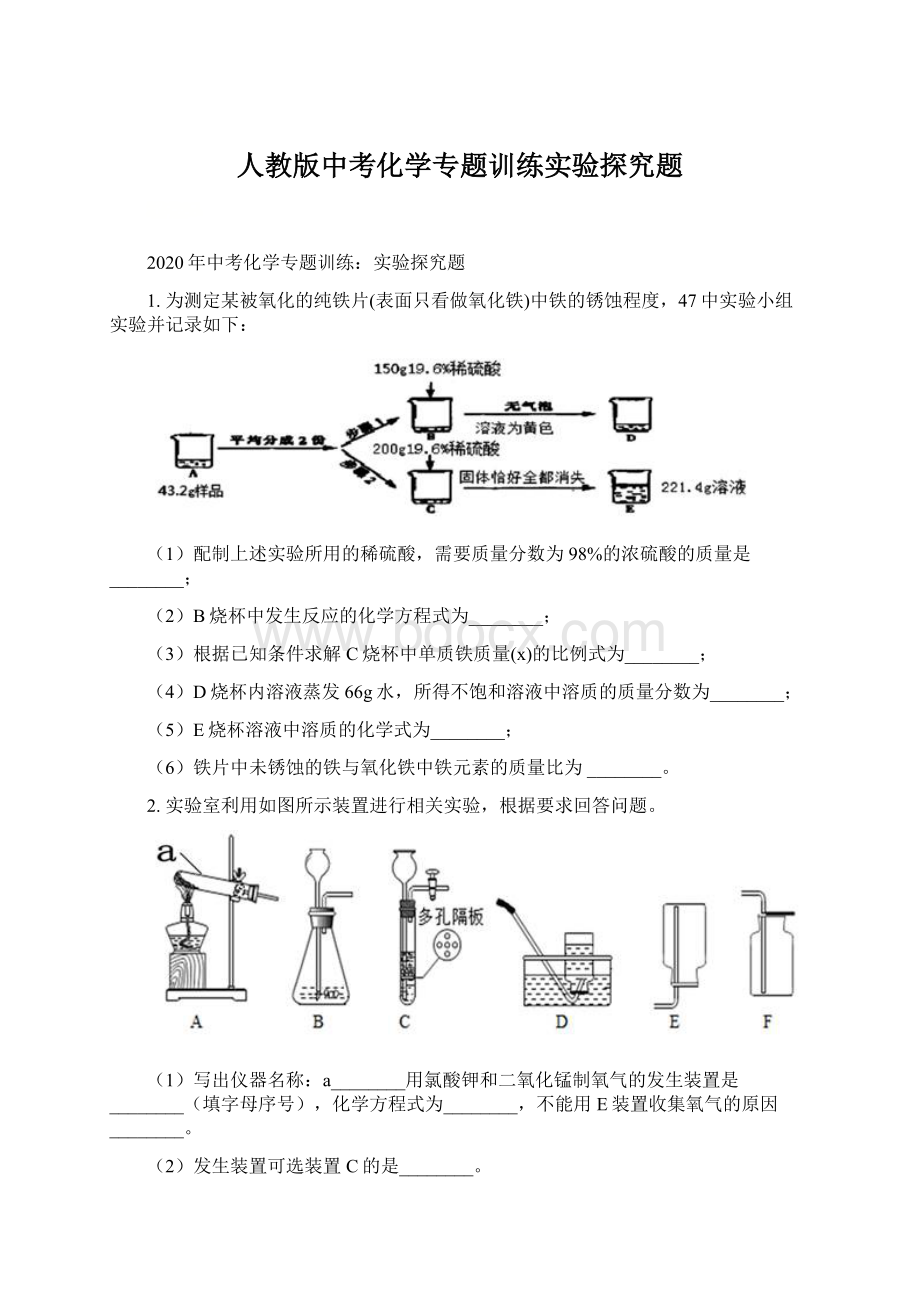
1.为测定某被氧化的纯铁片(表面只看做氧化铁)中铁的锈蚀程度,47中实验小组实验并记录如下:
(1)配制上述实验所用的稀硫酸,需要质量分数为98%的浓硫酸的质量是________;
(2)B烧杯中发生反应的化学方程式为________;
(3)根据已知条件求解C烧杯中单质铁质量(x)的比例式为________;
(4)D烧杯内溶液蒸发66g水,所得不饱和溶液中溶质的质量分数为________;
(5)E烧杯溶液中溶质的化学式为________;
(6)铁片中未锈蚀的铁与氧化铁中铁元素的质量比为________。
2.实验室利用如图所示装置进行相关实验,根据要求回答问题。
(1)写出仪器名称:
a________用氯酸钾和二氧化锰制氧气的发生装置是________(填字母序号),化学方程式为________,不能用E装置收集氧气的原因________。
(2)发生装置可选装置C的是________。
I.石灰石和稀盐酸制二氧化碳II.双氧水和二氧化锰制氧气III.锌块和稀硫酸制氢气
(3)石灰石与稀盐酸制二氧化碳的化学方程式为________。
为测定产生二氧化碳的质量(假设二氧化碳已完全放出,忽略空气中物质的影响),设计如右图装置:
产生二氧化碳的质量________(填“大于”、“小于”或“等于”)氢氧化钠固体增加的质量。
(4)对锥形瓶中反应后的剩余溶液成分进行探究(杂质不溶于水且不参加反应),剩余溶液中一定有的溶质是________。
把剩余溶液分成两份,分别置于两个试管中进行实验。
实验I.往一个试管中滴加硝酸银溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解。
实验II.往另一个试管中逐滴滴入碳酸钠溶液,并用pH传感器连续监测试管内溶液的pH,得下图
根据实验________(填编号)可知,剩余溶液中还有盐酸。
(5)曲线上M点溶液的溶质成分是________。
3.
(1)同学们利用下图所示装置进行气体的制备实验(A~F为装置编号)
①写出上图D装置中甲仪器的名称________。
②用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为________,其中二氧化锰起________作用;收集氧气可选择________ (填装置编号)。
③实验室制备二氧化碳通常选择下列药品中的________(填药品序号)。
a.稀盐酸b.熟石灰c.块状石灰石d.稀硫酸
通常检验二氧化碳气体的反应可用化学方程式表示为________ 。
④常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,若要控制滴加液体的速率,可选择的发生装置是________(填装置编号)。
⑤制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是________ (填序号)。
a.将烧杯换成水槽b.导管伸入水中位置过深,气体无法逸出
c.将水换成冰水d.先用手捂住试管壁,再将导管另一端插入水中
(2)为什么汗水有咸味?
学习小组同学为此开展探究。
【提出问题】汗水中产生咸味的物质是什么?
【假设与猜想】根据生活经验推测,汗水中产生咸味的物质可能是________。
(3)【查阅资料】用铂丝醮取少许含有钠元素的溶液(或物质)在酒精灯火焰上灼烧,会呈现黄色火焰。
【制订计划】为了证明咸味物质是猜想中的物质,一是要证明汗水溶液中含有阴离子________(填写离子符号),二是要证明汗水溶液中有阳离子________(填写离子符号)。
(4)【进行实验】证明阴离子的实验:
向汗水溶液中滴加________溶液,再加入少量稀硝酸,振荡,仍有白色沉淀产生。
证明阳离子的实验:
________。
(5)【结论】经上述实验证明,汗水中的咸味物质就是猜想中的物质。
【分析与交流】上述实验中,证明阴离子存在的化学反应方程式为:
________,该化学反应属于________反应。
4.利用物质的性质能帮助我们开展科学探究。
(1)【认识物质】
俗名
所含原子团
用途
氢氧化钠
________、火碱、苛性钠
氢氧根
精炼石油等
碳酸钠
纯碱、苏打
________
生产玻璃制品等
(2)【定性检测】
为检测久置空气中的氢氧化钠是否变质,设计并进行了如下图的实验:
①试管1中观察到的现象是________ 。
②试管2中观察到产生气泡,反应的化学方程式为________。
③试管3中观察到产生白色沉淀。
④能达到实验目的的是试管________(选填”1”、“2”或“3”)中的实验。
⑤若要判断氢氧化钠是部分变质还是全部变质,请你选择上述实验后三支试管中的液体继续实验,完成下表。
试管的编号
实验操作
现象和结论
试管________(选填“1”、“2”或“3”)
________
________
(3)【定量测定】
为了测定ag变质氢氧化钠中碳酸钠的质量分数,设计了如下的实验方案(浓硫酸具有吸水性):
实验步骤和数据:
①组装装置,检查气密性(气密性良好);②加入药品,称量C处装置质量为bg,滴入足量稀硫酸:
③完全反应后称量C处装置质量为cg;④后续处理。
实验分析:
Ⅰ.判断碳酸钠已完全反应的实验现象是________。
Ⅱ.利用实验数据,可得变质氢氧化钠中碳酸钠的质量分数为________ (用字母表示)。
Ⅲ.所得实验结果存在一定的误差,可能的原因是________(写出一点即可)。
5.实验室中常用分解过氧化氢来简便快速的制备氧气,化学小组II进一步探究外界条件对过氧化氢分解速率的影响,并进行了氧气性质实验。
(查阅资料)有些水果、蔬菜对过氧化氢的分解有催化作用。
(实验探究I)探究苹果和土豆对过氧化氢分解是否有催化作用及催化效果;各量取6mL5%的过氧化氢溶液,分别倒入1、2、3号三支试管中,取大小、形状基本相同的苹果块和土豆块,分别放入2、3号试管中,并把带火星的木条分别同时伸入三支试管口内,观察现象并记录如下:
试管编号
1
2
3
材料名称
无
苹果
土豆
反应速率
很慢
稍快
较快
产生气泡
很少
比1中多
较快
复燃情况
不复燃
复燃
很快复燃
实验结论
___________________________
苹果和土豆对过氧化氢都有催化作用,土豆的催化效果更好
(1)写出土豆催化过氧化氢的文字表达式:
________。
(2)试管编号1实验的目的是________。
(3)(实验探究2)探究浓度对过氧化氢分解速率的影响。
取三份不同浓度的过氧化氢溶液,测定收集到100mL氧气所用的时间,(其它实验条件均相同)记录如下:
试验编号
1
2
3
过氧化氢溶液浓度
5%
15%
30%
所用时间(秒)
205
25
3
实验结论
________
用上述收集的氧气与不同物质进行反应,其中有一固体能在氧气中燃烧,发出明亮的蓝紫色火焰,生成刺激性气味的气体,该反应的文字表达式:
________。
(4)为了测量生成氧气的体积可用如图装置,氧气从________端进入(填序号),装置内的空气对测量结果________(填“有”或“无")影响。
(5)该实验通过测定收集相同体积氧气所需的时间来比较过氧化氢分解的快慢,还可以通过测定________来比较过氧化氢分解的快慢。
6.教育部从2018年开始,要求在学校普及垃圾分类回收处理的相关知识。
某化学活动小组结合新学的知识对此进行一系列实践活动。
(1)I.活动探究
学会识图分拣垃圾:
下列垃圾应投入带有右图图标的垃圾箱内的是________(填字母序号)。
A.塑料版 B.果皮 C.碎瓷片
(2)学会检验有害气体:
含氯塑料焚烧时会产生氯化氢等气体,若要检验焚烧后的气体中有氯化氢,可将其通入________溶液中,有白色沉淀生成即可。
(3)Ⅱ.实验探究
【提出问题】如何回收处理废旧电池中的镉?
【查阅资科】
①废旧电池中含有镉、汞等元素,这些元素会危害人类健康。
②镉(Cd)从溶液中析出时呈海绵状固体,在化合物中通常表现为+2价。
③碳酸镉(CdCO3)、氢氯化镉[Cd(OH)2]都是白色固体,难溶于水。
【设计实验】先将废旧电池进行处理以制得硫酸镉(CdSO4)溶液,用于以下实验。
实验设计
实验步骤
实验现象
实验结论
与金属反应
取少许溶液于试管中,加入足量的Zn粉,充分反应。
________
Zn可以置换出Cd。
与碱反应
取少许溶液于试管中,加入足量的NaOH溶液,充分反应。
产生白色沉淀
用化学反应方程式表示为________
取少许溶液于试管中,加入足量的________溶液,充分反应。
产生白色沉淀
可用该试剂除去CdSO4.。
(4)【回收处理】
实验结束后,将反应后的混合物通过过滤、洗涤、加热,进而再制得镉。
【交流反思】
请同学们基于化学视角说明垃圾分类回收处理的重要意义________(答一点即可)。
7.MgO在医药建筑等行业应用广泛。
硫酸镁和木炭高温煅烧的产物为MgO(固体)、SO2、CO2、CO、硫蒸气。
(1)工业上,SO2的任意排放会引起的环境问题是________。
化石燃料燃烧是产生SO2的主要原因,下列做法能减少SO2排放的是________(填字母)。
a.开发新能源替代化石燃料 b.向高空排放SO2
(2)在高温、催化剂条件下,CO和H2可化合成燃料甲醇(CH3OH),该反应中CO和H2的分子个数比为________。
若CO和H2中混有H2S气体,H2S会与催化剂中的Cu在高温下发生置换反应,其中一种产物为CuS,该反应的化学方程式为________。
(3)利用如图装置对硫酸镁和木炭进行高温煅烧,并对产生的四种气体进行分步吸收或收集。
已知:
常温下,硫为固体;SO2、CO2均能与NaOH溶液反应。
①装置B、C中的溶液分别是________、________。
(填字母)
a.NaOH溶液
b.KMnO4溶液
②装置B、C的作用分别是________、________。
③装置D的作用是________。
④若将装置A中的固体隔绝空气加热至500℃,就会变成蒸气,其中有一种相对分子质量为128的气体。
该气体的化学式为________。
8.用如图装置在相应条件下完成下列实验
(1)探究燃烧条件:
B盛木炭粉。
①由A处通N2一段时间后,加热B,B、C无明显变化。
②待B冷却至室温,由A处通入O2一段时间,B、C无明显变化。
③由A处继续通入O2,加热B,木炭粉燃烧,C中溶液变浑浊。
结论:
由①、③可知燃烧需要________;由②、③可知燃烧需要________。
(2)探究CO与金属氧化物反应:
B盛金属氧化物。
I、模拟工业炼铁:
A处通CO,B盛Fe2O3粉末,B处下方放酒精喷灯,D处放酒精灯。
实验:
在A处通入CO时,应立即点燃________处(填“B”或“D”)酒精(喷)灯。
在B处加热一段时间后可观察到的现象是________。
II、探究金属氧化物的组成:
A处通CO,B盛金属氧化物,B处下方放酒精喷灯、D处放酒精灯。
已知:
CuO、Fe3O4均为黑色物质,B中所盛粉末:
CuO或Fe3O4或两者混合物。
实验:
同Ⅰ操作、B中可观察到既有红色固体生成,又有黑色固体生成。
实验结论(定性):
该黑色粉末为________。
定量分
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 人教版 中考 化学 专题 训练 实验 探究
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
