 高中化学《选修4》单元测试难度系数070056.docx
高中化学《选修4》单元测试难度系数070056.docx
- 文档编号:4731026
- 上传时间:2022-12-08
- 格式:DOCX
- 页数:25
- 大小:326.46KB
高中化学《选修4》单元测试难度系数070056.docx
《高中化学《选修4》单元测试难度系数070056.docx》由会员分享,可在线阅读,更多相关《高中化学《选修4》单元测试难度系数070056.docx(25页珍藏版)》请在冰豆网上搜索。
高中化学《选修4》单元测试难度系数070056
高中化学单元测试(难度系数:
0.70-0.56)-20161014
满分:
班级:
_________ 姓名:
_________ 考号:
_________
一、单选题(共20小题)
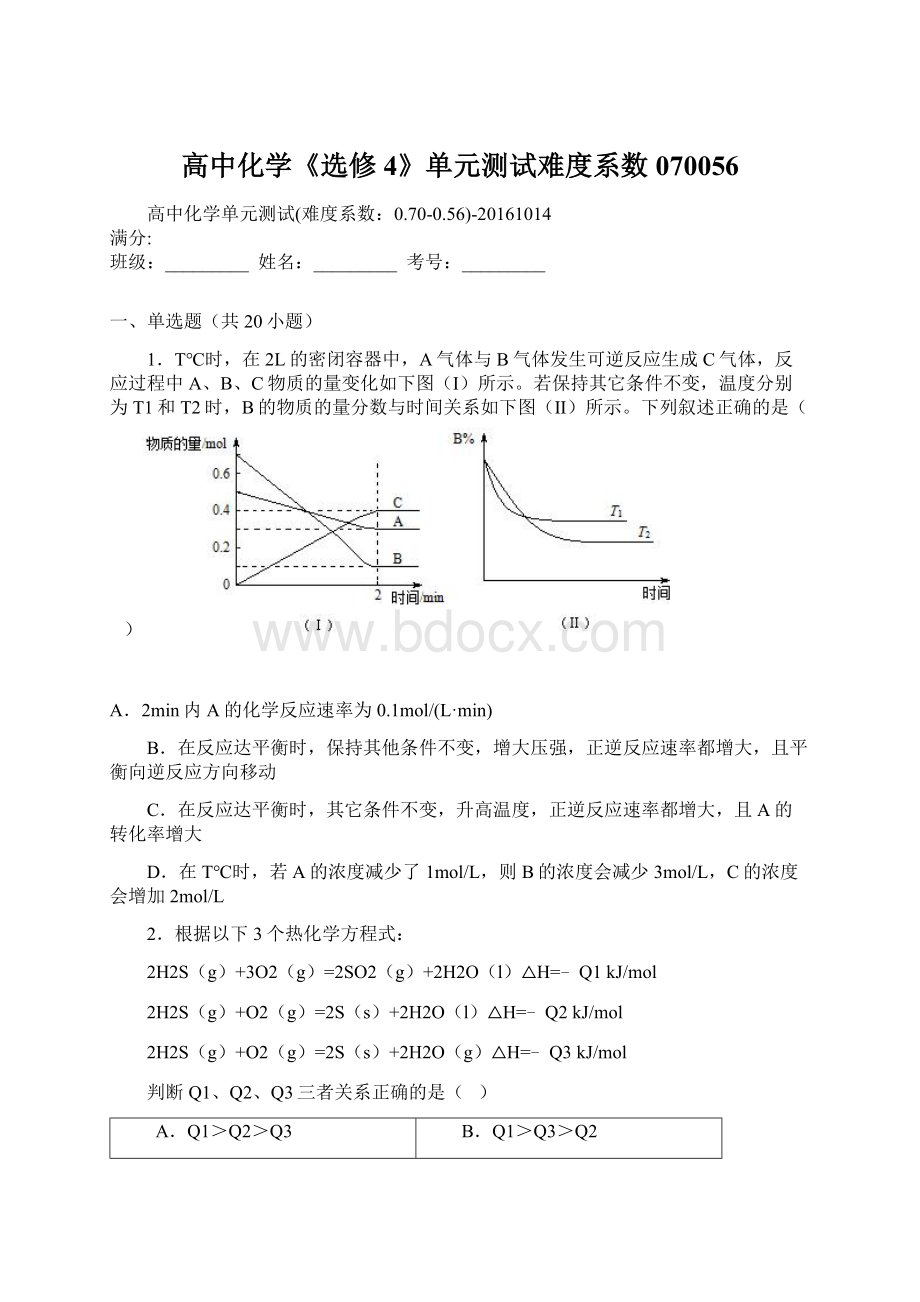
1.T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B、C物质的量变化如下图(Ⅰ)所示。
若保持其它条件不变,温度分别为T1和T2时,B的物质的量分数与时间关系如下图(Ⅱ)所示。
下列叙述正确的是( )
A.2min内A的化学反应速率为0.1mol/(L·min)
B.在反应达平衡时,保持其他条件不变,增大压强,正逆反应速率都增大,且平衡向逆反应方向移动
C.在反应达平衡时,其它条件不变,升高温度,正逆反应速率都增大,且A的转化率增大
D.在T℃时,若A的浓度减少了1mol/L,则B的浓度会减少3mol/L,C的浓度会增加2mol/L
2.根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=﹣Q1kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(l)△H=﹣Q2kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(g)△H=﹣Q3kJ/mol
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3
B.Q1>Q3>Q2
C.Q3>Q2>Q1
D.Q2>Q1>Q3
3.已知反应:
①C+CO2⇌2CO△H>0;②N2+3H2⇌2NH3△H<0.达平衡后升温,正反应速率的变化是( )
A.①加快,②减慢
B.均加快
C.均减慢
D.①减慢,②加快
4.1gH2完全燃烧生成液态水放出aKJ的热量,下列热化学方程式正确的是( )
A.H2(g)+1/202(g)=H2O(l) △H=-aKJ.mol-1
B.2H2(g)+O2(g)= 2H2O(l) △H=-4aKJ.mol-1
C.2H2(g)+O2(g)= 2H2O(l) △H=+4aKJ.mol-1
D.H2(g)+1/2O2(g)=H2O(g)△H=-2aKJ.mol-1
5.汽车尾气中,产生NO的反应为:
N2(g)+O2(g)
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。
下列叙述正确的是( )
A.温度T下,该反应的平衡常数
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
6.已知C(s)+H2O(g)=CO(g)+H2(g)ΔH=akJ·mol-1;2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1;H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为( )
A.-332
B.-118
C.+350
D.+130
7.一定温度下,在容积为2L的密闭容器中发生反应CO(g)+H2O(g)
CO2(g)+H2(g),部分数据见下表(表中t2>t1)( )
下列说法错误的是( )
A.反应在t1min末的速率为v(H2)=0.2/t1mol·L-1·min-1
B.平衡时水蒸气的转化率为66.67%
C.该温度下反应的平衡常数为l
D.其他条件不变,若起始时,n(CO)=0.60mol,n(H2O)=1.20mol,则平衡时水蒸气的转化率为33.33%
8.某温度下在2L密闭容器中加入一定量A,发生以下化学反应:
2A(g)
B(g)+C(g);ΔH=-48.25kJ·mol-1
反应过程中B、A的浓度比与时间t有下图所示关系,若测得第15min时c(B)=1.6mol·L-1,下列结论正确的是( )
A.该温度下此反应的平衡常数为3.2
B.A的初始物质的量为4mol
C.反应到达平衡时,放出的热量是193kJ
D.反应达平衡时,A的转化率为80%
9.可逆反应mA(g)+nB(g)=pC(g)+gD(g)的v-t图象如下图甲,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如下图乙。
①a1=a2 ②a1 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧乙图阴影部分面积更大 以上正确的为( ) A.②④⑤⑦ B.①④⑥⑧ C.②③⑤ D.①③⑥⑦ 10.根据下列实验及现象,下列能量关系正确的是( ) A.A B.B C.C D.C 11.已知298K、100kPa条件下: ①4Al(s)+3O2(g)===2Al2O3(s)ΔH=-2834.9kJ·mol-1 ②4Al(s)+2O3(g)===2Al2O3(s)ΔH=-3119.1kJ·mol-1 由此得出的正确结论是( ) A.等质量的O2比O3能量低,由O2变O3为吸热反应 B.等质量的O2比O3能量低,由O2变O3为放热反应 C.O3比O2稳定,由O2变O3为吸热反应 D.O2比O3稳定,由O2变O3为放热反应 12.对于反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下( ) A.加入催化剂,改变了反应的途径,反应的ΔH也随之改变 B.改变压强,平衡不发生移动,反应放出的热量不变 C.升高温度,反应速率加快,反应放出的热量不变 D.若在原电池中进行,反应放出的热量不变 13.对下列图像的描述正确的是( ) A.根据图①可判断反应的ΔH<0 B.根据图②,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 C.图③可表示压强(p)对反应2A(g)+2B(g) 3C(g)+D(s)的影响 D.图④可表示向醋酸溶液中通入氨气时,溶液导电性随氨气量的变化 14.下列图象表达正确的是( ) A. 浓硫酸的稀释 B. 过量的盐酸与等量的锌粉反应 C. 氢气与氧气反应中的能量变化 D. 微粒电子数 15.下列说法正确的是( ) A.若2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1,则H2燃烧热为241.8kJ·mol-1 B.原子弹爆炸是放热反应 C.若C(石墨,s)=C(金刚石,s) ΔH>0,则石墨能量低且键能小 D.由BaSO4(s)+4C(s)=4CO(g)+BaS(s)△H1=+571.2kJ•mol-1① BaSO4(s)+2C(s)=2CO2(g)+BaS(s)△H2=+226.2kJ•mol-1 ② 可得反应C(s)+CO2(g)=2CO(g)的△H=+172.5kJ•mol-1 16.已知2SO2(g)+O2(g) 2SO3(g) H=-197kJ·mol-1。 向同温、同体积的三个密闭容器中分别充入气体: (甲)2molSO2和1molO2,(乙)1molSO2和0.5molO2,(丙)2molSO3。 恒温、恒容下反应达平衡时,下列关系一定正确的是( ) A.容器内压强p: p甲=p丙>2p乙 B.SO3的质量m: m甲=m丙>2m乙 C.c(SO2)与c(O2)之比k: k甲=k丙>k乙 D.反应放出或吸收热量的数值Q: Q甲=Q丙>2Q乙 17.在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。 则下列有关推断正确的是( ) A.该反应的化学方程式为: 3X+2Y 2Z B.若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0 C.若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态 D.若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应 18.下列 关于各图的叙述正确的是( ) A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ·mol-1 B.乙表示A、B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数ω(B)>ω(A) C.丙表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度NaB溶液的pH D.丁表示0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1醋酸溶液得到的滴定曲线 19.室温下,将1mol的CuSO4•5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2,CuSO4•5H2O受热分解的化学方程式为: CuSO4•5H2O(s) CuSO4(s)+5H2O(l),热效应为△H3。 则下列判断正确的是( ) A.△H2>△H3 B.△H1<△H3 C.△H1+△H3=△H2 D.△H1+△H2>△H3 20.在一容积不变的密闭容器中充入0.1mol/LCO2和0.1mol/LCH4,在一定条件下发生反应: CH4(g)+CO2(g) 2CO(g)+2H2(g)。 测得平衡时CH4的转化率与温度、压强的关系如下图: 下列有关说法正确的是( ) A.上述反应的ΔH<0 B.压强p1>p2>p3>p4 C.1100℃时该反应的平衡常数约为1.64 D.压强为p4时,y点的v正 二、解答题(共5小题) 21.随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。 根据判断出的元素回答问题: (1)f在元素周期表的位置是__________。 (2)比较d、e常见离子的半径的小(用化学式表示,下同)_______>__________;比较g、h的最高价氧化物对应的水化物的酸性强弱是: _______>__________。 (3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。 (4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式: ___________________。 (5)上述元素可组成盐R: zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下: ①R离子浓度由大到小的顺序是: __________。 ②写出m点反应的而离子方程式_________________。 ③若R溶液改加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。 22.上述反应进程中能量变化示意图如下,试在图像中用虚线表示在反应中使用催化剂后能量的变化情况。 该反应的平衡常数表达式为K=__________。 升高温度,其平衡常数________(选填“增大”、“减小”或“不变”)。 23.合成氨反应是化学上最重要的反应之一: (1)合成氨原料气中的氢气可利用天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应制得,反应中每生成2molCO2吸收316kJ热量,该反应的热化学方程式是__________该方法制得的原料气中主要杂质是CO2,若用K2CO3溶液吸收,该反应的离子方程式是__________. (2)已知N2(g)+3H2(g)⇌2ΝΗ3(g)△H<0.如图是当反应器中按n(N2): n(H2)=1: 3投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线, ①曲线a对应的温度是__________. ②关于工业合成氨的反应,下列叙述正确的是__________(填序号) A.上图中M、N、Q点平衡常数K的大小关系为K(M)=K(Q)>K(N) B.加催化剂能加快反应速率但H2的平衡转化率不变 C.相同压强条件下,投料相同,达到平衡所需时间关系为c>b>a D.由曲线a可知,当压强增加到100MPa以上,NH3的物质的量分数可达到100% E.及时分离出NH3可以提高H2的平衡转化率 ③N点时c(NH3)=0.2mol•L﹣1,N点的化学平衡常数K=__________(精确到小数点后两位). (3)合成氨工业中含氨废水的处理方法之一是电化学氧化法,将含氨的碱性废水通入电解系统后,在阳极上氨被氧化成氮气而脱除,阳极的电极反应式为__________. (4)NH3可以处理NO2的污染,方程式如下: NO2+NH3 N2+H2O(未配平)当转移0.6mol电子时,消耗的NO2在标准状况下的体积是__________L. 24.甲醇是一种重要的可再生能源,工业上可用CO和H2合成。 (1)已知: CO(g)+1/2O2(g)=CO2(g) △H=—283kJ·mol—1 CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) △H=—725kJ·mol—1 若要求得CO(g)+2H2(g)=CH3OH(l)的△H,还需要知道反应(用化学方程式表示) 的焓变。 (2)在Cu2O/ZnO做催化剂的条件下,将CO(g)和H2(g)充入容积为2L的密闭容器中合成CH3OH(g),反应过程中,CH3OH的物质的量(n)与时间(t)及温度的关系如右图。 根据题意回答下列问题: ①反应达到平衡时,平衡常数表达式K= ;升高温度,K值 (填“增大”、“减小” 或“不变”)。 ②在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)= 。 ③若其它条件不变,对处于Z点的体系,将体积压缩至原来的1/2,达到新的平衡后,下列有关该体系的说法正确的是 。 a.氢气的浓度与原平衡比减少 b.正、逆反应速率都加快 c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大 ④据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量的CO2有利于维持Cu2O的量不变,原因是: (写出相关的化学方程式并辅以必要的文字说明)。 25.将4molSO2与2molO2的混合气分别置于容积相等的甲、乙两容器中,发生反应: 2SO2(g)+O2(g) 2SO3(g);ΔH<0,在相同温度下使其均达到平衡状态。 甲是恒压容器,乙是恒容容器。 甲容器达到平衡状态时,测得混合气体的物质的量为4.2mol;乙容器经50s达到平衡状态。 请回答: (1)甲容器达到平衡时SO2的转化率是,其所需时间_______50s(填“大于”、“小于”或“等于”)。 (2)达到平衡状态后,要使甲、乙两容器中SO2的物质的量相等,可采取的措施是_______(填字母)。 A.保持温度不变,适当扩大甲容器的容积 B.保持容积不变,使乙容器升温 C.保持容积和温度不变,向乙容器中加入适量SO3(g) D.保持容积和温度不变,向甲容器中加入适量SO3(g) 三、计算题(共2小题) 26.将相同物质的量的SO3充入下面的两个容器中,已知甲容器有活塞可以上下移动,乙容器体积固定,在相同的温度、压强下开始发生反应: 2SO3(g) 2SO2(g)+O2(g),在反应过程中维持体系温度不变。 (1)求达到平衡状态时SO3气体的转化率的大小关系? 图2-2 (2)达到平衡状态时分别充入一定量的Ar气,平衡是否会移动? 会怎样移动? 27.在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应: A(g) B(g)+C(g)ΔH=+85.1kJ·mol-1。 反应时间(t)与容器内气体总压强(p)的数据见下表: 回答下列问题: (1)欲提高A的平衡转化率,应采取的措施为__________________________________。 (2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为____________,平衡时A的转化率为________,列式并计算反应的平衡常数K____________________。 (3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=________mol,n(A)=________mol。 ②下表为反应物A的浓度与反应时间的数据,计算: a=________。 分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是____________,由此规律推出反应在12h时反应物的浓度c(A)为________mol·L-1。 四、实验题(共1小题) 28.醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应: i.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ii.2CH3OH(g)⇌C2H4(g)+2H2O(g) I.上述反应过程中能量变化如图所示: (1)在某密闭容器中,充人一定量CH3OH(g)发生上述两个反应,反应 (填“i”或“ii”)的速率较大,其原因为 .若在容器中加入催化剂,使ii的反应速率增大,则E1和E2﹣E1的变化是: E1 ;E2﹣E1 (填“增大”、“减小”或“不变”). (2)已知: CH3CH2OH(g)=CH3OCH3(g)△H=+50.7kJ.mol﹣1.则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H= . Ⅱ,某研究小组通过控制反应条件,在三个容积均为2L的密闭容器中只发生反应i,起始反应温度均为T℃,起始投料如下表所示: (3)比较平衡时容器1中c1(H2O)和容器2中c2(H2O)的大小: c1(H2O) c2(H2O)(填“>”、“<”或“=”);三个容器中反应的化学平衡常数分别记为K1、K2和K3,三者的大小关系为 .(4)若容器l中平衡时CH3OH(g)的转化率为80%,则该温度下反应i的平衡常数K= . 答案部分 1.考点: 化学平衡 试题解析: A、2min时反应达平衡,A的物质的量变化量为0.5mol﹣0.2mol=0.2mol,计算A的浓度变化量,根据v= 计算v(A)=0.05mol/(L•min); B、由图Ⅰ可知,A、B、C的物质的量变化量分别为0.2mol、0.6mol、0.4mol,化学计量数之比等于物质的量之比为0.2mol: 0.6mol: 0.4mol=1: 3: 2,反应方程式为A+3B⇌2C,增大压强,正逆反应速率都增大,平衡向体积减小方向进行,向正反应方向移动; C、由图Ⅱ可知,T1先到达平衡,故温度T1>T2,温度越高B的物质的量分数越高,升高温度正逆反应速率都增大,平衡向逆反应移动,A的转化率减小; D、浓度变化量之比等于化学计量数之比,故若A的浓度减少了1mol/L,则B的浓度会减少为2×1mol/L=3mol/L,C的浓度会增加为2×1mol/L=2mol/L; 答案: D 2.考点: 化学反应热的计算 试题解析: 解: 已知①2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=﹣Q1kJ/mol, ②2H2S(g)+O2(g)=2S(s)+2H2O(l)△H=﹣Q2kJ/mol, ③2H2S(g)+O2(g)=2S(s)+2H2O(g)△H=﹣Q3kJ/mol, ①与②相比较,由于S→SO2放热,则Q1>Q2, ②与③相比较,由于H2O(l)→H2O(g)吸热,则Q2>Q3, 则Q1>Q2>Q3, 故选A. 答案: A 3.考点: 影响化学反应速率的因素 试题解析: 化学反应无论是吸热反应还是放热反应,温度升高,活化分子的百分含量增大,有效碰撞的次数增大,化学反应速率都增大. 故选B. 答案: B 4.考点: 化学反应热的计算 试题解析: 燃烧热是可燃物完全燃烧,生成1mol的稳定氧化物放出的热量。 放热△H为负数,正确答案B。 答案: B 5.考点: 化学平衡化学反应进行的方向 试题解析: 平衡时生成NO为(C0-C1),依据平衡常数的定义, ,A正确;反应前后气体的质量、体积都木改变,其混合气的密度不变,B错误;曲线b虽然平衡时间短,但转化的氮气也增加,其改变条件不可能是使用了催化剂,C错误;D没有说明是升高或降低温度,无法判断△H大小。 答案: A 6.考点: 化学反应热的计算 试题解析: 可设两个反应分别是①和②,利用盖斯定律,②-①×2得: 2H2(g)+O2(g)=2H2O(g)△H=(2a+220)KJ/mol,依题意: 2a+220=2×436+496—4×462,解得: a=+130KJ/mol,答案选D。 答案: D 7.考点: 化学反应速率 试题解析: A、反应速率只能表示平均速率不能表示瞬时速率,反应在tlmin内的平均速率为v(H2)=0.2/t1mol·L-1·min-1,错;B、由表中的数据可知t2时刻一定达到平衡状态,则水蒸气的平衡转化率=(0.4/0.6)×100%=66.67%,对;C、根据方程式可知K=c(CO2)·c(H2)/c(CO)·c(H2O)=(0.2×0.2)/(0.4×0.1)=1,对;D、温度不变,平衡常数不变,设反应平衡时水蒸气的反应了xmol,则产物的物质的量也为xmol,代入平衡常数表达式得x=0.4,又n(H2O)=1.20mol,通过计算即可得到答案,对。 答案: A 8.考点: 化学平衡化学反应热的计算 试题解析: 根据c(B)=1.6mol·L-1,n(B)=3.2mol,看图可推知n(A)=1.6mol,根据三步法计算可知 2A(g) B(g)+C(g) 开始 x 0 0 变化 x-1.6 3.2 3.2 平衡 1.6 3.2 3.2 可以计算出x=8mol,B错误;K= =4,A错误;A的转化率为(8-1.6)/8=80%,D正确;到达平衡生成B是3.2mol,放出的热量是3.2×48.25=154.4kJ,C错误。 答案: D 9.考点: 化学反应速率 试题解析: 加入催化剂反应速率加快,达平衡时间缩短,但不影响转化率,即.②④⑤⑦正确。 答案: A 10.考点: 化学反应与能量变化 试题解析: A.将充满NO2的密闭玻璃球浸泡在热水中,红棕色变深,说明升高温度反应N2O4(g) 2NO2(g)平衡正反应方向移动,因此△H>0,故A错误; B.由于NaOH与HCl溶
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 选修4 高中化学 选修 单元测试 难度 系数 070056
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
