 专题05 非金属及其化合物原卷版.docx
专题05 非金属及其化合物原卷版.docx
- 文档编号:5900724
- 上传时间:2023-01-02
- 格式:DOCX
- 页数:24
- 大小:550.21KB
专题05 非金属及其化合物原卷版.docx
《专题05 非金属及其化合物原卷版.docx》由会员分享,可在线阅读,更多相关《专题05 非金属及其化合物原卷版.docx(24页珍藏版)》请在冰豆网上搜索。
专题05非金属及其化合物原卷版
专题05非金属及其化合物
【学习目标】
1.了解硅单质、氯单质、硫单质、氮单质及其重要化合物的主要性质及应用。
2.了解氯元素、氮元素、硫元素及其重要化合物对环境质量的影响。
3.掌握氯气、氨气、二氧化硫的实验室制法。
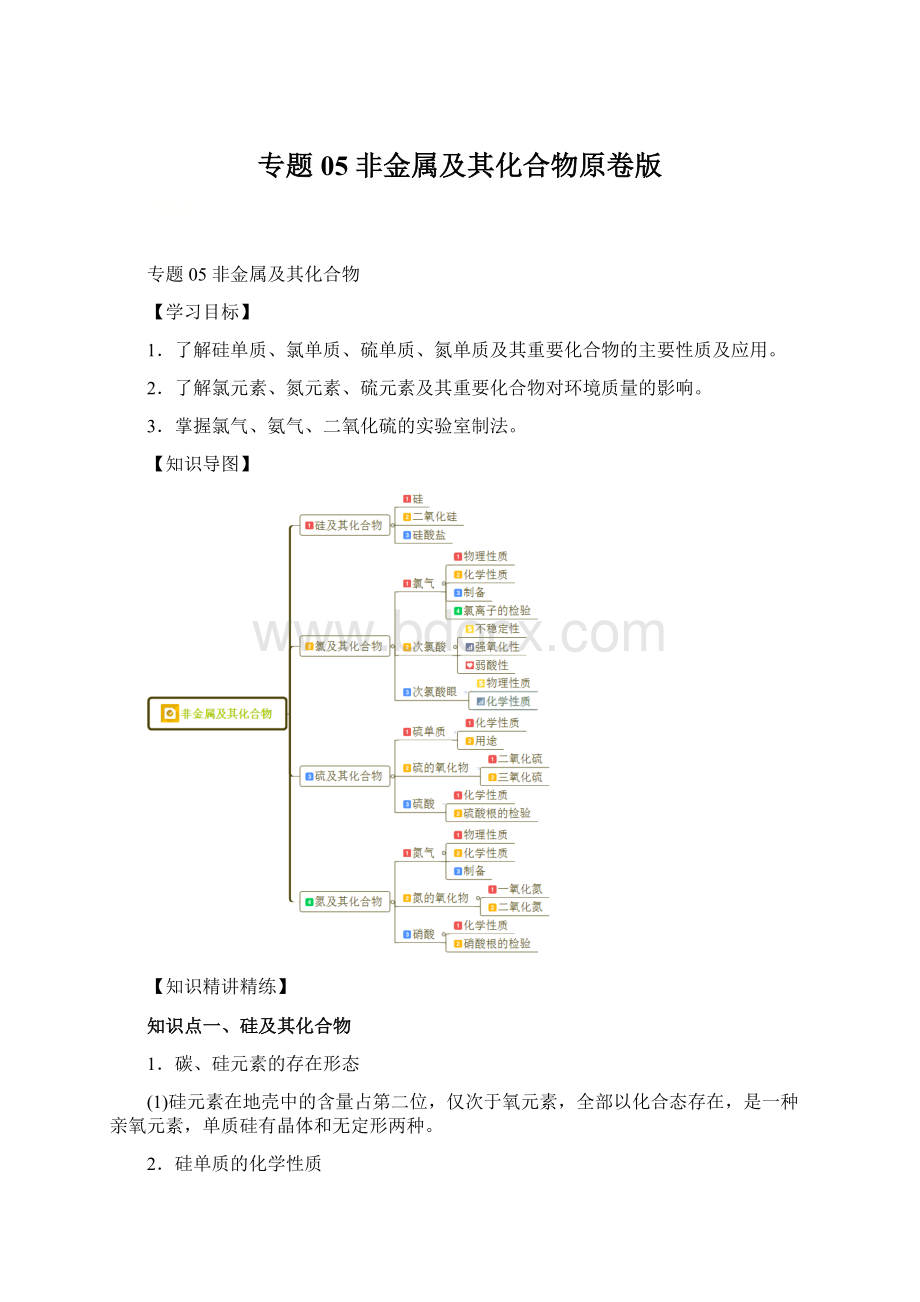
【知识导图】
【知识精讲精练】
知识点一、硅及其化合物
1.碳、硅元素的存在形态
(1)硅元素在地壳中的含量占第二位,仅次于氧元素,全部以化合态存在,是一种亲氧元素,单质硅有晶体和无定形两种。
2.硅单质的化学性质
1、___________________________________
2、___________________________________
3、___________________________________
4、___________________________________
5、___________________________________
6、___________________________________
7、___________________________________
8、___________________________________
9、___________________________________
10、___________________________________
11、___________________________________
(1)与Cl2反应:
Si+2Cl2
SiCl4
(2)硅的工业制法:
________________________________________________________________
提醒:
①自然界中没有游离态硅,工业上常用焦炭在电炉中还原SiO2得到粗硅。
②Si的还原性强于C,但C能还原SiO2生成Si,且氧化产物为CO:
2C+SiO2
Si+2CO↑,其原因是产物CO为气体,它的放出降低了生成物浓度,促使反应向正反应方向进行。
且该反应必须在隔绝空气的条件下进行。
3.硅单质的结构、物理性质与用途
硅
结构
晶体硅:
与金刚石类似的空间网状结构
物理性质
晶体硅为灰黑色固体,有金属光泽、硬度大、熔点高
用途
晶体硅用作半导体材料,制造硅芯片和硅太阳能电池
4.二氧化碳和二氧化硅的比较
物质
二氧化硅
结构
空间立体网状结构,不存在单个分子
主要物理性质
硬度大,熔、沸点高,常温下为固体,不溶于水
化
学
性
质
水
不反应
酸
只与氢氟酸反应:
SiO2+4HF===SiF4↑+2H2O
碱
SiO2+2NaOH===Na2SiO3+H2O(盛碱液的试剂瓶用橡胶塞)
盐
如与Na2CO3反应:
SiO2+Na2CO3
Na2SiO3+CO2↑
碱性氧化物
如与CaO反应:
SiO2+CaO
CaSiO3
用途
光导纤维、光学仪器、电子部件
提醒:
①SiO2是酸性氧化物,与碱反应生成盐和水;但SiO2不溶于水,故不能用SiO2与水反应制备硅酸。
②SiO2不能与盐酸、硝酸、硫酸等酸反应,但能与氢氟酸反应。
③不能依据反应SiO2+Na2CO3
Na2SiO3+CO2↑说明SiO2对应的水化物(即H2SiO3)的酸性比H2CO3强。
5.硅酸、硅酸盐、无机非金属材料
1.硅酸
2.硅酸盐
(1)Na2SiO3水溶液俗称水玻璃,常用于制作黏合剂、防腐剂和耐火材料。
3.常见无机非金属材料
(1)传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
例1.(2019•红岗区校级一模)下列说法正确的是( )
A.因为HF与SiO2反应,故用氢氟酸在玻璃器皿上刻蚀标记
B.下列转化在一定条件下能够实现:
SiO2
SiCl4
Si
C.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
D.Si和SiO2都用于制造光导纤维
练习1.(2019•安徽一模)化学无处不在,下列说法不正确的是( )
A.硅既可制作光导纤维,也可制作电脑芯片
B.乙酸既可做调味剂,也可除水垢
C.氢氧化铝既可做阻燃剂,也可治疗胃酸过多
D.食盐既可做融雪剂,也可做防腐剂
练习2.(2019•南开区三模)化学与生活密切相关。
下列叙述不正确的是( )
A.二氧化硅是将太阳能转变为电能的常用材料
B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
C.使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力差
D.汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏土
练习3.(2019•濮阳二模)化学与社会、生活密切相关。
下列说法正确的是( )
A.人造太阳中热核聚变产生的核能不属于新能源
B.地沟油和矿物油的主要成分都是不饱和烃
C.光伏高速公路中使太阳能转化为电能的特殊材料为单质硅
D.铁粉和生石灰均可用作食品中的抗氧化剂
练习4.(2019•安徽一模)新型光电材料多孔硅是通过电化学腐蚀单晶硅片的方法形成的,下列说法不正确的是( )
A.反应不能在玻璃容器中进行B.Si电极的反应式:
Si+4HF+4e﹣=SiF4+4H+
C.制备过程需要采用微电流减慢反应速率D.硅电极凹面内的硅原子更易氧化形成空洞
练习5.(2019•西湖区校级模拟)下列说法不正确的是( )
A.干冰可用于人工降雨B.单质硅可用于制取普通玻璃
C.硫酸铜可用于游泳池消毒D.氧化铁可用于制作颜料
知识点二、氯及其化合物
1.氯气的性质
1.物理性质
2.化学性质
1._____________________________________________________
2._____________________________________________________
3._____________________________________________________
4._____________________________________________________
5._____________________________________________________
6._____________________________________________________
7._____________________________________________________
8._____________________________________________________
9._____________________________________________________
10._____________________________________________________
11._____________________________________________________
12._____________________________________________________
13._____________________________________________________
14._____________________________________________________
(1)与非金属反应。
与H2反应:
H2+Cl2
2HCl,
(2)与还原性无机化合物反应。
①与碘化钾溶液反应:
_________________________________。
②与SO2水溶液反应:
_________________________________。
③与FeCl2溶液反应:
离子方程式为_________________________________。
提醒:
①Cl2可使湿润的有色布条褪色,不能使干燥的有色布条褪色,说明Cl2没有漂白性,而是HClO起漂白作用。
②Cl2可使湿润石蕊试纸先变红后褪色,原因是Cl2与水反应生成的酸使石蕊先变红,HClO使变色后的石蕊褪色。
③常温下液态氯与铁不反应,故可用钢瓶贮运液氯。
2.氯的重要化合物
(1)次氯酸
(2)漂白粉
提醒:
①HClO不稳定,不能单独存在,只存在于氯水、次氯酸盐溶液或次氯酸盐与酸反应的混合物中。
②不能用pH试纸测量氯水的pH,原因是氯水中的HClO具有漂白性。
③工业上制取漂白粉是用氯气与石灰乳反应制得,而不是用氯气与石灰水反应。
④“84”消毒液的主要成分为NaClO,漂粉精的有效成分为Ca(ClO)2。
“84”消毒液和洁厕灵不能混合使用,其原因是ClO-+Cl-+2H+===Cl2↑+H2O。
3.氯水的成分及性质的多样性
1.氯水成分的多样性
(1)组成微粒——三分子:
Cl2、H2O、HClO,四离子:
H+、Cl—、ClO—、OH—
(2)三个平衡。
Cl2+H2O
HClO+HCl、HClO
H++ClO-、H2O
H++OH-。
2.氯水性质的多重性
新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反应的微粒不同。
所加试剂
参与反应的微粒
实验现象
离子方程式或解释
AgNO3溶液
Cl-
白色沉淀
Cl-+Ag+==AgCl↓
Na2CO3固体
H+
有气泡产生
2H++CO32-==CO2↑+H2O
有色布条
HClO
布条颜色褪去
发生氧化还原反应
FeCl2溶液
Cl2
溶液变棕黄色
2Fe2++Cl2==2Fe3++2Cl-
石蕊溶液
HClO、H+
先变红后褪色
酸性和漂白性
镁粉
Cl2、H+
氯水的颜色褪去并有气泡产生
Mg+Cl2==Mg2++2Cl-
Mg+2H+==Mg2++H2↑
4、氯气的实验室制法及性质的实验探究
1774年瑞典化学家舍勒制取了氯气。
1.原理:
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
2.发生装置:
固+液加热型
3.净化:
将气体通过盛有饱和食盐水的洗气瓶
4.干燥:
将气体通过盛有浓硫酸的洗气瓶
5.收集:
用向上排空气法或排饱和食盐水法。
6.尾气吸收:
用NaOH溶液吸收多余的氯气,防止污染空气。
7.验满方法
①将湿润的淀粉-KI试纸靠近盛Cl2的瓶口,观察到试纸立即变蓝,则证明已集满。
②将湿润的蓝色石蕊试纸靠近盛Cl2的瓶口,观察到试纸先变红后褪色,则证明已集满。
5.卤离子的检验
(1)AgNO3溶液——沉淀法:
未知液
生成
(2)置换——萃取法:
未知液
有机层呈
(3)氧化——淀粉法检验I-:
未知液
蓝色溶液,表明有I-
例1.(2019•西湖区校级模拟)下列关于氯水性质现象的描述和相关解释正确的是( )
操作
现象
解释
A
将氯水加入紫色石蕊试液中
石蕊试液先变红色后褪色
氯水中有H+
B
氯水中加入硝酸银溶液
产生白色沉淀
氯水中Cl﹣
C
氯水中加入碳酸钠溶液
产生气体
氯水中HClO
D
氯水中加入有色布条
有色布条褪色
氯水中有Cl2
A.AB.BC.CD.D
练习1.(2019•浙江模拟)不能与CuBr2溶液发生反应的是( )
A.AgNO3溶液B.FeCl3溶液C.氨水D.新制氯水
练习2.(2019•西湖区校级模拟)下列物质与其用途相符合的是( )
①Cl2﹣制消毒剂②碘﹣预防甲状腺肿大③AgI﹣人工降雨④AgBr﹣制胶卷,感光纸
⑤淀粉﹣检验I2的存在⑥NaClO﹣漂白纺织物
A.②③④⑤⑥B.①②③④⑤C.②③④⑤D.全部
练习3.(2019•西湖区校级模拟)下列试剂中不能使淀粉﹣KI试纸变色的是( )
A.AgNO3溶液B.溴水C.FeCl3溶液D.SO2气体
练习4.(2019•青浦区二模)将氯气持续通入紫色石蕊试液中,溶液颜色呈如下变化:
关于溶液中导致变色的微粒Ⅰ、Ⅱ、Ⅲ的判断正确的是( )
A.H+、HClO、Cl2B.H+、ClO﹣、Cl﹣C.HCl、ClO﹣、Cl﹣D.HCl、HClO、Cl2
练习5.(2019•海淀区模拟)某化学实验兴趣小组的同学从海带中提取碘单质的实验流程图如下:
依据实验下列说法不正确的是( )
A.从上述实验可以得出海带中含有可溶性的含碘化合物
B.步骤⑤中可能发生的反应为:
5I﹣+IO3﹣+6H+═3I2+3H2O
C.若步骤④中用CCl4做萃取剂,步骤⑥应取上层溶液得到后续的混合物C
D.整个过程中的操作是利用了物质的溶解性实现了碘元素的富集、分离与提纯
练习6.(2019•潍坊一模)某化学学习小组用如图所示装置制备、收集Cl2,并进行性质验证实验(夹持装置略去)。
下列说法正确的是( )
A.用KMnO4和浓盐酸制备Cl2时,只选①
B.③用于Cl2收集时,a为进气口
C.④中加入NaBr溶液和CCl4,通入Cl2反应后振荡、静置,下层溶液呈橙红色
D.⑤中通入Cl2使品红溶液褪色后,取出溶液加热可恢复红色
练习7.(2019•广东模拟)某同学取海带灰加蒸馏水意沸2~3min,冷却,过滤,获得含I﹣的溶液,并设计以下实验方案从中提取I2。
下列说法中错误的是( )
A.试剂b可能是CCl4B.“I2的悬浊液→粗碘”需萃取
C.“下层溶液”可在流程中循环利用D.反应1、反应2、反应3都是氧化还原反应
知识点三、硫及其化合物
1.单质硫在自然界中的的存在。
游离态的硫:
存在于火山口附近或地壳的岩层里。
化合态的硫:
主要以硫化物和硫酸盐的形式存在。
如硫铁矿(FeS2)、黄铜矿(CuFeS2)、石膏(CaSO4·2H2O)等。
硫还存在于石油、天然气、煤等化石燃料中。
硫的物理性质:
单质硫的颜色是黄色,非常脆,容易粉碎;熔点比较低,稍微受热,就会熔化成液体;硫蒸气的颜色也是黄色;硫单质的溶解性比较特殊:
不溶于水,微溶于酒精,易溶于二硫化碳(CS2是一种有机物)。
2.硫的化学性质
1、___________________________________________________________
2、___________________________________________________________
3、___________________________________________________________
4、___________________________________________________________
5、___________________________________________________________
6、___________________________________________________________
7、___________________________________________________________
8、___________________________________________________________
9、___________________________________________________________
10、___________________________________________________________
11、___________________________________________________________
12、___________________________________________________________
13、___________________________________________________________
14、___________________________________________________________
15、___________________________________________________________
16、___________________________________________________________
17、___________________________________________________________
18、___________________________________________________________
19、___________________________________________________________
20、___________________________________________________________
提醒:
①实验室中,残留在试管内壁上的硫可用CS2溶解除去,也可用热的NaOH溶液除去,反应化学方程式为3S+6NaOH∆2Na2S+Na2SO3+3H2O。
②硫单质的氧化性较弱,与变价金属反应时一般生成低价态金属硫化物(和Cl2与变价金属的反应情况相反),如FeS、Cu2S等。
③汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
④单质硫燃烧时,产物只能是SO2,无论O2的量是否充足,均不会生成SO3。
2.二氧化硫
物理性质
颜色
气味
毒性
密度
溶解性
无色
刺激性
有毒
比空气大
易溶于水
提醒:
①SO2不能漂白酸碱指示剂,如只能使紫色的石蕊试液变红,但不能使之褪色,只能漂白品红溶液。
②SO2能使溴水、酸性KMnO4溶液褪色,体现了SO2的还原性,而不是漂白性。
③SO2可以与有色的有机物生成不稳定的无色化合物,受热又可以分解得到原物质,因此SO2漂白作用不持久。
3.三氧化硫
物理性质:
熔点16.8℃,沸点44.8℃,在常温下为液态,在标准状况下为固态。
4.浓硫酸的性质
(1).硫酸的物理性质
H2SO4是无色油状液体,能与水以任意比互溶,溶解时可放出大量的热,浓H2SO4稀释的方法是将浓H2SO4沿烧杯内壁缓缓倒入水中并用玻璃棒不断搅拌。
(2).稀硫酸的化学性质
硫酸是强电解质,在水溶液中发生电离的化学方程式为H2SO4===2H++SO
,具有酸的通性。
(3).浓H2SO4的特性
实验
实验现象
硫酸的特性
少量胆矾加入浓硫酸中
蓝色固体变白
吸水性
用玻璃棒蘸取浓硫酸滴在滤纸上
沾有浓H2SO4的滤纸变黑
脱水性
将铜片加入盛有浓硫酸的试管中加热
铜片逐渐溶解,产生无色刺激性气味的气体
强氧化性
(2)分别写出浓硫酸与Cu、C反应的化学方程式:
Cu+2H2SO4(浓)∆CuSO4+SO2↑+2H2O、C+2H2SO4(浓)∆CO2↑+2SO2↑+2H2O。
(3)常温下,铁、铝遇浓H2SO4
可用铝槽车运浓H2SO4。
提醒:
①浓硫酸能氧化(必要时加热)除Au、Pt以外的所有金属,其还原产物是SO2而不是H2。
②常温下,浓硫酸与Fe、Al并不是不反应,而是发生了“钝化”,“钝化”是浓硫酸将Fe、Al氧化而在其表面形成一层致密的氧化物薄膜,阻止了浓硫酸与Fe、Al的继续反应,体现了浓硫酸的强氧化性。
③浓硫酸的吸水性和脱水性。
吸水性:
浓硫酸能吸收物质中游离的水,可用作干燥剂。
脱水性:
浓硫酸可将有机物中的H、O以2∶1比例脱去。
5.硫酸根离子的检验
检验SO42-的正确操作方法:
被检液
取清液
观察有无白色沉淀(判断有无SO42-)
先加稀盐酸的目的是防止CO32-、SO32-、Ag+干扰,再加BaCl2溶液,有白色沉淀产生,可能发生反应的离子方程式:
CO32-+2H+===CO2↑+H2O、SO32-+2H+===SO2↑+H2O、Ag++Cl-===AgCl↓、Ba2++SO42-===BaSO4↓。
例1.(2019•邵阳三模)某化学课题小组将二氧化硫的制备与多个性质实验进行了一体化设计,实验装置如图所示。
下列说法不正确的是( )
A.a、b、c中依次盛装70%硫酸、Na2SO3固体、NaOH溶液
B.此设计可证明SO2水溶液的酸性,SO2气体的氧化性、还原性、漂白性
C.SO2使KMnO4溶液褪色的原理:
5SO2+2MnO4﹣+2H2O═2Mn2+5SO42﹣+4H+
D.实验时,湿润的pH试纸、鲜花、品红溶液、KMnO4溶液均褪色
练习1.(2019•静安区二模)为验证SO2的相关性质,所选用试剂错误的是( )
A.漂白性﹣﹣品红溶液B.氧化性﹣﹣饱和Na2SO3溶液
C.酸性﹣﹣滴有酚酞的NaOH溶液D.还原性﹣﹣酸性KMnO4溶液
练习2.(2019•西湖区校级模拟)下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( )
A.在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性)
B.浓硫酸可用来干燥某些气体(吸水性)
C.蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性)
D.在加热的条件下铜与浓硫酸反应(脱水性)
练习3.(2019•崇明区二模)如图所示,将大烧杯丙扣在甲乙两个小烧杯(口向上)上。
向两个小烧杯中分别装入如下表所列的试剂进行实验。
实验现象与预测现象不同的是( )
甲中试剂
乙中试剂
预测现象
A
浓盐酸
硝酸银溶液
乙中产生白色沉淀
B
浓氨水
硫酸铁溶液
乙中产生红褐色沉淀
C
浓盐酸
浓氨水
丙中产生白色烟雾
D
氯化铝溶液
浓氨水并加入
固体氢氧化钠
甲中先产生白色沉淀,后又沉淀消失
A.AB.BC.CD.D
练习4.(2019•湖北模拟)某学习小组设计用98%的浓硫酸制取SO2并验证其部分性质的实验装置图如下(夹持装置省略)。
下列叙述不正确的是( )
A.装置A中发生的离子反应方程式为:
2H++SO32﹣═SO2↑+H2O
B.若装置B中装有品红溶液,观察到B中溶液红色褪去,则说明SO2具有漂白性
C.若装置B中装有酸性高锰酸钾溶液,观察到B中溶液褪色,则说明SO2具有还原性
D.装置C产生的白色沉淀为BaSO4
练习5.(2019•北京)化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。
Ⅰ、用已准确称量的KBrO3固体配制一定体积的amol•L﹣1KBrO3标准溶液;
Ⅱ、取v1mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色;
Ⅲ、向Ⅱ所得溶液中加入v2mL废水;
Ⅳ、向Ⅲ中加入过量KI;
Ⅴ、用bmol•L﹣1Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v3mL。
已知:
I2+2Na2S2O3═2NaI+Na2S4O6
Na2S2O3和Na2S4
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 专题05 非金属及其化合物原卷版 专题 05 非金属 及其 化合物 原卷版
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
