 无机化工生产技术教案头.docx
无机化工生产技术教案头.docx
- 文档编号:8160029
- 上传时间:2023-01-29
- 格式:DOCX
- 页数:95
- 大小:239.81KB
无机化工生产技术教案头.docx
《无机化工生产技术教案头.docx》由会员分享,可在线阅读,更多相关《无机化工生产技术教案头.docx(95页珍藏版)》请在冰豆网上搜索。
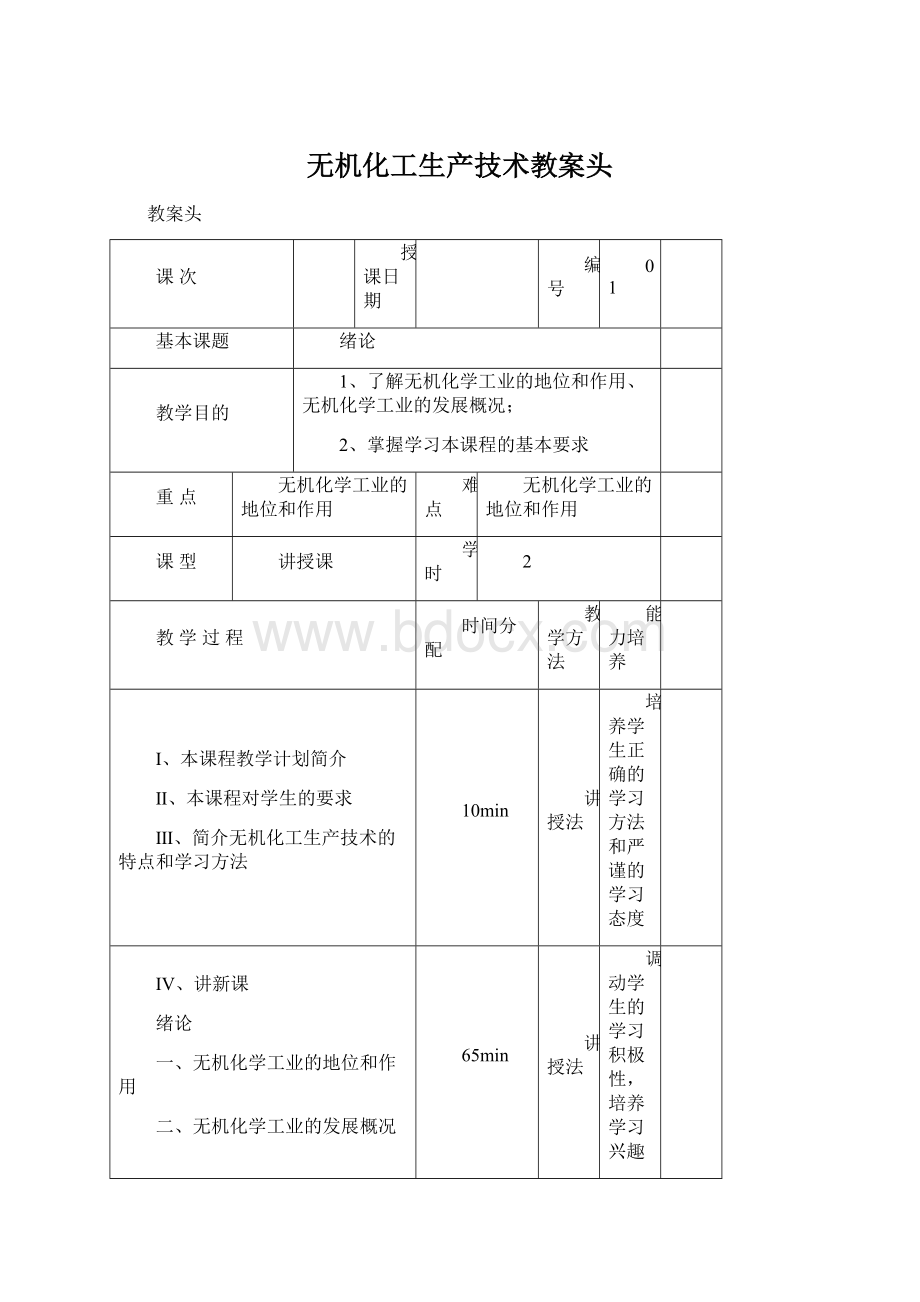
无机化工生产技术教案头
教案头
课次
授课日期
编号
01
基本课题
绪论
教学目的
1、了解无机化学工业的地位和作用、无机化学工业的发展概况;
2、掌握学习本课程的基本要求
重点
无机化学工业的地位和作用
难点
无机化学工业的地位和作用
课型
讲授课
学时
2
教学过程
时间分配
教学方法
能力培养
Ⅰ、本课程教学计划简介
Ⅱ、本课程对学生的要求
Ⅲ、简介无机化工生产技术的特点和学习方法
10min
讲授法
培养学生正确的学习方法和严谨的学习态度
Ⅳ、讲新课
绪论
一、无机化学工业的地位和作用
二、无机化学工业的发展概况
65min
讲授法
调动学生的学习积极性,培养学习兴趣
三、学习本课程的基本要求
15min
讲授法
培养与训练学生学习本课程的基本要求
课后记:
教学过程
一、本课程教学计划简介、对学生的要求;及无机化工生产技术的特点和学习方法
二、讲授新课
一、典型无机化工产品在国民经济中的重要地位及其发展概况
(一)合成氨堪称现代化学工业的领头羊
(二)硫酸曾被誉为“工业之母”
(三)硝酸唯一兼有强酸性和强氧化性
(四)化学肥料是现代农业的基石
(五)纯碱与烧碱是重要的基本化工原料
无机盐是化学工业的基础
典型无机化工产品主要包括合成氨、化学肥料、硫酸与硝酸、纯碱与烧碱、主要无机盐等五个方面。
都属于大宗化学品和典型无机化工产品。
本书重点介绍典型无机化工产品的生产原理、生产原料路线选择、工艺流程组织、生产运行与操作条件的优化,以及典型设备选型、操作控制要点及常见故障排除措施等
典型无机化工产品概况。
一般认为,现代化学工业的标志----1913年德国的哈伯和博施首次采用铁为催化剂、直接以氢气和氮气为原料、在高温高压下成功合成氨。
划时代意义的人工固氮技术的重大突破。
合成氨工业化被公认为化学方面最重要的发明之一和对高压化学合成技术上作出的重大贡献,哈伯和博施先后分别于1918年和1931年荣获诺贝尔化学奖。
这种直接合成氨法称为哈伯-博施法。
合成氨工业化的成功极大地促进了高压机生产技术、高压化学合成技术和催化剂生产技术的发展,使德国一跃成为当时世界工业强国。
我国合成氨工业发展现状
硫酸产量与合成氨相当,工业化生产已有270年历史,曾被誉为“工业之母”。
化肥工业中,每生产一吨硫酸铵,就要消耗纯硫酸760kg。
每生产一吨过磷酸钙,消耗硫酸360kg;
农药方面如硫酸铜、硫酸锌是植物的杀菌剂,硫酸铊可作杀鼠剂,硫酸亚铁、硫酸铜可作除莠剂;
冶金工业中电解液就需要使用硫酸;
石油工业中每吨原油精炼需要硫酸约24kg,每吨柴油精炼需要硫酸约31kg;
化学纤维每生产1t环氧树脂,需用硫酸2.68t,号称“塑料王”的聚四氟乙烯,每生产1t,需用硫酸1.32t;
硫酸曾被誉为“工业之母”
染料工业几乎没有一种染料(或其中间体)的制备不需使用浓硫酸或发烟硫酸。
浓硫酸为浓缩硝酸生产中的脱水剂;
氯碱工业中,以浓硫酸干燥氯气、氯化氢;
无机盐工业中,如冰晶石、氟化铝、硼砂、磷酸三钠、磷酸氢二钠、硫酸铅、硫酸锌、硫酸铜、硫酸亚铁以及其他硫酸盐的制备;
许多无机酸和有机酸的制备,也常需要硫酸作原料。
此外,电镀业、制革业、颜料工业、橡胶工业、造纸工业、工业炸药和铅蓄电池制造业等等,都消耗相当数量的硫酸。
我国硫酸工业发展现状
1t硫磺可以生产3t硫酸,2t蒸气,336度电量,且无三废排放,良好的生产环境与经济效益是硫磺法生产硫酸得到快速发展最主要的因素。
近几年来,随着我国有色金属工业的迅猛发展,冶炼烟气制酸也获得快速发展,铜陵有色、江西铜业、甘肃金川等硫酸产量在100万t/a以上的特大型企业,均以冶炼烟气制酸为主,2008年我国烟气吸收法制酸已占24%。
硫酸装置的大型化、规模化、集约化发展取得了巨大进步。
将进一步淘汰4万t/a的硫铁矿制酸装置,限制10万t/a硫铁矿制酸装置,硫酸企业有望向“能源工厂”转变,实现以硫资源为主线,以能源循环为辅线,实现了以硫酸为核心的循环经济。
硝酸兼有强酸性和强氧化性的特点,各类酸中产量仅次于硫酸的重要化工原料;
主要用于无机化工制造硝酸铵、硝酸铵、硝酸磷肥、氨磷钾等复合肥料。
在有机工业、染料工业、涂料工业、医药工业、印染工业、橡胶工业、塑料工业、冶金工业中和国防工业等也有广泛用途。
硝酸唯一兼有强酸性和强氧化性
我国硝酸工业发展现状
至2008年底我国已拥有先进的双加压法工艺的硝酸生产装置20套,占我国硝酸总产能的50%,大大缩短了我国与世界先进水平的差距。
但我国还不算是硝酸工业强国,世界发达国家均普遍采用27万t级和50万t级硝酸装置,我国年产27万t双加压法完全国产化硝酸装置目前国内仅有几家企业正在筹建,随着取缔和关闭落后生产装置,淘汰配置低、规模小、能耗高的装置,我国硝酸工业正在向规模化发展
化肥是农作物增产增收的物质基础,粮食的“粮食”。
化肥对我国粮食单产增长的贡献率高达40%~50%。
使用化肥以提高粮食单产,已经成为确保全球粮食安全的关键和现代农业的基石。
中国能以世界7%的耕地养活占世界约22%的人口,应该说一半功劳归于化肥。
另外一半功劳呢?
化学肥料是现代农业的基石
建国初我国化肥工业只有硫酸铵和硝酸铵两个品种,年产量6000t。
目前我国化肥生产量约占世界总量的约1/3,表观消费量约占35%,世界上最大的化肥生产国和消费国。
一是化肥工业的基本特征是“多氮少磷缺钾”;
二是高浓度化肥比例低。
为什么?
三是复合肥料比例低。
⑴纯碱。
建材方面主要用于制造玻璃,这是纯碱的最大消费部门,每t玻璃消耗纯碱0.2t。
在轻工方面:
洗衣粉、三聚磷酸钠、保温瓶、灯泡、白糖、搪瓷、皮革、日用玻璃、造纸等;
在化工方面:
制取钠盐、金属碳酸盐、小苏打、硝酸钠、亚硝酸钠、硅酸钠、硼砂、漂白剂、填料、洗涤剂等;
冶金工业:
冶炼助熔剂、选矿用浮选剂、炼钢和炼锑用作脱硫剂;
在陶瓷工业中制取耐火材料和釉也要用到纯碱;
印染工业用作软水剂;
制革工业用于原料皮的脱脂、提高铬鞣液碱度;
食用级纯碱用于生产味精、面食等。
纯碱与烧碱是重要的无机碱性化工原料
我国纯碱工业发展现状
氨碱法/%
联碱法/%
2008年我国纯碱企业平均年产量37.34万吨。
氨碱法路线的山东海化集团有限公司的年产能为300万吨;
联碱法的湖北双环化工集团有限公司年产能为100万吨。
但在节能减排方面与世界先进水平仍有较大差距。
例如:
氨碱企业,液氨平均消耗大于4.5kg/t碱,是世界最好水平的1.5-2倍;制碱装备运行周期和稳定性低于国外;自控技术水平参差不齐,劳动效率低下;能源消耗偏高等。
⑵烧碱
使用烧碱最多的部门是化学药品制造;
其次是造纸、炼铝、炼钨、人造丝、人造棉和肥皂制造业。
在生产染料、塑料、药剂及有机中间体,旧橡胶再生;
无机盐生产中,制取硼砂、铬盐、锰酸盐、磷酸盐等,也要使用大量的烧碱。
如普通肥皂;
造纸行业主要是制浆耗碱,烧碱起苛化作用;
印染、纺织工业上,用大量碱液去除棉纱、羊毛的油脂;
生产人造纤维也需要烧碱或纯碱。
例如,制粘胶纤维首先要用18~20%烧碱溶液(或纯碱溶液)去浸渍纤维素,使它成为碱纤维素。
我国烧碱工业发展现状
隔膜法/%
离子膜法/%
氯产品
数量
盐酸、液氯
、漂白粉
等几种
200余种,
主要品种
70多个
我国最早的氯碱工厂是1930年投产的上海天原电化厂,日产烧碱2t。
离子交换膜法制碱技术,具有设备占地面积小、能连续生产、生产能力大、产品质量高、能适应电流波动、能耗低、污染小等优点,是氯碱工业发展的方向。
目前我国隔膜法烧碱占55%,离子膜法烧碱占45%。
氯碱工业企业平均生产规模7.9万t/a;
大多数企业的规模较小,日本、欧盟的前5家企业分别集中了它们烧碱生产能力的50%,美国的5家大公司80%,而我国前5家企业不到全国总生产能力的16%。
教案头
课次
授课日期
编号
02
基本课题
煤气化
教学目的
1、熟练掌握煤气化的基本原理、工艺条件的选择及工艺流程;
2、了解煤气化的反应机理及动力学方程;
重点
煤气化的基本原理、工艺条件的选择及工艺流程;
难点
煤气化的基本原理、工艺条件的选择及工艺流程
课型
讲授课
学时
2
教学过程
时间分配
教学方法
能力培养
Ⅰ、复习上次课内容
10min
提问法
温故知新
Ⅱ、讲新课
第一章合成氨原料气的生产
第一节煤气化
一、气化原理
二、制取半水煤气的工业方法
三、间歇式生产半水煤气
40min
讲授法
使学生具有识读和绘制生产工艺流程图的初步能力
四、煤间歇法制气原始开车的基本步骤——化工生产操作之一
五、氧—蒸汽连续气化法
Ⅲ、作业P421.2.3
40min
讲授法
使学生具有编制开停车方案的初步能力
课后记:
教学过程
一、简介
1.以焦炭或煤为原料,在一定的高温条件下通入空气、水蒸气或富氧空气-水蒸汽混合气,经过一系列反应生成含有CO、CO2、H2、N2及CH4等混合气体。
2.气化过程中所使用的空气、水蒸气或富氧空气-水蒸汽混合气等称为气化剂。
气化过程所得到的混合气体,称为煤气。
3.用于实现煤气化过程的主要设备称为煤气发生炉。
4.煤气的成分取决于燃料和气化剂的种类及气化工艺条件。
二、煤气化的原理
⑴吹风反应
以一定量的空气或富氧空气为气化剂,碳和氧之间发生剧烈放热反应,为制气反应提供能量,也称吹风反应。
其主要反应如下:
C+O2==CO2-393.777kJ/mol(主反应)(2-1)
C+CO2==2CO+172.28kJ/mol(2-2)
2C+O2==2CO-221.189kJ/mol(2-3)
⑵制气反应
炽热的碳将氢从水蒸气中还原出来,在煤气生产中称之为蒸汽分解,主要还原反应:
C+H2O(g)==CO+H2131.390kJ/mol(主反应)
C+2H2O(g)==CO2+H290.196kJ/mol
C+2H2==CH4-74.90kJ/mol
该反应是吸热反应,产物是水煤气,是半水煤气的有效成分
⑶其他副反应
在燃料气化过程中,副反应,产生少量或微量的H2S和有机硫化物、氰化物、氨等杂质组分。
四、半水煤气生产的特点
半水煤气的特征:
(CO+H2)/N2=3.1~3.2;
从气化系统的热平衡来看,吹风反应是放热反应,制气反应是吸热反应,如果外界不提供热源,而是通过前者的反应热为后者提供反应所需要的热量,并维持系统的自热平衡的话,理论上,1mol氧气的吹风反应热仅可供1.68mol碳和水蒸气进行制气反应,其(CO+H2)/N2=1.43<3.1~3.2。
反之,若欲获得组成合格的半水煤气,该系统就不能维持自热平衡。
⑴间歇制气法
•在间歇式固定床煤气发生炉中,吹风反应和制气反应是交替进行的。
•首先进行吹风反应,将燃料层温度(即炉温)提到必要的温度(如1100℃~1200℃),所得吹风气大部分放空。
•吹风反应停止后,送入蒸汽进行制气反应,吸热反应,料层的温度、反应速度和水煤气质量(煤气中CO+H2含量)都将下降。
•水煤气+部分吹风气=半水煤气。
如此交替进行吹风和制气反应,故称间歇制气法。
在我国目前中小型氮肥企业、联醇企业得到广泛应用。
⑵富氧空气或纯氧连续气化法
•空气中氧气气含量过低是以空气和水蒸汽为气化剂时不能实现连续制取合格半水煤气的根本原因。
•如果采用富氧空气或纯氧来代替空气作为气化剂,以上问题将迎刃而解,并且可以实现连续制气。
•富氧空气中氧气的浓度需要多少呢?
?
?
•若(CO+H2)/N2=3.1,则富氧空气中氧气理论含量为:
1/(1+1.68)=36.6%。
•实际生产中连续气化法所需富氧空气中氧气含量约50%,此即为富氧空气-蒸汽连续气化法。
三、间歇式造气炉的工作循环
⑴吹风阶段:
空气——煤气炉底部——灰渣层——氧化层(燃烧气化反应)——还原层(CO2还原反应)——炉顶。
吹风反应提高炭层温度的同时,其中的氧气几乎被消耗殆尽,CO2还原反应吹风气中CO含量迅速增长,所以,吹风气必须经燃烧室或者集中到废热锅炉中回收显热和CO的潜热后才能放空。
⑵一次上吹阶段:
将放空阀倒换为制气阀向气柜送气。
水蒸气煤气炉底部——灰渣层——气化层(制气反应)——炉顶。
由于炉温高、气化反应速度快、蒸汽分解率较高、所得水煤气质量好,生成的水煤气经除尘和回收显热后送入气柜。
一次上吹过程中,由于水蒸气温度较低,加上制气反应大量吸热,使气化区温度显著下降,而燃料层上部却因灼热的煤气通过使温度有所上升,导致炉层热点(气化层)上移,煤气带走的显热损失显著增加,因此,在上吹制气进行一段时间后,应改变气体方向。
⑶下吹阶段:
上吹结束后,关闭下部蒸汽阀,打开上部蒸汽阀和下吹煤气阀,从炉顶自上而下送入蒸汽。
饱和蒸汽先经燃烧室预热为过热蒸汽、再经燃料层预热后到达气化区进行气化反应,同时使上层燃料层温度降低,并使炉层热点重新回到正常位置,而生成水煤气通过灰层时使灰层温度提高,有利于燃尽残碳,煤气经除尘降温后送气柜。
下吹制气阶段炉温高、蒸汽温度高、煤气质量好,所以下吹时间要长于一次上吹时间。
⑷二次上吹阶段:
下吹制气后,如果立即进行吹风,空气将与残留在炉底的下行煤气相遇,导致爆炸。
所以,为了将炉底部的下吹煤气吹净并回收送入气柜,以防止吹入空气时发生爆炸,进行二次上吹制气是必要的,其目的是回收炉底煤气和进行安全准备。
⑸空气吹净阶段:
二次上吹制气后,煤气发生炉上部空间、出气管道及有关设备都充满了煤气,如立即进行吹风阶段,不仅造成浪费,且这部分煤气排至烟囱和空气接触时也可能发生爆炸。
因此,在转入吹风之前,从炉底自下而上吹入空气,所产生的空气煤气与原来残留的水煤气一并送入气柜,这一阶段叫做空气吹净阶段。
空气吹净的主要目的是为了回收炉上部及管道中剩余的煤气,在半水煤气的生产过程中属于加氮操作,是调节氢氮比的关键步骤。
三、总结知识
四、布置作业
教案头
课次
授课日期
编号
03
基本课题
烃类制气
教学目的
1、掌握烃类蒸汽转化的基本原理、工艺条件的选择及工艺流程
2、理解甲烷蒸汽转化催化剂的组成、还原与使用,主要设备的基本结构
重点
烃类蒸汽转化的基本原理、工艺条件的选择及工艺流程
难点
烃类蒸汽转化的基本原理、工艺条件的选择及工艺流程
课型
讲授课
学时
2
教学过程
时间分配
教学方法
能力培养
Ⅰ、复习上次课内容
10min
提问法
温故知新
Ⅱ、讲新课
第二节烃类制气
一、气态烃类蒸汽转化法
40min
讲授法
使学生掌握烃类蒸汽转化的基本原理、工艺条件的选择及工艺流程
二、石脑油蒸汽转化
Ⅲ、作业P428、9、10
40min
讲授法
使学生具有节能减排、降低能耗的意识
课后记:
教学过程
一、提问上次课的知识
二、讲授新课
1.甲烷蒸汽转化反应的基本原理
CH4+H2O=CO+3H2+206kJ/mol
CH4+2H2O=CO2+4H2+165kJ/mol
CO+H2O=CO2+H2–41.19kJ/mol
•副反应主要是析炭反应
CH4=C+2H2+74.9kJ/mol
2CO=C+CO2–172.5kJ/mol
CO+H2=C+H2O–131.4kJ/mol
图不同条件下的甲烷平衡含量
2、影响因素
①温度
②压力
③水碳比
3、烃类蒸汽转化催化剂
催化剂的组成一般由活性组分、少量助催化剂和承载活性组分的载体组成。
①活性组分:
活性组分为镍(Ni),含量4~30%。
镍含量越高,催化剂活性越高。
镍以氧化镍(NiO)形式存在,使用时必须将氧化镍还原为金属镍。
②助催化剂(促进剂):
添加少许促进剂能提高催化剂的活性、稳定性和选择性。
助催化剂为金属铝、铬、镁、钛、钙等的氧化物。
③载体:
载体是活性组分镍的骨架和黏合剂,可以使镍晶体高度分散,达到较大的比表面积,防止镍晶体熔融。
常用的载体有氧化铝、氧化镁、氧化钙等,一般采用浸渍法或沉淀法将氧化镍附着在载体上。
4.工业生产的二段转化法
目前大型氨厂普遍采用。
一段转化将甲烷转化到一定程度后,再在二段转化炉中通入适量空气进一步转化。
空气和一段转化气中部分可燃气体反应,以提供转化反应所需的热量和合成氨所需的氮气。
工艺条件
①压力:
3.5~4.0MPa。
②温度:
1000℃,一、二段转化炉温差:
10~30℃。
③水碳比:
2.5~2.75。
④空间速率:
1000~2000h-1。
三、总结知识
教案头
课次
授课日期
编号
04
基本课题
原料气脱硫、一氧化碳变换
教学目的
1、熟练掌握原料气脱硫、一氧化碳变换的基本原理、工艺条件的选择集工艺流程的分析
2、理解一氧化碳变换催化剂的分类、特点、组成及使用。
重点
原料气脱硫、一氧化碳变换的基本原理、工艺条件的选择集工艺流程的分析
难点
原料气脱硫、一氧化碳变换的基本原理、工艺条件的选择集工艺流程的分析
课型
讲授课
学时
2
教学过程
时间分配
教学方法
能力培养
Ⅰ、复习上次课内容
10min
提问法
温故知新
Ⅱ、讲新课
第二章合成氨原料气的净化
第一节原料气脱硫
一、干法脱硫
二、湿法脱硫
30min
讲授法
使学生具有分析选择工艺条件的初步能力
第二节一氧化碳变换
一、基本原理
二、变换催化剂
三、工艺条件
四、工艺流程
五、变换反应器的类型
六、降低能耗的方法
七、耐硫低温变换原始开车及正常开停车的原则步骤
Ⅲ、作业P801、4、6、8
50min
讲授法
使学生具有开停车方案初步确定的能力
课后记:
教学过程
一、提问上次课的知识
二、讲授新课
第一节原料气脱硫
一、干法脱硫:
特点:
脱硫精度高、操作简便、设备简单、生产成本较高。
1.钴钼加氢-氧化锌法:
在钴钼催化剂作用下,有机硫加氢转化成无机硫;再采用ZnO脱除
CS2+H2→H2S+CH4
COS+H2→CO+H2S
ZnO+H2S→ZnS+H2O
2.氧化锌法:
原理:
利用氧化锌脱硫剂内表面积大、硫容高的特点脱硫,可直接吸收H2S及R-SH。
ZnO+H2S→ZnS+H2O
RSH+ZnO→ZnS+H2O+RH
氧化锌法脱硫速度快,精度高(0.1×10-6),一般采用钴钼加氢串联氧化锌法同时脱除原料气中的有机硫及无机硫化物。
加氢串氧化锌脱硫工艺流程
1-钴钼加氢脱硫槽;2-氧化锌槽
3.活性炭法
原理:
利用活性炭较强的吸附作用。
由反应机理不同,可分为吸附、氧化、催化三种方式。
氧化反应:
在活性炭表面上吸附的硫化氢在碱性溶液的条件下和气体中的氧反应生成硫和水。
催化反应:
活性炭上浸渍铁铜等的盐类,可催化有机硫转化为硫化氢,然后吸附脱除。
活性炭法可再生,用蒸汽加热使单质硫升华。
然后气体冷凝后得到硫磺固体
二、湿法脱硫
优点:
吸收速度快、生产强度大、脱硫剂可再生、可回收硫磺,适用于硫含量高,因而应用范围广泛。
缺点:
脱硫精度较差,有物料损耗。
方法:
物理法、化学法、物理化学法。
重点讨论:
化学法中的湿式氧化法
1.湿式氧化法脱硫的基本原理
吸收:
H2S+OH-→HS-+H2O
吸收剂为碱性物质
再生:
载氧体(氧化态)+H2S→S+载氧体(还原态)
载氧体(还原态)+1/2O2→H2O+载氧体(氧化态)
2.ADA法湿式氧化法脱硫
a.原理
脱硫:
Na2CO3+H2S→NaHS+NaHCO3
NaVO3+NaHS+H2O→Na2V4O9+S+NaOH
ADA(氧化态)+Na2V4O9→ADA(还原态)+NaVO3
再生:
ADA(还原态)+1/2O2→H2O+ADA(氧化态)
副反应:
NaHS+O2→Na2S2O3+H2O
b.工艺条件
(1)溶液的pH值:
高不易于单质硫的生成。
8.5~9.5。
(2)钒酸盐的含量:
过多易形成“钒-氧-硫”黑色沉淀,一般约高于理论用量。
同时还加入酒石酸钾钠防止其黑色沉淀产生。
(3)温度:
高易产生硫代硫酸盐副反应。
(4)压力:
没有多大的影响。
第二节一氧化碳变换
1.变换的基本原理
1.1化学平衡
CO(g)+H2O(g)CO2(g)+H2(g)-41.19kJ/mol
反应特点:
可逆的、气体体积不变的、放热反应。
(1)变换率x
变换率x:
已变换的CO量与变换前的CO量之比;
平衡变换率x*:
反应达到平衡时的变换率。
实际变换率x
(2)平衡变换率的影响因素
T↑,Kp↓;T↓,Kp↑,PCO↓,变换率增大;
H2O/CO↑,PCO↓,变换率增大;
P:
压力变化对变换率无影响。
1.2反应速率
反应速率的影响因素:
T:
存在最佳温度Tm;P:
P↑,反应速率增大;
H2O/CO↑,反应速率增大;
内扩散:
采用小颗粒催化剂,以增强内扩散效果。
2、变换催化剂
催化剂选择的主要依据
根据合成氨原料气净化流程和工艺要求。
具体说:
原料气和变换气CO含量,原料气中H2S和有机硫化物的含量。
残余CO:
原料气精制中脱除。
催化剂主要品种
铁铬系中温变换催化剂300~550℃;
铜锌系低温变换催化剂200~280℃;
钴钼系耐硫变换催化剂180~500℃。
2.1铁铬系中温变换催化剂
2.2铜锌系低变催化剂
2.3钴钼系耐硫变换催化剂
3.工艺条件
3.1温度:
Tm与催化剂种类及原料气组成等因素有关
(1)应在催化剂的活性温度范围内操作催化床温度
(2)催化床温度应可能接近最佳温度
变换反应器采用多段换热式。
3.2压力:
0.7~1.8MPa
故提高压力对变换反应是有利的。
3.3水碳比(H2O/CO):
一般取3~5
增加水蒸气用量,既有利于提高CO的变换率,又有利于提高变换反应速率。
三、总结知识
四、布置作业
教案头
课次
授课日期
编号
05
基本课题
二氧化碳脱除、原料气精制
教学目的
1、熟练掌握二氧化碳脱除和原料气精制的基本原理、工艺条件的选择及工艺流程的分析;
2、了解原料气净化的反应机理及动力学方程;冷法净化与热法净化的工艺组合
重点
二氧化碳脱除和原料气精制的基本原理、工艺条件的选择及工艺流程的分析
难点
二氧化碳脱除和原料气精制的基本原
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 无机 化工 生产技术 教案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
广东省普通高中学业水平考试数学科考试大纲Word文档下载推荐.docx
 置与管理_精品文档_001PPT文档格式.ppt
置与管理_精品文档_001PPT文档格式.ppt
