 EDTA标准溶液的配制与标定实验报告.doc
EDTA标准溶液的配制与标定实验报告.doc
- 文档编号:1694434
- 上传时间:2022-10-23
- 格式:DOC
- 页数:2
- 大小:40KB
EDTA标准溶液的配制与标定实验报告.doc
《EDTA标准溶液的配制与标定实验报告.doc》由会员分享,可在线阅读,更多相关《EDTA标准溶液的配制与标定实验报告.doc(2页珍藏版)》请在冰豆网上搜索。
EDTA标准溶液的配制与标定
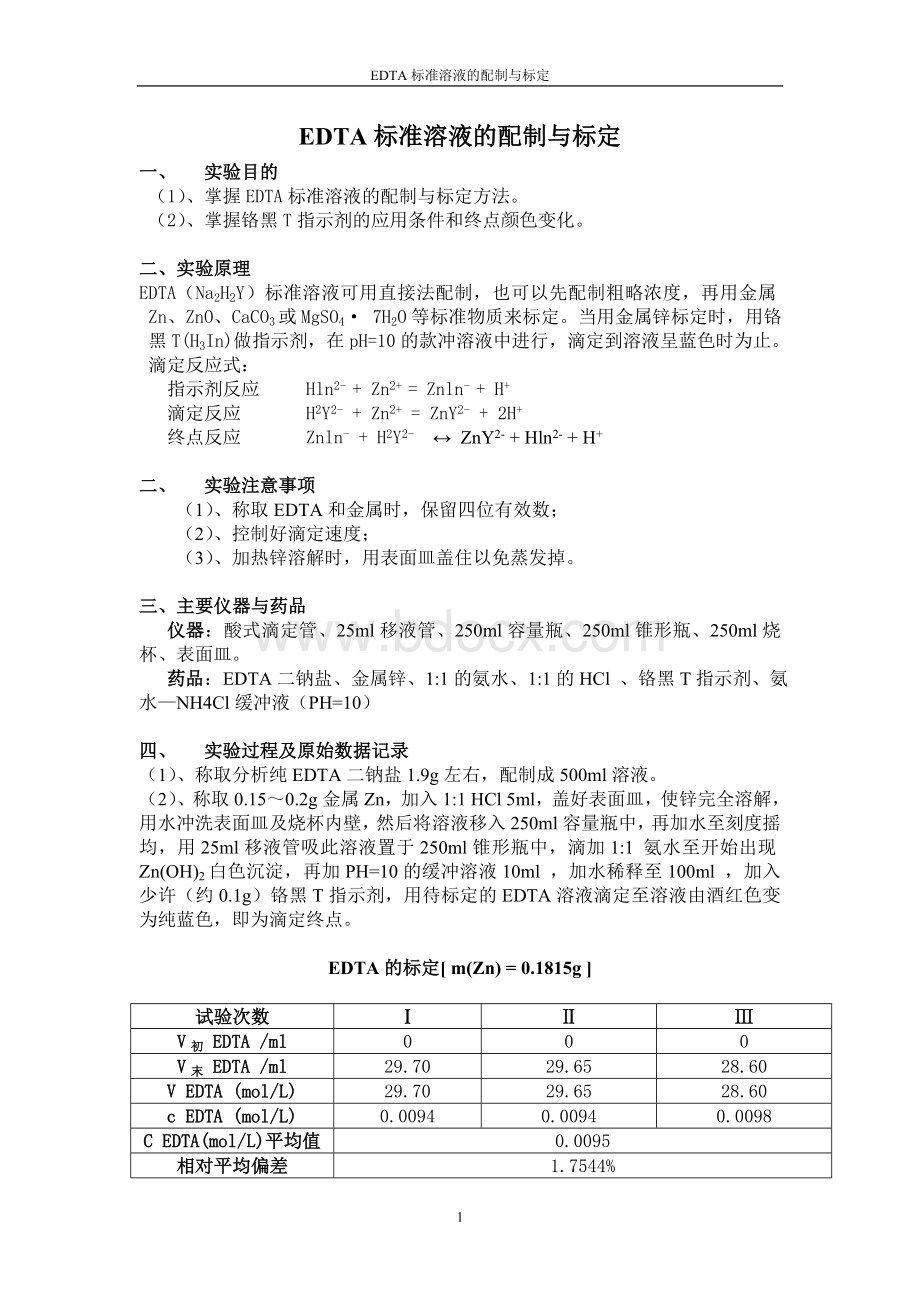
EDTA标准溶液的配制与标定
一、实验目的
(1)、掌握EDTA标准溶液的配制与标定方法。
(2)、掌握铬黑T指示剂的应用条件和终点颜色变化。
二、实验原理
EDTA(Na2H2Y)标准溶液可用直接法配制,也可以先配制粗略浓度,再用金属Zn、ZnO、CaCO3或MgSO4·7H2O等标准物质来标定。
当用金属锌标定时,用铬黑T(H3In)做指示剂,在pH=10的款冲溶液中进行,滴定到溶液呈蓝色时为止。
滴定反应式:
指示剂反应Hln2-+Zn2+=Znln-+H+
滴定反应H2Y2-+Zn2+=ZnY2-+2H+
终点反应Znln-+H2Y2-↔ZnY2-+Hln2-+H+
二、实验注意事项
(1)、称取EDTA和金属时,保留四位有效数;
(2)、控制好滴定速度;
(3)、加热锌溶解时,用表面皿盖住以免蒸发掉。
三、主要仪器与药品
仪器:
酸式滴定管、25ml移液管、250ml容量瓶、250ml锥形瓶、250ml烧杯、表面皿。
药品:
EDTA二钠盐、金属锌、1:
1的氨水、1:
1的HCl、铬黑T指示剂、氨水—NH4Cl缓冲液(PH=10)
四、实验过程及原始数据记录
(1)、称取分析纯EDTA二钠盐1.9g左右,配制成500ml溶液。
(2)、称取0.15~0.2g金属Zn,加入1:
1HCl5ml,盖好表面皿,使锌完全溶解,用水冲洗表面皿及烧杯内壁,然后将溶液移入250ml容量瓶中,再加水至刻度摇均,用25ml移液管吸此溶液置于250ml锥形瓶中,滴加1:
1氨水至开始出现Zn(OH)2白色沉淀,再加PH=10的缓冲溶液10ml,加水稀释至100ml,加入少许(约0.1g)铬黑T指示剂,用待标定的EDTA溶液滴定至溶液由酒红色变为纯蓝色,即为滴定终点。
EDTA的标定[m(Zn)=0.1815g]
试验次数
Ⅰ
Ⅱ
Ⅲ
V初EDTA/ml
0
0
0
V末EDTA/ml
29.70
29.65
28.60
VEDTA(mol/L)
29.70
29.65
28.60
cEDTA(mol/L)
0.0094
0.0094
0.0098
CEDTA(mol/L)平均值
0.0095
相对平均偏差
1.7544%
计算过程
cEDTA(mol/L)=m(Zn)/[M(Zn)*V]*1000*25/250
式中m(Zn)为称取分析纯Zn的质量(g);M(Zn)为Zn的摩尔质量(g/mol);V为标定时所用EDTA的体积(ml)。
第一次:
c(EDTA)=0.185/(65*29.7)*1000*25/250=0.0094mol/L
第二次:
c(EDTA)=0.1815/(65*29.65)*1000*25/250=0.0094mol/L
第三次:
c(EDTA)=0.1815/(65*28.6)*1000*25/250=0.0098mol/L
cEDTA(mol/L)平均值=(0.0094+0.0094+0.0098)/3=0.0095
cEDTA(mol/L)平均偏差=(|0.0094-0.0095|+|0.0094-0.0095|+|0.0098-0.0095|)/3=0.0001667
cEDTA(mol/L)相对平均偏差=平均偏差/平均值*100%=0.0001667/0.0095*100%=1.7544%
实验日期:
2012.10.25学生:
庄永招
2
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- EDTA 标准溶液 配制 标定 实验 报告
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
