 高中化学必修一第一章物质的量学案和练习题.doc
高中化学必修一第一章物质的量学案和练习题.doc
- 文档编号:1871767
- 上传时间:2022-10-24
- 格式:DOC
- 页数:11
- 大小:132.50KB
高中化学必修一第一章物质的量学案和练习题.doc
《高中化学必修一第一章物质的量学案和练习题.doc》由会员分享,可在线阅读,更多相关《高中化学必修一第一章物质的量学案和练习题.doc(11页珍藏版)》请在冰豆网上搜索。
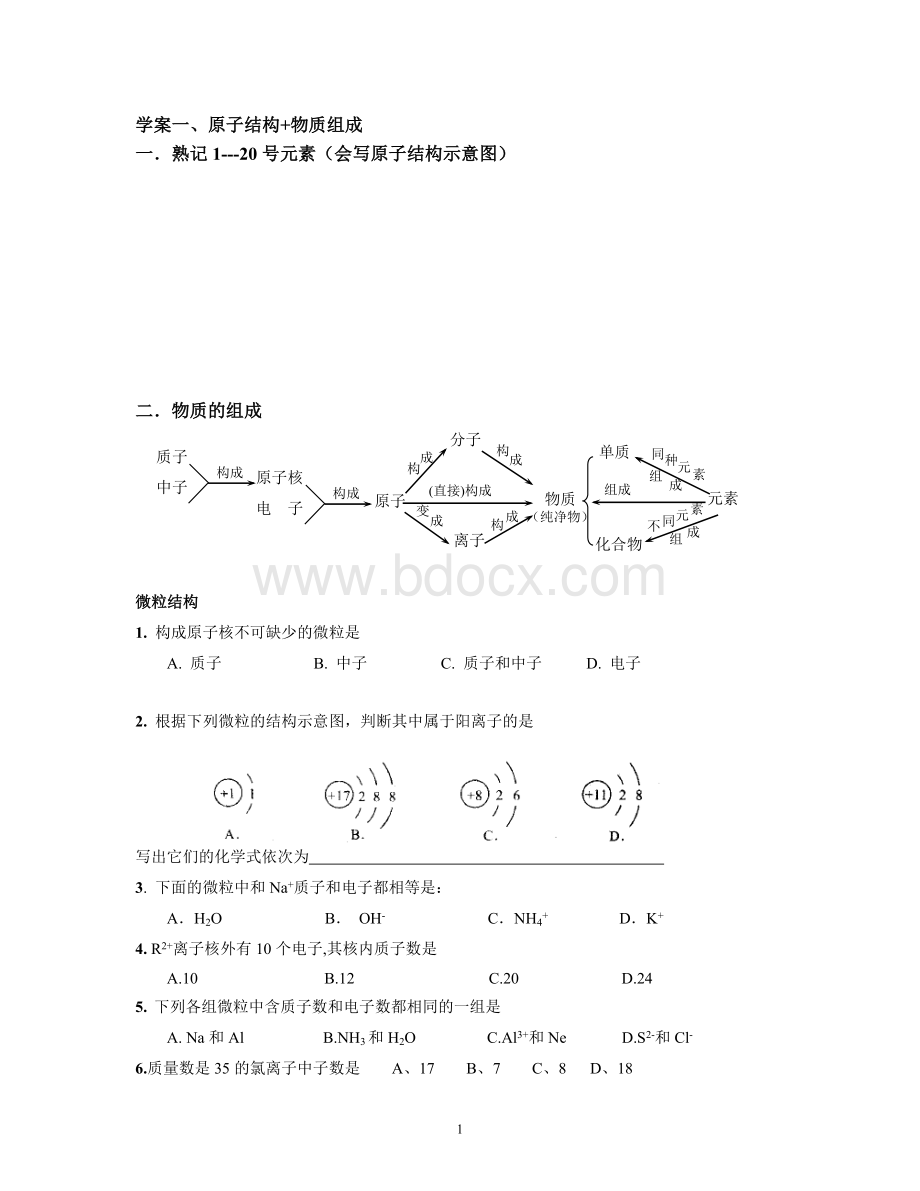
学案一、原子结构+物质组成
一.熟记1---20号元素(会写原子结构示意图)
二.物质的组成
质子
中子
构成
原子核
电子
构成
原子
(直接)构成
物质
组成
元素
离子
分子
构
成
变
成
构
成
构
成
(纯净物)
单质
化合物
同
种
元
素
成
组
不
同
元
素
组
成
微粒结构
1.构成原子核不可缺少的微粒是
A.质子 B.中子 C.质子和中子 D.电子
2.根据下列微粒的结构示意图,判断其中属于阳离子的是
写出它们的化学式依次为
3.下面的微粒中和Na+质子和电子都相等是:
A.H2OB.OH-C.NH4+D.K+
4.R2+离子核外有10个电子,其核内质子数是
A.10B.12C.20D.24
5.下列各组微粒中含质子数和电子数都相同的一组是
A.Na和AlB.NH3和H2OC.Al3+和NeD.S2-和Cl-
6.质量数是35的氯离子中子数是A、17B、7C、8D、18
学案二、物质的量与阿伏伽德罗常数
三、物质的量
1.定义:
表示物质所含微粒多少的物理量,也表示含有一定数目粒子的集合体。
2.物质的量是以微观粒子为计量的对象。
3.物质的量的符号为“n”。
四、摩尔
1.物质的量的单位
2.符号是mol。
使用“物质的量”与“摩尔”时的注意事项
1、“物质的量”四个字是一个整体概念,不得简化或增添任何字,如不能说成“物质量”“物质的质量”或“物质的数量”等。
2、物质的量是七个基本物理量之一;同“时间”,“长度”等一样,其单位是摩尔(mol)。
例题1、判断正误
H2的物质量为1.
3、物质的量表示的是微观粒子或微观粒子的特定组合的集合体,不适用于宏观物质,如1mol苹果的说法是错误的。
4、物质的量中所指粒子包括分子、原子、离子、质子、中子、电子、原子团等微观粒子或微观粒子的特定组合(如NaCl、Na2SO4等)。
例题2、判断正误
(1)1molH2中有2molH原子,0.5molH2
(2)4molNa2SO4有4mol钠原子,4mol硫原子,16mol氧原子。
※※※已知与所求之间列比例式
5、使用摩尔表示物质的量时,应该用化学式指明粒子的种类。
例如:
1molH表示mol氢原子,1molH2表示1mol氢分子(氢气),1molH+表示1mol氢离子,但如果说“1mol氢”就违反了使用标准,因为氢是元素名称,不是微粒名称,也不是微粒的符号或化学式。
例题3、下列说法中正确的是()
A.1mol氧B.1molH2SO4C.1mol米D.1mol面粉
五、阿伏加德罗常数NA
阿伏加德罗常数:
1摩尔的物质具有的微粒个数,单位是mol-1。
nmol某微粒集合体中所含微粒数约为n×6.02×1023。
物质的量、阿伏伽德罗常数以及微粒数之间关系式
n=N/NA
N=n·NA
NA=N/n
物质的量与阿伏伽德罗常数的计算练习
7、1mo1O2的分子数约为___________,2.5molSO2的分子数为___________;
3.01×1023个CO2的物质的量是______mol,其中碳原子的物质的量是________;氧原子的物质的量是________
1.204×1023个H2O的物质的量是_____mo1,其中氢原子的物质的量是________。
8、下列说法中正确的是()
A.1mol氧B.1molH2SO4C.1mol米D.1mol面粉
9、在.1molH2O中()
A.含1molHB.含6.02×1023个氢原子
C.含6.02×1023个水分子D.含3.01×1023个氧原子
10.在0.5molNa2SO4中,含有的Na+数约为()
A.3.01×1023B.6.02×1023C.0.5D.1
11.1mol下列气体中所含原子数最多的是()
A.H2B.CO2C.CH4D.O2
12.氢原子数目为9.03×1023的NH3是()
A.1.5molB.1molC.0.5molD.2mol
13.下列说法中正确的是(NA代表阿伏加德罗常数的值)()
A.1molN2和1molCO所含的分子数都是NA
B.1molH2和1molCO2所含的原子数都是NA
C.1molCO和1molCO2所含的氧原子数都是NA
D.1molH2SO4和1molH3PO4所含的原子数都是4NA
14.物质的量相同的甲烷和氨气具有不同的()
A.电子数目B.质子数目C.分子数目D.原子数目
15.相同物质的量的SO2和SO3,所含分子的数目之比为_______,所含O的物质的量
之比为_______。
学案三、物质的量与摩尔质量
六、摩尔质量:
一摩尔的物质所具有的质量,单位是g/mol或kg/mol
摩尔质量以g/mol为单位时,在数值上等于其相对分子质量或相对原子质量;
物质的量、摩尔质量以及质量之间关系式
n=m/M
m=n·M
M=m/n
使用“物质的量”与“摩尔质量”时的注意事项
1、“摩尔质量”四个字是一个整体概念,不得简化或增添任何字。
2、“摩尔质量”摩尔质量以g/mol为单位时,在数值上等于其相对分子质量或相对原子质量;
例题O的相对原子质量为16,1molO的质量为16g;则O的摩尔质量为 _______
Na+的相对原子质量为23,1molNa的质量为23g。
Na+的摩尔质量为_______
S的相对原子质量为32,1molS的质量为32g。
S的摩尔质量为_______
Na2SO4的摩尔质量为_______
七、六个关系
1.物质的量与摩尔的关系
物质的量和长度、质量、时间、电流强度等概念一样,是一个物理量的整体名词。
摩尔是物质的量的单位。
例如:
长度的单位是米,物质的量的单位是摩尔。
2.摩尔质量与相对分子质量的关系
数值相同,单位不同。
3.物质的量与物质的质量的关系
不能把物质的量理解为物质的质量。
物质的质量在物理学上是早已明确了的物理量,其单位为千克。
虽然两者的意义不同,但它们之间可以通过物质的摩尔质量联系起来
4、摩尔质量(M)和阿伏加德罗常数的关系
阿伏加德罗常数个粒子的物质的量是1mol,其质量在数字上即为摩尔质量。
二者通过物质的量联系起来。
公式
物质的量与摩尔质量的计算练习
16、下列关于摩尔质量的说法正确的是()
A、氯气的摩尔质量是71克B、氯化氢的摩尔质量为36.5g/moL
C、1摩氢气的质量为2克D、O2的摩尔质量为16g/moL。
17、0.2molAl2(SO4)3中含有Al3+mol、SO42- g。
18、8g氧气为 mol;0.1mol氧气共有 mol电子。
19、已知铁的相对原子质量是56,则1个铁原子的质量是 g。
20、某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO42-的物质的量是 ,
该溶液中Na2SO4的质量为克。
21、下列关于摩尔质量的说法正确的是()
A、氯气的摩尔质量是71克B、氯化氢的摩尔质量为36.5g/moL
C、1摩氢气的质量为2克D、O2的摩尔质量为16g/moL。
22、对于相同质量的二氧化硫和三氧化硫来说,下列关系正确的是()
A、含氧原子的个数比为2∶3B、含硫元素的质量比是5∶4
C、含氧元素的质量比为5∶6D、含硫原子的个数比为1∶1
23、1克氯气含有n个Cl2分子,则阿佛加德罗常数可表示为()
A、71nB、(1/71)nC、35.5nD、(1/35.5).n
24、某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO42-的物质的量是 ,
该溶液中Na2SO4的质量为克。
25、与16g氧气所含有分子数相同的氨气是g,与16g氧气所含原子总数相同的氨气是g。
学案四、物质的量与气体摩尔体积
八、气体的摩尔体积
一摩尔单位物质的量的气体所占的体积,符号Vm,单位:
L/mol
一定温度,压强下,任何气体的气体摩尔体积是相同的。
标准状况下:
Vm=22.4L/mol
物质的量、气体摩尔体积以及气体体积之间关系式
n=V/Vm
V=n·Vm
Vm=V/n
使用“物质的量”与“气体摩尔体积”时的注意事项
1、注意温度和压强
如果在标况下,VA=22.4mol/L
如果温度和压强相同,Vm相同
2、气体摩尔体积的“四要素”即状态(气体)、状况(条件:
温度、压强)、
定量(1mol)、数值(体积)
物质的量与气体摩尔体积的计算练习
26.14g氮气的体积是()
(A)1.12L(B)22.4L(C)5.6L(D)不确定
27.同温同压下,下列气体等质量时所占体积最小的是()
(A)SO2(B)CO2(C)H2(D)Cl2
28.S原子的摩尔质量是__________,1molH2SO4的质量是_________,1molH2SO4约含有
_________个硫酸分子,_________个氢原子,________个氧原子。
0.49kgH2SO4
中含有_______个H2SO4分子
29.在标准状况下,4gH2、11.2LO2、1molH2O中,所含分子数最多的是__
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 必修 第一章 物质 量学案 练习题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 保育笔记.doc
保育笔记.doc
 幼儿园日常安全检查记录表.xls
幼儿园日常安全检查记录表.xls
