 安徽省黄山市届高三上学期一模考试化学解析版.docx
安徽省黄山市届高三上学期一模考试化学解析版.docx
- 文档编号:2129928
- 上传时间:2022-10-27
- 格式:DOCX
- 页数:18
- 大小:307.89KB
安徽省黄山市届高三上学期一模考试化学解析版.docx
《安徽省黄山市届高三上学期一模考试化学解析版.docx》由会员分享,可在线阅读,更多相关《安徽省黄山市届高三上学期一模考试化学解析版.docx(18页珍藏版)》请在冰豆网上搜索。
安徽省黄山市届高三上学期一模考试化学解析版
安徽省黄山市2019届高三上学期一模考试
一、单选题
1.化学与生活、生产密切相关,下列说法错误的是( )
A. 用灼烧的方法可以区分蚕丝和人造纤维
B. 按照规定对生活废弃物进行分类放置有利于保护环境
C. 纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附
D. 光导纤维是无机非金属材料,合成纤维是有机高分子材料
2.NA为阿伏加德罗常数的值。
下列说法正确的是( )
A. 1molH2和1molI2在加热条件下充分反应,生成HI的分子数为2NA
B. 10g质量分数为46%的乙醇溶液含有的氢原子数目为0.6NA
C. 20mL0.1mol/LAlCl3溶液中,水解形成Al(OH)3胶体粒子数为0.002NA
D. 0.1molNa2O2和Na2O的混合物中含有的离子总数等于0.3NA
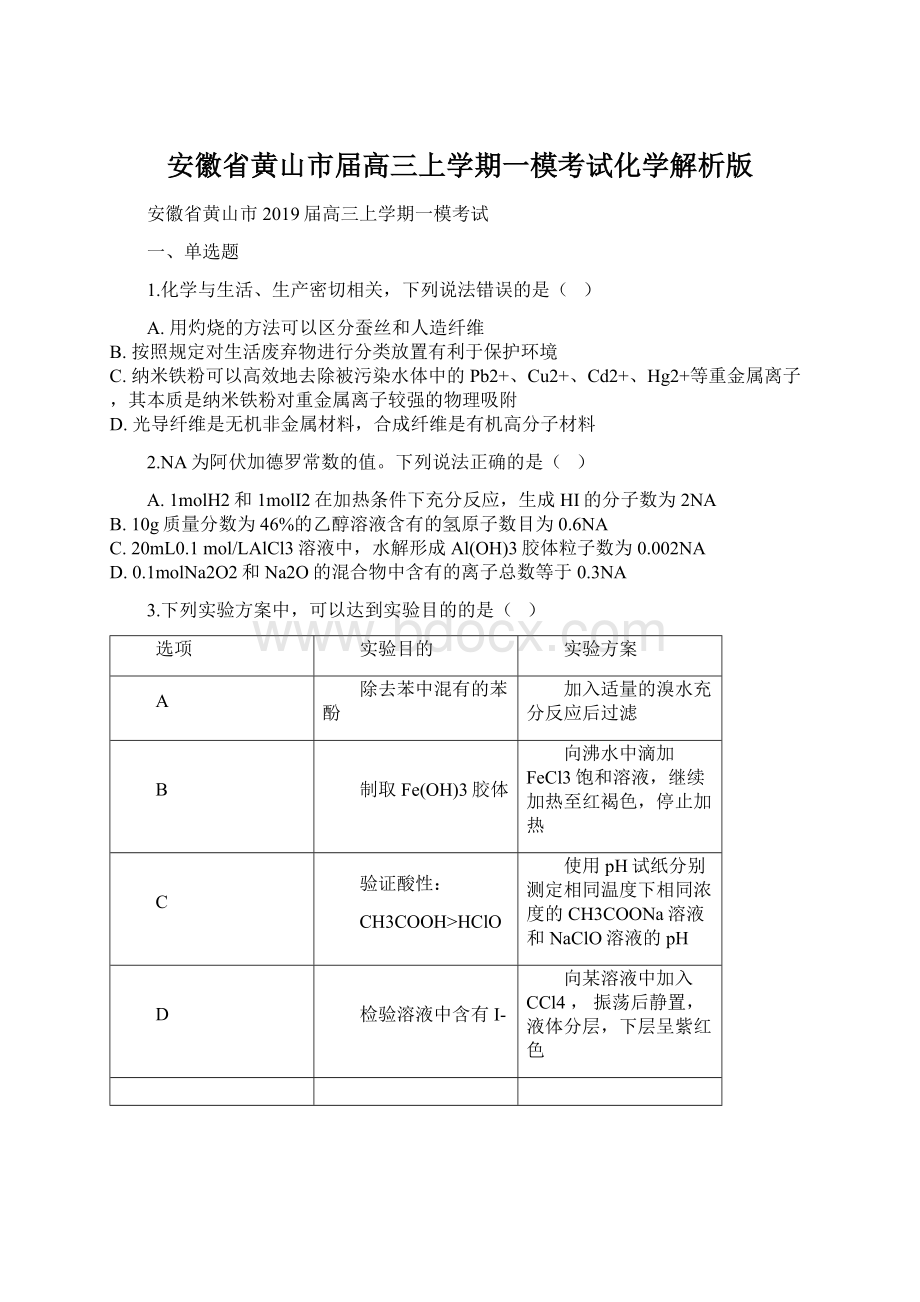
3.下列实验方案中,可以达到实验目的的是( )
选项
实验目的
实验方案
A
除去苯中混有的苯酚
加入适量的溴水充分反应后过滤
B
制取Fe(OH)3胶体
向沸水中滴加FeCl3饱和溶液,继续加热至红褐色,停止加热
C
验证酸性:
CH3COOH>HClO
使用pH试纸分别测定相同温度下相同浓度的CH3COONa溶液和NaClO溶液的pH
D
检验溶液中含有I-
向某溶液中加入CCl4,振荡后静置,液体分层,下层呈紫红色
4.下列有关有机化合物(a)(b)(c)的说法正确的是( )
A. (a)(b)(c)均能与溴水发生化学反应 B. (b)二氯代物有两种
C. (a)(b)(c)互为同分异构体 D. (a)中所有原子可能共平面
5.W、X、Y、Z是四种短周期非金属元素,原子序数依次增大。
W是原子半径最小的元素,X、Y原子核外L层的电子数之比为3∶4,X与Z同主族,W、X、Y、Z的最外层电子数之和为17。
下列说法正确的是( )
A. 单质的沸点:
X>Z B. X与W形成的化合物中一定只有极性键
C. 氢化物的热稳定性:
Z>Y D. W、X、Y可形成离子化合物
6.电解絮凝净水可用如图装置模拟探究,下列叙述正确的是( )
A. 电子从X极经电解液流入Y极
B. 铝电极表面的反应有:
Al-3e-=Al3+,4OH--4e-=O2↑+2H2O
C. Y的电极反应:
Pb-2e-+SO42-=PbSO4
D. 电路每通过2mol电子,理论上电解池阴极上有22.4LH2生成
7.室温下,向H2C2O4溶液中滴加NaOH溶液,若pc=-lgc,则所得溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)与溶液pH的关系如图所示。
下列说法正确的是( )
A. M点时,2c(HC2O4-)+c(C2O42-)>c(Na+) B. pH=x时,c(HC2O4-) C. 常温下,Ka2(H2C2O4)=10-1.3 D. 随pH的升高而减小 二、实验题 8.长期缺碘和碘摄入过量都会对健康造成危害,目前加碘食盐中碘元素绝大部分以IO3-存在,少量以I-存在。 现使用Na2S2O3对某碘盐样品中碘元素的含量进行测定。 (1)Ⅰ.I-的定性检测 取少量碘盐样品于试管中,加水溶解,滴加硫酸酸化,再滴加数滴5%NaNO2和淀粉的混合溶液,若溶液变为________色,则存在I-,同时有无色气体产生(该气体遇空气变成红棕色)。 试写出该反应的离子方程式为________________________________。 (2)Ⅱ.硫代硫酸钠的制备 工业制备硫代硫酸钠的反应原理为,某化学兴趣小组用上述原理实验室制备硫代硫酸钠如图: 先关闭K3打开K2,打开分液漏斗,缓缓滴入浓硫酸,控制好反应速率。 y仪器名称______________,此时B装置的作用是________________________________。 (3)反应开始后,C中先有淡黄色浑浊,后又变为澄清,此浑浊物为________(填化学式)。 装置D的作用是______________________________________。 (4)实验结束后,关闭K2打开K1,玻璃液封管x中所盛液体最好为_______。 (填序号) ANaOH溶液 B.浓硫酸 C饱和NaHSO3溶液 (5)Ⅲ.碘含量的测定 已知: ①称取10.00g样品,置于250mL锥形瓶中,加水100mL溶解,加2mL磷酸,摇匀。 ②滴加饱和溴水至溶液呈现浅黄色,边滴加边摇,至黄色不褪去为止(约1mL)。 ③加热煮沸,除去过量的溴,再继续煮沸5min,立即冷却,加入足量15%碘化钾溶液,摇匀。 ④加入少量淀粉溶液作指示剂,再用0.0002mol/L的Na2S2O3标准溶液滴定至终点。 ⑤重复两次,平均消耗Na2S2O3溶液9.00mL 相关反应为: ,, 请根据上述数据计算该碘盐含碘量为________mg·kg-1。 三、工业流程 9.经多年勘测,2018年11月23日省自然资源厅发布消息称在皖江地区发现特大铜矿床,具有重大实际意义。 以黄铜矿(主要成分为CuFeS2,含有少量PbS、Al2O3、SiO2)为原料制取胆矾的流程如下图: 已知: 常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=3.0×10-33,Ksp[Cu(OH)2]=3.0×10-20。 (1)CuFeS2中硫元素的化合价为________,硫元素在周期表中的位置是______________。 写出上述流程中生成亚硫酸铵的离子方程式: ______________________________________。 (2)最适合的试剂A是________(写化学式)溶液,固体2的成份为PbSO4和________。 当试剂A的浓度为6mol·L-1时,“浸出”实验中,铜的浸出率结果如图所示。 所采用的最佳实验条件(温度、时间)为________。 (3)最适合的试剂B是________(填序号),最适合的试剂C是________(填序号),固体3的成份为__________________________。 a.Cl2b.CuO c.酸性高锰酸钾溶液 d.NaOH e.H2O2溶液 f.K2CO3 (4)操作1如在实验室中进行,用到的玻璃仪器有烧杯、玻璃棒和________,操作2的步骤为________过滤、洗涤。 (5)根据已知信息,请计算: 当Fe3+完全沉淀时,溶液中Al3+理论最大浓度为________。 (提示: 当离子浓度≤1×10-5mol·L时,认为该离子沉淀完全) 四、综合题 10.游离态氮称为惰性氮,游离态氮转化为化合态氮称之为氮的活化,在氮的循环系统中,氮的过量“活化”,则活化氮开始向大气和水体过量迁移,氮的循环平衡被打破,导致全球环境问题。 (1)Ⅰ.氮的活化 工业合成氨是氮的活化重要途径之一,在一定条件下,将N2和H2通入到体积为0.5L的恒容容器中,反应过程中各物质的物质的量变化如图所示: 10min内用NH3表示该反应的平均速率,v(NH3)=________。 (2)在第10min和第25min改变的条件可能分别是________、________(填字母)。 A.加了催化剂 B.升高温度 C.增加NH3的物质的量 D.压缩体积 E.分离出氨气 (3)下列说法能说明该可逆反应达到平衡状态的是__________(填字母)。 A. 容器中气体密度不变 B. 容器中压强不变 C. 3v(H2)正=2v(NH3)逆 D. N2、H2、NH3分子数之比为1∶3∶2 (4)Ⅱ.催化转化为惰性氮 已知: SO2、CO、NH3等都可以催化还原氮氧化物生成惰性氮。 在25℃、101KPa时,N2(g)+3H2(g)2NH3(g) △H1=-92.4kJ/mol. 2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ/mol N2(g)+O2(g)=2NO(g) △H3=+180kJ/mol 则NO与NH3反应生成惰性氮的热化学方程式______________________________________________________________。 (5)在有氧条件下,新型催化剂M能催化CO与NOx反应生成N2。 现向某密闭容器中充入等物质的量浓度的NO2和CO气体,维持恒温恒容,在催化剂作用下发生反应: 4CO(g)+2NO2(g)N2(g)+4CO2(g) △H<0,相关数据如下: 0min 5min 10min 15min 20min c(NO2)/mol·L-1 2.0 1.7 1.56 1.5 1.5 c(N2)/mol·L-1 0 0.15 0.22 0.25 0.25 ①计算此温度下的化学平衡常数K=________, ②实验室模拟电解法吸收NOx装置如图,(图中电极均为石墨电极)。 若用NO2气体进行模拟电解法吸收实验(a ________。 五、填空题 11.铁和钴是两种重要的过渡元素。 (1)钴位于元素周期表第四周期Ⅷ族,其基态原子中未成对电子个数为________。 (2)基态Fe3+的核外电子排布式________ (3)铁氧体是一种磁性材料,工业上制备时常采用水解法,制备时常加入尿素(CO(NH2)2)、醋酸钠等碱性物质。 尿素分子中所含非金属元素的电负性由大到小的顺序是________,分子中σ键与π键的数目之比为________。 醋酸钠中碳原子的杂化类型________。 (4)铁氧体也可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱,已知氨(NH3熔点: -77.8%℃、沸点: -33.5%℃),联氨(N2H4熔点: 2℃、沸点: 113.5°C)解释其熔沸点高低的主要原因____________________________________________。 (5)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数为6,为确定钻的配合物的结构,现对两种配合物进行如下实验: 在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,则第一种配合物的配体为________。 在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。 则第二种配合物的配体为________。 (6)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如上图所示,则该物质的化学式为________。 若品体密度为dg·cm-3,则晶胞中最近的两个碳原子的距离为________pm(阿伏加德罗常数的值用NA表
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 安徽省 黄山市 届高三 上学 期一模 考试 化学 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
