 高考化学复习专题之离子大量共存规律总结.docx
高考化学复习专题之离子大量共存规律总结.docx
- 文档编号:24931289
- 上传时间:2023-06-02
- 格式:DOCX
- 页数:8
- 大小:27.13KB
高考化学复习专题之离子大量共存规律总结.docx
《高考化学复习专题之离子大量共存规律总结.docx》由会员分享,可在线阅读,更多相关《高考化学复习专题之离子大量共存规律总结.docx(8页珍藏版)》请在冰豆网上搜索。
1. 离子共存问题是离子反应条件
所谓几种离子在同一溶液中能大量共存,就是指离子之间不发生任何反应;若离子之间能发生反应,则不能大量共存。
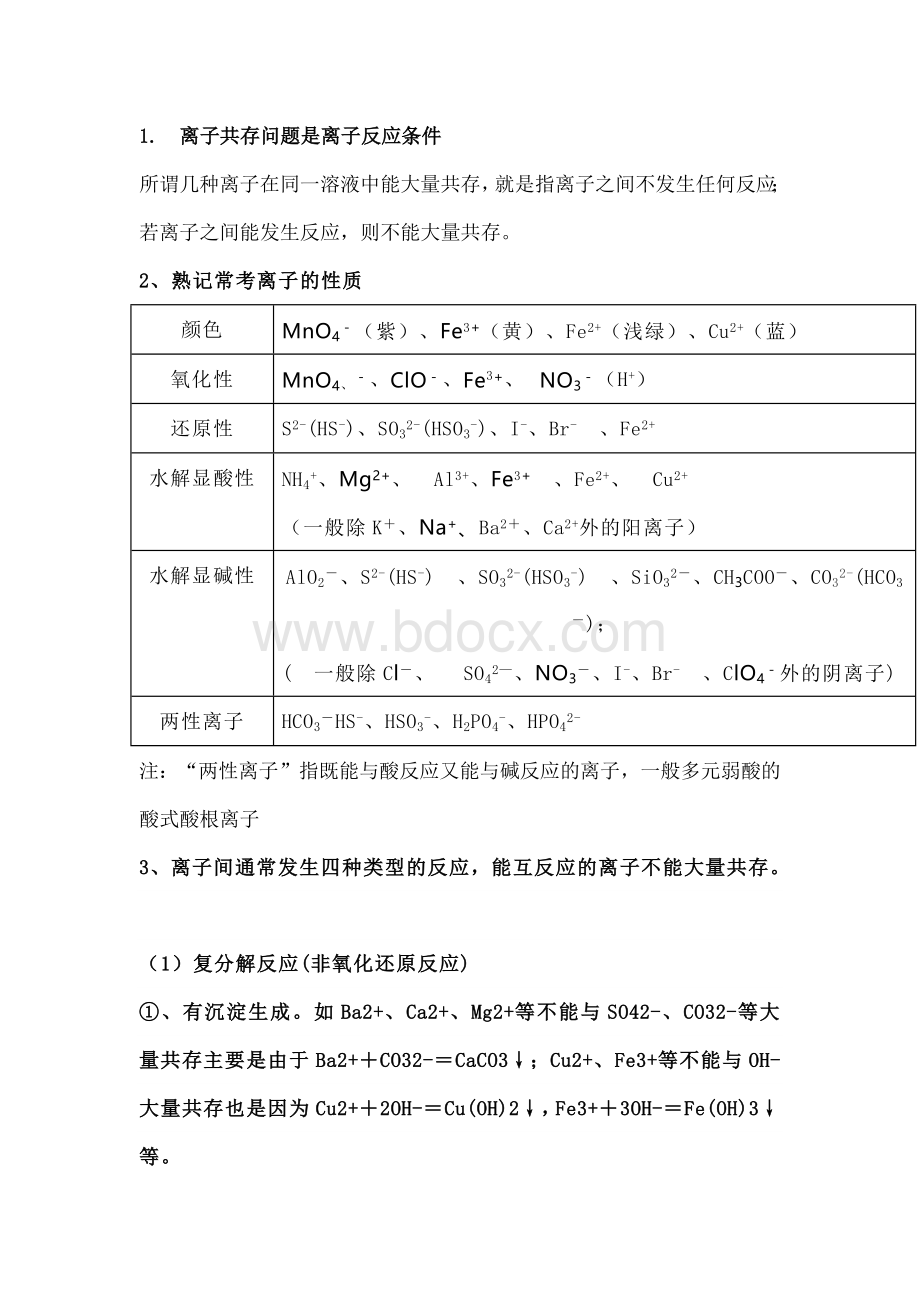
2、熟记常考离子的性质
颜色
MnO4-(紫)、Fe3+(黄)、Fe2+(浅绿)、Cu2+(蓝)
氧化性
MnO4、-、ClO-、Fe3+、 NO3-(H+)
还原性
S2-(HS-)、SO32-(HSO3-)、I-、Br- 、Fe2+
水解显酸性
NH4+、Mg2+、 Al3+、Fe3+ 、Fe2+、 Cu2+
(一般除K+、Na+、Ba2+、Ca2+外的阳离子)
水解显碱性
AlO2-、S2-(HS-) 、SO32-(HSO3-) 、SiO32-、CH3COO-、CO32-(HCO3-);
( 一般除Cl-、 SO42—、NO3-、I-、Br- 、ClO4-外的阴离子)
两性离子
HCO3-HS-、HSO3-、H2PO4-、HPO42-
注:
“两性离子”指既能与酸反应又能与碱反应的离子,一般多元弱酸的酸式酸根离子
3、离子间通常发生四种类型的反应,能互反应的离子不能大量共存。
(1)复分解反应(非氧化还原反应)
①、有沉淀生成。
如Ba2+、Ca2+、Mg2+等不能与SO42-、CO32-等大量共存主要是由于Ba2++CO32-=CaCO3↓;Cu2+、Fe3+等不能与OH-大量共存也是因为Cu2++2OH-=Cu(OH)2↓,Fe3++3OH-=Fe(OH)3↓等。
②有气体产生。
如CO32-、S2-、HS-、HSO3-、等易挥发的弱酸的酸根与H+不能大量共存,主要是由于CO32-+2H+=CO2↑+H2O、HS-+H+=H2S↑。
③有弱电解质生成。
如OH-、CH3COO-、PO43-、HPO42-、H2PO4-(一般除Cl-、SO42—、NO3-、I-、Br-、ClO4-外的阴离子)等与H+不能大量共存,主要是由于OH-+H+=H2O、CH3COO-+H+=CH3COOH;一些酸式弱酸根不能与OH-大量共存是因为HCO3-+OH-=CO32-+H2O、HPO42-+OH-=PO43-+H2O、NH4++OH-=NH3·H2O等。
(2)、发生氧化还原反应:
具有较强还原性的离子不能与具有较强氧化性的离子大量共存
常见的氧化性离子:
MnO4、-、ClO-、Fe3+、NO3-(H+)
常见的还原性离子:
S2-(HS-)、SO32-(HSO3-)、I-、Br-、Fe2+
注:
Fe3+与Fe2+、Br-能大量共存
(3)发生双水解反应:
能水解的阳离子跟能水解的阴离子在水溶液中不能大量共存。
常见的双水解:
①Al3+、Fe3+和CO32(HCO3-)、S2-(HS-)、AlO2-、ClO-等
②NH4+和SiO32-、AlO2-
(4)络合反应:
如Fe3+和SCN-、C6H5O-,由于Fe3++SCN-=[Fe(SCN)]2+等络合反应而不能大量共存。
4、审题时应注意题中给出的附加条件和隐含条件。
(1)一色:
溶液的颜色。
溶液无色时,则溶液中肯定没有有色离子存在。
有色离子MnO4-,Fe3+,Fe2+,Cu2
(2)二性:
溶液的酸性、碱性。
酸碱性
表 述
酸性
①加入甲基橙或紫色石蕊试液变红色
②加入镁产生气体
③常温下,溶液的pH﹤7
④常温下,溶液中c(H+) >1×10-7mol/L
⑤溶液中c(H+)/c(OH-)>1
碱性
①加入酚酞试液呈红色或石蕊试液变蓝色
②常温下,溶液的pH>7
③常温下,溶液中c(OH-)>1×10-7mol/L或c(H+)<1×10-7mol/L
④溶液中c(H+)/c(OH-)<1
酸性或
碱性
①加入甲基橙呈黄色
②加入铝,有氢气产生(不能是HNO3)
③加入碳酸氢铵产生气体
④常温下,水电离的c(H+)<1×10-7mol/L或c(H+)>1×10-7mol/(盐类水解)
(3)三特殊:
注意三种特殊情况①注意溶液的酸性对离子间发生氧化还原反应的影响。
如:
Fe2+与NO3-能共存,但在强酸性条件下(即Fe2+、NO3-、H+相遇)不能共存;MnO4- 与Cl-在强酸性条件也不能共存;S2O32-在酸性条件下发生氧化还原反应,不能共存:
S2O32-+2H+=S↓+SO2↑+H2O②HCO3-与AlO2-发生双水解,不能大量共存。
③NH4+和CO32、HCO3-、CH3COO-等,虽然能发生双水解,但总的水解程度较小,因此能大量共存。
(4)注意题目要求“一定能大量共存”还是“可能大量共存”;“能大量共存”还是“不能大量共存”。
离子共存习题
1.某无色透明的溶液,在pH=0和pH=14的条件下都能大量共存的是( )
A.Fe2+、K+、SO42-、NO3- B.Mg2+ 、NH4+、SO42-、Cl-
C.Na+、K+、SO42-、NO3- D.Ba2+ 、Na+ 、MnO4- 、SO42-
2.下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
A.H3O+、NO3-、Fe2+、Na+ B.Ag+、NO3-、Cl-、K+
C.K+、Ba2+、OH-、SO42- D.Cu2+、NH4+、Br-、OH-
3.某溶液中加入铝粉有氢气产生,该溶液中一定可以大量共存的离子组是( )
A.Na+、NO3-、Cl-、SO42- B.Na+、K+、Ba2+、HCO3-
C.Fe3+、H+、SO42-、Cl- D.Na+、K+、Cl-、SO42-
4.室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是
A.NH4+、Cu2+、Cl-、NO3- B.K+、Na+、SO32-、S2-
C.K+、Na+、AlO2-、SO42- D.Ba2+、Fe2+、NO3-、Br-
5(双选).下列各组离子在碱性条件下可以大量共存,而在强酸性条件下不能大量其存的是
A.Ca2+、Fe3+、NO3-、Cl- B.K+、Mg2+、HCO3-、SO42-
C.Na+、K+、S2-、SO32- D.Ba2+、Na+、I一、NO3-
6.下列各组离子一定能大量共存的是( )
A.在含大量Fe3+的溶液中:
NH4+、Na+、Cl—、SCN—
B.在强碱溶液中:
Na+、K+、AlO2—、CO32—
C.在c(H+)=10—13 mol/L的溶液中:
NH4+、Al3+、SO42—、NO3—
D.在pH=1的溶液中:
K+、Fe2+、Cl—、NO3—
7.下列各组无色溶液的离子组在pH=l时能大量共存的是
A.NH4+、C1-、Mg2+、SO42- B.A13+、Cu2+、SO42-、C1-
C.Ba2+、K+、NO3-、OH- D.Ca2+、Na+、C1-、A1O2-
12.在给定的四种溶液中,各离子能大量共存的是
A.滴加石蕊试液显红色的溶液:
Fe3+、NH4+、Cl-、I-
B.能使pH试纸变为蓝色的溶液:
Na+、CO32-、NO3-、SO32-
C.含有大量H+的无色溶液:
Na+、Fe3+、NO3-、MnO4-
D.所含溶质为NaNO3的溶液:
K+、HSO4-、C1-、S2-
8.(双选)某无色溶液与NH4HCO3作用能产生气体(可加热),此溶液中可能大量共存的离子组是
A. Mg2+、H+、Zn2+、SO B.Na+、Ba2+、OH、SO
C.MnO、K+、H+、SO D.K+、NO、OH-、Na+
9.某溶液能使红色的石蕊试纸先变蓝色后褪色,则该溶液中可能大量共存的离子组是
A.K+、I—、AlO2—、MnO4— B.Na+、S2—、NO3—、SO42—
C.Al3+、NH4+、NO3—、F— D.K+、Cl—、ClO—、CO32—
10.在下列溶液中,各组离子一定能够大量共存的是
A.使酚酞试液变红的溶液:
Na+、Cl-、SO42-、Fe3+
B.使紫色石蕊试液变红的溶液:
Fe2+、Mg2+、NO3-、Cl-
C.c(H+)=10-12 mol·L-1的溶液:
K+、Ba2+、Cl-、Br-
D.碳酸氢钠溶液:
K+、SO42-、Cl-、H+
11.(双选)下列各组离子能大量共存,当溶液酸性时,有气体产生;而当溶液中碱性时,又能生成沉淀。
该组离子可能是
A.Na+、Cu2+、NO3-、CO32- B.Ba2+、K+、Cl-、HCO3—
C.Fe2+、Na+、SO42-、NO3- D.Mg2+ 、NH4+、SO42-、Cl—
12.在pH=1的溶液中,大量存在着的阳离子是NH4+、Mg2+、Al3+、Fe2+,则溶液中还可能大量存在的阴离子是
A.Cl— B.ClO— C.HCO3— D.NO3—
13.已知pH=1的某溶液中存在较多的Ba2+、NO3-,则该溶液中还可能大量存在的离子组是
A.Fe3+、F-、Cl- B.Mg2+、SO42-、Br-
C.Mg2+、Cl-、Fe2+ D.Na+、NH4+、Cu2+
14.向某溶液里加入过量的氨水或过量的氢氧化钠溶液,均有沉淀产生;若加入铁粉或铜粉,溶液的质量都增加,则该溶液里一定含有下列离子中的
A.Al3+ B.Fe2+ C.Fe3+ D.Cu2+
15.(双选)下列各组离子能大量共存于同一溶液中,且加入少量NaOH溶液或适量稀H2SO4时,都能产生沉淀的是
A.Ba2+、Mg2+、NO3-、CO32- B.Na+、Al3+、Cl-、AlO2-
C.Ca2+、K+、Cl-、HCO3- D.NH4+、Fe3+、Ba2+、Cl-
16.某溶液中含有CH3COO-、SO42-、SO32-、HCO3-、CO32-等五种离子。
将过量的Na2O2固体加入其中后,仍能大量存在的离子是
A.CH3COO-、SO42-、HCO3- B.SO42-、SO32-、CO32-
C.SO32-、HCO3-、SO42- D.CH3COO-、SO42-、CO32-
17.某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍为无色,则下列关于该溶液组成的判断正确的是
①肯定不含I- ②肯定不含Cu2+ ③肯定含SO32- ④可能含I-
A.①②
B.①②③
C.①③
D.②③④
参考答案
1.C
2.A3.D(在强酸溶液中,存在硝酸根离子,相当于硝酸溶液不会产生氢气)
4.D 5.CD 6.B 7.A 8.AD 9.D
10.C11.BC A.Cu2+和CO32-会生成沉淀,C会生成NO气体)
12.A 13.D 14.C 15.CD
16.D (Na2O2强氧性可氧化SO32)-) 17.D
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 复习 专题 离子 大量 共存 规律 总结
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 策略与技巧培训课件.ppt
策略与技巧培训课件.ppt
 建筑安装工程承包合同-2.doc
建筑安装工程承包合同-2.doc
 安全文明施工措施费详细清单.xls
安全文明施工措施费详细清单.xls
