 金属的性质.docx
金属的性质.docx
- 文档编号:28539238
- 上传时间:2023-07-18
- 格式:DOCX
- 页数:18
- 大小:357.43KB
金属的性质.docx
《金属的性质.docx》由会员分享,可在线阅读,更多相关《金属的性质.docx(18页珍藏版)》请在冰豆网上搜索。
金属的性质
金属的化学性质
方程式梳理
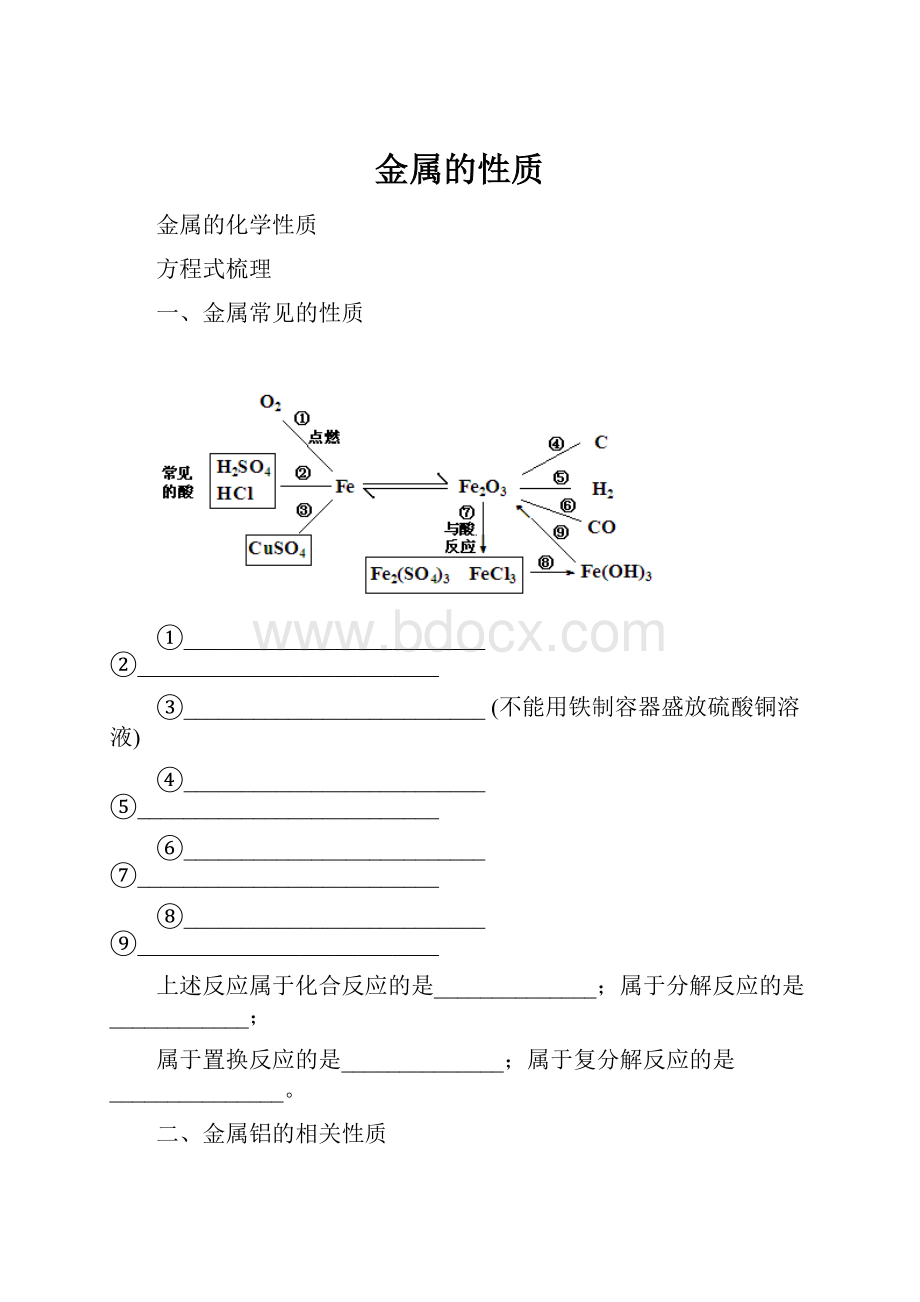
一、金属常见的性质
①__________________________②__________________________
③__________________________(不能用铁制容器盛放硫酸铜溶液)
④__________________________⑤__________________________
⑥__________________________⑦__________________________
⑧__________________________⑨__________________________
上述反应属于化合反应的是______________;属于分解反应的是____________;
属于置换反应的是______________;属于复分解反应的是_______________。
二、金属铝的相关性质
①__________________________(铝制品具有抗腐蚀性的原因)
②__________________________
③__________________________④__________________________
三、金属铜的相关性质
①__________________________②__________________________
③__________________________④__________________________
⑤__________________________⑥__________________________
金属与盐溶液反应后过滤,判断滤液中溶质和滤渣中固体的成分
例:
将铁粉不断加入一定质量的硝酸铜、硝酸银溶液中
铁粉量
滤渣
滤液的溶质
少量
银
硝酸亚铁、硝酸铜、硝酸银
与硝酸银恰好完全反应
银
硝酸亚铁、硝酸铜
与硝酸银恰好完全反应,与部分硝酸铜反应
铜、银
硝酸亚铁、硝酸铜
与硝酸铜、硝酸银恰好完全反应
铜、银
硝酸亚铁
过量
铁、铜、银
硝酸亚铁
例2.将铁粉不断加入一定质量的硝酸铜、硝酸银、硝酸锌溶液中,则溶液中溶质中一定有__________________________.
练习:
在硝酸铜、硝酸银和硝酸铝的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,没有气泡产生。
(1)请说出滤出的固体中一定含有哪些成分?
滤液中一定含有哪些成分?
(2)写出反应过程中一定发生的化学方程式。
例3.某化学小组向一定量硝酸银和硝酸铝的混合溶液中加入铜粉和锌粉,充分反应后过滤,得到溶液中甲和乙,如图所示,则:
(1)若溶液甲是蓝色,则溶液甲一定含有____________。
(2)若向固体乙上滴加盐酸有气泡产生,则固体乙中一定含有______________。
(3)写出一个图中所发生的化学方程式_______________________________。
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,
则:
①溶液甲中一定含有Al(NO3) 3和Zn(NO3)2
②固体乙中一定含有Ag,可能含有Cu和Zn
③若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2
④向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2.上述四种说法正确的个数为( )
A.1个B.2个C.3个D.4个
二、金属与酸反应的图像
例3.将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量反应时间的关系如图所示,下列说法错误的是( )
A.反应结束后镁一定有剩余
B.反应消耗盐酸的总质量一定相等
C.0﹣t1时段,产生氢气的质量镁比铁大
D.0﹣t2时段,参加反应的镁的质量与铁相等
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且质量相同的稀硫酸中,反应生成H2的质量与反应时间的关系如图所示。
根据图中所提供的信息,得出的结论正确的是(已知:
A、B、C在生成物中均为+2价)
A.硫酸反应完,A、B、C均可能有剩余
B.反应速率最大的是A
C.相对原子质量是A>B>C
D.金属活动性顺序是C>B>A
备考猜押
一、选择题
1、制造飞机的外壳需要用到硬铝,硬铝属于()
A、合成材料B。
金属材料C。
天然材料D。
复合材料
2.夏天防雷电,远离金属。
这是因为金属具有()
A导电性B导热性C.延展性D.光泽
3.根据金属活动性顺序判断,下列化学方程式正确的是()
A.2Fe+6HCl=2FeCl3+3H2↑B.Zn+SnCl2=Sn+ZnCl2
C.Cu+H2SO4=CuSO4+H2↑D.Cu+ZnSO4=Zn+CuSO4
4.下列措施中,不宜用于博物錧保存枪支大炮等铁制文物的是()
A.外表涂抹一层油B.保持展馆内空气干燥
C.半浸在敞口水箱中存放D.提醒观众不要用手触摸
5.将锌和铜的混合粉末加入到硝酸银溶液中,,充分反应后过滤。
下列对滤液中溶质成分的判断,其中一定错误的是()
A.硝酸锌B.硝酸铜和硝酸锌C..硝酸银和硝酸锌D..硝酸锌、硝酸银、硝酸铜
6.将一定质量铜和锌的粉末加入到一定质量的硝酸银溶液中,充分反应后过滤,向滤渣中滴加少量的稀盐酸,无气泡产生.则下列说法中正确的是( )
A. 滤渣中一定含有银和铜B. 滤渣中一定含有银、可能含有铜
C. 滤液中的溶质一定含有硝酸锌D. 滤液中的溶质一定不含有硝酸银
7.探究镁、铁、铜三种金属的活动性顺序,下列试剂的选择方案不可行的是()
A.镁、铜、硫酸亚铁溶液B.镁、铁、铜、稀硫酸
C.铁、铜、硫酸镁溶液D.铁、硫酸镁溶液、硫酸铜溶液
8、在硝酸银、硝酸铜的混合溶液中加入一定量的锌粉,反应停止后过滤,滤液仍为蓝色。
有关判断正确的是()
A.滤渣中一定有银、没有铜和锌
B..滤渣中一定有银和锌,可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银
D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
9、相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中正确的是()
10、下列事实可用于判断X、Y两种金属的活动性顺序的是()
①X能和稀盐酸反应而Y不能;②X能从Y的盐溶液中置换出Y;③常温下X能与氧气反应而Y不能;④在化合物中X显+3价,Y显+2价。
A.①②B.①②③C.③④D.①②④
11.2015苏州下列关于金属的说法正确的是()
A. 波尔多液的配制可以在铁质容器中进行
B. 铝制品抗腐蚀能力较铁制品强
C. 用FeSO4溶液、Cu和Ag三种物质可以验证Fe、Cu、Ag三种金属的活动性强弱顺序
D. 铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe3O4
12.郑州市地铁正式开通方便了人们的生活,修建地铁需要大量钢铁制品。
现代工业利用磁铁矿炼铁的主要反应原理是________________________________________(用化学方程式表示)。
疏松的铁锈不能阻碍里层的铁继续与________反应,因此铁制品可以全部锈蚀。
用盐酸除铁锈的化学方程式为_____________。
13.金属及金属材料在生产生活中应用广泛。
(1)铜可以拉成铜丝,这是利用金属的_________。
(2)铝具有很好的抗腐蚀性能,原因是____________________(用化学方程式表示)。
(3)小明在学习金属的化学性质时,做了如下探究实验(金属片已打磨):
①将铁片插入硫酸铜溶液中,铁片表面的现象是_____________________;
②将铜片插入硝酸银溶液中,反应的化学方程式是__________________。
此探究实验的目的是________________________________。
(4)某同学将一小包铜粉和铁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体和蓝色滤液。
滤液中的溶质组成可能为____________________。
铜和硝酸银溶液反应的化学方程式为________________。
14.将锌粉加入含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,若滤液中只含有一种溶质,则滤渣中一定含有_________,,可能含有________;若滤渣中只含有两种金属,则滤液中一定含有的金属离子是__________。
14.在Cu(NO3)2和AgNO3的混合溶液中,加入一定量的锌粉,使之充分反应后有下列情况:
(1)若反应后锌有剩余,则溶液中所含溶质为______.
(2)若反应后,将溶液过滤,所得固体物质加盐酸没有气体产生,则固体物质中一定有______,可能有______.
(3)若反应后,将析出的金属过滤,向滤液中滴加NaCl溶液,有不溶于稀HNO3的白色沉淀生成,则此时溶液中含有的溶质为______.
15.某同学设计如图所示的装置。
将铁丝放在潮湿的空气中,一周后,除观察到铁丝生锈,还观察到的现象是;打开K后,观察到铁锈消失,写出该反应的化学方程式____________________________________;随着盐酸的滴加,过一会观察到烧杯内的导管口有气泡冒出,请解释产生该现象的原因。
16.。
某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示。
请回答有关问题:
(1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是C和D,导管接口的连接顺序为a→( )→( )→( )。
C装置中NaOH的作用是
(2)实验开始时,应 (填“先加热再通CO”或“先通CO再加热”),目的是 。
(3)实验进行一段时间后,玻璃管A中出现的现象为 ,反应方程式
为____________________.
(4)除CO外,还有哪些物质可以还原Fe2O3 (请写一物质的化学式)。
16.某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示。
请回答有关问题:
(1)为避免一氧化碳污染空气,并回收利用一氧化碳,B装置应连接c.、d.哪个装置?
(2)实验形如时应先通CO的目的是什么?
(3)实验进行一段时间后,A中玻璃管出现的现象有什么?
写出该反应的化学方程式。
满分冲关
1、现有铁与另一种金属组成的混合物1.2g,与足量稀硫酸反应生成H20.1g,则混合物中的另一种金属可能是( )
A.MgB.AlC.ZnD.Cu
2.金属M与AgNO3溶液反应的化学方程式为:
M+2AgNO3=M(NO3)2+2Ag.则下列说法错误的是()
A.金属M可能是铝B.M的金属活动性比Ag强
C.该反应属于分解反应D.该反应前后M的化合价发生了改变
3.向硝酸银和硝酸镁的混合溶液中加入一定质量的铝和铁的混合粉末,充分反应后过滤,得到滤渣和浅绿色溶液。
关于滤渣和滤液有下列说法:
①向滤渣中加入稀盐酸,可能有气泡产生;②向滤液中加入稀盐酸,一定有沉淀产生③滤渣中一定含有银④滤液中一定含有硝酸亚铁和硝酸镁,可能含有硝酸铝。
以上说法正确的个数为()
A.0个B.1个C.2个D.3个
4.将5.6克含有一种杂质的铁粉与足量的稀盐酸反应,生成0.21克氢气,则该铁粉中,混入的导体是(填铜或铝)。
把这种铁粉放入硝酸银溶液中,充分反应后过滤,将滤渣洗净,滴入稀硫酸,如果无气泡产生,则滤液中一定含有的溶质是________________(填化学式);如果有气泡产生,则滤渣的成分中一定有____________(填化学式)
5.金属材料在生产生活中应用广泛,铝、铁、铜是三种常见的金属。
(1)高铁列车车体用铝合金材料而不用纯铝的原因是什么?
(2)若用实验验证AlFeCu三种金属的活动性顺序,请写出一种可行方案所需的物质。
(3)化学小组为回收实验室废液(含硫酸铝和硫酸铜)中的铜,设计了如图的实验方案:
1写出溶液乙中溶质的化学式
②写出反应b的化学方程式。
6.金属的活动性:
为了探究铜、锌、铁的活动性,把等表面积的铁片放入硫酸铜的溶液中。
(1)如何判断它们是否发生了化学反应?
(2)反应后,其中一个试管的溶液质量会增加,请写出该试管中发生反应的化学方程式________________________________________________________。
(3)上述实验不能证明三种金属的活动性顺序,需补做的实验是________________。
金属活动性顺序及应用专项训练
类型一金属与盐溶液反应后滤液、滤渣成分的判断
1.将一定质量的铁粉加至H2SO4、MhSO4和CuSO4的混合溶液中,充分反应后过滤,得滤液M和滤渣N.。
下列有关说法中,不合理的是
A.滤液M中一定存在Fe2+
B.滤渣N的质量一定小于加入铁粉的质量
C.滤渣N中一定没有单质镁
D.滤液M中至少含有两种金属阳离子
2.向某FeSO4和CuSO4的混合溶液中加入一定质量的锌粉,充分反应后过滤,得到滤液和滤渣。
向滤渣中加入稀盐酸,有气泡产生。
根据实验现象判断,下列说法中正确的是()
A、滤液中一定存在FeSO4B。
\滤液的颜色呈蓝色
C、滤渣中一定含有ZnD.、滤渣中一定含有铁和铜
2.在FeSO4和CuSO4的混合溶液中加入一定量锌粉,充分反应后得到一定量固体。
过滤后向固体中加入少量稀硫酸,有气泡产生。
对固体成分的说法正确的是
①一定含有Zn ②一定含有Fe ③一定含有Cu
④可能含有Zn ⑤可能含有Fe
A.①②③B.②③④C.③④⑤D.①②④
3、向Al(NO3)3和AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤出的固体中加稀盐酸时,有气泡产生。
则滤液中含有的金属离子有________,有关反应的化学方程式为______________________。
(写一个即可)
4.某溶液中含有Cu(NO3)2和AgNO3,现向其中逐渐加入一定质量的铁粉,若完全反应后溶液中溶质为3种,则溶液中存在的金属单质为________________。
该反应过程中质量的变化情况为________________________。
5.向一定质量Cu(NO3)2和AgNO3,的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示。
请回答下列问题:
(1)取a点溶液,滴加稀盐酸,观察到的现象是什么?
(2)若取c---d段固体,滴加稀盐酸,观察到的现象是什么?
(3)写出该反应过程中溶液发生变化的化学方程式。
6.向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如右图所示,下列说法正确的是
A.a点溶液中的溶质有2种
B.c点溶液中溶质为Zn(NO3)2
C.若取b~c段溶液,滴加稀盐酸,有白色沉淀
D.取d点的固体,加入稀盐酸,无气泡产生
7.在AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,没有气泡产生。
(1)请说出滤出的固体中一定含有哪些成分?
滤液中一定含有哪些成分?
(2)写出反应过程中一定发生的化学方程式。
8.某化学小组的同学进行了如图实验,把固体乙洗涤后加入稀盐酸有气体放出。
(1)固体乙的成分可能是什么?
(2)溶液甲中一定含有的溶质是_____ (写化学式)
(3)写出上述过程中可能发生反应的一个化学方程式_____.
9.某校实验室废水中含有AgNO3、Cu(NO3)2、Zn(NO3)2三种物质,该校化学兴趣小组的同学为了从中分享、回收金属铜和银,设计了如图实验方案(实验中未引进其他金属离子),回答问题:
(1)分别写出固体X的化学式和滤液B中溶质的化学式。
(2(写出实验过程中发生反应的化学方程式。
某实验室的废水中含有大量AgNO3、Zn(NO3)2和Fe(NO3)2,课外小组同学欲从该废液中回收银,并得到副产品硫酸亚铁晶体.实验方案如下:
(1)操作①的名称是_________,固体甲中含有的物质是(填化学式)_________;溶液乙中所含溶质的化学式为_________.
(2)写出步骤①的化学方程式:
_________.
(3)检验步骤①向废水中加入A过量的方法是_______
某化工厂排出的废液中含有AgNO3、Zn(NO3)2和Cu(NO3)2三种物质.为了分离并回收金属银和铜,化学课外小组的同学设计了如下实验方案:
根据以上实验方案你认为:
(1)当所加入的铜粉恰好完全反应,固体X是______;滤液B的溶质有______.操作1、2的名称都是______.
(2)写出废液加入适量铜粉发生的反应方程式______,该反应的基本类型是______.
(3)写出固体Y中除去过量铁粉的化学实验方法:
______.
类型二金属活动性顺序的实验设计及判断
1.为了探究abc三种金属的活动性顺序,某同学设计了如下实验。
实验结论正确的是()
A.b>a>c B.a>b>c C.c>b>a D.c>a>b
2.将X、Y两种金属片分别插人硫酸铜溶液中.X没有发生明显变化,Y表面析出金属铜.据此判断这三种金属的活动顺序是()
A.Y>铜>XB.X>铜>YC.铜>Y>XD.Y>X>铜
3.下列可用于验证FeCuAg三种金属的活动性顺序的一组药品是()
A.Cu、Ag、FeSO4溶液
B.Cu、Fe、AgNO3溶液
C.Ag、Fe、CuSO4溶液
D.Ag、Cu(NO3)2溶液、FeSO4溶液
4.小明为了比较X、Y、Z、W四种金属的活动性顺序,利用这四种金属单质、稀盐酸、Z的硝酸盐溶液和W的硝酸盐溶液,进行有关实验,结果如下表(“√”表示能反应,“—”表示不能反应,“空白”表示未做该实验)。
请你判断四种金属的活动性顺序为
A.Y>Z>X>W B.X>Y>W>Z
C.X>W>Y>Z D.W>X>Y>Z
5.为验证铝、铁、铜三种金属的活动性强弱,小佳用三支试管,只取一次稀盐酸就达到了目的。
实验流程如图所示:
(1)能证明铜的活动性较铁弱的现象是________________________。
(2)D处试管中可观察到的现象为________________________。
(3)三种金属的活动性由强到弱的顺序为____________________。
(4)实验中要求所加铁粉过量,如果加入铁粉不足,为保证实验成功,应该注意的事项是________________________。
(5)写出实验中发生的置换反应的化学方程式________________(任写一个)
同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案.请你和他们一起完善下表的探究方案并回答有关问题.
(1)填表
实验步骤
观察到的现象
①在试管中取少量盐酸,插入铁丝,充分作用.
_________
②在①所得的溶液中,插入______,充分作用.
无明显现象
③在②所得的溶液中,插入______,充分作用.
_________
(2)将铝丝插入前应进行的操作是________________________________ ;
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出
Al>Fe>H>Cu的结论.小华要补充的实验是________________________________ ;
(4)分析反应①和②,可以得到:
铝、铁、铜三种金属的活动性由强到弱的顺序是________________________________.
(5)实验总结:
要探究铝、铁、铜三种金属的活动性强弱,方案有两种,其一取其中两种金属和一种金属的盐溶液进行反应,则这种盐溶液可以是________ 溶液;其二取其中两种金属的盐溶液和一种金属进行反应,则这种金属是________ .
在Cu(NO3)2和AgNO3的混合溶液中,加入一定量的锌粉,使之充分反应后有下列情况:
(1)若反应后锌有剩余,则溶液中所含溶质为________ .
(2)若反应后,将溶液过滤,所得固体物质加盐酸没有气体产生,则固体物质中一定有________ ,可能有________ .
(3)若反应后,将析出的金属过滤,向滤液中滴加NaCl溶液,有不溶于稀HNO3的白色沉淀生成,则此时溶液中含有的溶质为________ .
7.康康把等质量的X、Y、Z三种金属分别加入到同体积、同浓度的足量稀盐酸中;反应关系如图;Z加入YNO3的溶液中有Y生成.请判断:
(1)X、Y、Z三种金属的活动性由强到弱的顺序.
(2)试举出一种符合要求的X,然后写出X与ZSO4溶液反应的现象.
(3)试举出一种符合要求的Z,然后写出Z与YNO3溶液反应的化学方程式.
8.为探究锌、铁、铜、银四种金属活动性顺序,某同学设计了如如图所示的一组实验.这组实验并不能达到实验目的,需要再补充一个实验才能完全证明四种金属的活动性顺序.请写出所补充实验步骤、现象及有关反应的化学方程式.
9.在探究金属化学性质时,小组同学进行了如下实验:
①取一根铜丝、一枚铁钉和一小块银片分别用砂纸打磨;②向三支试管中分别加入适量的硝酸银溶液、稀盐酸、氯化亚铁溶液;③将打磨好的铜丝插入硝酸银溶液中,将打磨好的铁钉放入稀盐酸中,将银片放入氯化亚铁溶液中;④一会儿之后将铜丝、铁钉和银片取出,将三支试管中的液体倒入烧杯中待处理。
(1)写出A试管中发生反应的化学方程式,根据该反应可得出的结论是什么?
(2)仅由上述实验无法比较铁、铜、银三种金属的活动性强弱,为比较三种金属的活动性强弱,还必须补充的实验是什么?
(写出操作及现象)?
(3)步骤④中观察到烧杯底总有白色沉淀。
写出该沉淀的化学式。
如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题:
(1)A中的实验现象是________________________________________________
(2)写出C中发生反应的化学方程式________________________________ .
反应完后溶液显酸性,此时向其中滴入紫色石蕊溶液,溶液显____________ 色.
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是____________ (填序号).
(4)开始反应后,D中溶液逐渐变为黄色,反应的化学方程式是________________。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 金属 性质
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
