 广东省深圳市中考一模化学试题答案和解析.docx
广东省深圳市中考一模化学试题答案和解析.docx
- 文档编号:9325095
- 上传时间:2023-02-04
- 格式:DOCX
- 页数:16
- 大小:204.89KB
广东省深圳市中考一模化学试题答案和解析.docx
《广东省深圳市中考一模化学试题答案和解析.docx》由会员分享,可在线阅读,更多相关《广东省深圳市中考一模化学试题答案和解析.docx(16页珍藏版)》请在冰豆网上搜索。
广东省深圳市中考一模化学试题答案和解析
【最新】广东省深圳市中考一模化学试题
学校:
姓名:
班级:
考号:
一、单选题
1.下列化学用语表达正确的是()
A.两个氮分子:
2N2
B.三个氧原子:
03
C.钙离子:
6+2
D.
硫酸饮:
FeSO4
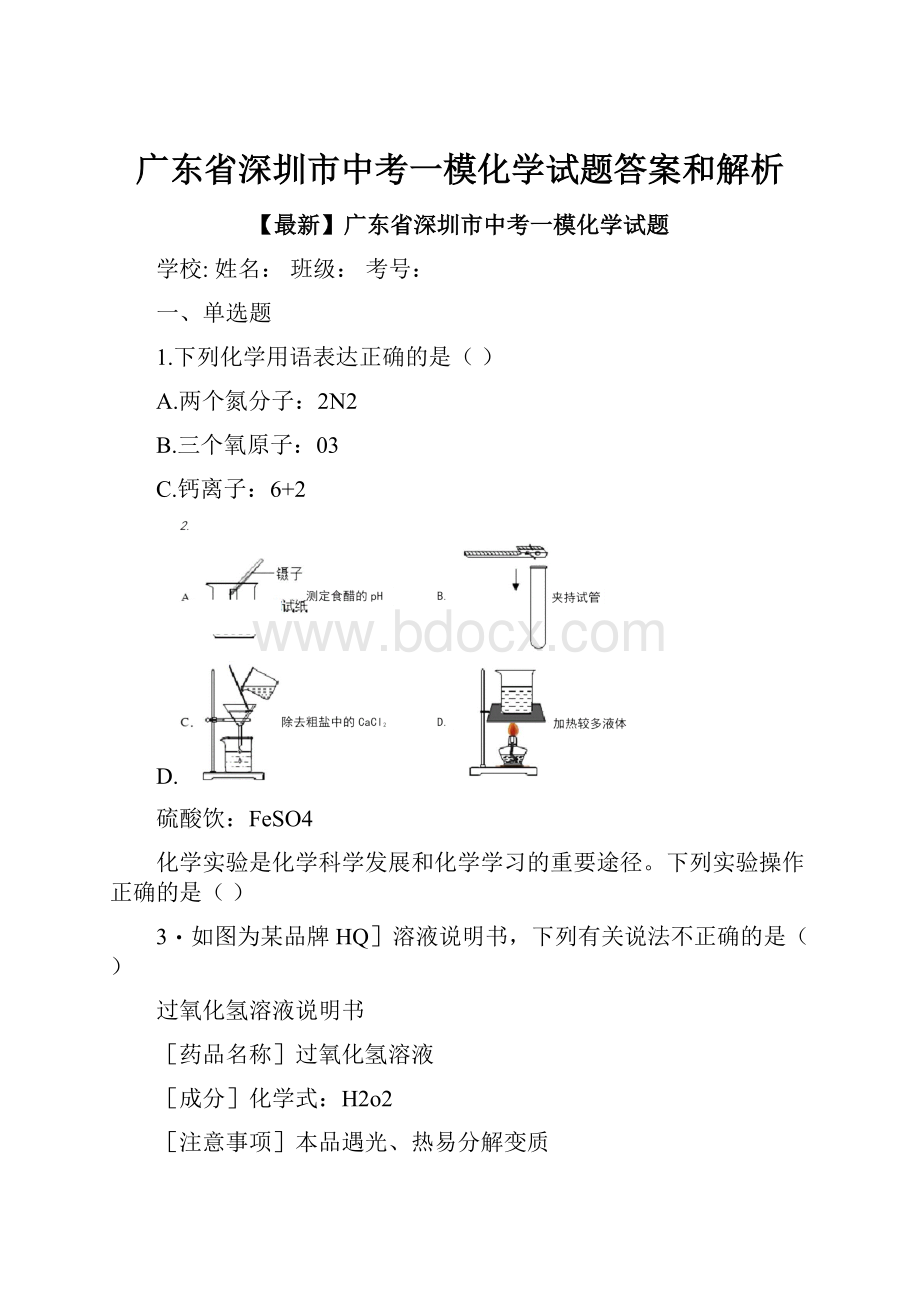
化学实验是化学科学发展和化学学习的重要途径。
下列实验操作正确的是()
3・如图为某品牌HQ]溶液说明书,下列有关说法不正确的是()
过氧化氢溶液说明书
[药品名称]过氧化氢溶液
[成分]化学式:
H2o2
[注意事项]本品遇光、热易分解变质
[溶质质量分数]30%
[净含量]500111L
[贮藏]遮光、密闭、在阴凉处(不超过20°C)保存。
A.该溶液中各成分均属于氧化物
B.该溶液应保存在棕色试剂瓶中
C.一瓶该溶液中H9?
的质量为150g
D.lOg该溶液加水桶释町得50g6%的溶液
4.锂(L1)的元素信息图和氯(C1)元素的结构示意如图。
下列描述正确的是(
A.L1的相对原子质量为6.941g
B.Li、Cl元素形成的化合物为LiClz
C.Cl-的结构:
x=8,质子数=17
D.Li与6反应生成氧化锂:
Li+O.=L1.O
5・蜂蜡可由十六烷酸(化学式为C16H32On,相对分子质量为256)与另一种物质反应制成。
下列关于十六烷酸的说法正确的是()
A.十六烷酸中含16个碳原子
B.十六烷酸的化学式中:
n=2
C.氢元素质量分数比氧元素小
D.碳、氢元素质量比为1:
2
6.工业上用甲和乙两种物质在一定条件下反应生成丙和X,反应的微观过程如图所示。
参加反应的甲、乙与丙的质量比为23:
®+逐—定条件-、
甲乙丙
A.甲、丙均是由分子构成的物质
B.物质X化学式为NaNH2
C.乙与丙的化学计量数之比为2:
1
D.该反应类型属于置换反应
7.卞列实验方案,设计不合理的是(
某小组用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁(如图所示)。
下
讪阴喚或变隔这种关系的“⑥㉛①
选项
甲
乙
丙
T
A
化合物
盐酸
M11O:
铁粉
B
合成材料
合金
合成纤维
合成橡胶
C
化学变化
置换反应
化合反应
复分解反应
D
放热反应
硫在空气中燃烧
NaOH溶液与H2SO4反应
咼温分解石灰石
A・AE・BC・CD・D
9.甲、乙试管中各盛有lOg水,向其中一支试管中加入3gNaCO3粉末,另一支试管中
加入3gNaCl粉末,按图1、2进行实验,下列说法正确的是()
A.乙中加入的粉末是NaCl
E•图2中,甲溶液可能是饱和溶液
C•图1中,甲、乙溶液变饱和,添加相应溶质的质量:
甲〉乙
D.可采用冷却热饱和溶液的方法除去Na2CO3中少量NnCl
10.
用桶酸M探究物质的性质。
下列叙述正确的是()
A・②处有气泡、③处无现彖,则金属活动性:
Zii>Cu
B.④处铁锈消失,有气泡产生,则铁锈与稀酸反应生成了H?
C.④⑤处有明显现象,则M—定为桶HC1
D.若⑥处为NaOH溶液,滴加酚駄呈无色,则溶液的pH=7
二实验題
11・根据图示器材(省略夹持仪器)回答问题:
b
止水夹玻璃片
c
图2
(1)仪器e的名称是。
(2)加热分解暗紫色粉末制取02的化学方程式为,制取并收集一瓶O,用于做铁
丝燃烧实验,应选取的仪器是c、h、i、(填序号),铁丝在6中燃烧现彖:
。
(3)用锌粒和桶盐酸制备H:
为便于控制反应发生或终止,则发生装置应选取仪器c、
J、组合(填序号)。
(4)氢化钙(CaHJ常温下能与水反应生成一种碱和吐,放热可用作便携式热源。
小明利用(3)中产生的H?
与金属钙反应制取CaH:
(见图2)。
请回答:
1洗气瓶中p为NaOH溶液,则q应选F列试剂的(填序号)。
ANaHCOs溶液
BKOH溶液
C浓H2SO4
2为防止Ca被氧化,在加热Ca之前必须进行的操作是o
3CaH:
与水反应的化学方程式为o
三、流程題
12.为了防上污染,用黄铜矿(主要皮分是CuFeS2及少量含Zn的化合物)炼铜时,将
产生的废气、废液转换成工业原料,设计流程如卞:
黄铜矿
(1)己知步骤①为化合反应且反应前后各元素的化合价均不变,则X的化学式为.
(2)写出步骤②中反应的化学方程式o(任写一个)
(3)步骤③的操作是,固体B的化学式为o
(4)写出固体D的一种用途:
滤液a和b中相同溶质的名称为o
(5)若操作过程中物质的损失忽略不计,要生成2.8gB和3.2gD,则加入Zn的质量应
大于go
四-综合应用题
13.胃舒平(含Al(OH)J、小苏打片(含NaHCO,)、胃酸抑制剂(主要含CaCO,、
Mg(OH)2)都是常用的中和胃酸的药物。
(1)胃舒平与胃酸发生反应的化学方程式为:
。
(2)为了探究工业小苏打中是否含少量的NaCb设计如下实验:
(假设小苏打片中其
他物质均不含C1J
实验步骤
实验现彖
实验结论
第一步:
取1片小苏打于试管中,加入适量水充分溶解,再滴加足量的稀HNO3o
有产生
说明小苏打片中含有NaHCOjo
第二步:
再往上述溶液中滴加
少溶液。
(写化学式)
有产生
说明小苏打片中含有NaCl0
(3)胃酸抑制剂每片lg,取10片于烧杯中,再加入50gMHCl,烧杯中剩余物的质量与时间的关系如下表:
(己知其他物质不与桶盐酸反应)
时间/s
0
10
20
30
40
50
剩余物的质量/g
60
59.12
5&24
5736
56.48
56.48
求每片胃酸抑制剂中CaCOs的质量分数(写出计算过程)。
参考答案
1.A
【解析】
【详解】
A、一个氮分子有两个氮原子。
在分子前加上数字表示分子的个数。
则两个氮分子可表示为:
2N2oA正确;
B、氧原子的元素符号为O。
在元素符号前加上相应的数字,表示原子的个数。
故三个氧原子可表示为:
30。
B错误;
C、离子的表示方法为在元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。
钙离子可表示为:
Ca2\C错误;
D、硫酸铁中铁元素显+3价,硫酸根显-2价,其化学式为:
Fe2(SO4)3oD错误。
故选A。
2.D
【详解】
A、测定溶液的pH的方法是:
将pH试纸放在白瓷板或玻璃片上,用干燥的玻璃棒籠取少量待测液滴到pH试纸上,变色后,将其与标准比色卡对比。
A错误;
B、使用试管夹夹持试管,应该将试管夹从下向上套,夹持在距离试管II1/3处。
E错误;
C、氯化钙溶于水会形成溶液,过滤只能除去难溶于水的杂质。
C错误;
D、加热较多的液体应该用烧杯,并且放在石棉网上进行加热。
D正确。
故选D。
3.D
【分析】
氧化物:
由两种元素组成,其中一种元素为氧元素的化合物
【详解】
A、过氧化氢溶液是指过氧化氢的水溶液,溶质是过氧化氢,溶剂是水。
过氧化氢、水都符合氧化物的概念,属于氧化物。
A正确;
B、过氧化氢溶液见光易分解,所以应该保存在透光性差的棕色瓶中。
E正确:
C、溶质质量分数的定义是溶质的质量和溶液的质量的比值,而不是溶液的体积。
题目中已知过氧化氢溶液的体积,没有过氧化氢溶液的密度,所以不能求出溶液中过氧化氢的质屋。
C错误;
D、该溶液的溶质质量分数是30%,则10g溶液中溶质的质量为:
10gx30%=3g°加水稀释后,溶质的质量不变,则6%浓度的溶液的质量为:
3g一6%=50g。
D正确。
故选D。
4.C
【详解】
A、根据图示可知,锂的相对原子质量为6.941oA错误;
B、根据图示可知,Li在化学反应中,易失去1个电子,显+1价。
C1在化学反应中易得到1
个电子,显」价。
Li、C1元素形成的化合物为LiCLE错误;
C、氯离子的质子数为17,核外电子数为18。
则2+8+x=18,解得x=8。
C正确;
D、Li与6反应生成氧化锂,化学反应方程式为:
4Li+O2=2Li2OoD错误。
故选C。
5.B
【详解】
A、该物质是由十六烷酸分子构成。
一个十六烷酸分子有16个碳原子。
A错误;
B、十六烷酸的相对分子质量为256,则12xl6+lx32+16xn=256,解得n=2。
E正确;
C、十六烷酸中,碳、氢、氧三种元素的质量比为:
(12x16):
(1X32):
(16x2)=192:
32:
32。
则氢元素的质量分数和氧元素的质量分数相等。
C错误;
D、十六烷酸中,碳、氢、氧三种元素的质量比为:
(12x16):
(1X32):
(16x2)=192:
32:
32。
则碳、氢元素的质量比为192:
32=6:
1。
D错误。
故选E。
6.A
【分析】
根据图示可知,甲是Na,乙是NHs,丙是H”根据题意分析可知,设该反应方程式中,甲的化学计量数为x,乙的化学计量数为y,丙的化学计量数为z。
参加反应的甲、乙与丙的质量比为23:
17:
1,则(23xX):
(17xy):
(2")=23:
17:
1,解得x:
y:
z=2:
2:
lo则该反应的一定条件
方程式为:
2Na+2NH3H,+2NaNHz。
置换反应:
单质和化合物反应生成另一种单质和另一种化合物。
【详解】
A、甲是钠,是由钠原子构成的物质。
丙是氢气,是由氢分子构成的物质。
A错误;
B、根据分析可知,X是NaNH2oB正确;
C、根据分析可知,乙和丙的化学计量数之比为2:
1。
C正确;
D、根据分析可知,该反应属于置换反应。
D正确。
故选A。
7.C
【详解】
A、碳和二氧化碳在高温的条件下反应生成一氧化碳,可以除去杂质。
A正确;
B、食用油难溶于水,但是易溶于汽油形成溶液。
可以探究不同物质在同一溶剂中的溶解性。
B正确:
C、氢氧化钠溶液和碳酸钠溶液呈碱性,则加入酚猷后,溶液均变为红色,无法鉴别。
C错误;
D、利用激光笔,可以达到白磷的着火点,从而使白磷燃烧,消耗装置内的氧气,从而进行
测定。
D正确。
故选C。
8.D
【详解】
A、盐酸是氯化氢的水溶液,属于混合物。
二氧化鎰是由怯、氧两种元素组成的化合物。
铁粉是由铁元素组成的单质。
A错误:
B、合金是金属材料。
合成纤维、合成橡胶属于合成材料。
E错误:
C、置换反应、化合反应、复分解反应均属于化学反应。
C错误;
D、物质的燃烧、中和反应都是放热反应。
高温分解石灰石需要吸收热量,属于吸热反应。
D正确。
故选D。
9.D
【详解】
A、降温后乙中明显析出晶体,故乙是碳酸钠,甲是氯化钠。
A错误;
B、甲中是氯化钠,含有溶质3g,而在0C时氯化钠的溶解度为35.7g,故不会是饱和溶液,
B错误;
C、图1中,30°C时碳酸钠的溶解度大于氯化钠的溶解度,故甲、乙溶液变饱和,添加相应溶质的质量:
甲<乙。
C错误;
D、碳酸钠的溶解度随温度的升高而增人且变化趋势明显,故除去碳酸钠中的少量氯化钠应该利用冷却热饱和溶液(或降温结晶)的方法。
D正确。
故选D。
10.A
【详解】
A、②处有气泡则说明锌在金属活动性顺序中排在氢之前,③处无现彖则说明在金属活动性顺序中铜排在氢之后,则金属活动性:
Zn>Cu0A正确;
B、铁锈的主要成分是氧化铁,氧化铁和酸反应生成铁盐和水,④处铁锈消失后,铁再与桶酸反应生成亚铁盐和氢气,会看到有气泡产生。
E错误;
C、紫色石蕊溶液遇酸变红,锌和常见的桶盐酸、桶硫酸反应生成氢气,铁锈可以和桶盐酸、桶硫酸反应形成黄色溶液,大理石可以和桶盐酸、桶硫酸等常见的酸反应生成二氧化碳,①②④⑤处有明显现象,则M不一定为桥HC1,也可能是其他酸。
C错误;
D、若⑥处为NaOH溶液,滴加酚酥呈红色,溶液的pH>7oD错误。
故选A。
A
11.量筒2KMiiO4=K2MnO4+MnO2+O2ta.b、g、1、o剧烈燃烧,火星四
射,放出大量的热,生成照色固体f、nC先通入一段时间的氢气,排出装置内
空气CaH2+2H2O=Ca(OH)2+2H2f
【详解】
(1)仪器e是量筒。
故答案为:
量筒;
(2)暗紫色固体是高猛酸钾,高镭酸钾在加热的条件下分解出鎰酸钾、二氧化怯和氧气。
制取并收集氧气的装置为:
铁架台、试管、酒精灯、单孔橡胶塞、导管、水槽、集气瓶、玻璃片。
铁丝在氧气中燃烧的现象是:
剧烈燃烧,火星四射,放出大量的热,生成黑色固体。
A
故答案为:
2KMiiO4=K2MnO4+MnO2+O,t.a、b、g、1、o、剧烈燃烧,火星四射,放
出人量的热,生成黑色固体;
(3)用锌粒和桶盐酸制备H“为便于控制反应发生或终止,应该选择的发生装置为:
试管、带孔塑料片的长颈漏斗、双孔橡胶塞、带止水夹的导管。
故答案为:
f、m
(4)①利用金属钙和氢气制取氢化钙时,应该先将生成的氢气除去杂质氯化氢气体并干燥。
所以q瓶中应该放浓硫酸。
故答案为:
C;
2为了防止钙被氧化,应该先通入一段时间的氢气,将装置内的氢气排尽,然后再与其反应。
故答案为:
先通入一段时间的氢气,排出装置内空气;
3根据题意分析可知,氢化钙和水反应生成氢氧化钙和氢气。
故答案为:
CaH2+2H2O=Ca(OH)2+2H2To
12.H2SO4Zu+FeSO尸ZnSCb+Fe(或Zn+CuSO尸ZnSCU+Cu)用磁铁吸引Fe
做导线硫酸锌6.5
【详解】
(1)步骤①是化合反应,三氧化硫和水反应,而且反应前后各个元素的化合价不变,则该反应为三氧化硫和水反应生成硫酸。
硫酸和三氧化硫中,硫元素的化合价均为+6价。
故答案为:
H2SO4;
(2)步骤②中,锌和硫酸铜能反应生成硫酸锌和铜,锌和硫酸亚铁反应生成硫酸锌和铁,滤液a的溶质为硫酸锌。
故答案为:
Zn+FeSO尸ZnSObFe(或ZnHuSO尸ZnSCU+Cu);
(3)步骤③中为了分离铁和另外的锌、铜金属,可以用磁铁吸引。
则固体B是铁,固体C是锌、铜。
故答案为:
用磁铁吸引、Fe;
(4)固体C是锌、铜,向其中加入X,即硫酸后,锌和硫酸反应生成硫酸锌,铜不反应。
则固体D是金属铜,滤液b是硫酸锌溶液。
滤液a、b共有的溶质为硫酸锌。
故答案为:
做导线、硫酸锌;
(5)固体E是铁,固体D是铜。
则要生成2.8g的铁和3.2g的铜。
根据锌和硫酸铜反应的方程式、锌和硫酸亚佚反应的方程式可知:
每消耗65份质量的锌就会生成64份质量的铜,每消耗65份质量的锌就会56份质量的铁。
则将数据代入后,通过计算可知,需要3.25g的锌能生成2.8g的铁,需要3.25g的锌能生成3.2g的铜,则至少需要6.5g的锌。
故答案为:
6.5o
13.A1(OH)3+3HC1=A1C13+3H9气泡AgNCh白色沉淀80%
【详解】
(1)胃酸的主要成分是盐酸。
盐酸和氢氧化铝反应生成氯化铝和水。
故答案为:
A1(OH)3+3HC1=A1C13+3H9:
(2)取1片小苏打于试管中,加入适量水充分溶解。
在滴加足量的桥硝酸,桶硝酸和碳酸氢钠反应生成硝酸钠、水和二氧化碳气体。
再向其中加入少量硝酸银溶液,硝酸银溶液和氯化钠反应生成硝酸钠和氯化银沉淀。
故答案为:
气泡、AgNOs、白色沉淀;
(3)设10片样品中含有碳酸钙的质量为X。
反应生成二氧化碳的质量为:
60g-56.48g=3.52g
CaCO3+2HCl=CaCl2+H2O十C02T
10044
x3.52g
100_x
石_3.52g
解得x=8g
所以样品中碳酸钙的质量分数为:
浮"00%=80%。
10g
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 广东省 深圳市 中考 化学试题 答案 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《JAVA编程基础》课程标准软件16级.docx
《JAVA编程基础》课程标准软件16级.docx
