 高三化学一轮复习元素周期表及其应用Word文档格式.docx
高三化学一轮复习元素周期表及其应用Word文档格式.docx
- 文档编号:13786922
- 上传时间:2022-10-13
- 格式:DOCX
- 页数:10
- 大小:92.07KB
高三化学一轮复习元素周期表及其应用Word文档格式.docx
《高三化学一轮复习元素周期表及其应用Word文档格式.docx》由会员分享,可在线阅读,更多相关《高三化学一轮复习元素周期表及其应用Word文档格式.docx(10页珍藏版)》请在冰豆网上搜索。
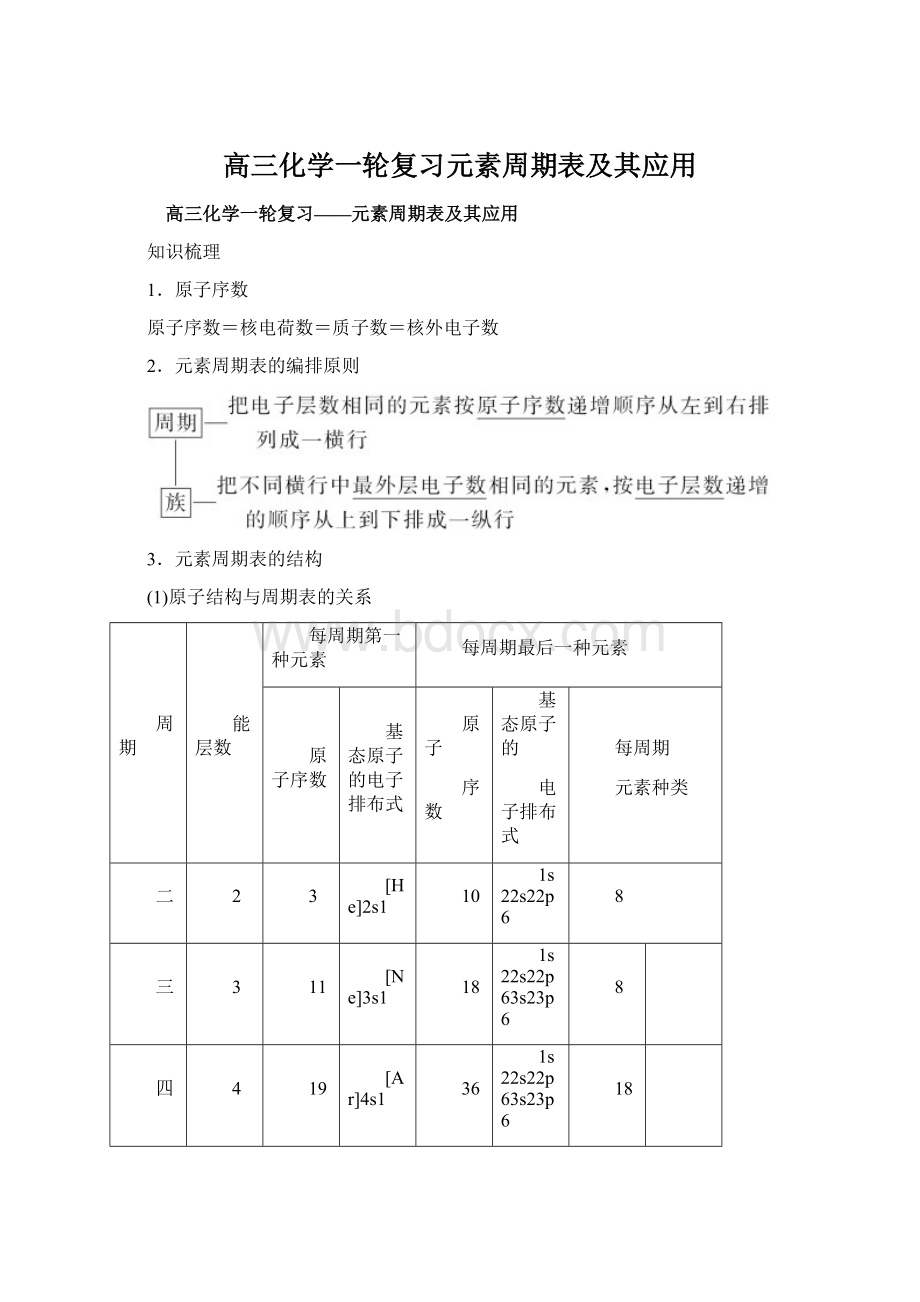
1s22s22p6
8
三
11
[Ne]3s1
18
1s22s22p63s23p6
四
4
19
[Ar]4s1
36
3d104s24p6
五
5
37
[Kr]5s1
54
1s22s22p63s23p63d10
4s24p64d105s25p6
六
6
55
[Xe]6s1
86
1s22s22p63s23p63d104s24p6
4d104f145s25p65d106s26p6
32
(2)每族元素的价电子排布特点
①主族
主族
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
排布特点
ns1
ns2
ns2np1
ns2np2
ns2np3
ns2np4
ns2np5
②0族:
He:
1s2;
其他ns2np6。
③过渡元素(副族和第Ⅷ族):
(n-1)d1~10ns1~2。
(3)元素周期表的分区
①根据核外电子排布分区
a.分区简图
b.各区元素化学性质及原子最外层电子排布特点
分区
元素分布
外围电子排布
元素性质特点
s区
ⅠA族、ⅡA族
ns1~2
除氢外都是活泼金属元素;
通常是最外层电子参与反应
p区
ⅢA族~ⅦA族、0族
ns2np1~6(He除外)
d区
ⅢB族~ⅦB族、Ⅷ族(除镧系、锕系外)
(n-1)d1~9ns1~2(除钯外)
d轨道可以不同程度地参与化学键的形成
ds区
ⅠB族、ⅡB族
(n-1)d10ns1~2
金属元素
f区
镧系、锕系
(n-2)f0~14(n-1)d0~2ns2
镧系元素化学性质相近,锕系元素化学性质相近
②根据元素金属性与非金属性分区
b.特别说明:
处于金属与非金属交界线(又称梯形线)附近的非金属元素具有一定的金属性,又称为半金属或准金属,但不能叫两性非金属。
[名师点拨]
①ⅠA族元素不等同于碱金属元素,H元素不属于碱金属
②第8、9、10三列是Ⅷ族,不是ⅧB族
③周期数=能层数=电子层数
主族序数=价电子数=最外层电子数
④对于主族元素,价电子层就是最外层,而对于过渡元素价电子层不仅包括最外层,还可能包括次外层,倒数第三层,如Fe的价电子排布式为3d64s2。
[考在课外]
教材延伸
判断正误
(1)同一周期中,从左到右,各元素最外层电子数都是从1个逐渐增加到8个(×
)
(2)同一主族元素最外层电子数相等(√)
(3)第ⅢB族所含元素种数最多,第ⅣA族元素形成化合物种类最多(√)
(4)0族元素原子的最外层均有8个电子(×
(5)铁位于元素周期表的第四周期ⅧB族(×
(6)金属元素和非金属元素分界线右侧都是非金属,左侧的都是金属元素(×
(7)元素周期表中位于金属与非金属分界线附近的元素属于过渡元素(×
(8)最外层电子数为2的元素一定属于ⅡA族元素(×
(9)从元素周期表的分区中可以看出,非金属性最强的是F,金属性最强的是Cs(放射性元素除外)(√)
(10)过渡元素都是金属元素,金属元素只有正价,没有负价(√)
(11)元素所在的主族序数与最外层电子数相等的元素都是金属元素(×
(12)短周期元素中,若两种元素的原子序数相差8,则它们一定是同主族元素(×
(13)两短周期元素原子序数相差8,则周期数一定相差1(√)
(14)原子及离子的核外电子层数等于该元素所在的周期数(×
(15)短周期元素中,若两种元素的原子序数相差2,则它们一定不是同主族元素(×
(16)某元素原子的核电荷数为53,则该元素位于第五周期ⅦA族(√)
(17)s区全部是金属元素。
(×
(18)价电子排布为5s25p1的元素位于第五周期ⅠA族,是s区元素(×
(19)正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族(√)
(20)价电子排布式为4s24p3的元素位于第四周期ⅤA族,是p区元素(√)
拓展应用
请在下表中画出元素周期表的轮廓,并在表中按要求完成下列问题:
①标出主族序数。
②画出金属与非金属的分界线,并用阴影表示出过渡元素的位置。
③标出镧系、锕系的位置。
④写出各周期元素的种类。
⑤写出稀有气体元素的原子序数。
答案
(2)结合如图所示的元素周期表,回答下列问题:
①表中所列元素,属于短周期元素的有________(填字母,下同),属于主族元素的有________;
g元素位于第________周期________族;
i元素位于第________周期________族。
②f元素位于第________周期第________族,请按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量。
答案 ①a、b、c、d、e、f、g a、b、c、d、e、f 三 0 四 ⅡB
②三 ⅥA
思维探究
(1)若甲、乙分别是同一周期的ⅡA族和ⅢA族元素,则甲、乙两元素的原子序数之差是多少?
答案 二、三周期差1,四、五周期差11,六、七周期差25。
(2)若甲、乙分别是同一主族的相邻周期的两种元素,则甲、乙两元素的原子序数之差是多少?
答案 ①位于过渡元素左侧的主族元素,差为上一周期元素所在周期所含元素种数。
②位于过渡元素右侧的主族元素,差为下一周期元素所在周期所含元素种数。
[基础点巩固]
1.下列关于现行元素周期表的说法正确的是( )
A.元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的
B.最外层电子数相同的元素都是同一族
C.同族元素的最外层电子数一定相同
D.同周期元素的电子层数相同
解析 元素周期表是按原子核电荷数递增的顺序排列而成的,A错误;
最外层电子数相同的元素不一定是同一族,如He和Mg最外层都有2个电子,但分别处于0族和第ⅡA族,B错误;
对于副族元素和第Ⅷ族及0族元素来说,同族的最外层电子数不一定相同,C错误;
同周期元素具有相同的电子层数,D正确。
答案 D
2.在元素周期表中,铂元素如图所示,下列有关说法正确的是( )
A.铂是非金属元素,在常温下呈固态
B.
78Pt和
78Pt的核外电子数相同,互为同位素
C.“195.1”是铂的质量数
D.由78可以推出Pt为第五周期元素
解析 铂为金属元素,A项错误;
78Pt的质子数相同,中子数不同,是两种不同核素,二者互为同位素,B项正确;
“195.1”是铂元素的相对原子质量,C项错误;
由78推出Pt为第六周期元素,D项错误。
答案 B
3.下列说法中正确的是( )
A.所有非金属元素都分布在p区
B.最外层电子数为2的元素都分布在s区
C.元素周期表中第ⅢB族到第ⅡB族10个纵行的元素都是金属元素
D.同一主族元素从上到下,金属性呈周期性变化
解析 非金属元素中氢在s区,其余非金属元素均分布在p区,A项错误;
最外层电子数为2的元素可能在s区(如Mg)、p区(如He)或d区(如Ti、Fe)等,B项错误;
同主族元素从上到下,金属性逐渐增强,非金属性逐渐减弱,属递变性质而不是周期性变化,D项错误。
答案 C
4.已知元素周期表中共有18纵行,如图实线表示元素周期表的边界。
按电子排布,可把周期表里的元素划分为几个区:
s区、p区、d区、ds区等。
除ds区外,其他区的名称来自按轨道能量顺序最后填入的电子的轨道类型的符号。
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影
表示d区和ds区。
(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在 区。
(3)请在元素周期表中用元素符号标出4s轨道半充满的元素。
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:
_________________________________________________________________。
(5)随着科学技术的发展,不断有新的元素被发现。
若把第七周期排满,则元素周期表共可以排布 种元素。
解析
(1)正确理解题意,明确按构造原理分区的含义即可,注意把握关键信息“……最后填入的电子的轨道类型的符号”。
(2)ds区外围电子排布为(n-1)d10ns1和(n-1)d10ns2,而d区内6纵行外围电子排布为(n-1)d5ns1,7纵行外围电子排布为(n-1)d5ns2,因此类比可以放在ds区。
(3)4s轨道半充满,即为4s1,根据轨道能量顺序和能量最低原理、洪特规则,该元素原子的电子排布式可能为1s22s22p63s23p64s1(K)或1s22s22p63s23p63d54s1(Cr)或1s22s22p63s23p63d104s1(Cu),分别标在元素周期表中相应位置即可。
(4)Fe外围电子排布为3d64s2,Fe2+为3d6,Fe3+为3d5,Fe3+为半充满状态较稳定。
(5)根据0族元素原子序数知,第7周期排满,其0族元素的原子序数应为2+8+8+18+18+32+32=118。
答案
(1)如图
(2)ds (3)见上图
(4)Fe2+为3d6不稳定结构,Fe2+失去一个电子后变为Fe3+,Fe3+为3d5的半充满稳定结构 (5)118
[能力点提升]
5.某元素基态原子的价电子排布式为3d54s2,则下列说法不正确的是( )
A.该元素为Mn元素
B.该元素原子核外有4个能层
C.该元素原子最外层共有7个电子
D.该元素属于d区元素
6.A~H元素在元素周期表中的相对位置如图。
B与F的原子序数相差6,F元素形成的单质呈黄绿色,D与H元素原子核外的电子层数相同,下列判断不正确的是( )
A.原子半径:
H>
F>
E
B.金属性:
D>
B>
A
C.C与G的原子核外电子数相差16
D.简单阴离子的还原性:
H
解析 由F的单质呈黄绿色可判断出F为Cl元素,由B、F的原子序数相差6可判断出B为Na元素,结合A、B、C、D的位置关系可知A、C、D分别为Li、K、Ca,结合E、F、G、H的位置关系,可知E、G、H分别为F、Br、Se。
A项原子半径Se>
Br>
Cl>
F,正确;
B项金属性Ca>
Na>
Li,正确;
C项,K与Br的核外电子数分别为19、37相差16,正确;
D项,阴离子的还原性:
Se2->
Br->
Cl-,错误。
7.甲~戊五种短周期元素(除稀有气体元素外)在元素周期表中的位置如下所示,其中元素戊的原子半径在同周期中最小。
下列有关判断一定正确的是( )
A.甲、丁位于第ⅠA族,均为碱金属元素
B.五种元素中,原子半径最大的元素为丁
C.甲、乙、丙三种元素组成的物质中只含共价键
D.五种元素的最高价氧化物对应的水化物中只有一种强酸
解析 由于第一、二、三周期为短周期,故甲只能是H,丁为Na,乙、丙为第二周期元素,戊为第三周期原子半径最小的元素,故戊为Cl,根据乙、丙和戊的位置关系可知乙、丙分别为N、O。
A项,H位于第ⅠA族,但不是碱金属元素,错误;
B项,同主族元素从上到下原子半径逐渐增大,同周期
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学 一轮 复习 元素 周期表 及其 应用
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
