 高中化学选修物质结构与性质全册知识点总结文档格式.docx
高中化学选修物质结构与性质全册知识点总结文档格式.docx
- 文档编号:15168703
- 上传时间:2022-10-28
- 格式:DOCX
- 页数:15
- 大小:86.09KB
高中化学选修物质结构与性质全册知识点总结文档格式.docx
《高中化学选修物质结构与性质全册知识点总结文档格式.docx》由会员分享,可在线阅读,更多相关《高中化学选修物质结构与性质全册知识点总结文档格式.docx(15页珍藏版)》请在冰豆网上搜索。
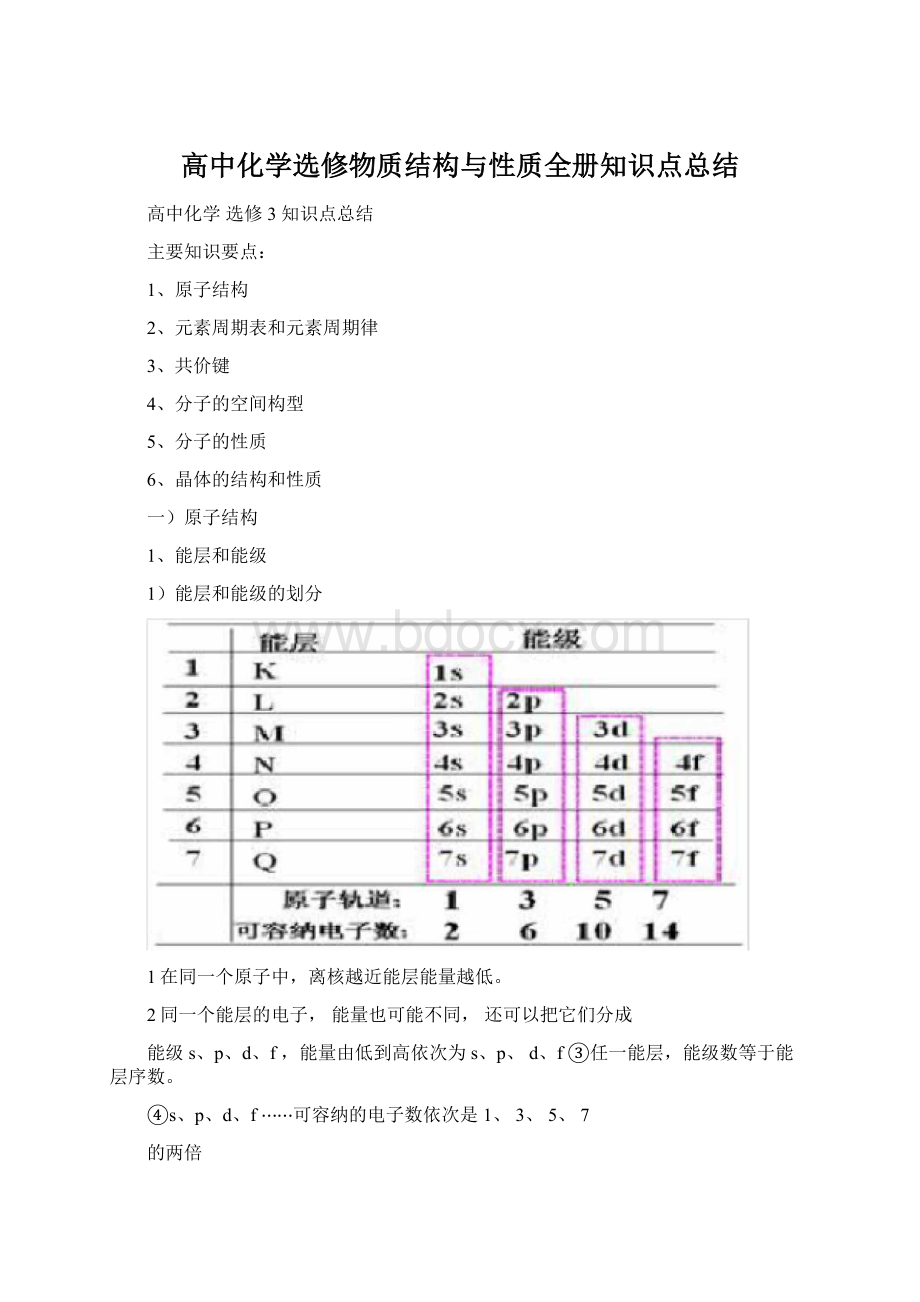
(3)不同能层的能级有交错现象,如E(3d)>E(4s)、
E(4d)>E(5s)、E(5d)>E(6s)、E(6d)>E(7s)、E(4f)>E(5p)、E(4f)>E(6s)等。
原子轨道的能量关系是:
<
(2)f<
(1)d<
(4)能级组序数对应着元素周期表的周期序数,能级组原子轨道所容纳电子数目对应着每个周期的元素数目
根据构造原理,在多电子原子的电子排布中:
各能层最多容纳的电子数为2n2;
最外层不超过8个电子;
次外层不超过18个电子;
倒数第三层不超过32个电子。
(5)基态和激发态
1基态:
最低能量状态。
处于最低能量状态的原子称为基态原子。
2激发态:
较高能量状态(相对基态而言)。
基态原子的电子吸收能量后,电子跃迁至较高能级时的状态。
处于激发态的原子称为激发态原子。
3原子光谱:
不同元素的原子发生电子跃迁时会吸收(基态→激发态)和放出(激发态→较低激发态或基态)不同的能量(主要是光能),产生不同的光谱——原子光谱(吸收光谱和发射光谱)。
利用光谱分析可以发现新元素或利用特征谱线鉴定元素。
3、电子云与原子轨道
(1)电子云:
电子在核外空间做高速运动,没有确定的轨道。
因此,人们用“电子云”模型来描述核外电子的运动。
“电子云”描述了电子在原子核外出现的概率密度分布,是核外电子运动状态的形象化描述。
(2)原子轨道:
不同能级上的电子出现概率约为90%的
电子云空间轮廓图称为原子轨道。
s电子的原子轨道呈球形对称,能级各有1个原子轨道;
p电子的原子轨道呈纺锤形,能级各有3个原子轨道,相互垂直(用、、表示);
能级各有5个原子轨道;
能级各有7个原子轨道。
4、核外电子排布规律
(1)能量最低原理:
在基态原子里,电子优先排布在能量最低的能级里,然后排布在能量逐渐升高的能级里。
(2)泡利原理:
1个原子轨道里最多只能容纳2个电子,且自旋方向相反。
(3)洪特规则:
电子排布在同一能级的各个轨道时,优先占据不同的轨道,且自旋方向相同。
(4)洪特规则的特例:
电子排布在p、d、f等能级时,当其处于全空、半充满或全充满时,即p0、d0、f0、p3、d5、f7、p6、d10、f14,整个原子的能量最低,最稳定。
能量最低原理表述的是“整个原子处于能量最低状态”,而不是说电子填充到能量最低的轨道中去,泡利原理和洪特规则都使“整个原子处于能量最低状态”。
(5)
(1)d能级上电子数等于10时,副族元素的族序数能级电子数
(二)元素周期表和元素周期律
1、元素周期表的结构元素在周期表中的位置由原子结构决定:
原子核外的能层数决定元素所在的周期,原子的价电子总数决定元素所在的族。
1)原子的电子层构型和周期的划分
周期是指能层(电子层)相同,按照最高能级组电子数依次增多的顺序排列的一行元素。
即元素周期表中的一个横行为一个周期,周期表共有七个周期。
同周期元素从左到右(除稀有气体外),元素的金属性逐渐减弱,非金属性逐渐增强。
(2)原子的电子构型和族的划分族是指价电子数相同(外围电子排布相同),按照电子层数依次增加的顺序排列的一列元素。
即元素周期表中的一个列为一个族(第Ⅷ族除外)。
共有十八个列,十六个族。
同主族周期元素从上到下,元素的金属性逐渐增强,非金属性逐渐减弱。
(3)原子的电子构型和元素的分区
按电子排布可把周期表里的元素划分成5个区,分别为s区、p区、d区、f区和区,除区外,区的名称来自按构造原理最后填入电子的能级的符号。
2、元素周期律
元素的性质随着核电荷数的递增发生周期性的递变,叫做元素周期律。
元素周期律主要体现在核外电子排布、原子半径、主要化合价、金属性、非金属性、第一电离能、电负性等的周期性
变化。
元素性质的周期性来源于原子外电子层构型的周期性。
(1)同周期、同主族元素性质的递变规律
同周期(左右)
同主族(上下)
原子结构
核电荷数
逐渐增大
增大
能层(电子层)数
相同
增多
原子半径
逐渐减小
元素
性质
化合价
最高正价由+1+7负价数=(8
—族序数)
最高正价和负价数均相同,最高正价数=族序数
元素的金属性和非金属性
金属性逐渐减弱,非金属性逐渐
增强
金属性逐渐增强,非金属
性逐渐减弱
第一电离能
呈增大趋势(注意反常点:
ⅡA族和ⅢA族、ⅤA族和ⅥA族)
电负性
(2)微粒半径的比较方法
1同一元素:
一般情况下元素阴离子的离子半径大于相应原
子的原子半径,阳离子的离子半径小于相应原子的原子半径。
2同周期元素(只能比较原子半径):
随原子序数的增大,原子的原子半径依次减小。
如:
>
>
P>
S>
3同主族元素(比较原子和离子半径):
随原子序数的增大,原子的原子半径依次增大。
<
<
K<
,<
4同电子层结构(阳离子的电子层结构与上一周期0族元素原子具有相同的电子层结构,阴离子与同周期0族元素原子具有相同的电子层结构):
随核电荷数增大,微粒半径依次减小。
如:
2+>
3+
3)元素金属性强弱的判断方法
本质
原子越易失电子,金属性越强。
判断依据
1.在金属活动顺序表中越靠前,金属性越强
2.单质与水或非氧化性酸反应越剧烈,金属性越强
3.单质还原性越强或离子氧化性越弱,金属性越强(电解中在阴极上得电子的先后)
4.最高价氧化物对应水化物的碱性越强,金属性越强
5.若则y比x金属性强
6.原电池反应中负极的金属性强
7.与同种氧化剂反应,先反应的金属性强
8.失去相同数目的电子,吸收能量少的金属性强
4)非金属性强弱的判断方法
原子越易得电子,非金属性越强
判断方法
1.与H2化合越易,气态氢化物越稳定,非金属性越强
2.单质氧化性越强,阴离子还原性越弱,非金属性越强(电解中在阳极上得电子的先后)
3.最高价氧化物的水化物酸性越强,非金属性越强
4.则B比A非金属性强
5.与同种还原剂反应,先反应的非金属性强
6.得到相同数目的电子,放出能量多的非金属性强
三)共价键
1、共价键的成键本质:
成键原子相互接近时,原子轨道发
生重叠,自旋方向相反的未成对电子形成共用电子对,两原子核间电子云密度增加,体系能量降低。
2、共价键类型:
(1)σ键和π键
σ键
π键
成键方向
沿键轴方向“头碰头”
平行或“肩并肩”
电子云形状
轴对称
镜像对称
牢固程度
强度大,不易断裂
强度小,易断裂
成键判断规律
单键是σ键;
双键有一个是σ键,另一个是π键;
三键中一个是σ键,另两个为π键。
2)极性键和非极性键
非极性键
极性键
定义
由同种元素的原子形成的共价
键,共用电子对不发生偏移
由不同种元素的原子形成的共价键,共用电子对发生偏移
原子吸引电子能力
不同
共用电子对位置
不偏向任何一方
偏向吸引电子能力强的一方
成键原子的电性判
断依据
不显电性
显电性
举例
单质分子(如H2、2)和某些化合物(如2O2、H2O2)
气态氢化物,非金属氧化物、
酸根和氢氧根等
(3)配位键:
一类特殊的共价键,一个原子提供空轨道,另一个原子提供一对电子所形成的共价键。
1配位化合物:
金属离子与配位体之间通过配位键形成的化
合物。
(H2O)44、(3)4()2、(3)2、()3等。
2配位化合物的组成:
3、共价键的三个键参数
概念
对分子的影响
键长
分子中两个成键原子核间距
离(米)
键长越短,化学键越强,形成的分子越稳定
键能
对于气态双原子分子,拆开1
键所需的能量
键能越大,化学键越强,越牢固,
形成的分子越稳定
键角
键与键之间的夹角
键角决定分子空间构型
(1)键长、键能决定共价键的强弱和分子的稳定性,键角决定分子空间构型和分子的极性。
(2)键能与反应热:
反应热=生成物键能总和-反应物键能总和
四)分子的空间构型
1、等电子原理
原子总数相同、价电子总数相同的分子具有相似的化学键特征,许多性质是相似的,此原理称为等电子原理。
(1)等电子体的判断方法:
在微粒的组成上,微粒所含原子数目相同;
在微粒的构成上,微粒所含价电子数目相同;
在微粒的结构上,微粒中原子的空间排列方式相同。
(等电子的推断常用转换法,如2222—3—或
2232=2)
(2)等电子原理的应用:
利用等电子体的性质相似,空间构型相同,可运用来预测分子空间的构型和性质。
2、价电子互斥理论
(1)价电子互斥理论的基本要点:
型分子(离子)中中心原子A周围的价电子对的几何构型,主要取决于价电子对数(n),价电子对尽量远离,使它们之间斥力最小。
2)型分子价层电子对的计算方法:
1对于主族元素,中心原子价电子数=最外层电子数,配位
原子按提供的价电子数计算,如:
5中
2O、S作为配位原子时按不提供价电子计算,作中心原子时价电子数为6;
3离子的价电子对数计算
3、杂化轨道理论
(1)杂化轨道理论的基本要点:
1能量相近的原子轨道才能参与杂化。
2杂化后的轨道一头大,一头小,电子云密度大的一端与成键原子的原子轨道沿键轴方向重叠,形成σ键;
由于杂化后原子轨道重叠更大,形成的共价键比原有原子轨道形成的共价键稳定。
3杂化轨道能量相同,成分相同,如:
每个3杂化轨道占有1个s轨道、3个p轨道。
4杂化轨道总数等于参与杂化的原子轨道数目之和。
2)s、p杂化轨道和简单分子几何构型的关系
杂化类型
2
3
3不等性杂化
轨道夹角
180
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 选修 物质 结构 性质 知识点 总结
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
