 酸碱盐知识归纳复习.docx
酸碱盐知识归纳复习.docx
- 文档编号:27776638
- 上传时间:2023-07-04
- 格式:DOCX
- 页数:21
- 大小:254.33KB
酸碱盐知识归纳复习.docx
《酸碱盐知识归纳复习.docx》由会员分享,可在线阅读,更多相关《酸碱盐知识归纳复习.docx(21页珍藏版)》请在冰豆网上搜索。
酸碱盐知识归纳复习
酸、碱、盐知识归纳复习
【知识回顾】
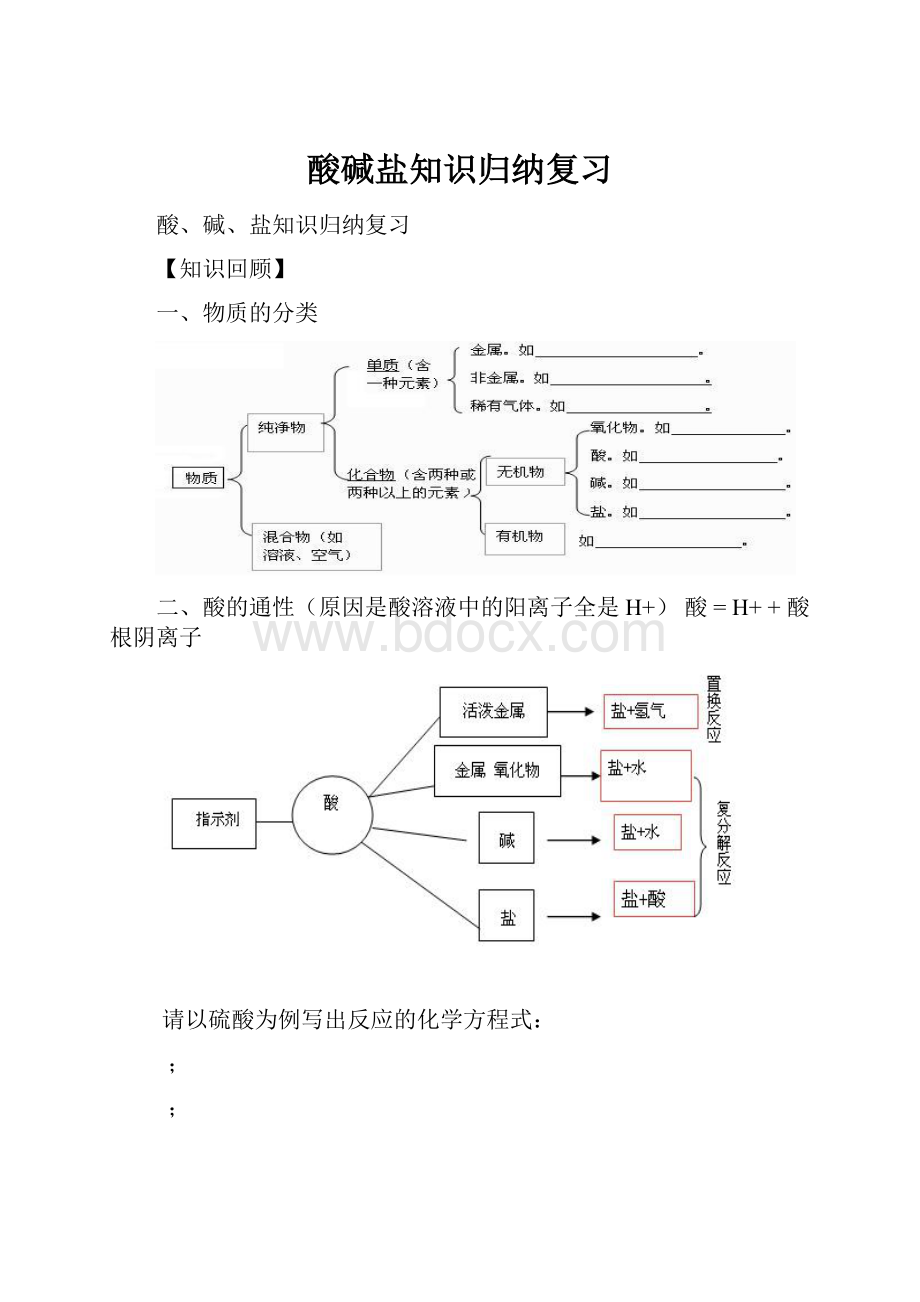
一、物质的分类
二、酸的通性(原因是酸溶液中的阳离子全是H+)酸=H++酸根阴离子
请以硫酸为例写出反应的化学方程式:
;
;
三、碱的共性:
(原因是碱溶液中的阴离子全是OH-) 碱 = 金属阳离子(或NH4+)+OH--
请以氢氧化钠为例写出反应的化学方程式:
;
;
四、盐的化学性质(由金属阳离子(或NH4+)和酸根阴离子组成的化合物)多数盐溶液呈中性,PH=7例:
Na2CO3是盐,但水溶液为碱性。
指示剂变化情况
请写出符合上面变化规律的化学方程式:
;
;
五、化学变化的4种基本反应类型
六、六大离子的鉴别。
见学案
【实践应用】
●复分解反应发生的条件:
生成物中是否水、沉淀或气体生成。
实质是溶液中是否存在不共存的离子。
离子共存问题:
两种离子不会组合成水、沉淀或气体则可共存。
常见不共存的离子有:
CO32-H+SO42-Ca2+和CO32-
NH4+
H+OH-OH-Cu2+Ba2+Cl-
Mg2+Ag+
HCO3-Fe3+CO32-CO32-
Al3+
1、下列各组物质在水溶液中能大量共存,且溶液为无色的是()
A.Na2CO3、KNO3、NaClB.Na2SO4、KCl、Fe(NO3)3
C.Na2SO4、BaCl2、NaNO3D.KNO3、NaCl、CuSO4
2、下列物质能大量共存于水溶液的是()
A.HNO3Ca(OH)2NaClB.KNO3CuCl2(NH4)2SO4
C.NaOHMgSO4BaCl2D.HClNa2CO3Ca(NO3)2
3、下列各组物质在溶液中能大量共存的是()
A.FeCl3、Na2SO4、HClB.NaOH、NaCl、HNO3
C.MgSO4、NaNO3、KOHD.NaHCO3、KNO3、HCl
4、在pH=0的溶液中能够大量共存的一组物质是
(A)Na2CO3、K2CO3、CuCl2(B)FeCl3、NaCl、Ca(NO3)2
(C)NaOH、KNO3、CaCl2(D)Ca(NO3)2、FeCl3、Na2CO3
5、下列各组物质在PH=14的无色溶液中,能大量共存的是()
A.FeCl3NaClKNO3B.NaClNaOHNaNO3
C.CaCl2NaNO3Na2CO3D.KNO3H2SO4NaCl
6、下列各组离子能在PH=1的水溶液中大量共存的是()
A.H+SO42-K+Na+B.SO42-Na+Cu2+Ba2+
C.OH-NO3-Fe3+Mg2+D.K+CO32-Na+NO3-
7、在碱性溶液中能大量共存的是().
A.Ca2+Mg2+Cl-CO32-B.Ba2+Fe3+SO42-Cl-
C.H+Ba2+NO3-Cl-D.K+Na+SO42-NO3-
8.下列各物质中,分别加入足量的水,混合后能得到无色透明的溶液的是()
A.NaOHCuSO4FeCl3B.H2SO4HClBaCl2
C.CaOH2SO4CuSO4D.H2SO4NaClHCl
9、稀硫酸和下列物质能发生中和反应,又能生成白色沉淀的是()
A.Mg(OH)2B.BaCl2C.K2CO3D.Ba(OH)2
10、两种溶液混合后能发生化学反应,且总质量不会发生变化的是( )
A.食盐溶液和稀盐酸B.碳酸钠溶液和稀盐酸
C.氢氧化钾溶液和硫酸溶液D.石灰水和氢氧化钠溶液
11、下列物质既能与水反应,又能与盐酸反应的是( )
A.CO2B.CaOC.CaCl2D.CaCO3
●除杂注意问题:
1、除杂质问题的原则是除去原有杂质时,一般不应消耗原主要成分,更不能引入新的杂质,即使非带入新的杂质不可,也应在后面的实验中采取适当方法除去.
除去下列物质中的杂质(括号中为杂质),应选什么试剂?
写出有关反应方程式
①NaOH(Ca(OH)2)②NaCl(Na2CO3)③BaSO4(BaCO3)④NaCl(MgSO4)
⑤Na2SO4(Na2CO3)
⑥KNO3(KCl)
⑦HNO3(HCl)
⑧HCl(H2SO4)
⑨NaOH(Na2CO3)
⑩NaNO3(CuSO4)
⑾KCl(CaCl2)
⑿ZnSO4(CuSO4)
2、特别要注意,除杂试剂必须适量,否则过量后也会成为新的杂质.
常见气体吸收剂见下表:
吸收剂
吸收的气体杂质
吸收剂
吸收的气体杂质
水
可溶性气体:
HCl、NH3等
NaOH固体
CO2、HCl、H20
无水CuSO4
H2O
碱石灰
CO2、HCl、H20
灼热的铜网
O2
NaOH溶液
CO2、HCl
灼热的CuO
H2、CO
浓硫酸
H20
提纯物
杂质
提纯的有关化学方程式(可一题多解)
(1)Cu
Fe
(2)Cu
CuO
(3)Fe
Fe2O3
(4)CO
CO2
(5)CO2
CO
3、除去下列物质中的少量杂质(括号内为杂质),写出所用试剂和有关的化学方程式
物质
所用试剂
化学方程式
盐酸(硫酸)
4、下列各组物质中的杂质(括号内为杂质),只需加入适量稀硫酸就能除去的是()
A.NaCl(Na2CO3)B.Fe(Cu)C.Na2CO3(CaCO3)D.HCl(BaCl2)
5、用括号中的试剂除去下列物质中所含杂质,所用药品错误的是()
A.NaOH溶液中混有Na2CO3(稀硫酸)B.NaCl溶液中混有Na2SO4(BaC12溶液)
C.KCl溶液中混有K2CO3(稀盐酸)D.CO中混有CO2(NaOH溶液)
6、除去下列物质中所含少量杂质的方法正确的是()
物质
杂质
除杂试剂
提纯方法
A
CO2
CO
O2
点燃
B
KCl
MnO2
水
溶解、过滤、蒸发
C
H2O
NaNO2
活性炭
吸附、过滤
D
Na2CO3
Na2SO4
BaCl2
溶解、过滤、洗涤
7、下列除杂的实验过程都正确的是(括号内为杂质)()
A.KCl(K2CO3)加足量稀硫酸、过滤、蒸发、结晶
B.BaSO4(BaCO3)加足量稀盐酸、过滤、洗涤、干燥
C.CuO(Cu)加足量稀盐酸、过滤、洗涤、干燥
D.MnO2(KCl)加水溶解、过滤、蒸发、结晶
8下列除杂质的方法正确的是 ( )
A.CaO中混有少量的CaCO3[适量的稀盐酸]
B.NaNO3溶液中混有少量的Na2SO4[加适量Ba(OH)2溶液]
C.CuO中混有少量的炭粉[加热至高温]
D.Cu粉中混有少量的Zn粉[加适量的稀硫酸]
9除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是()
选项
物质(括号内为杂质)
试剂
操作方法
A
KCl(KClO3)
少量MnO2
加热
B
NaOH(NaCl)
适量稀盐酸
蒸发、结晶
C
CO2(CO)
足量O2
点燃
D
稀盐酸(稀硫酸)
适量氯化钡溶液
过滤
10、现有AgCl、FeCl3、NaCl三种物质的固体混合物,若要将它们一一分离得到纯净的AgCl、FeCl3、NaCl,所加试剂的顺序和主要成分正确的是()
A、H2OKOHHClB、H2ONaOHHCl
C、H2ONaOHHNO3D、H2OKOHHNO3
11下列除去杂质的方法错误的是()
选项
物质(括号内为杂质)
除去杂质的方法
A
CO2(CO)
通过NaOH溶液
B
N2(O2)
通过灼热的铜网
C
CaCl2(CaCO3)
加水、过滤、蒸发
D
HNO3溶液(HCl)
加适量AgNO3溶液、过滤
7、在含有少量氯化钠的氯化钙溶液中,要除去氯化钠,以得到纯净的氯化钙溶液。
请你补充完整下列实验过程。
实验步骤
实验目的
有关化学方程式
1向样品中加
入过量的Na2CO3溶液,
过滤
2向滤渣中加入稀盐酸至
。
思考:
①加入的Na2CO3溶液为什么要过量?
;
②被提纯的物质发生改变,应该怎么做?
。
中考链接:
1、[08佛山]实验室有A、B两瓶溶液:
A瓶是含有少量BaCl2的KCl溶液;B瓶是含有少量KCl的BaCl2溶液。
小松和小思为回收试剂进行了如下实验探究。
(1)小松欲从A瓶中得到纯净的KCl晶体,可向A溶液加入稍过量的溶液,过滤后,在滤液中滴加盐酸至pH=7,再蒸发、结晶、烘干即得到纯净的KCl。
(2)小思欲从B瓶中得到纯净的BaCl2晶体,设计了如下的实验方案,请你填写以下部分实验报告:
(a)向B溶液中加入过量的碳酸钾溶液,其实验现象为。
(b)过滤、(填“蒸发结晶”、“洗涤沉淀”或“冷却结晶”)。
(c)将(b)操作中得到的物质加入适量盐酸,其实验现象为,
反应的化学方程式为。
(d)将(c)操作中得到的滤液经蒸发、结晶、烘干即得到纯净的BaCl2。
2、[09佛山]通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。
以下是制备精盐的实验方案,各步操作流程如下:
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是。
(2)第②步操作的目的是除去粗盐中的(填化学式,下同),第⑥步操作的目的是除去滤液中。
(3)第⑤步“过滤”操作中得到沉淀的成分有:
泥沙、BaSO4、Mg(OH)2、
(填化学式)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是
。
3、今有AgNO3溶液、BaCl2溶液、Ba(NO3)2溶液、Ba(OH)2溶液、Na2CO3溶液和Zn粉供选用。
若欲除去稀硝酸中混有的少量硫酸,以得到纯净的稀硝酸,应加入适量,发生反应的化学方程式为。
若欲除去氯化钠溶液中混有的少量盐酸,以得到纯净的氯化钠溶液,应加入适量,发生反应的化学方程式为,该反应的类型是
4、为了除去氯化钠样品中的碳酸钠杂质,兴趣小组最初设计了如下的方案并进行实验。
(1)写出沉淀A的化学式。
(2)加入CaCl2溶液后,分离除去沉淀A的实验操作方法是。
(3)同学在实验过程中,又发现了新的问题:
此方案很容易引入新的杂质,请写出固体物质B的成分(用化学式表示)。
(4)同学继续探究后又提出新的方案:
将混合物溶解,若滴加盐酸至不再产生气体为止,则既能除去Na2CO3杂质,又能有效地防止新杂质的引入。
写出有关反应的化学方程式:
。
●鉴定鉴别题
不用试剂的鉴别题:
先观察颜色,找出与其它物质不同色的物质,再利用该物质与其它物质反应产生的特别现象一一鉴别出来。
1、有四瓶失去标签的溶液,它们所含有的溶质分别是:
①硝酸钡、②硝酸银、③氯化钠、④氯化铜。
不用别的试剂就能鉴别出的最优顺序应是()
A、①③②④B.④②③①C.③②④①D.②③①④
2、现有①KCl②MgSO4③KOH④CuCl2四种溶液,不用其他试剂,仅用观察法和相互反应就可以将其区别开来,则鉴别出来的先后顺序是()
A、④③①②B、③④②①C、④②③①D、④③②①
3、现有四种白色固体:
①氯化钠②氯化钡③无水硫酸铜④硫酸钠,不使用其它试剂(可以用水)就可以把它们区分开,区分出的先后顺序是()
A、②③④① B、②④③①C、③①④② D、③②④①
只用一种试剂的鉴别题
4、只用酚酞一种指试剂就能鉴别的一组溶液是()
A、NaOH、HCl、NaClB、NaOH、BaCl2、NaNO3
C、NaOH、NaCl、MgCl2D、NaOH、KOH、HCl
5、要将KCl、K2CO3、BaCl2三种无色溶液鉴别开,仅选用一种试剂,可选用()
A.盐酸B.稀硫酸C.氢氧化钠溶液D.石蕊试液
6、鉴别氯化钡、硝酸银、碳酸钠三种无色溶液时,最好选用的一种试剂是()
A.稀盐酸B.稀硫酸C.氢氧化钠溶液D.氯化钠溶液
7、鉴别氯化钡、硝酸银、碳酸钠三种无色溶液时,最好选用的一种试剂是()
A.稀盐酸B.稀硫酸C.氢氧化钠溶液D.氯化钠溶液
8.只用紫色石蕊试液就能将组内三种物质的稀溶液区别出来的是()
A.Ba(OH)2、NaCl、H2SO4B.KCl、NaOH、NaCl
C.KOH、HCl、H2SO4D.KCl、NaOH、KOH
9、下列各物质中,能将(NH4)2SO4溶液、Na2CO4溶液、BaCl2溶液一次就鉴别开来的是溶液()A、AgNO3B、NaOHC、Ba(OH)2D、HCl
10.鉴别NaOH溶液和Ca(OH)2溶液,可选用的试剂是()
A.酚酞试液B.石蕊试液C.碳酸钠溶液D.盐酸
11.区分稀盐酸和稀硫酸,应选用的药品是()
A.BaCl2溶液B.NaCl溶液C.稀HNO3D.酚酞试液
12、用水不能鉴别开的一组物质是()
A.
和
B.稀硫酸和浓硫酸
C.
和
D.硫酸铜和无水硫酸铜
13、为了鉴别稀硫酸和澄清的石灰水,可选用的物质为()
①
溶液②
溶液③石蕊试液④酚酞试液
A.只有①和③B.只有②和④
C.只有①、②和③D.①、②、③和④
●推断题
解推断题时需具备的知识见错题集
1、在下图所示的转化关系中,A、B、C、D是四种不同的含铁化合物,A为铁锈的主要成分,E、F为两种无色溶液。
(1)写出E、F中溶质的化学式:
E;F。
(2)用化学方程式表示下列变化:
A→C
B→D
2.下图是初中化学所学的常见化合物之间的相互转化关系
(反应条件和生成产物中的水已略去)。
其中A是一种常见的建筑材料,B是一种常见的气体,H是一种含钠的化合物。
请回答下列问题:
(1)写出A、F、D的化学式:
A____________;F_____________;H________________。
(2)写出反应的化学方程式:
①E+HCl___________________________________________;
②E+G_____________________________________________;
③B+D_____________________________________________。
10.(5分)被誉为”江南小三峡”的南京胭脂河是明代初年开凿的一条人工运河。
卤其“石有胭脂色”而得名。
胭脂河沿岸的那些红色石块的成分是什么?
某研究性学习小组取一小块这种红色石块A,粉碎后对其成分进行实验探究,实验记录如下图所示。
请你根据实验推断:
A中含有的原子团是(写离子符号)。
B中肯定含有的溶质是(写化学式)。
写出实验中有关反应的化学方程式:
②
⑤
3、有A、B、C、D四种物质的溶液,他们分别是硫酸钠、盐酸、氢氧化钡、碳酸钠中的一种,它们之间能发生如下的反应:
①A+C→E↓+F②B+C→G↓+F
③B+D→H+J+K↑根据以上关系推断:
(填化学式)
A.为__________B.为__________C.为__________D.为__________
4.已知A、B、C、D都是初中化学常见的物质,其中B是一种有刺激性气味的气体,它们之间的转化关系如下:
试回答以下问题:
(1)白色沉淀D的化学式为:
___________,气体B的化学式为___________;
(2)如果A为纯净物,则A的化学式为:
___________,请写出由A生成气体B的化学
方程式:
__________________________________;
(3)如果A为混合物,则A的组成可能是:
_____________________(写一种组合即可)。
5、A.、B、C、D、E、F、G、H、I都是初中化学学过的物质。
其中E、F、H均为黑色固体B为紫红色固体,D为混合物。
他们之间有下图的转化关系(部分生成物已省去)
写出上述反应所有化学方程式:
6、A、B、C、D、E、F六种物质都是初中化学内容中涉及的化合物,转化关系如下图所示,其中D是最常见的溶剂。
⑴根据上图推断,C是,D是,E是(填写化学式)。
⑵写出反应①的化学方程式,
反应④属于反应(填写基本反应类型)。
7.已知下列各物质的相互转化关系如图所示,ⅹ为气体单质,C、Y中含有钠元素,D中含有氯元素。
假设每次反应都恰好完全反应。
(1)写出下列物质(属溶液的写出溶质)的化学式:
B ;Z ;Y ;C 。
(2)写出②处发生反应的化学方程式:
。
(3)简要写出C物质的推理过程:
。
8、A~H都是初中化学中的常见物质,它们之间的转化关系如图14所示。
A是天然气的主要成分,E是一种常见的食品干燥剂。
请回答:
(1)A的化学式为;
(2)反应③的基本反应类型是;
(3)反应②的化学方程式为;
(4)反应④的化学方程式为。
9、有一色白色粉末,可能含有CaCO3、CuSO4、BaCl2和K2SO4四种物质中的一种或几种,将此粉末放入足量的水中充分搅拌,得无色溶液和白色沉淀。
过滤,向沉淀中加入盐酸,沉淀完全溶解,并放出使澄清的石灰水变浑浊的气体,则白色沉淀中一定不存在___________,一定有_________,可能有_______
10、现有初中化学中常见的易溶于水的三种钠盐组成的混合物,将其溶于水后得无色溶液A,进行如下实验并得到相应结果:
试回答下列问题:
(1)无色气体D的化学式为,白色沉淀E的化学式为,钡盐B的化学式为。
(2)原混合物中含有的三种易溶于水的钠盐的化学式分别为、、。
11、现有一包白色固体混合物,可能由BaCl2、KNO3、CuSO4、FeCl3、Na2CO3、Na2SO4、NaCl等中的几种混合而成,为证明其组成,做如下实验:
(1)取一定量该固体混合物加入足量的水,充分搅拌,得到白色沉淀和无色溶液。
过滤得到白色沉淀A,无色滤液B。
(2)向白色沉淀A中加入过量的盐酸溶液,沉淀部分溶解。
(3)向无色滤液B中加入硝酸银溶液,产生不溶于稀硝酸的白色沉淀;则该固体混合物中一定含有________________________,可能含有___________________;一定没有________________________。
(用化学式填空)。
12、某固体可能由
、
、
、
中的一种或几种组成,现进行如下实验:
试回答:
(1)白色沉淀A的化学式为,无色气体D的化学式为。
(2)原固体中一定含有,一定不含有,可能含有。
(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:
①取少量固体溶于水,加入足量的
溶液,充分反应后,过滤;
②取滤液加入
溶液,观察有无白色沉淀生成,由此得出结论。
在上述某同学的实验方案①中,加入足量的
溶液的目的是。
13、今有一固体物质,只可能含有以下离子中的若干种:
Na+、NH4+、Ba2+、CO32-、
SO42-。
现取10克的两份固体加入足量的水中,全部溶于水;进行如下实验:
①第一份加足量NaOH溶液,加热,有刺激性气味气体产生;②第二份加足量BaCl2溶液后,得干燥沉淀19.7g,根据上述实验,回答下列问题:
(1)从步骤①中可知该溶液中一定含有的离子是:
(填离子符号)
(2)小红同学对步骤②中得到的白色沉淀继续进行探究:
作如下猜想:
①沉淀只含有BaCO3②只含有BaSO4③还可能是__________________。
实验步骤
现象
结论
取沉淀少量于试管中加入足量稀盐酸
固体全部溶解,____________
猜想_________正确
(3)对于该溶液的组成,小刚同学认为该溶液的阳离子可能含有Ba2+,但小红立即否定了他,你认为小红的理由是:
(4)小强同学通过数据分析得出该溶液中(填“一定”或不一定“或一定”)含有Na+
14、某溶液由Na2CO3、Na2SO4、H2SO4、Cu(NO3)2、KNO3、NaCl六种中的两种组成。
对该溶液进行如下实验,所观察到的现象记录在下表中。
试根据各步实验及其现象先进行分步推断,再综合推断该溶液的可能组成。
实验操作步骤
实验现象
对溶液组成分步推断的结论
(1)取溶液少许,观察
溶液无色、澄清
(2)用pH试纸测定溶液的pH
pH=2
(3)向溶液中滴入过量的Ba(NO3)2溶液
有白色沉淀出现
(4)过滤,向滤液中滴加AgNO3溶液
无明显现象
溶液可能的组成(写出溶质的化学式,有几组要写几组)
15、废旧电池有着非常重要的意义。
那么,废旧电池的组成物质有哪些呢?
带着这个问题,
小茜和小蓝对一节废旧干电池进行了探究。
【查阅资料】1、干电池的主要组成示意图(见右图)
2、碱性溶液能使红色石蕊试纸变蓝。
小茜在剥开电池锌壳时,闻到一股淡淡的刺激性气味。
于是她取出少量电池内的白色糊状A物质与熟石灰混合置于试管中,微热,用湿润的红色石蕊试纸置于试管口,观察到试纸变蓝。
【猜想】产生的气体可能是下列气体中的一种:
①H2②NH3③SO2
小蓝立刻说,这种气体肯定不是①,理由是:
______;
也不是③,理由是:
__。
由此得出,糊状物中一定有(填离子符号)。
小蓝认为,白色糊状物中所含阴离子可能是OH-、CO32-、Cl-、SO42-中的一种或几种。
【设计与实验】
操作步骤
实验现象
相应结论
1、取样,溶于适量的水中,静置,过滤。
取少量滤液于一支试管中,滴加紫色石蕊试液
石蕊试液不变色
2、取少量滤液于另一支试管中,滴加稍过量的
无明显现象
没有CO32-存在
3、再向第2步所得溶液中继续滴加少量的溶液
没有SO42-存在
4、向第3步所得溶液中再滴加少量硝酸银溶液
有白色沉淀产生
有存在
5、取白色糊状物,滴加少量碘液
有蓝色出现
则说明有淀粉存在
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 酸碱 知识 归纳 复习
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
