 红外光谱在席夫碱中的应用.docx
红外光谱在席夫碱中的应用.docx
- 文档编号:28128741
- 上传时间:2023-07-08
- 格式:DOCX
- 页数:15
- 大小:1.19MB
红外光谱在席夫碱中的应用.docx
《红外光谱在席夫碱中的应用.docx》由会员分享,可在线阅读,更多相关《红外光谱在席夫碱中的应用.docx(15页珍藏版)》请在冰豆网上搜索。
红外光谱在席夫碱中的应用
红外光谱在席夫碱中的应用
一:
红外光谱的简单介绍
1、红外光谱的原理
当一束具有连续波长的红外光通过物质,物质分子中某基团个的振动频率或转动频率和红外光的频率一样时,分子就吸收能量由原来的基态振(转)动能
级跃迁到能量较高的振(转)动能级,分子吸收红外辐射后发生振动和转动能级的跃迁,该处波长的光就被物质吸收。
所以,红外光谱法实质上是一种根据分子内部原子间的相对振动和分子转动等信息来确定物质分子结构和鉴别化合物的分析方法,简单的基本原理如下:
辐射一分子振动能级跃迁一红外光谱一官能团一分子结构
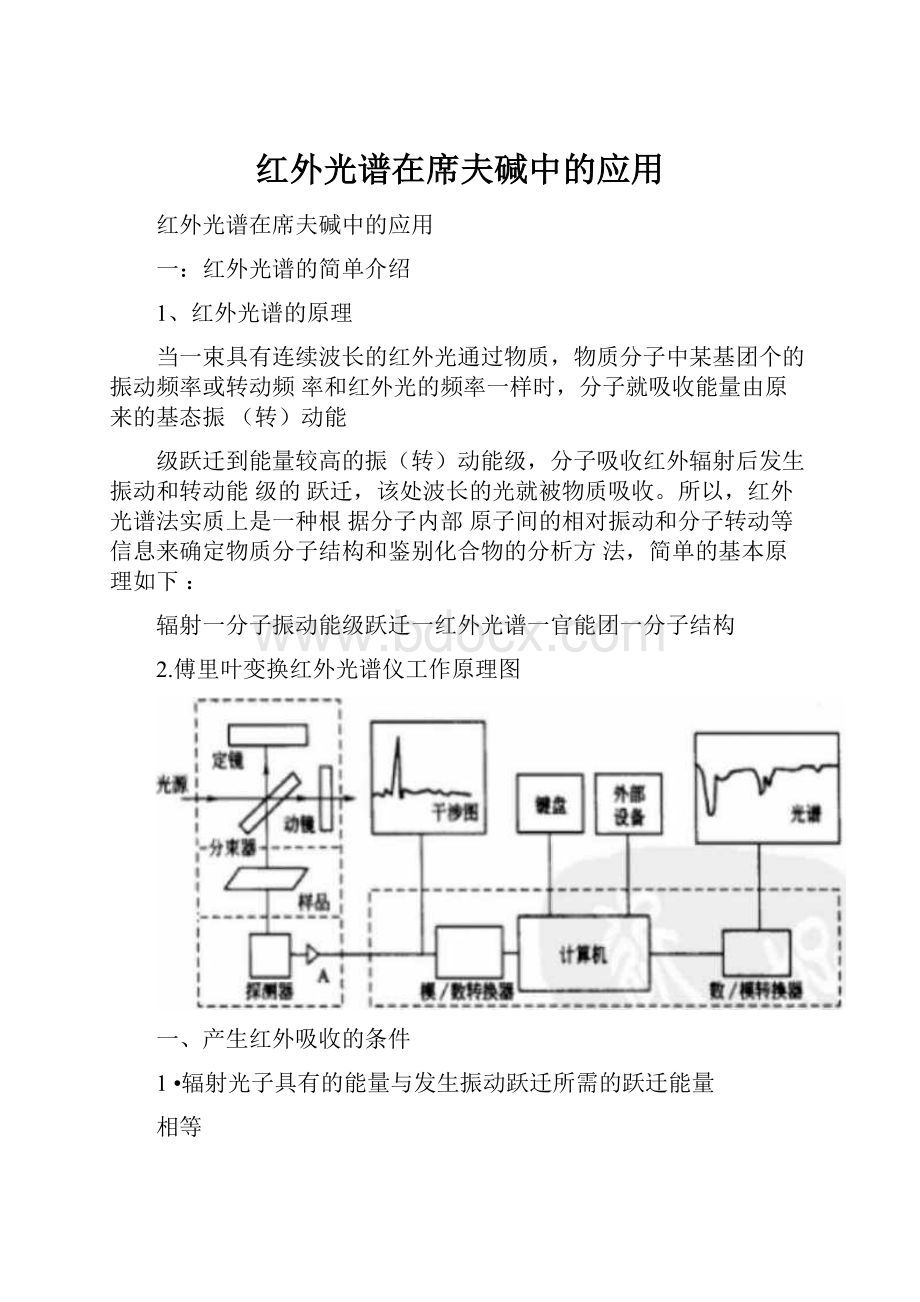
2.傅里叶变换红外光谱仪工作原理图
一、产生红外吸收的条件
1•辐射光子具有的能量与发生振动跃迁所需的跃迁能量
相等
(2)辐射与物质之间有耦合作用;分子振动必须伴随偶极矩的变化。
红外跃迁是偶极矩诱导的,即能量转移的机制是通过振动过程所导致的偶极矩的变化和交变的电磁场(红外线)相互作用发生的。
2、红外光谱的三要素
1峰位
2分子内各种官能团的特征吸收峰只出现在红外光波谱的一定范围,女口:
C=O的伸缩振动一
般在1700crn-1左右°
2•峰强
红外吸收峰的强度取决于分子振动时偶极矩的变化,振动时分子偶极矩的变化越小,谱带强度也就越弱。
一般说来,极性较强的基团(如C=O,C・X)振动,吸收强度较大;极性较弱的基团
(如
C=C,N-C等)振动,吸收强度较弱;红外吸收强度分别用很强(vs)、强(s卜中(m)、弱(w)表示.
3•峰形
不同基团的某一种振动形式可能会在同一频率范围内都有红外吸收,如・OH、・NH的伸缩振
动峰都在3400.3200cm-1但二者峰形状有显著不同。
此时峰形的不同有助于官能团的鉴别。
3、红外光谱的应用
一、定T生分析
1.已知物的鉴定
将试样的谱图与标准的谱图进行对照,或者与文献上的谱图进行对照。
如果两张谱图各吸收峰的位置和形状完全相同,峰的相对强度一样,就可以认为样品是该种标准物。
如果两张谱图不一样,或峰位不一致,则说明两者不为同一化合物,或样品有杂质。
如用计算机谱图检索,则采用相似度来判别。
使用文献上的谱图应当注意试样的物态、结晶状态、溶剂、测定条件以及所用仪器类型均应与标准谱图相同。
2•未知物结构的测定
测定未知物的结构,是红外光谱法定性分析的一个重要用途。
如果未知物不是新化合物,
可以通过两种方式利用标准谱图进行查对:
(1)查阅标准谱图的谱带索引,与寻找试样光谱吸收带相同的标准谱图;
(2)进行光谱解析,判断试样的可能结构,然后在由化学分类索引查找标准谱图对照核实。
在对光谱图进行解析之前,应收集样品的有尖资料和数据。
了解试样的来源、以估计其可能是哪类化合物;测定试样的物理常数,如熔点、沸点、溶解度、折光率等,作为定性分析的旁证;根据元素分析及相对摩尔质量的测定,求出化学式并计算化合物的不饱和度
门=1+n4+(n3-n1)/2
式中门4、n3、n1、分别为分子中所含的四价、三价和一价元素原子的数目。
当计算得0=0时,表示分子是饱和的,应在链状疑及其不含双键的衍生物。
当=1时,可能有一个双键或脂环;
当「=2时,可能有两个双键和脂环,也可能有一个巻键;
当「|=4时,可能有一个苯环等。
但是,二价原子如S、O等不参加计算。
谱图解析一般先从基团频率区的最强谱带开始,推测未知物可能含有的基团,
判断不可能含有的基团。
再从指纹区的谱带进一步验证,找出可能含有基团的相尖峰,
用一组相尖峰确认一个基团的存在。
对于简单化合物,
确认几个基团之后,便可初步确定分子结构,然后查对标准谱图核实。
二、定量分析
红外光谱定量分析是通过对特征吸收谱带强度的测量来求出组份含量。
其理论依据是朗
伯•比耳定律。
由于红外光谱的谱带较多,选择的余地大,所以能方便地对单一组份和多组份进行定量分
析。
此外,该法不受样品状态的限制,能定量测定气体、液体和固体样品。
因此,红外光谱定量分析应用广泛。
但红外唱定量灵敏度较低,尚不适用于微量组份的
测定。
席夫碱的简单介绍
1'席夫碱定义
(一)席夫碱定义
席夫碱主要是指含有亚胺或甲亚胺特性基团(-RC=N・)的一类有机化合物,
通常席夫碱是由胺和活性拨基缩合而成。
席夫碱类化合物及其金属配合物主要在药学、催化、分析化学、腐蚀以及光致变色领域的重要应用。
在医学领域,席夫碱具有抑菌、杀菌、抗肿瘤、抗病毒的生物活性;在催化领域,席夫碱的钻、镰和耙的配合物已经作为催化剂使用;在分析化学领域,席夫碱作为良好配体,可以用来鉴别、鉴定金属离
子和定量分析金属离子的含量〔1〕;在腐蚀领域,某些芳香族的席夫碱经常作为铜的缓
蚀剂〔2〕;在光致变色领域,某些含有特性基团的席夫碱也具有独特的应用〔3〕。
R2C=O+R*NH2——R2C=NR*+H20
席夫碱的制备在催化下反应,但是不能用强酸,因为氢离子和拨基结合成于羊盐而增加拨基的亲电性能,但亲离子和氨基结合后形成鞍离子的衍生物,丧失了胺的亲核能力,所以本类反应条件要求非常严格。
席夫碱类化合物的C=N基团中杂化轨道的
N原子具有易于流动的二维平面孤对电子,能够有效配位金属离子和中性小分子,使席夫碱成为配位化学研究的重要的配体。
2、席夫碱的种类
(1)按配体结构分:
单席夫碱、双席夫碱、大环席夫碱。
单希夫碱合成采用单胺类和单拨基化合物的缩合。
这类希夫碱化合物的结构形式如图1所示〔4〕。
双希夫碱多采用二胺和戦基化合物反应制备得到这类配体的结构如图2所示。
大环希夫碱在合成中经常采用碱土金属阳离子或斓系金属作为模板试
齐形成(1+1)、(2十2)、(3+3)型大环希夫碱,结构如图3所示:
(a)、(b)、
(c)分别对应所1+1,2+2和3十3型大环希夫碱。
(2)按缩合物质不同可分为缩胺类希夫碱、缩酮类希夫碱等。
希夫碱的早期研究为缩胺
类,后来发展为缩酮类、缩胺类、缩氨基腺类、脈类、氨基酸类及氨基酸酯类〔4〕。
近
年来,人们不再满足于传统原料缩合而成的希夫碱,而转向于一些其它新型材料合成希夫碱配合物,如酚类、嚎吩类、咲喃类、非环多醍类,,并对它们的性质,诸如均衡性、稳定性、溶解性等进行了研究。
考虑形成配合物后的功能性、广谱性。
由于席夫碱配合物的广谱作用,故尖于这类化合物的研究是近半个世纪以来生物无机领域的研究热点。
3•席夫碱金属配合物的简单介绍
席夫碱主要是指含有碳氮双键的亚胺或甲亚胺特性基团(一RC=
N—)的一类有机化合物,早期的研究一般为缩胺类席夫碱。
席夫碱类化合物具有抑菌、杀菌、抗肿瘤、3抗病毒的生物活性,且其生物活性与金属的配合
物有尖,一直是引人注目的研究对象。
目前,席夫碱类化合物及其配合物在医学、催化、
分析化学、腐蚀4〜8以及光致变色领域有着重要的应用。
近年来,研究席夫碱配合物
不仅讲究选择功能性原料,从其形成机理,光谱性质等方面进行深入研究,而且综合
考虑形成配合物后的功能性、广谱性。
由于席夫碱配合物的广谱作用,故尖于这类化合物
的研究是近半个世纪以来生物无机领域的研究热点。
研究金属离子和席夫碱配体之间的合
成、结构、相互作用,对于深入考察其生理、药理活性的作用机理、构造、稳定性等方面有着十分重要的作用。
下面是简要介绍近年来研究一些席夫碱配合物及其结构的实例:
(一)席夫碱双核金属铜配合物
王瑾玲课题组利用20mmoL1■苯基・3■甲基・5毗口坐i林酮(PMP)和水杨酰胺在适当的条件下制备了PMP缩水杨酰胺席夫碱及其铜(II)配合物〔5〕取少量的Cu(ll)配合物溶于DMF溶剂中,室温下自然蒸发一周后得到适用于X射线衍射分析用的单晶体,化学
式:
Cu2(C18H13N3O3)2(C3H7NO)2
PMP缩水杨酰胺席夫碱配体
F图是利用X射线衍射方法研究了配合物的晶体结构图
结果表明配合物为桥联双核铜结构,铜原子为五配位的四方锥构型,每个铜原子与一
个配体中酮上的氧原子、席夫碱上的N原子、水杨酰的酚氧原子和溶剂DMF中
的氧原子配位,而相邻配体中水杨酰的酚氧原子也参加配位并将两个铜原子连接起来形成桥联双核铜配合物
,两个Cu(ll)原子间的距离为0.3268nm•芳环堆积作用和分子内
及分子间氢键的存在增强了配合物分子的稳定性•双核铜配合物中毗哩临环上的氧原
子[0
(1),0(4)]、亚胺氮原子[N⑴,N
(2)]和水杨酰上的酚氧原子[0(3),0(6)]分别与Cu
(1)
和Cu
(2)形成顺式的双六元螯合平面,相邻的六元螯合环平面形成了一个较大的共觇体系增加了配合物分子的稳定性。
席夫碱的铜配合物研究较多,对其杀菌、抗
菌、抑菌、抗癌活性,以及催化作用、02・■(超氧阴离子自由基)的清除能力目前有较多
的报道。
贵州大学朱必学老师课题组用了Schiff碱C29H29N5O4与CU(OAC)2.H2O合
成席夫碱双核铜配合物C29H27N5O5CU2〔6〕。
其合成方法如下:
几何结构相似的配体和配合物分子。
在双核配合物的晶体结构相似的分子经分子间氢键作用连接成二聚体,这些二聚体再通过其与乙醇分子之间形成的桥联氢键扩展为一维链状结构
C?
K
(二)席夫碱三核金属锌配合物
英国RalphA.Zingaro[8]课题组也合成了三核Zn配合物,他们是利用Schiff碱大环化合物配体与Zn
配位:
三核Zn配合物单晶结构
Schiff碱大环化合物配体。
这类配体作为一类有用的手性配体,手性配体可以和金属配
位在不对称催化反应被利用的。
通过X射线衍射分析结构如下。
最引人注目的是Schiff
碱大环化合物配体的结构特征如图是循环的螺旋结构[8],这是不寻常的,是一个等边
三角形的形式,其腔中有氮氧端口。
这有利于低聚多核手性配合物的形成。
(二)席夫碱四核Ni配合物
簇化物因其独特的结构吸引了化学、生物化学以及磁学界的广泛尖注[9],一直成为研究
的热点。
基于席夫碱所形成的过度金属配合物,配体是以N、0原子进行配位的,其结构
接近于生物体系的真实情况,适宜于进行生物体系的模拟研究’受到人们的普遍重视〔10〕°朱必学老师课题组用邻氨基酚、苯甲酰丙酮为原料'经缩合得到了席夫碱配体与Ni(°AC)
2.4H2O反应得到四核Ni(II)的簇化物〔9〕,其合成方法如下:
1
并单晶衍射法测定了它的晶体结构:
席夫碱在一定条件下还可以与大部分金属元素形成稳定性不一的金属配合物〔11〕°由
于席夫碱配合物具有广阔的应用前景,今后必定会吸引越来越多的学者'科研人员从
事其研究随着研究的深入进行,席夫碱配合物的应用将更加广泛°
三:
红外光谱在席夫碱中的应用
1、红外光谱在席夫碱合成表征的应用
南开大学朱志昂课题组利用邻苯二胺、哌旋、原甲酸三乙酯、乙醇、甲醇、四
氢咲喃、为分析纯试剂在适当的条件下制备了席夫碱(A)〔5〕并用IR对其进行了表征
席夫碱(A)的合成
红外光谱采用KBr压片在4000-400范围内摄谱,其数据见表1,由表中的数据可以看出
在3252-3440区域内没有吸收峰存在,说明单元化合物A上的伯胺与拨基氧缩合失水,形成
席夫碱结构,所以不存在伸缩振动峰,同时从配合物谱图上1700附近未观测到酮基
(C=0)的振动峰,而在1650-1590范围内有很强的C=N缩振动峰产生;在2920和2850附近分别出现
CH2对称伸缩振动和反对称伸缩振动吸收峰,说明配合物结构中有亚甲基存在,由此
可以说明席夫碱单元A的形成。
表1席夫碱红外特征吸收峰
tu
Lc
th
2ii
2h
2jc
3M
Jibs
1
,、359(r
却:
巧9(昨)
八57(w)
3<)56(w)
讯IQfU仙)
J
讯总0(机S
20Jfe
H
3O19C»l>
1
£Ml7<«rtj
919W1
2T5(T
2F
2y]?
(W>
29W(w1
言囂炸H(材1
2^50(a
2M51(札0
2M5ZC«i
2154(»i
2850(«b
2853C»1
M£.aA1
iri和屛
ifjiyc*!
lf?
2UC#*
IftIMC#)
H620C»)
H
mW
J597(«>
J59*(iu}
1594⑷
卩hrinf眼•【4:
i
1S83C#)
]577(i4)
1575(w|
J577Chi>
]582(H
J545O4)
fi577(>i)
1$鳥泓胡
1贮3■(-
8525n
1wsgn
mu
i525(w)
】S3Uf幅)
1510(141
L5O>5(m|
ISOOCm)
052*3
D505(v»)
[HwkiicR巧
14P八-0
145A(Ti
14S7(
1484(n>I
I46PD
♦・455(w)
14K-Icrn}
145,、(j4b
]45R(in>
1430(wl
145H(m)
⑷了d
14Vg*
13K(Kin: i) 13M3(fiO ]37O(niJ ]3K2(m) ]37O(in> ■H. 「辭2齢〉 1m) 1Wl(H) 1(rn} U盟心〔•> P« ]zyjCmI ]ZK2( 12S3(wJ J2MOCwJ DZNiJCu1 J27&&〃 1276(wh JZ43(s-.| 123W1 1240P1 1225n ]256(wP ]23B(si) 12.^1C.屮 12^1(VM| 刃 12 J2()5(wfc 1205(#) ]161(FII> 12OK(幅! 1 1157(-1 116O(rii> H2UM(w1 1160S) 1 1162: (rii> J144(m> : I16ACm> j141(n.> 1141(ivi Il37(nn) ]049(rn> II2D(wfc 1Mfttni} ]-054{rii} 1143Crii} 112d( 1J21(»1 jj2iCm> •a; 1lOU(mi) IW9(ni> 1IOO(ni> 芜JllRMT-B 973(w8 975严1 9i4.V(wi 973(ftn> 979W 9>71(.feu> 八6R(ni} 97S(m> 925(w) 023(wS i ■9/(wI! 1 phrtrfrHMi uK95(w& 八4((11> J 1 S5O(w) S79(wH J 八25>C忖I H: 26(tu> 825(«) SZJtuj) (bi: i]> 553-Cta] 579(Hi> 575Cul S7BCTb 1 57ft(! «I 57Rg1 5fjN.(ni> 579(th) 515(rn> 5八&(m} 54K(ml- 2、红外光谱在席夫碱金属配合物表征的应用四: 红外光谱在席夫碱中的应用展望
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 红外 光谱 席夫碱 中的 应用
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
