 高中化学无机化学推断复习题.docx
高中化学无机化学推断复习题.docx
- 文档编号:30268330
- 上传时间:2023-08-13
- 格式:DOCX
- 页数:22
- 大小:322.11KB
高中化学无机化学推断复习题.docx
《高中化学无机化学推断复习题.docx》由会员分享,可在线阅读,更多相关《高中化学无机化学推断复习题.docx(22页珍藏版)》请在冰豆网上搜索。
高中化学无机化学推断复习题
例:
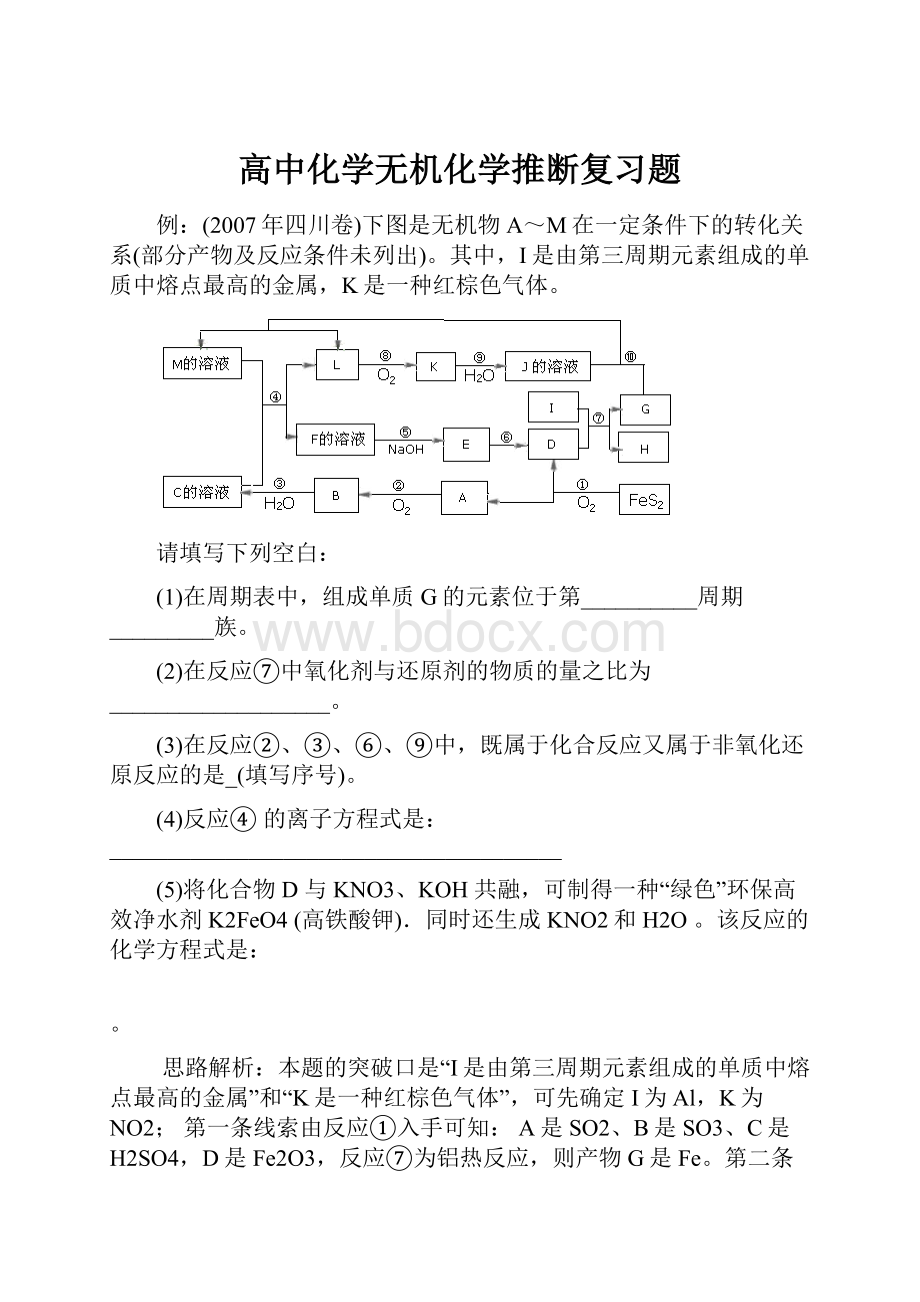
(2007年四川卷)下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。
其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第__________周期_________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为___________________。
(3)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_(填写序号)。
(4)反应④的离子方程式是:
_______________________________________
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾).同时还生成KNO2和H2O。
该反应的化学方程式是:
。
思路解析:
本题的突破口是“I是由第三周期元素组成的单质中熔点最高的金属”和“K是一种红棕色气体”,可先确定I为Al,K为NO2;第一条线索由反应①入手可知:
A是SO2、B是SO3、C是H2SO4,D是Fe2O3,反应⑦为铝热反应,则产物G是Fe。
第二条线索是由K是NO2入手,推出L是NO,J为HNO3,M是Fe和HNO3反应得到的产物,可能是Fe(NO3)3或Fe(NO3)2,而根据M与C溶液反应可生成NO气体,可断定发生了氧化还原反应,故M只能为Fe(NO3)2溶液;第三条线索是Fe(NO3)2(M)与H2SO4(C)反应得F为Fe(NO3)3,E为Fe(OH)3,到此框图中的物质全部推出。
[答案](l)四(或4)、VIII;
(2)l:
2;(3)③;
(4)3Fe2++NO3-+4H++=3Fe3++NO↑+2H2O
(5)Fe2O3+3KNO3+4KOH
2K2FeO4+3KNO2+2H2O
此题以物质的性质入手进行分析,抓住典型物质的物理性质(如气味、颜色、状态、溶解性、熔沸点等)。
先确定个别物质,再根据框图寻找线索进行推断。
如上题中的物质I和K就用此法确定。
(二)物质结构理论推断题
该类试题常与物质结构、元素周期律(表)有联系,通过阅读第一条信息,往往有多种可能答案,但把多条信息综合考虑就可逐渐缩小范围,最终确定唯一答案。
例:
由短周期元素组成的A、B、C、D、E、F六种粒子,其中只有C、D是分子,其余四种均是离子,且每个微粒中都含有10个电子。
已知A、E是由非金属元素组成的阳离子,六种粒子间有下列关系:
①A、B两种离子在加热条件下可生成C、D两种分子;
②通常状况下C的聚集状态为气态,且可使湿润的红色石蕊试纸变蓝;
③1molB离子与1molE离子作用可生成2molD分子;
④向含F离子的溶液中加入C的溶液,可生成白色沉淀W,C溶液过量沉淀也不消失,若加入含大量B离子或大量E离子的溶液,沉淀W都会溶解。
(1)微粒B的电子式是_____________;粒子E的名称是____________;粒子F对应的元素在周期表中的位置是_________________________________。
(2)写出下列反应的离子方程式:
F+过量C的溶液:
___________________________________________________
W+含大量B离子的溶液:
(3)六种微粒中的两种可与硫酸根形成一种复盐,向该复盐的浓溶液中滴加浓苛性钠溶液,依次产生的现象有:
a.溶液中出现白色沉淀b.沉淀逐渐增多c.有刺激性气味气体放出d.沉淀逐渐减少e.沉淀完全消失
该复盐的化学式为 ,在水溶液中的电离方程式是___________。
解析:
由②可知C为NH3,根据A、E是非金属元素组成的阳离子,可知A、E分别是NH4+和H3O+中的一种。
由①和③可确定A为NH4+,B为OH-,D为H2O,E为H3O+。
白色沉淀W不溶于过量的氨水,却既溶于“酸”又溶于“碱”,那么F离子只能是Al3+
答案:
(1)[
H]-;水合氢离子;第三周期ⅢA族
(2)Al3++3NH3·H2OAl(OH)3↓+3NH4+;Al(OH)3+OH-AlO2-+2H2O
(3)NH4Al(SO4)2;NH4Al(SO4)2NH4++Al3++2SO42-
(三)综合型推断题
无机推断题涉及到的知识面很广,涉及到的知识包括元素化合物、物质结构、计算、实验以及与生活环境、工业生产等,是一种综合性很强的题目,解决这类题目最好的办法是立足于酸、碱、盐、单质、氧化物间的基本转化关系,有意识地跨越中学各知识板块云展开思考。
所幸的是一般涉及的物质基本都是教材中常见的物质,这也是一条思考的线索。
例:
下图中各方框中的字母表示有关的一种反应物或生成物(某些物质略去)其中常温下B、D、G、I、J为气体,其中B可使湿润的红色石蕊试纸变蓝,A~N的所有物质中只有G为单质,其余为化合物。
N为不溶于水的无机酸。
回答下列问题:
(1)A的名称为 ,F的化学式是 ;
H的化学式是 ,L的化学式是
(2)写出实验室制取I的离子方程式:
(3)写出G的一种同素异形体的化学式:
该物质与G在化学性质上的共同点是 。
(4)已知工业上生产0.1molB放出4.62kj热量,写出该反应的热化学方程式:
(5)在反应C+E→G+F中,每生成1molG转移 mol电子。
解析:
B为可使湿润的红色石蕊试纸变蓝的气体,故B为NH3;N为不溶于水的无机酸,应为H2SiO3(或H2SiO4);根据B+G
I,I+G J,G为气体单质,B为NH3,可以判断G应为O2,I为NO,J为NO2;化合物E与C、D反应都能产生O2,则E为Na2O2;C、D分别为CO2和H2O,F、H分别为NaOH、Na2CO3;由J(NO2)+CK,故C应为H2O,K为HNO3;M可由NaOH或Na2与L反应得到,M与K(HNO3)反应生成HSiO3(或H4SiO4),故M为H2SiO3,L为SiO2由L+H M可确定H为Na2CO3,因此F为NaOH,C为H2O,D为CO2。
最后由A
NH3+H2O+CO2,可以确定A为NH4HCO3或(NH4)2CO3.
答案:
(1)碳酸铵或碳酸氢铵;NaOH;Na2CO3;SiO2
(2)3Cu+8H++2NO3- 3Cu2++2NO↑+4H2O
(3)O3;具有氧化性
(4)N2(g)+3H2(g)2NH3(g);△H=-92.4kJ·mol-1
(5)2
小结:
无论推断题属于哪种物质形式,均遵循这样的推理思路:
迅速浏览、整体扫描、产生印象、寻找突破口、注意联系、大胆假设、全面分析(正推或逆推)、验证确认。
解题的关键是仔细审题,依物质的特性或转移特征来确定“突破口”,顺藤摸瓜,进而完成全部未知物的推断(借助推断题的形式表示如下)。
无机推断题经常人为制造一些“陷阱”引导学生走入“思考的误区”,应对“陷阱”的良策一般是:
①做完题后一定要代入验证;②给“陷阱”假设后,推不下去时及时回头,切忌“一头撞死”。
另外,答非所问是考生解答此类试题经常出现的错误。
要求写元素名称而错写成元素符号,而要求写元素符号又答成元素名称或分子式;要求写离子方程式而错写成化学方程式;要求画离子结构示意图而错答为原子结构示意图;把相对原子质量、相对分子质量、摩尔质量的单位写成“克”;把物质的量、摩尔浓度、气体体积、质量、溶解度、密度、压强等的单位漏掉;化学方程式、离子方程式不配平;热化学方程式不注明物质的状态等。
因此在答题时必须注意:
①答名称还是答符号、化学式;②答离子方程式还是化学方程式;③答现象还是答结论;④答规律还是答具体物质或具体内容。
高中化学专题练习——推断题
1.下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。
常温下X是固体,B和G是液体其余均为气体。
根据图中关系推断:
E
(1)化学式XAB
(2)写出C→E的化学反应方程式
(3)实验室收集气体D和F的方法依次是法和法。
2分)有X、Y、Z三种单质,X是金属,常温下Y是液体,Z是气体,反应关系为:
(1)据此推断X、Y、Z的化学式为:
X_________,Y_________,Z__________。
(2)C+Y→A的离子方程式:
___________________________________________
(3)X元素的核电荷数小于36,它是不是主族元素,简述理由。
___________________________________________________________________________
________________________________
3.(6分)下图中每一个方框内的字母代表一种物质,常温常压下,A、B、C、D、均为单质,且B为金属,其它三个为双原子分子的气体,它们在一定条件下,发生图中所示的化合反应,得到化合物E、F、G、H、I和J,这些化合物在常温常压下的状态及颜色已在图中注明,有关反应的化学计量数为:
(1)A与B按物质的量之比n(A)∶n(B)=1∶2完全反应生成G
液
(2)B与C按物质的量之比n(B)∶n(C)=3∶1完全反应生成F
(3)C与D按物质的量之比n(C)∶n(D)=1∶3完全反应生成E
请填空:
(1)物质B是 ,物质D是
(2)B与C反应生成F的化学方程式为:
(3)A与H反应生成I的化学方程式为:
。
4.(10分)有A、B、C、D四种单质,在一定条件下,A、B、C分别跟D发生化合反应相应生成甲、乙、丙(甲、乙、丙每个分子中都含有10个电子)而B跟C发生化合反应生成丁,这些单质和化合物之间发生如下反应关系:
(1)写出下列物质的化学式
甲______________
乙___________
丙____________
_丁_____________
(2)写出反应①②③的化学方程式
①____________________________________
②_________________________________________
③_________________________________________________________。
(3)反应①的化学方程式是。
5.(14分)A、B、C、是单质,X、Y、Z、H、J、L是化合物,组成B的元素是绿色植物生活所必需的微量元素之一,且B在空气中燃烧可以得到X和J,X和J均为固体,X水
解可生成两种碱性物质。
在适当条件下,它们相互之间有下图所所示的转化关系:
(1)用化学式表示化合物L单质C。
(2)物质Z的分子空间构型是。
(3)反应①的化学方程式________________。
(4)反应⑤的化学方程式。
(5)在常温下用气体密度测定NO2的相对分子质量,实验值比理论纸值偏(填
“高”或“低”),其原因是。
6.下图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,其余为化合物。
它们存在如下转化关系,反应中生成的水及次要产物均巳略出。
(1)写出化学式:
B_____________、E_____________;
(2)指出MnO2在相关反应中的作用;反应①中是________剂,反应②中是_____剂。
(3)完成F与B发生反应的化学方程式______________________________________。
(4)若反应①是在加热条件下进行,A是_______;若反应①是在常温条件下进行,A是_________。
若在上述两种条件下得到等量的C单质.反应中转移的电子数之比为__________。
7.已知a、I、e为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
粒子代码
a
I
e
原子核数
单核
四核
双核
粒子的电荷数
一个单位正电荷
0
一个单位负电荷
物质A由a、e构成,B、C、D、K都是单质,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
请填写下列空白:
(1)写出下列物质的化学式:
。
(2)写出下列反应的离子方程式:
①H+E(溶液)→M②I溶于G。
(3)在通常状况下,若1gC气体在B气体中燃烧生成H气体时放出92.3kJ热量,则2molH气体完全分解生成C气体和B气体的热化学方程式为
8.(17分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大。
B元素原子最外层电子数比次外层多2;A、B两元素的核电荷数之差等于它们的原子最外层电子数之和;D和E的原子序数和为30;在元素周期表中,C是E的不同周期邻族元素。
五种元素两两形成的化合物有甲、乙、两、丁四种,分子中原子个数比如下表:
甲
乙
丙
丁
化合物中各元
素原子个比
A:
C=1:
1
B:
A=1:
2
D:
E=1:
3
B:
E=1:
4
(1)写出元素符合:
BE
(2)A元素某原子核内中子数比质子数多1,则该核素的核组成符合为。
物质丁的分子为分子(填“极性”或“非极性”)。
(3)向甲的水溶液中加入MnO2,氧化产物是。
(4)已知有机物乙的分子为平面结构,碳氢键间的夹角约为120°,实验室制取乙的化学方程式为。
(5)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式为。
9.A、B、C是常见单质,X、Y、Z是氧化物,它们之间有如下转化关系:
请写出符合下列要求的化学方程式:
(1)若X为CO2,则:
反应① ;
反应② 。
(2)若X为Fe3O4,则:
反应① ;
反应② 。
10.A、B、C、D、E、F是中学化学中常见的六种物质,它们之间有如下转化关系:
其中B、D在通常情况下是气体物质,F溶液呈强碱性。
(1)写出C的化学式_____________。
(2)写出反应①的化学方程式________________________。
(3)配制F溶液时必须注意:
①_____________;②____________;③(“”有示有则填写,无则不填写)
(4)写出F与盐酸反应的离子方程式______________________。
11.A、B、C、D是四种人们熟悉的与生命运动密切相关的化合物,它们所含的元素不超过三种,并有下列关系(反应条件均未注明)
目前化合物B在自然界含量呈上升趋势,对环境产生了不利影响,E是一种生活中常见的化合物,在一定条件下可与单质N进一步发生如下变化:
E+3N→3A+2B
(1)A、B、C、D分别是什么物质,常温下,A和B转化为C的途径是什么?
(2)假设在上述转化中无损耗,如有0.1molE生成,求A和B转化为C时能产生多少克单质N?
12.(6分)已知甲、乙、丙为常见单质,A、B、C、D、X、Y、Z为常见化合物,Y的摩尔质量比Z小16,乙与丙的摩尔质量相同,B的摩尔质量比D的小2,B与X的摩尔质量相同,各物质转化关系如下图(各反应条件已略去)。
(1)丙、B的分子式分别为、。
(2)Y转化为Z的化学方程式。
(3)E与F反应的离子方程式。
14.(14分)某无色溶液,其中有可能存在的离子如下:
Na+、Ag+、Ba2+、Al3+、AlO
、S2-、CO
、SO
、SO
,现取该溶液进行有关实验,实验结果如下图所示:
试回答下列问题:
(1)沉淀甲是____________,
(2)沉淀乙是__________,
(3)由溶液甲生成沉淀乙的离子方程式为:
_________________________。
(4)气体甲成分可能有哪几种?
(可以不填满也可以补充,多填要扣分)
1
2
3
4
5
6
(5)综合上述信息,可以肯定存在的离子:
_____________________________。
15、(10分)一定条件下发生如图所示的转化关系,其中A、B、C为中学化学中常见元素的化合物,甲、乙、丙均为单质。
甲
(1)若A是CO2,甲能在A中剧烈燃烧①化合物B的电子式为,
单质丙分子式;②现有下列药品和制气装置:
实验药品:
a.氯酸钾b.大理石
c.过氧化钠d.二氧化锰e.甲酸f.浓硫酸g.稀硫酸h.浓硝酸i.双氧水j蒸馏水
选择上述所给的一些药品,既可以制取CO2,又可以制取气体丙,制取CO2应选用的药品是,制取气体丙的化学反应方程式
(2)若A、B、C均为溶液,单质乙在常温下为液态,反应均在溶液中进行,写出A与甲按物质的量之比为1:
1发生反应的离子方程式
。
16.(8分)A、B、C、D是中学化学中四种常见的非金属单质,在标准状况下,它们之中有三种呈气态,只有一种呈固态。
B的相对分子质量很小。
甲、乙、丙、X、Y五种物质都是化合物,这些化合物和A、B、C、D之间有如图所示关系:
且知以上物质的所有组成元素均为短周期元素。
根据以上事实,回答下列问题:
(1)化合物乙与氢氧化钠按物质的量之比1:
3恰好完全反应,则乙的化学式是。
(2)图中的化学反应共有个化合反应,个氧化还原反应。
(3)Y与甲反应生成乙和丙的化学方程式为:
。
17.(6分)根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
(1)单质L是_______________。
(2)化合物B是_____________。
(3)图中除反应①外,还有两个用于工业生产的反应是______和_______(填代号)
它们的化学反应方程式分别是____________________和____________________。
18、已知甲、乙、丙是三种常见的单质,且组成它们的元素核电荷数之和为35;A-G是七种常见化合物:
上述各物质间的相互转化关系如下图所示(反应条件和其它生成物略)。
试回答:
(1)B的化学式是:
______,D的名称是_________;
(2)用电子式表示A:
(3)写出①、②两步变化的化学方程式:
19.(13分)有常见A、B、C三种短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素最外层电子数比B多一个。
甲、乙、丙是3种含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙溶液pH>7,乙溶液pH<7;丁为气体,戊为淡黄色固体。
甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如下图:
请回答:
(1)写出C元素的原子结构示意图_______________,写出丁和戊的电子式____________、_________________;
(2)用有关化学用语解释:
乙溶液呈酸性的原因____________________________;
丙溶液呈碱性的原因____________________________;
(3)写出有关反应的离子方程式:
①乙溶液+丙溶液→丁______________________________;
②己溶液+丙溶液→丁______________________________。
20.X、Y、A、B、C、D是中学化学教材中常见的化合物,且有如下转化关系。
气体C的式量比气体X的式量大2,产物中水已忽略。
回答下列问题:
(1)X分子的电子式是______________________。
(2)在上述转化过程中作还原剂的物质有(填物质的化学式)___________________
(3)A与浓HNO3反应的化学方程式为_______________________________________
(4)测定气体C的相对分子质量,测得的数值与气体的相对分子质量有差异的原因是(用化学方程式表示)_____________________________________________________。
21.已删除
22.(9分)下图①到⑩分别代表反应中的一种物质,且它们均为化学中的常见物质
(1)①的化学式为,⑤和⑥反应的化学方程式为。
(2)实验室由⑧制取⑨的离子方程式为,⑨转变为⑩的化学方程式为。
由⑨转变为⑩的反应现象为
参考答案:
1.
(1)NH4HCO3NH3H2O
(2)2CO2+2Na2O2=2Na2CO3+O2↑
(3)排水向上排空气
2.(8分)
(1)X-FeY-Br2Z-H2(各1分)
(2)2Fe2++Br2=2Fe3++2Br(2分)
(2)不是(1分),因X是前四周期元素。
且在A和C中显示不同正价。
(2分)
3.
(1)Mg(镁),H2(氢) (每空1分,共2分)
(2)3Mg+N2
Mg3N2(2分)
(3)O2+2NO
2NO2 (2分)
4.
(1)HF、H2O、NH3、NO(每空1分)
(2)2F2+2H2O==4HF+O24NH3+5O2==4NO+6H2O4NH3+NO==5N2+6H2O
5.(14分,每空2分)
(1)NOH2
(2)三角锥型(3)3Mg+N2Mg3N2
(4)4NH3+5O24NO+6H2O(5)高NO2分子相互反应有N2O4生成(2NO2N2O4)
6
(1)HCl、Fe
(2)催化氧化)(3)Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
(4)KClO3H2O22:
1
7.
(1)B.Cl2J.NO
(2)①H++ClO-=HClO(3)NH3+H2O
NH3·H2O
NH4++OH-(4)2HCl(g)=H2(g)+Cl2(g);△H=+184.6kJ·mol-1
浓硫酸
△
8.
(1)B:
CE:
Cl
(2)
;非极性
(3)O24)CH3CH2OHCH2=CH2↑+H2O
(5)Al3++3HCO3—=Al(OH)3↓+3CO2
9.
(1)、2Mg+CO2
2MgO+C,C+2CuO
2Cu+CO2
(2)、3Fe3O4+8Al
9Fe+4Al2O33Fe+4H2O(气)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 无机化学 推断 复习题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
