 高考优秀试题docx.docx
高考优秀试题docx.docx
- 文档编号:30425640
- 上传时间:2023-08-14
- 格式:DOCX
- 页数:26
- 大小:712.82KB
高考优秀试题docx.docx
《高考优秀试题docx.docx》由会员分享,可在线阅读,更多相关《高考优秀试题docx.docx(26页珍藏版)》请在冰豆网上搜索。
高考优秀试题docx
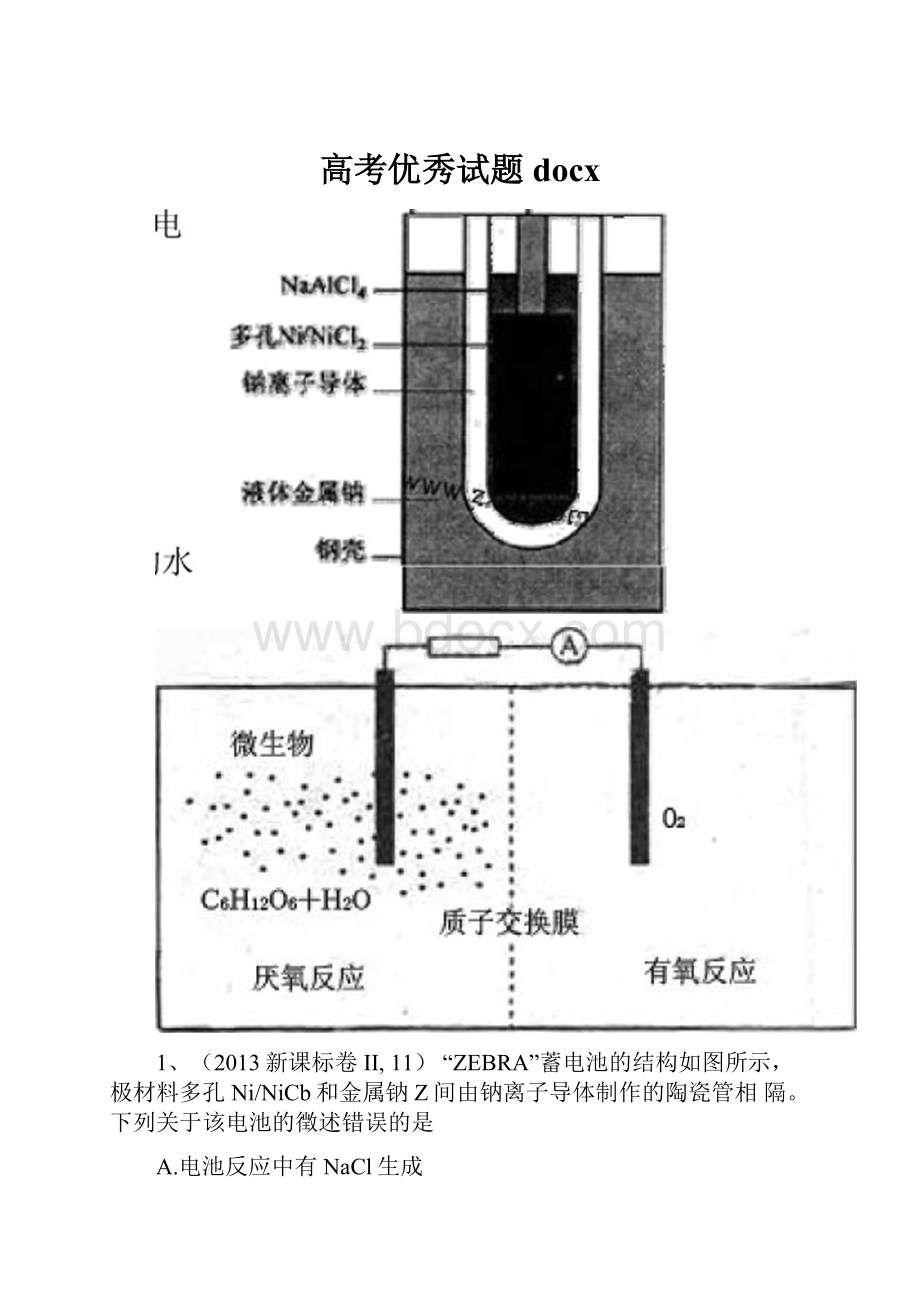
1、(2013新课标卷II,11)“ZEBRA”蓄电池的结构如图所示,极材料多孔Ni/NiCb和金属钠Z间由钠离子导体制作的陶瓷管相隔。
下列关于该电池的徴述错误的是
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三个铝离子
C.正极反应为:
NiCl2+2c"=Ni+2Cr
D.钠离子通过钠离子导体在两电极间移动
(2014新课标卷11,12)2013年3月我国科学家报道了如图所示笊溶液锂离子电池体系。
下列叙述错误的是
A.a为电池的正极
B.电池充电反应为LiMn2O4=Li]_xMn2O4+xLi
C.放电时,a极锂的化合价发生变化
D.放电时,溶液中的LF从b向a迁移
(2015新课标卷I,11)微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。
下列有关微牛•物电池的说法错误的是()
A.正极反应中有CO?
生成
B.微工物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2=6CO2+6H2O
2.(2014新课标卷1,13)利用右图所示装置进行下列实验,能得出相应实验结论的是()
选项
①
②
③
实验结论
A
稀硫酸
Na2S
AgNOs与AgCl的浊液
Ksp(AgCl)>Ksp(Ag2S)
)(D
B
浓硫酸
蔗糖
漠水
浓硫酸具有脱水性、氧化性
I?
C
稀盐酸
Na2SO3
Ba(NO3)2溶液
so2与可溶性锁盐均可生成口色沉淀
1)
D
浓硝酸
Na2CO3
Na2SiO3溶液
酸性:
硝酸〉碳酸〉硅酸
■
②j
[③
(2015新课标卷I,10)下列实验小,对应的现象以及结论都正确且两者具有因果关系的是()
选项
实验
现彖
结论
A.
将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液
有气体生成,溶液呈血红色
稀硝酸将Fe氧化为
Fe3+
B.
将铜粉加入1.0molL-'Fe2(SO4)3溶液
溶液变蓝、冇黑色固体出现
金属铁比铜活泼
C.
用塩圳钳夹住一小块用砂纸仔细打磨过的铝箔在酒粹灯上加热
熔化后的液态铝滴落下来
金属铝的熔点较低
D.
将0.1molL_IMgSO4溶液滴入NaOH溶液至不再有沉淀产牛,再滴加0.1mol-L,CuSO4溶液
先有口色沉淀牛成后变为浅蓝色沉淀
Cu(OH)2的溶度积比
Mg(OH)2的小
(2015新课标卷II,13)用右图所示装置进行下列实验:
将①屮溶液滴入②屮,预测的现
象与实际相符的是
选项
①中物质
②中物质
预测②中的现彖
A.
稀盐酸
碳酸钠与氢氧化钠的混合溶液
立即产生气泡
B.
浓硝酸
用砂纸打磨过的铝条
产生红棕色气体
C.
氯化铝溶液
浓氢氧化钠溶液
产生大量白色沉淀
D.
草酸溶液
高猛酸钾酸性溶液
溶液逐渐褪色
3.(2014新课标卷I,27)(15分)
次磷酸(H3PO2)是一种精细磷化工产品,具冇较强还原性。
回答下列问题:
(1)H3PO2是一种中元强酸,写出其电离方程式o
(2)H3PO2及NaH2PO2均可将溶液中的Ag*还原为银,从而可用于化学镀银。
1(H3PO2)中,P元素的化合价为。
2利用(H3PO2)进行化学镀银反应屮,氧化剂与还原剂的物质的量之比为4:
1,则氧化产
物为:
(填化学式)。
®NaH2PO2为(填“正盐”或“酸式盐其溶液显(填“弱
酸性,,、“中性”或“弱碱性”)。
(3)(H3PO2)的工业制法是:
将口磷(PJ与Ba(OH)2溶液反应住成PH3气体和Ba(H2PO2)2,
后者再与H2SO4反应。
写出白磷与Ba(OH)2溶液反应的化学方程式O
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
阳极室产品室原料室阴极室
1写出阳极的电极反应式O
2分析产品室可得到H3PO2的原因。
3早期采用“三室电渗析法"制备H3PO2,将“四室电渗析法叫邛口极室的稀硫酸用H3PO2
稀溶液代替,并撤去阳极室与产品室Z间的阳膜,从而合并了阳极室与产品室。
其缺点是产
品中混有朵质,该朵质产生的原因是O
4.
(2015新课标卷I,27)硼及其化合物在工业上冇许多用途。
以铁硼矿(主要成分为
Mg2B2O5H2O和Fe3O4,还有少SFe2O3.FeO、CaO、A12O3和SiO?
等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
铁硼矿粉
回答下列问题:
(1)写出Mg2B2O5H2O与硫酸反应的化学方程式。
为提高浸出速率,
除适当增加硫酸浓度外,还可采取的措就有(写出两条)。
(2)利用的磁性,可将其从“浸渣”屮分离。
“浸渣计还剩余的物质是(写
化学式)。
(3)“净化除杂"需先加H2O2溶液,作用是。
然后再调节溶液的pH约为5,F1
的是O
(4)“粗硼酸”屮的主要杂质是(填名称)。
(5)以硼酸为原料可制得硼氮化钠(NaBHQ,它是有机合成屮的重要还原剂,其电了
式为o
(6)单质硼可用于生产具有优良抗冲击性能硼钢。
以硼酸和金属镁为原料nJ制备单质
硼,用化学方程式表示制备过程o
5.(2013新课标卷II,28)(14分)厶
在1.0L密闭容器中放入O.lOmolA(g),在一定温度进行如下反应应:
A(g)^^B(g)+C(g)AH=+85.1kJ-mor,
反应时间⑴与容器内气体总压强(p)的数据见下表:
时间t/h
0
1
2
4
8
16
20
25
30
总压强p/lOOkPa
4.91
5.58
6.32
7.31
8.54
9.50
9.52
9.53
9.53
回答F列问题:
(1)欲提高A的平衡转化率,应采取的措施为o
(2)由总压强P和起始压强P。
计算反应物A的转化率(x(A)的表达式为o
平衡时A的转化率为,列式并计算反应的平衡常数Ko
⑶①由总压强p和起始压强po表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=mol,n(A)=mol。
②下表为反应物A浓度与反应时间的数据,计算沪
反应时间t/h
0
4
8
16
C(A)/(mol-L1)
0」0
a
0.026
0.0065
分析该反应中反应反应物的浓度c(A)变化与时间间隔(At)的规律,得出的结论
是,
由此规律推出反应在12h时反应物的浓度c(A)为mobL-1
(2014新课标卷I,28)(15分)
乙醇是重要的有机化工原料,可山乙烯气相直接水合法或间接水合法牛产。
回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生
成乙醇。
写出相应反应的化学方程式O
(2)已知:
甲醇脱水反应2CH3OH(g)=CH3OCH3(g)+H2O(g)△R=—23.9kJmolT甲醇制烯坯反应2CH3OH(g)=C2H4(g)+H2O(g)A//2=-29JUmoL
乙醇异构化反应2CH3OH(g)=CH3OCH3(g))△H3=+50.7kJ・molT
贝IJ乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的=kJ-mol^o与间接水合法相比,气相直接水合法的优点是o
(3)下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中nlh0:
■
乜弘=1:
1)。
1列式计算乙烯水合制乙醇反应在图中A点的平衡常数g=(用平
衡分压代替平衡浓度计算,分压=总压X物质的量分数)。
2图中压强P]、P2、P3、P4的人小顺序为,理由是O
3
气相直接水合法常采用的工艺条件为:
磷酸/硅藻土为催化剂,反应温度290°C,压
除了可以适当改变反应温度和压强外,还可以采取的措施有、O
6.
(2015重庆卷,5).某化妆品的纟R分Z具有美白功效,原从杨树屮提取,现可用如下反应制备:
下列叙述错谋的是()
A.X、Y和Z均能使渓水褪色
B.X和Z均能与NaHCCh溶液反应放岀CO?
C・Y既能发生取代反应,也能发生加成反应
D.Y可作加聚反应单体,X可作缩聚反应单体
7.
(2015安徽卷12)某同学将光亮的镁条放入盛有NH4C1溶液的试管小,有大量气泡产生。
卜•列叙述错误的是(
A.MOH的碱性强丁ROH的碱性
B.ROH的电离程度:
b点大于a点
C.若两溶液无限稀释,则它们的c(OHJ相等
lgi
D•当殆=2时,若两溶液同时升高温度,则c(M+)/c(R*)增大
9.(2015新课标卷II,26)(14分)酸性锌镒T电池是一种一次电池,外壳为金属锌,中间是碳棒,具周围是有碳粉,二氧化镒,
氯化锌和氯化饺等组成的填充物,该电池在放电过程产生MnOOH,冋收处理该废电池可以得到多种化工原
料,有关数据下图所示:
溶解度/(g/100g水)
化合物
0
20
40
60
80
100
NH4C1
29.3
37.2
45.8
55.3
65.6
77.3
ZnCl2
343
395
452
488
541
614
化合物
Zn(OH)2
Fe(OH)2
Fe(OH)3
Ksp近似值
IO'17
IO'17
IO'39
回答下列问题:
(1)该电池的正极反应式为,电池反应的离子方程式为
(2)维持电流强度为0.5A,电池工作五分钟,理论消耗Zn_go(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要冇氯化锌和氯化鞍,两者可以
通过—分离回收,滤渣的主耍成分是二氧化镒、和,欲从中得到较
纯的二氧化镒,最简便的方法是,其原理是c
(4)川废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,具方法是:
加入新硫酸
和双氧水,溶解,铁变为加碱调节PH为—,铁刚好完全沉淀(离
子浓度小于lxlO*5mol/L吋,即可认为该离子沉淀完全)。
继续加碱调节PH为锌开始沉淀(假定ZJ+浓度为O.lmol/L)o若上述过程不加双氧水的后果是—,原因是—o
10.(2015天津卷7)(14分)随原了序数的递增,八种短周期元素(用字母X表示)原了半径的相对大小、最高正价或最低负价的变化如下图所示。
根据判断出的元素回答问题:
(1)佈元素周期表的位置是。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)>;比
较g、h的最高价氧化物对应的水化物的酸性强弱是:
>o
(3)任选上述元素组成一种四原了共价化合物,写出其电了式o
(4)己知lmole的单质在足最ck中燃烧,恢复至室温,放i*ll255.5kJ热量,写出该反应的
热化学方程式:
o
(5)上述元索可纽成盐R:
zx4f(gd4)2,向盛^lOmLlmolL^R溶液的烧杯屮滴加
lmol-L^NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
1R离子浓度由大到小的顺序是:
。
2写出m点反应的而梨子方程式。
3若R溶液改加20mL1.2nwl・lJBa(OH)2溶液,充分反应后,溶液中产牛沉淀的物
质的量为molo
11.(2015新课标卷I,28)(15分)碘及其化合物在合成杀菌剂、药物等方面具冇广泛用途。
冋答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即
可得到【2,该反应的还原产物为。
(2)上述浓缩液中含有「、C「等离了,取一定量的浓缩液,向其屮滴加AgNO3溶液,
当AgCl开始沉淀时,溶液中。
(厂)为:
已知KSp(AgCl)=1.8xlO-10,
c(C厂)
Ksp(Agl)=8.5x10-|7o
(3)已知反应2HI(g)=H2(g)+I2(g)的AH=+llkJmol",lmolH2(g)、lmoll2(g)分
子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则ImolHI(g)分子中化学键断裂时需吸收的能量为kJo
(4)Bodensteins研究了下列反应:
2HI(g)、氏(g)+b(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min
0
20
40
60
80
120
兀(HI)
1
0.91
0.85
0.815
0.795
0.784
兀(HI)
0
0.60
0.73
0.773
0.780
0.784
1根据上述实验结果,该反应的平衡常数K的计算式为:
。
2上述反应中,正反应速率为vE=ks-x2(HI),逆反应速率为v^i«x(H2)x(I2),
其中k、k逆为速率常数,则k逆为(以K和k正表示)。
若R正=0.0027mm1,
在t=40min时,v正=min-1
3由上述实验数据计算得到卩正〜x(HI)和.,逆〜兀(出)的关系可川卜-图表示。
当升高至IJ
某一温度时,反应重新达到平衡,相应的点分别为(填字母)
HCKglyl<(>gZX
其中,反应①为:
2HCI(g)+CuO(s)=^^H2O(g)+CuCl2(g)AH,反应②空成lmolCl2(g)的反应热为AH?
则总反应的热化学方程式为,
(反应热J-MAH,和AH?
表示)。
(2)新型RuO2催化剂对上述HC1转化为Cl2的总反应具有更好的催化活性,
1
实验测得在一定压强下,总反应的HC1平衡转化率随温度变化的anci-T曲线如图
12,贝IJ总反应的Z\H0,(填“〉”、或y”);A、B两点的平衡常数K(A)
r-
%
70
与K(B)中较大的是oE
2在上述实验中若压缩体积使压强增大,画岀相应anct-T曲线的示意图,并简要
说明理由:
0
3下列措施中冇利于提咼anci的有。
HQ
(3)一定条件下测得反应过程中n(C12)的数据如下:
t(min)
0
2.0
4.0
6.0
8.0
n(Cl2)/10-3mol
0
1.8
3.7
5.4
7.2
计算2.0〜6.0min内以HC1的物质的量变化表示的反应速率(以molmin'为单位,写出计算过程)。
(4)Cb用途广泛,写出用Cb制备漂白粉的化学方程式。
13.(2015江苏卷19).(15分)实验室用下图所示装置制备KC10溶液,并通过KC10溶液与Fe(NO3)3溶液的反应制备高效水
处理剂K2Fc04o已知K2FcO4具有下列性质①可溶于水、微溶于浓KOH溶液,②在0C——5°C、强碱性溶
液中比较稳定,③在Fe”和Fe(OH)3催化作用下发生分解,④在酸性至弱碱性条件下,能与水反应生成
Fe(OH)3和O2。
取0.0100molL-1的AgNO3标准溶液装入滴定管,収100.00mL海带浸収原液至滴定池,用电势滴定法测定碘含量。
测的的电动势(E)反映溶液中c(I-)的变化,部分数据如下花
V(AgNO3)/mL
15.00
19.00
19.80
19.98
20.00
20.02
21.00
23.00
25.00
E/mV
■225
・200
・150
•100
50.0
175
275
300
325
实验
(二)碘的制取
另制海带浸取原液,「卩、乙两种实验方案如下:
已知:
3I2+6NaOH=5Nal+NaIO34-3H2O
请回答:
⑴实验
(一)屮的仪器名称:
仪器A,仪器B
(2)①根据表中数据绘制滴定曲线:
V(AgNO;)/mL^
②该次滴定终点时用去AgNOs溶液的体积为mL,计算得海带屮碘的百分含
量为%0
(3)①分液漏斗使用前须检漏,检漏方法为o
2步骤X屮,萃取后分液漏斗内观察到的现象是。
3下列有关步骤Y的说法,正确的是。
A.应控制NaOH溶液的浓度和体积
B.将碘转化呈离了进入水层
C.主要是除去海带浸取原液中的冇机杂质
D.NaOH溶液町以由乙醇代替
4实验
(二)中操作Z的名称是
(4)方案甲中采用蒸饰不合理,理由是o
15.(2015福建卷25)(15分)
某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一制取氯酸钾和氯水
利川右图所示的实验装置进行实验。
(1)制取实验结束后,取出B屮试管冷却结晶、过滤、洗涤。
该实验操作过程需要的
玻璃仪器有O
(2)若对调B和C装置的位置,(填“能”或“不能。
提高B中氯酸钾的产率。
实验二氯酸钾少碘化钾反应的探究
(3)在不同条件下KCIO3可将KI氧化为12或KIO3。
该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温卜•进行):
试管编号
1
2
3
4
0.20mol・L5]:
/inl
1.0
1.0
1.0
1.0
KC10:
(s)/g
0.10
0.10
0.10
0.10
e.Omol-L'^SO^ml
0
3.0
6.0
9.0
蒸餐水
9.0
6.0
3.0
0
实验现象
1系列a实验的实验n的是o
2设计1号试管实验的作用是0
3若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧
化产物唯一,还原产物为KC1,则此反应的离子方程式为o
实验三测定饱和氯水中氯元索的总虽
(4)该小组设计的实验方案为:
使用右图装置,加热15.0ml饱和氯水试样,测定产生气体的体积。
此方案不可行的主要原因是。
(不考虑实验装置及
操作失误导致不町行的原因)
(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):
资料:
i.次氯酸会破坏酸碱指示剂;ii.次氯酸或氯水可被SO?
、H2O2.FeCb等物质还原成
16.(2015北京卷27)(14分)研究CO?
在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
(1)溶于海水的CO2主要以4种无机碳形式存在,其中HC03-占95%,写出C02溶于
水产生HCO3•的方程式:
o
(2)在海洋循环中,通过右图所示的途径固碳。
1写出钙化作用的离子方程式:
=
2同位素示踪法证实光合作用释放出的02只来自于比0,用用0标记物质的光合
作用的化学方程式如下,将其补充完整:
+===(CH2O)x+x18O2+xH2O
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测罐溶解无机碳,可采用如下方法:
①气提、吸收C02,用N2从酸化后的还说中吹出CO?
并用碱液吸收(装置示意图如下),将虚线框中的装置补充完整并标出所用试剂。
②滴定。
将吸收液洗后的无机碳转化为NaHC03,再用xmol/LHCl溶液滴定,消耗ymlHCl溶液,海水中溶解无机碳的浓度二mol/Lo
(4)
利用右图所示装直从海水屮提取C02,有利于减少坏境温室气体含量。
1结合方程式简述提取CO?
的原理:
。
2用该装置产牛的物质处理b室排出的海水,合格后排回大海。
处理至合格的方法
是o
选做题:
17.【新课标卷II化学——选修2:
化学与技术】苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚
18.
和丙酮,其反应和工艺流程示意图如下:
畀丙苯过氧化氢
相关化合物的物理常数
物质
相对分子质量
密度(g/cm-3)
沸点/°C
异丙苯
120
0.8640
153
丙酮
58
0.7898
56.5
苯酚
94
1.0722
182
回答下列问题:
(1)在反应器A中通入的X是o
(2)反应①和②分别在装置和屮进行(填装置符号)。
(3)在分解釜c中加入的y为少置浓瞌酸.其作用是.优点是用st少.缺点是,
⑷反应②为一(填“放热”或“吸热”)反应。
反应温度控制在50-60°C,温度过高的安全隐患是0
⑸中和釜D中加入的Z最适宜的是(填编号。
已知苯酚是一种弱酸)
a.NaOHb.CaCOc.NaHCOd.CaO
(6)蒸饰塔F中的馅出物T和P分别为和,判断的依据是。
(7)用该方法合成苯酚和丙酮的优点是。
19.(2015L1I东卷33).(12分)[化学-•物质结构与性质]
氟在自然界中常以CaF2的形式存在。
(1)下列关于CaF?
的表述正确的是o
a.Ca*与F■间仅存在静电吸引作用
b.F■的离子半径小于CT,则CaF2的熔点高于CaCl2
c.阴阳离子比为2:
1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离了键,因此CaF?
在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含A严的溶液中,原因是(用离子方程式表示)。
已知AlFf在溶液中可稳定存在。
(3)F2通入稀NaOH溶液中可生成OF2,OF?
分子构型为,其中氧原子
的杂化方式为o
(4)F2与其他卤索单质反应可以形成卤索互化物,例如CIF3、BrFs等。
已知反应Cl2(g)
+3F2(g)=2ClF3(g)AH=-313kJmor,F-F键的键能为159kJmoL,C1-C1键的键能为242kJmoF1,则CIF3中Cl—F键的平均键能为kJ-moL。
CIF3的熔、沸
点比BrF3的(填“高诚“低)
20.[2015海南卷19选修3—物质结构与性质]
19-1(6分)卜•列物质的结构或性质与氢键无关的是
A.乙瞇的沸点B.乙醇在水中的溶解度
C.氢化镁的晶格能D.DNA的双螺旋结构
19-11(14分)锐(23V)是我国的丰产元素,广泛用于催化及钢铁工业。
回答下列问题:
(1)帆在元素周期表中的位宜为,其价层电子排布图为O
(2)锐的某种氧化物的品胞结构如图1所示。
晶胞中实际拥有的阴、阳离子个数分别
为、。
(3)V2O5常用作SO2转化为SO3的催化剂。
SO2分子中S原子价层电子对数是—对,分了的立体构型为—;SO3气态为单分子,该分子中S原子的杂化轨道类型为_;
SO3的三聚体坏状结构如图2所示,该结构屮S原子的杂化轨道类型为_;该结
构中S—O键长由两类,-•类键长约140pm,另一类键长约为160pm,较短的键为
(4)V2O5溶解
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 优秀 试题 docx
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
